家蚕血细胞特异表达新基因Bm04862的鉴定及表达
2016-06-23余霜苏晶晶徐曼张奎崔红娟家蚕基因组生物学国家重点实验室西南大学重庆400716
余霜,苏晶晶,徐曼,张奎,崔红娟家蚕基因组生物学国家重点实验室 西南大学,重庆 400716
家蚕血细胞特异表达新基因Bm04862的鉴定及表达
余霜,苏晶晶,徐曼,张奎,崔红娟
家蚕基因组生物学国家重点实验室 西南大学,重庆400716
余霜, 苏晶晶, 徐曼, 等. 家蚕血细胞特异表达新基因Bm04862的鉴定及表达. 生物工程学报, 2016, 32(2): 241–249.
Yu S, Su JJ, Xu M, et al. Identification and characterization of a novel hemocyte specific gene Bm04862 in silkworm, Bombyx mori. Chin J Biotech, 2016, 32(2): 241–249.
摘 要:通过家蚕组织芯片数据筛选得到家蚕血细胞特异表达基因Bm04862,并首次对该基因进行了克隆与鉴定。应用RACE技术获得该基因全长,并对其进行生物信息学分析。Bm4862基因开放阅读框819 bp,共编码273 个氨基酸残基,预测其为跨膜蛋白;通过qRT-PCR技术对其时空表达情况进行分析;结果显示Bm04862基因在家蚕血细胞中特异高表达,并在4龄眠期和预蛹2 d时达到表达高峰;构建Bm04862真核表达载体,转染Sf9细胞分析其蛋白的亚细胞定位情况,结果表明其定位于细胞核膜和部分细胞质中。此外,用大肠杆菌刺激蚕体24 h后,Bm04862基因表达水平显著上调,表明大肠杆菌可以诱导该基因的表达,由此推测该基因可能参与家蚕的免疫应答。这为深入研究该基因在家蚕免疫反应中的功能提供了参考。
关键词:家蚕,血细胞特异基因,Bm04862,表达特征,亚细胞定位
Received: March 17, 2015; Accepted: June 8, 2015
Supported by: National Natural Science Foundation of China (No. 31172268), National Basic Research Program of China (973 Program) (No. 2012CB114600).
国家自然科学基金 (No. 31172268),国家重点基础研究发展计划 (973计划) (No. 2012CB114600) 资助。
昆虫血细胞在修复组织损伤、清除体内凋亡组织与细胞以及对抗病原体、微生物等外源物侵袭的免疫反应中都发挥着至关重要的作用[1-4]。昆虫与哺乳动物的先天免疫系统在结构和功能上十分相似[5-6],且只具有先天性免疫系统,这为先天性免疫的研究提供了一个良好的模型。家蚕作为鳞翅目模式昆虫,研究家蚕血细胞特异性的表达基因及其功能,对于阐释家蚕以及哺乳动物血细胞的生长发育分子机理具有重要意义。鳞翅目昆虫血细胞主要分为5种类型:原血细胞 (Prohemocyte)、浆细胞(Plasmatocyte)、颗粒细胞 (Granular cell)、小球细胞 (Spherule cell) 以及拟绛色细胞(Oenocytoid)[6-8]。每种血细胞都具有并行使其特有的功能。原血球细胞是一种多潜能的血细胞,能分化成其他类型的血细胞;颗粒细胞的主要作用是吞噬微生物、病原体、死细胞以及凋亡细胞[7],拟绛色细胞通过调节黑化作用来参与免疫反应,浆细胞主要对病原体或死细胞进行包裹,维持内环境的稳定[8-9]。
近年来,昆虫血细胞相关新基因越来越多的被研究者发现,这为解析昆虫造血过程的分子调控机制以及免疫应答通路的研究提供了重要依据。2000年Hori等在麻蝇属Sarcophaga中发现并鉴定了一种具有18个表皮生长因子样结构域的新型Ⅰ型跨膜蛋白,该蛋白只在预蛹期的血细胞中特异性表达,并作为组织重塑清道夫受体,对变态过程中所产生的凋亡细胞及组织碎片的识别和消除起着至关重要的作用[10];2003年Kurucz等发现在果蝇中Hemese基因编码一种跨膜蛋白,其在3种果蝇血细胞中特异性表达并调控血细胞参与细胞免疫应答[11];2005年,Levin等研究表明在烟草天蛾中血细胞特异表达的整合素异质二聚体亚基β (Integrin β1),该基因具有刺激浆细胞发生包囊外源病原物的作用[12];2007年Gajewski等在果蝇中发现黑色细胞基因 (Black cells,Bc) 编码酚氧化酶 (Prophenoloxidase),并在成熟后期的结晶细胞中特异表达,参与黑化作用[13]。家蚕各组织全基因组芯片表达数据的完成为家蚕血细胞特异性表达基因的研究奠定了重要基础[14]。目前对家蚕血细胞特异表达基因的研究甚少,本研究针对血细胞特异表达基因Bm04862,对其组织表达情况以及亚细胞定位特征进行了研究,并初步探索了其在抵御外来微生物过程中的功能,我们的工作为深入研究Bm04862基因的结构及其功能奠定了基础。
1 材料与方法
1.1材料与试剂
试验所用家蚕品种大造 (P50) 由西南大学家蚕基因资源库提供,于25 ℃,湿度80%−90%条件下用新鲜桑叶人工饲养;Sf9细胞系由本实验室保存;RNA提取试剂盒、反转录试剂盒、荧光定量PCR试剂购自Promega公司;Trizol试剂、GeneRacerTMRACE Ready cDNA Kit购自Invitrogen公司;细胞转染试剂X-tremeGENE HP DNA Transfection Reagent 购自Roche公司;Grace昆虫细胞培养基和胎牛血清购自Gibco公司。
1.2基于家蚕组织芯片数据的筛选
基于本实验室家蚕组织芯片数据库,分析与预测家蚕基因在5龄3 d幼虫各组织基因的表达情况。对家蚕血细胞特异表达基因进行筛选,获得一个探针号为sw04862的基因,该基因在血细胞中有较高表达信号值,在其他组织中信号值较低。SW04862探针所代表的基因为血细胞特异表达候选基因,命名为Bm04862。
1.3总RNA提取以及cDNA的合成
解剖获得家蚕5龄3 d幼虫的血细胞、中肠、丝腺、马氏管、脂肪体、精巢等各组织,液氮研磨后,经Trizol消化后提取总RNA,并参照反转录试剂盒说明书合成第一链cDNA。
1.4RACE获得Bm04862全长
根据家蚕Bm04862探针序列以及家蚕基因组EST数据库序列,设计特异引物,扩增得到该基因的部分中间序列,最后设计该序列特异引物,GSP1、NGSP1、GSP2、NGSP2 (表1)。按照RACE试剂盒说明书分别进行5′RACE和3′RACE,检测到目的条带后,进行T克隆程序:回收、连接、转化和阳性克隆筛选,并将阳性质粒送至华大公司测序,利用BioEdit软件对5′RACE和3′RACE结果进行拼接,获取其cDNA全长。
1.5生物信息学分析
利用在线工具对Bm04862分子量、等电点(http://web.expasy.org/compute_pi/)、信号肽(http://www.cbs.dtu.dk/services/SignaIP/)、蛋白保守结构域 (http://smart. embl-heidelberg.de/)、跨膜结构域 (http://www.ch.embnet.org/software/ TMHMM_form.html) 和蛋白二级结构算法软件GOR4软件(https://prabi.ibcp.fr/htm/index.php) 对Bm04862蛋白进行预测。
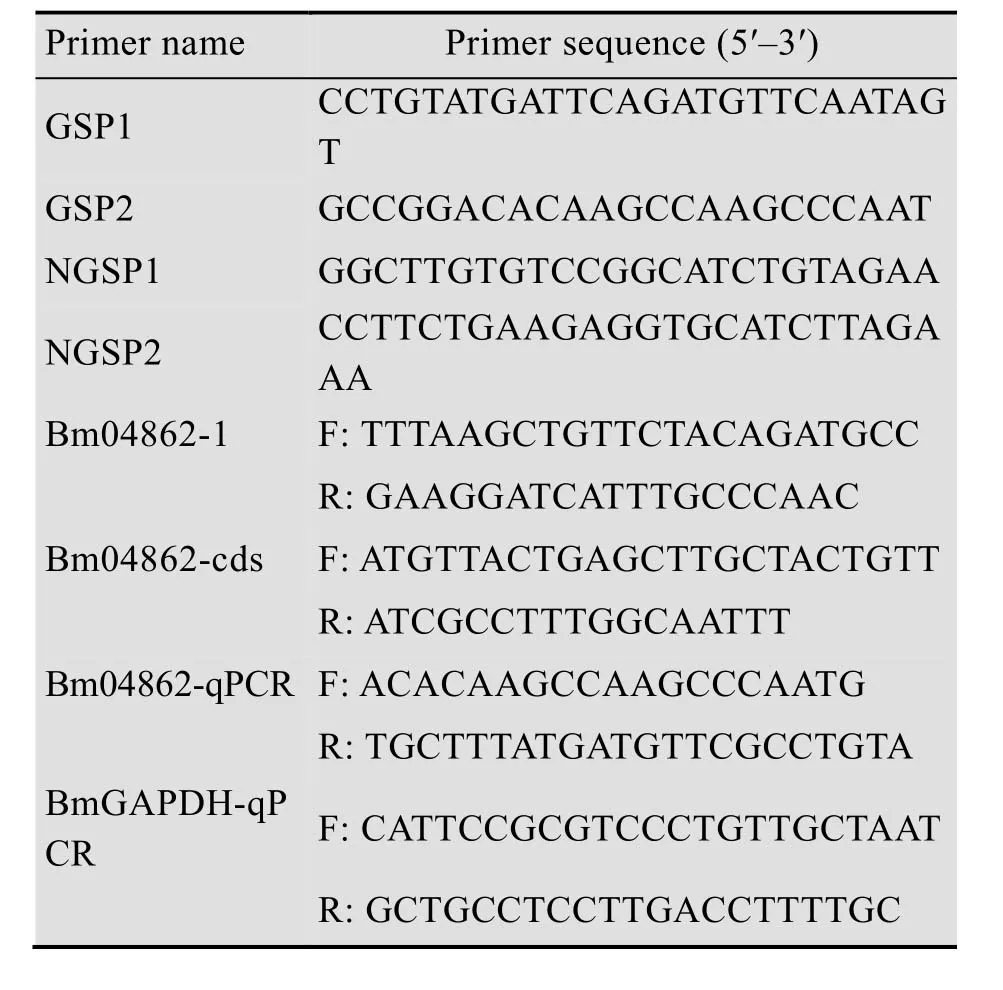
表1 PCR引物序列Table 1 PCR primer sequences
1.6Bm04862时空表达分析
基于家蚕EST数据库,设计Bm04862的特异引物Bm04862-1,选择家蚕持家基因BmGAPDH为内参基因,引物序列见表1。分别以5龄3 d幼虫各组织器官及家蚕不同发育时期血液cDNA为模板,进行qRT-PCR。反应条件为:95 ℃变性30 s;95 ℃ 3 s,60 ℃ 30 s,共40个循环,制备融解曲线,利用2-DD Ct进行计算[15]。
1.7Bm04862的亚细胞定位
通过PCR扩增得到 Bm04862全长ORF序列片段,将该片段限制性内切酶BamHⅠ酶切链接到pSL1180-A4-dsred-SV40载体上,挑选阳性克隆送至北京华大基因公司进行测序。阳性质粒命名为pSL1180-A4-Bm04862-dsred-SV40。27 ℃条件下,用含10%胎牛血清的Grace昆虫细胞培养基培养Sf9细胞,转染前将细胞接种于24 孔板 (1×105),当细胞生长状态良好,达到80%密度时进行质粒转染,转染按照转染操作说明进行,6 h后,换成完全Grace培养基,转染72 h后,用4%多聚甲醛固定15 min,再用DAPI进行细胞核染色10 min,最后在Olympus FV1000共聚焦荧光显微镜下观察。
1.8Bm04862微生物诱导分析
大肠杆菌DH5α于LB培养基中37 ℃,300 r/min 培养12 h后,在4 ℃以1 000 ×g离心15 min收集菌体,用PBS清洗2 次,最后用PBS配制大肠杆菌悬液备用。用毛细管对人工饲养5 龄3 d家蚕幼虫腹部第二对气孔注射10 μL已灭活的大肠杆菌 (1×106个/头)。对照组注射10 μL PBS。分别收集实验组和对照组注射后3、6、12、24、36和48 h的家蚕血液,于4 ℃、3 000×g离心5 min收集血细胞,提取RNA并反转录为cDNA,以大肠杆菌诱导后家蚕血细胞的cDNA为模板,PBS处理为对照,以Bm04862为定量引物,BmGAPDH为内参基因进行qRT-PCR反应,程序如上所述。
2 结果
2.1Bm04862克隆
根据家蚕组织芯片数据,分析目前已知家蚕基因在5龄3 d各个组织的表达情况,筛选出血液特异表达基因Bm04862,设计Bm04862基因特异性引物,以家蚕血细胞cDNA为模板进行PCR扩增,扩增产物用1%琼脂糖凝胶电泳,得到600 bp左右的条带。进一步利用RACE技术对Bm04862的5′端和3′端cDNA进行扩增,得到Bm04862基因cDNA,全长为936 bp。该全长包括23 bp的5′非编码区,94 bp 3′非编码区,以及819 bp开放阅读框,共编码272个氨基酸残基 (图2),蛋白分子量为30 kDa,等电点为7.87 (图1B)。该基因位于家蚕22号染色体上,基因全长20 796 bp,分别含有8个外显子,7个内含子 (图1C)。
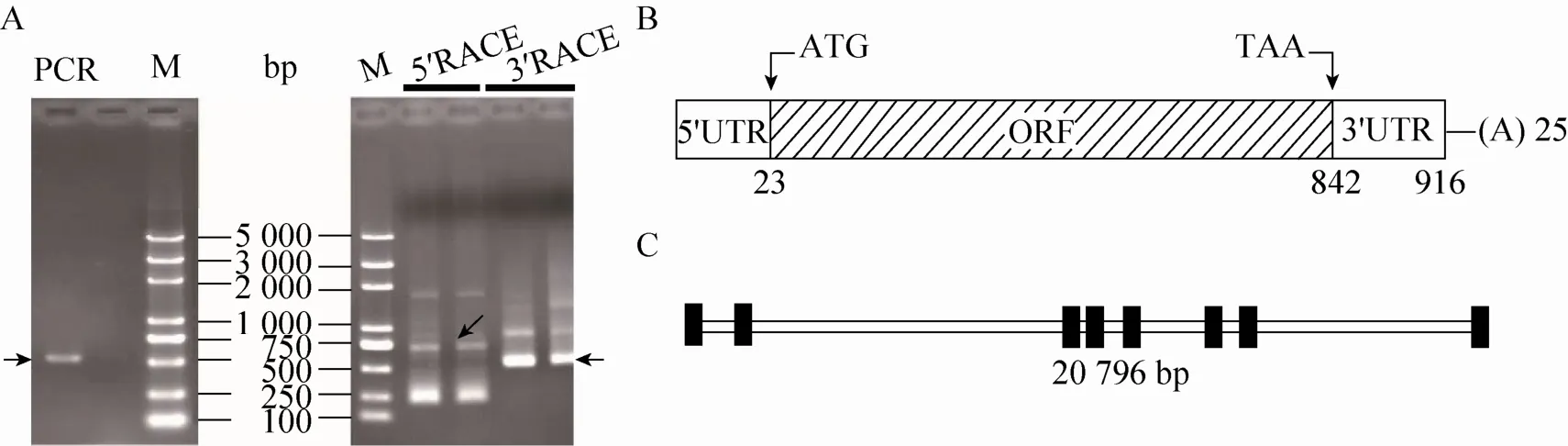
图1 家蚕Bm04862基因的克隆及分析Fig. 1 Cloning and analysis of Bm04862. (A) Agar gel analysis of the Bm04862 PCR product. M: DNA marker; PCR: the conservative sequence cloning; 5′RACE: fragment of 5′RACE; 3′RACE: fragment of 3′RACE. (B) The diagram of the Bm04862 complete cDNA sequence. (C) The diagram of the Bm04862 complete genomic sequence. : extron; : intron.

图2 家蚕Bm04862的全长cDNA序列及推导的氨基酸序列Fig. 2 The full length cDNA sequence of Bm04862 gene and its deduced amino acid.
2.2Bm04862蛋白结构分析
对Bm04862信号肽进行预测 (http://www. cbs.dtu.dk/services/SignaIP/),发现在1−17氨基酸区域为一个信号肽区域 (图3B)。利用蛋白保守结构域预测网址 (http://smart.embl-heidelberg.de/)在线分析Bm04862蛋白的保守结构域,发现2−16氨基酸、61−73氨基酸两个区域存着低密度保守区域,238−260氨基酸区域存在典型跨膜结构域 (图3A)。对跨膜结构域 (http:// www.ch.embnet.org/software/TMHMM_form.htm l) 等进行预测,发现该蛋白有1个跨膜螺旋区域 (图3C)。利用GORIV对蛋白二级结构进行预测,发现该蛋白主要有3种二级结构:56.25%无规卷曲 (Random coil)、23.9% α螺旋结构(α-Helix) 以及19.85%延伸主链 (Extended strand) 组成。在家蚕基因组数据库以及NCBI中BLASTp比对未发现相似性较高的同源蛋白,这一结果暗示该蛋白为一个未报道过的新蛋白。
2.3时空表达分析
家蚕基因组数据库前期芯片数据表明Bm04862为一个血细胞特异表达基因。利用qRT-PCR对该基因时空表达模式进行分析,结果表明在5龄3 d幼虫的不同组织中,Bm04862基因在血细胞中显著高表达,而在头部、精巢、卵巢、中肠、马氏管、体壁、丝腺、脂肪体中均无明显表达;4龄3 d幼虫到预蛹2 d蚕体发育过程血细胞中,检测到Bm04862均有表达,且分别在幼虫4龄眠期和预蛹2 d表达量达到峰值。此结果表明Bm04862是一个血细胞特异表达基因,且可能在眠期和预蛹期的变态发育过程中发挥着重要的功能 (图4)。

图3 家蚕Bm04862蛋白结构预测与分析Fig. 3 Prediction and analysis of the Bm04862 protein. (A) The prediction of Bm04862 protein domain. (B) The prediction of the Bm04862 protein signal peptide. (C) The prediction of Bm04862 transmembrane helices protein.

图4 Bm04862组织与时期表达Fig. 4 Tissue and stage expression profile of Bm04862. (A) The expression of Bm04862 mRNA in the different tissues of the 3rd day of the 5th larvae. He: hemocytes; Ha: head; Te: testis; Ov: ovary; Mi: midgut; Ma: malpighian tubules; Ep: rpidermis; Si: silk gland; Fa: fat body. (B) The expression of Bm04862 mRNA in hemocytes from the molting period of the 4th larvae to the 1st day of spinning. L4D3: day 3 of the fourth instar larval; L4M: molting stage of the fourth instar larval; W: wandering stage; PP1: day 1 of prepup.
2.4Bm04862基因全长过表达载体构建以及亚细胞定位分析
蛋白在细胞中的定位情况往往可以反应蛋白的功能,为了对Bm04862的亚细胞定位情况进行研究。我们采用PCR技术克隆得到的Bm04862基因ORF片段,将其连接到pSL1180-A4-dsred-SV40载体的BamHⅠ限制性酶切位点上,得到pSL1180-A4-Bm04862-dsred-SV40全长过表达载体。Sf9是一种经典的昆虫细胞系模式,具有转染效率高等优势,因此本论文选用Sf9细胞进行细胞定位实验。利用细胞转染技术将其转染进入Sf9细胞72 h后,在共聚焦显微镜下观察其dsred融合蛋白的表达情况。结果显示空白对照组的dsred荧光信号在细胞质中表达 (图5B),而实验组dsred信号在整个细胞核膜表达以及在局部细胞质中表达(图5A)。

图5 Bm04862蛋白在细胞系中的亚细胞表达定位Fig. 5 The subcellular localization of Bm04862 in embryonic cell line. (A) The cells transfected with pSL1180-A4-Bm04862-dsred-SV40 plasmid. (B) The cells transfected with pSL1180-A4-dsred-SV40 empty plasmid.
2.5微生物诱导分析
昆虫血细胞在昆虫代谢、发育变态以及先天免疫方面承担着重要的作用,Bm04862在血细胞中高表达,为研究Bm04862是否在免疫过程中发挥作用,我们用大肠杆菌Escherichia coli对家蚕5龄2 d幼虫进行了微生物诱导实验。在大肠杆菌分别诱导3、6、12、24、36和48 h后,利用qRT-PCR检测了Bm04862基因在血细胞中表达量变化情况 (图6),结果显示Bm04862基因在大肠杆菌刺激3−24 h表达量缓慢上调,其中刺激24 h后表达量上升显著,为对照组的2倍,之后恢复到正常表达水平。此结果表明大肠杆菌可以诱导Bm04862的表达,表明Bm04862基因可能参与到了家蚕抵御外源微生物侵袭的免疫反应过程,且在此过程中扮演着重要的角色。

图6 微生物诱导后Bm04862的表达量分析Fig. 6 Expression analysis of Bm04862 after induced by microbes. *P<0.05 vs control PBS, **P<0.01 vs control PBS, Student’s t-test. n=3.
3 讨论
昆虫基因在不同时间和空间的表达差异决定着生物体的发育、分化、细胞周期调控、衰老、程序性死亡等生理代谢过程[16]。越来越多的研究表明昆虫造血系统的发育及功能都与脊椎动物的血液系统存在着相似之处[1,17-18]。家蚕作为昆虫模式生物,对其血液系统相关基因的研究工作,有利于新的血细胞的类型和谱系的分子标记鉴定以及分子遗传工具和分析方法的改进,表达调控机理、免疫应答和应用研究具有重要的意义。本研究通过家蚕组织芯片数据库,获得了血细胞特异表达的Bm04862基因,通过各组织表达谱分析证实,该基因为血细胞特异表达基因,但与其他物种的比对中未发现相似性较高的同源基因,暗示该基因为一个未报道过的基因。血细胞时期表达模式分析表明该基因在4龄眠期以及预蛹2 d时期表达量显著上调,而眠期是家蚕变态发育中较为特别的时期,在此期间,其内部进行着大量旧组织衰退、新组织生成的剧烈过程,且容易受到外界病原微生物的入侵,该基因的表达特征反映了Bm04862基因可能在此过程中扮演着重要的角色[19-21]。经过序列分析以及亚细胞定位发现Bm04862蛋白拥有一个信号肽结构,一个跨膜结构并在细胞核膜表达,推测该基因为核膜蛋白。核膜蛋白对染色质组织、基因调控、信号转导等方面起着非常重要的作用[22-24]。结合微生物诱导实验,推测该基因参与对抗外源微生物的免疫应答中,可能在关键的免疫反应信号通路中扮演着关键的角色。本文为对血细胞特异基因Bm04862进一步的功能研究提供了数据参考。
REFERENCES
[1] Strand MR. The insect cellular immune response. Insect Sci, 2008, 15(1): 1–14.
[2] Wang L, Kounatidis I, Ligoxygakis P. Drosophila as a model to study the role of blood cells in inflammation, innate immunity and cancer. Front Cell Infect Microbiol, 2013, 3(1): 113.
[3] Gold KS, Brückner K. Drosophila as a model for the two myeloid blood cell systems in vertebrates. Exp Hematol, 2014, 42(8): 717–727.
[4] Grigorian M, Hartenstein V. Hematopoiesis and hematopoietic organs in arthropods. Dev Genes Evol, 2013, 223(1): 103–115.
[5] Evans CJ, Hartenstein V, Banerjee U. Thicker than blood: conserved mechanisms in Drosophila and vertebrate hematopoiesis. Dev Cell, 2003, 5(5): 673–690.
[6] Browne N, Heelan M, Kavanagh K. An analysis of the structural and functional similarities of insect hemocytes and mammalian phagocytes. Virulence, 2013, 4(7): 597–603.
[7] Zhang K, Tan J, Xu M, et al. A novel granulocyte-specific α integrin is essential for cellular immunity in the silkworm, Bombyx mori. J Insect Physiol, 2014, 71(2): 61–67.
[8] Yamamura T, Takahashi S, Satoh T, et al. Regulatory mechanism of silkworm hemocyte adhesion to organs. Zoolog Sci, 2011, 28(6): 420–429.
[9] Honti V, Csordás G, Kurucz É, et al. The cell-mediated immunity of Drosophila melanogaster: hemocyte lineages, immune compartments, microanatomy and regulation. Dev Comp Immunol, 2014, 42(1): 47–56.
[10] Hori S, Kobayashi A, Natori S. A novel hemocyte-specific membrane protein of Sarcophaga (flesh fly). Eur J Biochem, 2000, 267(17): 5397–5403.
[11] Kurucz E, Zettervall CJ, Sinka R, et al. Hemese, a hemocyte-specific transmembrane protein, affects the cellular immune response in Drosophila. Proc Natl Acad Sci USA, 2003, 100(5): 2622–2627.
[12] Levin DM, Breuer LN, Zhuang S, et al. A hemocyte-specific integrin required for hemocytic encapsulation in the tobacco hornworm, Manduca sexta. Insect Biochem Mol Biol, 2005, 35(5): 369–380.
[13] Gajewski KM, Sorrentino RP, Lee JH, et al. Identification of a crystal cell-specific enhancer of the black cells prophenoloxidase gene in Drosophila. Genesis, 2007, 45(4): 200–207.
[14] Xia Q, Cheng D, Duan J, et al. Microarray-based gene expression profiles in multiple tissues of the domesticated silkworm, Bombyx mori. Genome Biol, 2007, 8(7): R162.
[15] Livak KJ, Schmittgen TD. Analysis of relative gene expression data using real-time quantitative PCR and the 2-DDCTmethod. Methods, 2001, 25(4): 402–408.
[16] Horng T, Oberdoerffer S, Rao A. Gene regulationand signal transduction in the immune system. Genome Biol, 2008, 9(7): 315.
[17] Tan J, Xu M, Zhang K, et al. Characterization of hemocytes proliferation in larval silkworm, Bombyx mori. J Insect Physiol, 2013, 59(6): 595–603.
[18] Evans CJ, Banerjee U. Transcriptional regulation of hematopoiesis in Drosophila. Blood Cells Mol Dis, 2003, 30(2): 223–228.
[19] Liu QN, Zhu BJ, Wang L, et al. Identification of immune response-related genes in the Chinese oak silkworm, Antheraea pernyi by suppression subtractive hybridization. J Invertebr Pathol, 2013, 114(3): 313–323.
[20] Estevez-Lao TY, Hillyer JF. Involvement of the Anopheles gambiae Nimrod gene family in mosquito immune responses. Insect Biochem Mol Biol, 2014, 44: 12–22.
[21] Nakahara Y, Kanamori Y, Kiuchi M, et al. In vitro studies of hematopoiesis in the silkworm: cell proliferation in and hemocyte discharge from the hematopoietic organ. J Insect Physiol, 2003, 49(10): 907–916.
[22] Marmaras VJ, Lampropoulou M. Regulators and signalling in insect haemocyte immunity. Cell Signal, 2009, 21(2): 186–195.
[23] Jiang X, Xia L, Chen D, et al. Otefin, a nuclear membrane protein, determines the fate of germline stem cells in Drosophila via interaction with Smad complexes. Dev Cell, 2008, 14(4): 494–506.
[24] Holmer L, Worman H. Inner nuclear membrane proteins: functions and targeting. Cell Mol Life Sci, 2001, 58(12): 1741–1747.
(本文责编 陈宏宇)
Identification and characterization of a novel hemocyte specific gene Bm04862 in silkworm, Bombyx mori
Shuang Yu, Jingjing Su, Man Xu, Kui Zhang, and Hongjuan Cui
Southwest University, State Key Laboratory of Silkworm Genome Biology, Chongqing 400716, China
Abstract:Bm04862 is a novel hemocyte-specific gene, which has been identified and cloned through the microarray data in silkworm, Bombyx mori. Initially, we successfully obtained the full-length cDNA sequence of Bm04862 via the rapid amplification of cDNA ends (RACE). The sequence consists of an open reading frame (ORF) with 819 bp, which could encode 273 amino acid residues. The bioinformatics analysis predicted that Bm04862 was a transmembrane protein.Furthermore, qRT-PCR analysis revealed that the expression of Bm04862 was specifically detected in hemocyte and reached a peak at L4M and PP2 stage. Bm04862 was overexpressed in Sf9 insect cells, and the cellular localization indicated that Bm04862 was specifically located in cytoplasm and nuclei membrane. Interestingly, the expression of Bm04862 increased dramatically after challenged with Escherichia coli for 24 hours, which predicted its potential role in the innate immune system. Overall, this study could provide the fundamental knowledge for further research.
Keywords:Bombyx mori, hemocyte-specific gene, Bm04862, expression feature, subcellular localization
Corresponding author:Hongjuan Cui. Tel: +86-23-68251713; E-mail: hcui@swu.edu.cn, Hongjuan.cui@gmail.com
