结核分枝杆菌Rv1242蛋白抗原表位的预测>*
2016-06-17白雪娟吴雪琼
侯 英,白雪娟,梁 艳,吴雪琼#
1)北京卫生职业学院医学技术系 北京 100053 2)中国人民解放军第309医院全军结核病研究所;全军结核病防治重点实验室;结核病诊疗新技术北京市重点实验室 北京 100091#通信作者,女,1963年7月生,博士,研究员,研究方向:新型疫苗、诊断技术和新药的研究,E-mail:wu-xueqiong@263.net
结核分枝杆菌Rv1242蛋白抗原表位的预测>*
侯英1,2),白雪娟2),梁艳2),吴雪琼2)#
1)北京卫生职业学院医学技术系 北京 1000532)中国人民解放军第309医院全军结核病研究所;全军结核病防治重点实验室;结核病诊疗新技术北京市重点实验室 北京 100091#通信作者,女,1963年7月生,博士,研究员,研究方向:新型疫苗、诊断技术和新药的研究,E-mail:wu-xueqiong@263.net
关键词抗原表位;Rv1242蛋白;二级结构;结核分枝杆菌
摘要目的:预测结核分枝杆菌Rv1242蛋白的抗原表位。方法:利用DNAStar软件包中Protean软件对Rv1242氨基酸序列进行分析,采用包括二级结构、亲水性、抗原性、表面可能性、柔韧性等多参数预测其二级结构及T细胞和B细胞抗原表位。结果:Rv1242蛋白具有丰富的二级结构和多处抗原指数较高的区段,有7个亲水性区域,含有B细胞抗原肽表位(可能在17-38、72-82、84-90、116-130、134-143位氨基酸残基或其附近),这些表位抗原性较好,都含有β转角和不规则卷曲结构,表面可能性和柔韧性都较大。该蛋白还含有T细胞抗原肽表位(可能在24-33、42-59、68-77、90-108位氨基酸残基或其附近)。结论:Rv1242蛋白可能是一个既有T细胞抗原表位、也有B细胞抗原表位的抗原,该研究为进一步研究该蛋白抗原表位及其应用奠定了基础。
目前,结核分枝杆菌感染后如何与宿主相互作用尚不十分清楚。结核分枝杆菌抗原能够刺激机体产生免疫应答,并能与免疫应答产物如抗体和致敏淋巴细胞在体外结合,激发免疫效应。宿主免疫细胞通过其表面受体识别的并不是整个蛋白质抗原分子,而是抗原肽分子中由特殊的化学基团组成的结构即抗原决定簇,又称为表位。蛋白抗原不仅含有B细胞、T细胞[Th细胞与CD8+细胞毒性T 淋巴细胞(cytotoxic T lymphocyte,CTL)]、NK细胞等与免疫识别、免疫应答密切相关的表位结构,也含有一些对于保护性免疫不利的表位结构。因此,抗原优势表位的筛选和鉴定对表位疫苗的研制具有重要意义。结核分枝杆菌蛋白抗原表位的免疫学特性成为当前研究的热点之一。结核分枝杆菌 rv1242基因(vapC33)全长432 bp,并非结核分枝杆菌 H37Rv体外生长所必需;编码一个含143个氨基酸的跨膜蛋白,等电点5.892 1,预测相对分子质量为15 873.1,在培养滤液中检测不到;其作用尚不十分清楚,可能是一种含PIN结构域的vapC33毒素,在宿主-病原体相互作用中发挥重要作用[1-2]。结核分枝杆菌Rv1242蛋白(简称Rv1242蛋白)是一个膜蛋白,而膜蛋白通常参与结核分枝杆菌重要的生物代谢、合成过程和诱导宿主的免疫应答。目前对该蛋白的研究报道很少,对其免疫学特性不是很清楚。因此,该研究首次釆用生物信息学软件DNAStar对Rv1242蛋白进行抗原表位预测,为今后进一步深入研究和应用尤其是疫苗和免疫诊断试剂的开发奠定理论基础。
1材料与方法
1.1材料抗原表位分析软件:使用DNAStar生物软件包对DNA和蛋白质进行分析,并用其中的Protean软件分析和预测蛋白的二级结构和抗原表位[3]。Rv1242蛋白氨基酸全序列见GenBank(http://www.tbdb.org/),NP编号215758.1(143个氨基酸残基)。
1.2Rv1242蛋白二级结构的预测Rv1242蛋白二级结构采用Gamier-Robson方法、Chou-Fasman方法和Coiled Coil方法预测。
1.3Rv1242蛋白抗原表位的预测使用Kyte-Doolittle方法、Hopp-Woods方法和Eisenberg方法预测Rv1242蛋白的疏水性和亲水性,Emini方法预测表面可能性;Karplus-Schulz方法预测蛋白质骨架区的柔韧性,AMPHI方法预测蛋白免疫优势辅助性T淋巴细胞抗原位点,Jameson-wolf方法预测蛋白潜在的抗原表位,Rothbard-Taylor方法预测含有特定基序(motif)的潜在T淋巴细胞抗原表位,Sette MHC Motifs预测短肽上与小鼠MHC Ⅱ d型蛋白质相互作用的抗原位点;最终对Rv1242蛋白的抗原表位给出综合评价。
2结果
2.1Rv1242蛋白二级结构预测结果见图1。对Rv1242蛋白二级结构的预测结果显示α螺旋结构形成在22-29、50-54、62-75、86-96、92-102、108-114、116-124、126-138、140-143位氨基酸残基,数量较多,不存在跨膜区的α螺旋结构;β折叠分布较均匀(位于1-17、34-60、68-72、79-84、88-91、103-117位氨基酸残基)。该蛋白在各β折叠单元之间于18-23、25-26、30-33、73、76-79、85-88、97-100、124-125、127、136-137、139-142存在较多的转角;在18-21、24、30-32、34、61、74-77、85、125、138-140位氨基酸残基存在无规则卷曲。
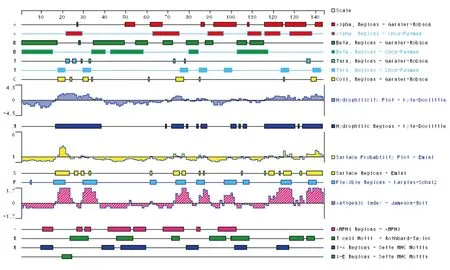
图1 Rv1242蛋白二级结构和抗原表位预测
2.2Rv1242蛋白的亲水性和疏水性预测结果显示:Rv1242蛋白存在7个亲水性区域(位于17-38、72-77、86、88、100-102、106-130、134-143位氨基酸残基)和7个疏水性区域(位于1-16、39-68、70-71、80-83、89、99、108-115位氨基酸残基)。
2.3Rv1242蛋白表面可能性和柔韧性预测Rv1242蛋白表面可能性较大的区域主要是在17-23、73-75、118-120、125-128、136-143位氨基酸残基,其他部位展示的可能性较小或表现为负值。
Rv1242蛋白含有较多的柔韧性区域(位于5、16-21、30-36、62-64、74-78、84-87、97-102、106-108、124-128、137-140位氨基酸残基),且均匀分布。
2.4Rv1242蛋白T细胞和B细胞抗原肽表位的预测综合二级结构、抗原性、亲水性、表面可能性和柔韧性分析结果,推测Rv1242蛋白潜在的B细胞抗原表位在17-38、72-82、84-90、116-130、134-143位氨基酸残基或其附近。
潜在的T细胞抗原表位在24-33、42-59、68-77、90-108位氨基酸残基或其附近,可能是免疫优势的辅助性 T 淋巴细胞抗原位点。10-15、20-24、39-44、48-59、79-84、102-107、122-127位氨基酸残基可能是与小鼠 MHC Ⅱ d 型蛋白质相互作用的抗原位点。
3讨论
结核分枝杆菌生长缓慢,天然蛋白抗原的获取较困难,通过基因工程技术获得重组蛋白抗原进行研究应用已成为一个简便、有效的途径。此外,近年来结核疫苗如重组蛋白疫苗、重组卡介苗、DNA疫苗的研发[4],有些已经进入临床试验,而生物信息技术的迅猛发展和互联网数据库的开发利用已为确定优势抗原表位提供了有效的方法。根据生物信息学软件的预测结果选择合成不同的多肽进行针对性的筛选、评价,可以显著降低候选肽段的数目,减少合成肽段的费用和体外实验鉴定的工作量,同时也缩短了时间,避免遗漏一些较长的表位。利用具有强大功能的生物信息学软件进行表位预测将为表位疫苗的发展、免疫诊断制剂的开发开辟新的路径[5]。
DNAStar软件包中Protean软件已被用于蛋白抗原表位的预测[6-7]。该研究应用Protean软件对Rv1242氨基酸序列进行分析,结果显示该蛋白同时含有B细胞抗原肽表位和T细胞抗原肽表位。B细胞表位绝大部分(约90%)是构象型表位[8],而DNAStar软件是在氨基酸一级结构的基础上应用多个参数预测B细胞抗原表位,如转角、折叠、卷曲、亲水性、抗原性、表面可能性、柔韧性等,忽略各氨基酸之间的分子作用力,因此,对构象型的B细胞表位的预测有一定局限性。可通过Western blot和ELISA分析其抗原抗体反应亲和力等实验鉴定细胞表位。
T细胞表位都是线性表位[8],但该研究预测的T细胞表位氨基酸残基42-59与McMurry等[9]鉴定细胞表位基本一致,而该研究预测到24-33、68-77、90-108这3段未得到证实,可能是因为DNAStar软件用于预测T细胞表位的参数较少,用生物信息学方法只能预测理论优势表位,不能完全反映机体免疫反应的真实情况,可以通过T 细胞增殖性实验、细胞杀伤实验、流式细胞术、ELISPOT技术等鉴定。鉴于抗结核免疫主要是细胞免疫,此次研究预测的T细胞表位可能在抗结核感染的保护性免疫应答中发挥重要和独特的作用。
总之,生物信息学分析显示Rv1242可能是一个既有T细胞抗原表位,也存在B细胞抗原表位的蛋白抗原。该研究结果为进一步深入研究该抗原可否成为疫苗组分之一或细胞免疫刺激原奠定了理论基础。
参考文献
[1]DE SOUZA GA, LEVERSEN NA, MALEN H.Bacterial proteins with cleaved or uncleaved signal peptides of the general secretory pathway[J].J Proteomics,2011,75(2):502
[2]HIWA MÅLEN,TINASØFTELAND,TINASØFTELAND,et al.Definition of novel cell envelope associated proteins in Triton X-114 extracts of Mycobacterium tuberculosis H37Rv[J].BMC Microbiol,2010,10:132
[3]朱育菁,刘波,郑伟文,等.基因序列蛋白质结构分析软件Protean使用技术[J].福建农业生物技术通讯,2004,6(4):8
[4]吴雪琼.新型结核病疫苗的研究现状与发展趋势[J].中国防痨杂志,2012,34(3):133
[5]李松,王英.生物信息学在生命科学研究中的应用[J].热带医学杂志,2009,9(10):1218
[6]黎明,于天飞.DNAStar软件在动物病毒研究中的应用实例[J].高师理科学刊,2010,30(3):61
[7]白雪娟,赵亚静,梁艳,等.结核潜伏感染蛋白Rv1737c B细胞、CTL及Th表位预测与分析[J].实用临床医药杂志,2015,19(3):5
[8]李海侠,毛旭虎.蛋白质抗原表位研究进展[J].微生物学免疫学进展,2007,35(1):54
[9]MCMURRY J,SBAI H,GENNARO ML,et al.Analyzing Mycobacterium tuberculosis proteomes for candidate vaccine epitopes[J].Tuberculosis(Edinb),2005,85(1/2):95
(2015-08-19收稿责任编辑徐春燕)
Prediction of epitopes ofMycobacteriumtuberculosisRv1242 protein
HOUYing1,2),BAIXuejuan2),LIANGYan2),WUXueqiong2)
1)DepartmentofMedicalTechnology,BeijingHealthVocationalCollege,Beijing1000532)InstituteforTuberculosisResearch,the309thHospitalofChinesePLA;ArmyTuberculosisPreventionandControlKeyLaboratory;BeijingKeyLaboratoryofNewTechniquesofTuberculosisDiagnosisandTreatment,Beijing100091
Key wordsepitope;Rv1242 protein;secondary structure;Mycobacterium tuberculosis
AbstractAim: To predict the epitopes of Mycobacterium tuberculosis Rv1242 protein. Methods: The amino acid sequence of Rv1242 protein was input and B cell and T cell epitopes were predicted using multi-parameters such as hydrophilicity,antigenicity,accessibility,flexibility,as well as the secondary structure by Protean software of DNAStar software package.Results: Rv1242 protein had rich secondary structure and multiple sections with higher antigenicity. There were 7 hydrophilic regions. There were potential B cell epitopes at 17-38,72-82,84-90,116-130,134-143 amino acid residues or nearby. These epitopes had better antigenicity, contained beta angle and irregular coil structure, and presented in the surface with larger probability and flexibility. There were also potential T cell epitopes at 24-33,42-59,68-77,90-108 amino acid residues or nearby. Conclusion: Mycobacterium tuberculosis Rv1242 is probably a protein antigen with both T and B cell epitopes, which will lay the foundation for its further study and application.
doi:10.13705/j.issn.1671-6825.2016.03.015
中图分类号R52
*国家重大传染病防治科技重大专项基金资助项目2012ZX10003008002;军队医学科技“十二·五”重点项目BWS11J050;北京市科技创新基地培育与发展工程专项Z141107004414021;北京高等学校青年英才计划项目YETP1999
