抗结核分枝杆菌DNA疫苗的构建及免疫原性研究①
2016-06-15饶桂荣张换敬石燕飞王洪敏杨富强陈光明
饶桂荣 张换敬 石燕飞 黄 彬 王洪敏 杨富强 陈光明
(解放军第四五八医院全军肝病中心,广州510600)
抗结核分枝杆菌DNA疫苗的构建及免疫原性研究①
饶桂荣张换敬石燕飞黄彬王洪敏杨富强陈光明
(解放军第四五八医院全军肝病中心,广州510600)
[摘要]目的:构建抗结核分枝杆菌(TB)DNA疫苗并进行体内外的鉴定。方法:采用PCR技术分别扩增TB (H37Rv) 抗原单基因Ag85a、Ag85b以及融合基因 Ag85a-Esat6和Ag85b-Esat6融合基因,其5′端均含人粒细胞-巨噬细胞集落刺激因子(GM-CSF)信号肽,将目的基因分别亚克隆于pVAX1真核表达载体,得到Ag85a/pVAX1、Ag85b/pVAX1、Ag85a-Esat6/pVAX1和Ag85b-Esat6/pVAX1四种质粒;经酶切和测序鉴定正确后,质粒转染COS-7细胞48 h,取上清液检测目的蛋白表达情况;利用在体电脉冲技术(EP)将质粒注射BALB/c小鼠双侧胫前肌,检测特异性的体液和细胞免疫应答。结果:四种质粒基因片段方向、序列正确;Western blot检测COS-7细胞转染48 h后的上清,均有清晰特异性的目的蛋白条带,并定量检测到Esat6蛋白的表达水平可达10 ng/ml;小鼠免疫实验结果表明,仅质粒Ag85b/pVAX1和Ag85a-Esat6/pVAX1可诱导针对结核抗原分泌高水平IFN-γ的Th1型免疫应答和特异性杀伤应答,其中通过ELISA检测小鼠血清的lgG和ELISPOT检测脾细胞分泌IFN-γ的实验结果阳性率均为100%,且Ag85a-Esat6/pVAX1的效果较好些,与卡介苗具有显著性差异。结论:成功构建了抗TB的DNA疫苗,其中Ag85a-Esat6/pVAX1质粒DNA疫苗的免疫效果较好,为进一步研发治疗性的TB DNA疫苗奠定基础。
[关键词]结核分枝杆菌; DNA疫苗;构建;转染;免疫
结核病是一种由结核分枝杆菌(Mycobacterium tuberculosis,TB)引起的严重危害人类健康的传染性疾病。卡介苗(Bacille calmette guerin,BCG)自1921年发现以来一直受到人们的关注,是目前唯一上市用于儿童期结核病的预防,但是,卡介苗的保护效率随时间的推移而逐渐降低,而且对于不同地区,不同人群,其保护率从0到80%不等。目前正在使用的卡介苗菌株都缺乏在致病结核杆菌和牛型结核分枝杆菌中存在的编码某些有保护性免疫效应的DNA片段,WHO已于1995年宣布BCG不是预防结核病的有效疫苗。20世纪40年代后相继出现多种抗结核药物(异烟肼、利福平等),但这些药物具有较多副作用,长期服用会导致TB菌株耐药突变,使药物治疗效果大大降低。据世界卫生组织(World Health Organization,WHO)2014年TB报告,全球每年大约有900万新增结核病患者,150万人死于结核病,其中36万人同时感染HIV;我国是仅次于印度的结核病第二大流行国家,年发病人数达120万[1]。
鉴于当前结核病流行的严重程度,以及不能有效预防和治疗结核病,国内外学者已经开始了结核分枝杆菌多种新一代疫苗的研究,主要为三种新型疫苗:重组rBCG、DNA疫苗及亚单位疫苗、灭活的分枝杆菌M.vaccae和RUT1。其中DNA疫苗由于制备简单,并且能诱导强烈的体液免疫和细胞免疫反应,尤其是它可诱导特异性CTL反应,使其在抗细胞内感染中独具优势,在治疗结核病方面应该更具有优势[2]。本文根据中国研究最多的三种抗原Ag85a、Ag85b和Esat6[3],构建了四种抗TB DNA疫苗Ag85a/pVAX1、Ag85b/pVAX1、Ag85a-Esat6/pVAX1和Ag85b-Esat6/pVAX1,分别进行体液免疫和细胞免疫检测实验,以期筛选出一种高效且特异性强的抗TB的DNA疫苗。
1材料与方法
1.1材料
1.1.1主要试剂限制性内切酶、pfu聚合酶和T4 DNA连接酶均购自大连宝生物公司;COS-7细胞株为本实验保存;pVAX1载体、Lipofecta mineTM2000 转染试剂购自Invitrogen公司; Mouse IFN-γ ELISPOT Kit购自BD公司;植物凝血素(PHA)、淋巴细胞分离液和牛血清蛋白(BSA)均购自Sigma公司;Ag85a和Ag85b抗原购自Prospec公司;二抗Goat polyclonal secondary antibody to mouse lgG(HRP), Goat Anti-Mouse IgG1 heavy chain(HRP),Goat Anti-Mouse IgG2a heavy chain(HRP)购自abcam公司;细菌基因组提取试剂盒购自天根公司;质粒中提试剂盒购自Qiagen公司;人结核分枝杆菌特异性蛋白ESAT6(MTB ESAT6)ELISA检测试剂盒购自上海卡奴公司;皮内注射用卡介苗(上海生物制品责任有限公司)由广州市疾病预防控制中心提供。
1.1.2菌株和实验动物结核分枝杆菌株H37Rv标准株由广州市胸科医院谭守勇教授惠赠,使用前已于121℃,5分钟高温灭活;大肠杆菌DH5ɑ由本室保存;BALB/c小鼠购自中山大学实验动物中心,雌性,6~8周龄,18~20 g,SPFⅢ级。
1.2方法
1.2.1质粒构建
1.2.1.1Ag85a/pVAX1和Ag85b/pVAX1单基因质粒构建为了增强目的基因的表达,在上游引物添加KOZAK系列(即ANNATGG,-3为A,+4为G),设计了Ag85a上游引物Ag85a-F1:5′-CGGGATCCAGGATGGGGCTGCAGAGCCTGCTGCTCTTG-GGCACTGTGGCCTGCAGCATCTCTCAGCTTGTTGAC-AGGG-TT-3′,下游引物Ag85a-R1:5′-GGTCTAGACTAGGCGCCCTGGGGCGC-3′; Ag85b上游引物Ag85b-F1:5′-CGGGATCCAGGATGGGGCTGCAGA-GCCTGCTGCTCTTGGGCACTGTGGCCTGCAGCATCT-CTACAGACGTGAGCCGAAAG-3′,下游引物Ag85b-R1:5′- GGTCTAGACTAGCCGGCGCCTAACGA-3′。上、下游引物5′端分别引入BamHⅠ和XbaⅠ酶切位点。上游引物还引入人粒细胞-巨噬细胞集落刺激因子(Ganulocyte-macrophage colony stimulating factor,GM-CSF)信号肽,以增强蛋白的分泌表达。引物由上海生工生物公司合成。以H37Rv菌株基因组为模板, PCR条件按95℃ 5 min,95℃ 50 s,55℃ 50 s,72℃ 60 s,30个循环,72℃ 5 min进行。凝胶电泳并回收PCR产物片段,以BamHⅠ和XbaⅠ进行双酶切,并和同样双酶切的pVAX1载体4℃过夜连接。按常规方法将连接产物转化感受态细胞DH5ɑ,挑取单菌落液体PCR扩增、酶切和测序鉴定。
1.2.1.2Ag85a-Esat6/pVAX1和Ag85b-Esat6/pVAX1融合基因质粒的构建设计PCR引物, Ag85a-F2:5′-CGGGATCCAGGATGGGGCTGCAGAG-3′, Ag85a-R2:5′-ACACGAACCCCCGCCTCCTGACCCGGCGCCCTGGGGCGC-3′;Ag85b-F2:5′-CGGG-ATCCAGGATGGGGGCTGCAG-3′,Ag85b-R2:5′-AC-ACGAACCCCCGCCTCCTGACCCGCCGGCGCCTAAC-GA-3′;Esat6-F1:5′-CGGGATCCAGGATGGCAGAGCAGCAGTGGAATTTC-3′,Esat6-R1:5′-GGTCTA-GACTACTGCAGCGCGTTGTTCAGC-3′。Esat6-F2:5′-GGGTCAGGAGGCGGGGGTTCGTGTATGACAGA-GCA-GCAGTGGAATTTC-3′,Esat6-R2:5′-GGTCTAGACTACTGCAGCGCGTTGTTCAGC-3′。其中斜体为Linker序列(G5S2C1),下划线为BamHⅠ和XbaⅠ酶切位点。首先使用Esat6-F1和Esat6-R1把Esat6单基因扩增出来,然后使用重叠引物PCR、酶切、连接等(方法同1.2.1.1)将单基因质粒Ag85a和Ag85b分别与Esat6连接,克隆到pVAX1载体,Ag85a-Esat6/pVAX1和Ag85b-Esat6/pVAX1融合基因质粒。
1.2.24种重组质粒的细胞转染和Western blot检测参照Invitrogen 公司脂质体转染试剂Lipofecta mineTM2000操作说明进行。COS-7细胞株按常规方法培养于含10%胎牛血清的RPMI1640培养基中,转染前24 h用胰酶消化贴壁细胞,重悬于含血清RPMI1640培养基,按3×105细胞/孔转种于6孔培养板中,待细胞生长至90%~95%融合度时,分别取4 μg纯化质粒Ag85a/pVAX1、Ag85b/pVAX1、Ag85a-Esat6/pVAX1和Ag85b-Esat6/pVAX1和10 μl转染试剂进行转染,同时设未转染细胞为空白对照。转染48 h后收集上清,对目的蛋白Ag85a或Ag85b进行Western blot检测,对目的蛋白Esat6进行ELISA检测。
1.2.3在体电脉冲(invivoelectroporation,EP)辅助质粒免疫健康BALB/c小鼠60只BALB/c小鼠随机分为6组,每组10只。第1组为生理盐水对照组,第2组为卡介苗(1×105CFU)阳性对照组,第3组为Ag85a组,第4组为Ag85b组,第5组为Ag85a-Esat6组,第6组为Ag85b-Esat6组,剂量均为20 μg/只。采用EP技术注射小鼠双侧胫前肌。初次免疫后第14天,以同样方法及剂量增强免疫各组小鼠1次,并于初次免疫后第28天,采用眼球后静脉丛穿刺法采血,ELISA测血清中抗-Ag85a或抗-Ag85b水平,再处死小鼠取脾脏淋巴细胞作ELISPOT检测。ELISPOT检测严格按BD公司试剂盒使用说明书方法操作。阳性判断标准:同一淋巴细胞密度(3×105个/孔)条件下,ELISPOT检测板中同一样品的抗原刺激与非抗原刺激的各3个复孔斑点均数(SFC)的差值应不小于5或比值应不小于2;TB DNA疫苗免疫组的细胞免疫应答阳性率应不低于60%。
1.3统计学结果处理用SPSS12.0软件进行统计分析,组间率比较用Fisher确切概率检验,P<0.05表示差异有统计学意义。
2结果
2.1TB DNA疫苗的构建PCR产物经琼脂糖凝胶电泳后可见明显目的条带,其中Ag85a、Ag85b、Esat6、Ag85a-Esat6和Ag85b-Esat6大小分别约为1 100、1 100、200、1 300和1 300 bp,结果见图1。与载体pVAX1连接所建的重组质粒经酶切和测序鉴定正确,结果见图2。
2.2重组质粒转染细胞与蛋白表达鉴定用Western blot方法检测目的蛋白Ag85(Ag85a或Ag85b)在COS-7细胞转染48 h后表达情况,结果表明,实验组均有清晰特异性的目的蛋白条带,无质粒转染空白组未检测到目的条带,说明质粒在细胞内成功表达并分泌到细胞外。见图3。用ELISA检测目的蛋白Esat6的定量表达,Ag85a-Esat6质粒转染组中转染上清的Esat6蛋白检测含量为(14.2±2.1)ng/ml,Ag85b-Esat6质粒转染组为(4.7±1.0)ng/ml,空白质粒组未检测出Esat6。结果见图4。

图1 PCR产物电泳图谱Fig.1 Electrophoretogram of PCR productionsNote: To each figure:Lane1.DL2000;Lane2.PCR product-ion.A.Ag85a;B.Ag85b;C.Esat6;D.Ag85a-Esat6;E.Ag85b-Esat6.To each figure:Lane 1.DL2000;Lane 2.PCR production.
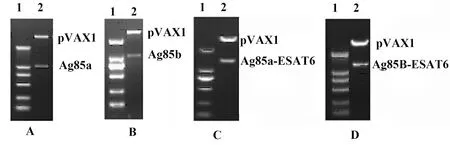
图2 重组质粒酶切图谱Fig.2 Restriction digestion maps of recombination plasmids Note: A.Ag85a;B.Ag85b;C.Ag85a-Esat6;D.Ag85b-Esat6.To each figure:Lane 1.DL2000;Lane 2.products digested by BamHⅠ and XbaⅠ including vector pVAX1 and target gene.
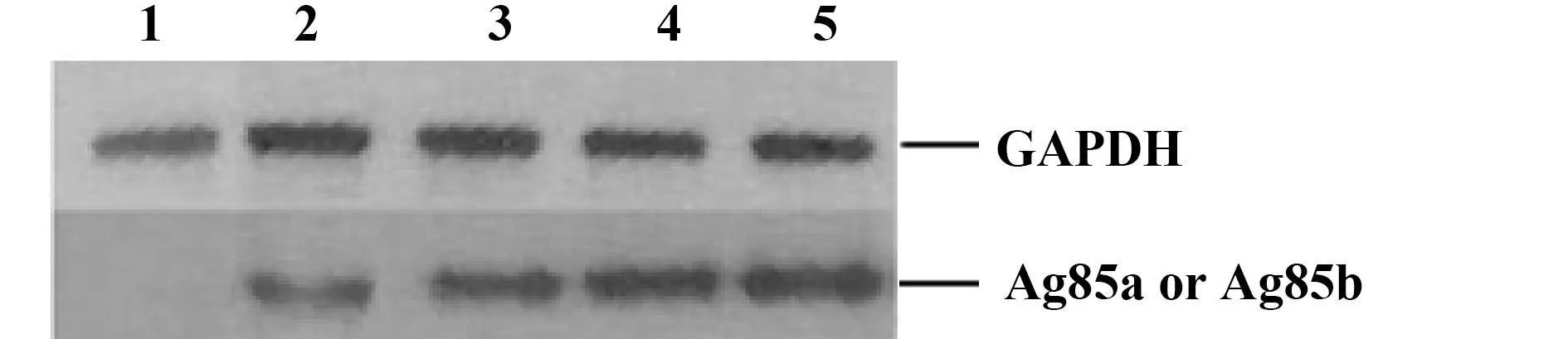
图3 转染COS-7细胞后上清的Western blot图谱Fig.3 Western blot map of supernatants of transfected COS-7Note: 1.Normal group;2.Ag85a;3.Ag85b;4.Ag85a-Esat6;5.Ag85b-Esat6.

图4 质粒Ag85a-Esat6和Ag85b-Esat6转染上清中Esat6的含量Fig.4 Concentration of Esat6 in supernatants of COS-7 transfected with Ag85a-Esat6 and Ag85b-Esat6
表1ELISA测定IgG抗体平均滴度GMT结果
Tab.1GMT of ELISA detecting antigen specific IgG
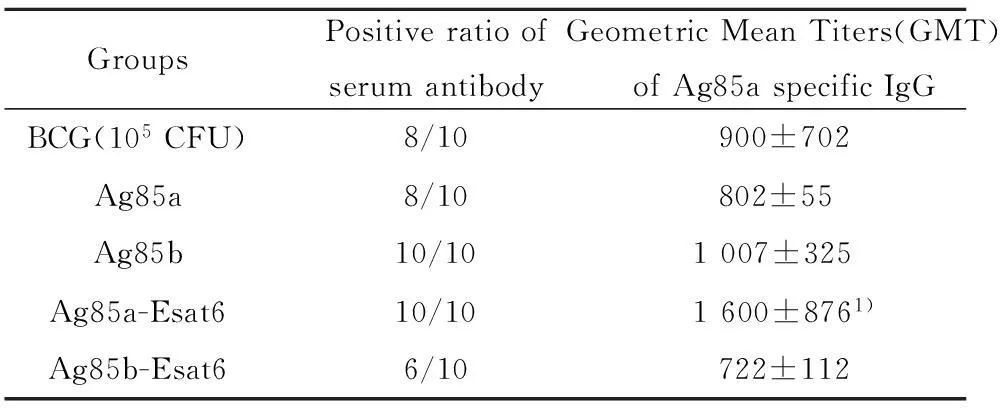
GroupsPositiveratioofserumantibodyGeometricMeanTiters(GMT)ofAg85aspecificIgGBCG(105CFU)8/10 900±702Ag85a8/10 802±55Ag85b10/101007±325Ag85a-Esat610/101600±8761)Ag85b-Esat66/10 722±112
Note:GMT of Saline group was less than 100;1)P<0.05.

图5 各组ELISPOT斑点计数结果Fig.5 SFC results of each group

图6 各组ELISPOT斑点直观图Fig.6 ELISPOT images of each groupNote: A.Negative;B.PHA;C.Saline;D.BCG;E.Ag85a;F.Ag85b;G.Ag85a-Esat6;H.Ag85b-Esat6.
表2Ag85a-Esat6/pVAX1产生的特异性抗体亚型分析
Tab.2Subtype analysis of Ag85a specific IgG induced by Ag85a-Esat6/pVAX1
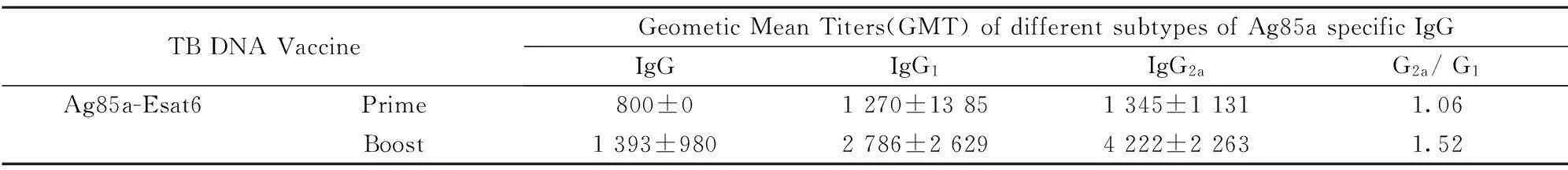
TBDNAVaccineGeometicMeanTiters(GMT)ofdifferentsubtypesofAg85aspecificIgGIgGIgG1IgG2aG2a/G1Ag85a-Esat6Prime800±01270±13851345±11311.06Boost1393±9802786±26294222±22631.52
表3ELISPOT检测结果
Tab.3Results of ELISOPT

GroupsSpotsofstimulatedholesminusnon-stimulatedholesPositiveratioBCG(105CFU)95.1±12.86/10Ag85a80.2±29.68/10Ag85b218.9±14.210/10Ag85a-Esat6302.9±19.51)10/10Ag85b-Esat618.8±6.72/10
Note:Saline groups spots of stimulated holes minus non-stimulated holes 0,positive ratio was 0,1)P<0.05.
2.3ELISA法测定小鼠血清特异性抗-Ag85a或抗-Ag85b的抗体水平加强免疫小鼠2周后用ELISA方法检测动物血清抗-Ag85蛋白含量,由表1可知Ag85a、Ag85b、Ag85a-Esat6和Ag85b-Esat6组产生的抗体阳性率分别为80%、100%、100%、60%,BCG组阳性率80%;动物血清特异性抗Ag85a的IgG抗体平均滴度GMT分别为802±55、1 007±325、1 600±876、722±112,与卡介苗组(900±702)比较具有显著性差异(P<0.05)。进一步分析Ag85a-Esat6组产生的特异性抗体亚型,其IgG2a/IgG1>1,并于加强免疫后,IgG2a/IgG1值升高,表明主要诱导Th1型免疫应答并得到加强,结果见表2。
2.4ELISPOT法测定小鼠脾淋巴细胞分泌IFN-γ的活性Ag85a/pVAX1、Ag85b/pVAX1、Ag85a-Esat6/pVAX1和Ag85b-Esat6/pVAX1这4组质粒DNA免疫注射小鼠后,脾细胞中特异性分泌IFN-γ的阳性细胞数见表3,分别为80%、100%、100%和20%,斑点计数和直观图分别见图5、6;可以看出,Ag85b/pVAX1和Ag85a-Esat6/pVAX1两组的免疫效果较好,表明这两种质粒诱导出的特异性的细胞免疫应答反应效果较佳,其中以Ag85a-Esat6/pVAX1组的斑点数较多,免疫效果最好,且与卡介苗组比较具有显著性差异(P<0.05),
3讨论
当前结核病流行程度较为严重,再加上与HIV共感染以及未有一种有效的预防和治疗措施,使结核病的防治工作迫在眉睫。英国Lowrie等[4,5]首次将DNA疫苗用于结核病的治疗,开拓了TB DNA疫苗的研究工作,其实验结果发现IL-12和HSP65 DNA疫苗可有效增加小鼠对结核杆菌的清除率,说明HSP65 DNA疫苗通过激活Th1 型的细胞免疫反应发挥作用,随后该研究小组还对TB感染的小鼠进行药物治疗后建立了潜伏感染模型,发现HSP65 DNA疫苗和药物联合使用,对感染小鼠具有很好治疗效果;Huygen等[6]报道了用结核分支杆菌Ag85编码基因的质粒DNA免疫小鼠,可诱导小鼠产生很强的细胞和体液免疫反应,抵御活结核分支杆菌和BCG的攻击。Lozes等[7]证明了Ag85a质粒DNA免疫的BALB/c和C57BL/6小鼠的脾细胞培养上清液中,IL-2、IFN-γ和TNF-α水平显著高于BCG免疫鼠,Ag85b DNA能产生与Ag85a类似的效果,而Ag85c DNA质粒对小鼠无保护作用;韩国科学家Ha等[8]将Ag85a和IL-12N220L DNA疫苗结合药物异烟肼和吡嗪酰胺治疗C57BL/6J小鼠结核病模型,Ag85a DNA疫苗和药物联合治疗组优于单纯药物组。我国科学家对抗结核病DNA疫苗也做了较多深入研究。北京309医院吴雪琼等[9,10]首先进行Ag85a DNA疫苗的研究。随后与李忠明等联合研究一种嵌合型DNA疫苗,即将两种结核杆菌的抗原蛋白基因嵌合在同一个载体上,该实验室的梁艳等先后验证了Ag85a、Ag85a/ Esat、Ag85a/B嵌合质粒DNA疫苗对耐药结核杆菌的治疗作用,实验结果表明,DNA疫苗和药物联合使用能够显著提高药物对耐药结核杆菌的治疗效果[11,12]。综上所述,目前研究已有多种结核DNA疫苗可诱导小鼠产生有效的免疫保护,但仍没有一种治疗性DNA疫苗在临床的验证。
与上述国内外TB疫苗研究不同,本研究构建的TB DNA疫苗特点包括:①根据2012年Lowrie[3]统计中国TB疫苗研究最多的抗原数据,优选Ag85a、Ag85b、Esat6为目的抗原基因。Ag85a和Ag85b是结核分枝杆菌和BCG的主要分泌性蛋白,也是结核杆菌重要的保护性抗原,能刺激细胞免疫反应,又能诱导体液免疫反应,二者均有特异性T细胞识别位点,可刺激记忆T细胞的产生,可诱导细胞因子分泌水平提高和产生CTL活性[13]。Esat6,又称Rv3875,在减毒株中没有这种抗原成分,它是重要的T细胞抗原,含有多个T细胞表位,在抗Mtb的保护性免疫应答中起重要作用,是免疫记忆应答中的主要靶抗原之一[14];②本文构建4种质粒中,Ag85a-Esat6/pVAX1诱导的细胞和体液免疫最强。该质粒为一种融合型 TB DNA疫苗,并在基因的5′端引入GM-CSF信号肽,可以提高蛋白的分泌,增强免疫效果;③载体采用美国FDA批准的唯一用于临床试验的DNA疫苗载体pVAX1作为DNA疫苗载体,不含SV40病毒复制基因,不含AMP抗性基因,仅有Kana抗性基因,较其他含有多个细菌基因组元件的载体如pcDNA3.1、pJW4303、pCI-neo等较安全;④采用肌注联合EP电转染技术导入质粒,其作用机制是使细胞膜双层磷脂结构在电场的作用下发生改变,形成瞬间可逆的微孔,使得外源大分子得以进入细胞,较大提高质粒的转染率,并且具有简单实用,易于推广等优点,有可能成为基因导入方法中的一项主导性技术。
本文实验结果提示,Ag85a和Esat6蛋白具有协同促进的作用,Ag85a-Esat6/pVAX1质粒体液和细胞免疫反应最强,为临床治疗结核病DNA疫苗的研究提供重要参考。但本研究也发现Ag85b-Esat6/pVAX1效果并不如卡介苗和Ag85b/pVAX1,可能是因为Ag85b和Esat6两种蛋白融合后空间构象有所改变而没有协同促进作用。关于Ag85a-Esat6/pVAX1对TB感染动物模型治疗和预防作用的实验研究目前正在进行中。
参考文献:
[1]Zumla A,George A,Sharma V,etal.The WHO 2014 global tuberculosis report--further to go[J].Lancet Glob Health,2015,3(1):10-12.
[2]Liu MA.DNA vaccines:an historical perspective and view to the future[J].Immunol Rev,2011,239(1):62-84.
[3]Lowrie DB.Tuberculosis vaccine research in China[J].Emerg Microbes Infect,2012,1(7):7.
[4]Silva CL,Lowrie DB.A single mycobacterial protein (hsp 65) expressed by a transgenic antigen-presenting cell vaccinates mice against tuberculosis[J].Immunol,1994,82(2):244-248.
[5]Lowrie DB,Silva CL,Colston MJ,etal.Protection against tuberculosis by a plasmid DNA vaccine[J].Vaccine,1997,15(8):834-838.
[6]Huygen K,Content J,Denis O,etal.Immunogenicity and protective efficacy of a tuberculosis DNA vaccine[J].Nat Med,1996,2(8):893-898.
[7]Lozes E,Huygen K,Content J,etal.Immunogenicity and efficacy of a tuberculosis DNA vaccine encoding the components of the secreted antigen 85 complex[J].Vaccine,1997,15(8):830-833.
[8]Ha SJ,Jeon BY,Kim SC,etal.Therapeutic effect of DNA vaccines combined with chemotherapy in a latent infection model after aerosol infection of mice with mycobacterium tuberculosis[J].Gene Ther,2003,10(18):1592-1599.
[9]吴雪琼,张俊仙,李洪敏,等.结核分支杆菌Ag85A DNA疫苗免疫治疗作用的研究[J].中国免疫学杂志,2002,18(1):17-19.
[10]梁艳,吴雪琼,张俊仙,等.结核分支杆菌Ag85A质粒DNA疫苗和抗结核药物联合治疗小鼠耐药结核病[J].广东医学,2007,28(9):1398-1400.
[11]梁艳,吴雪琼,张俊仙,等.结核分枝杆菌Ag85A/ESAT-6嵌合型质粒DNA疫苗和抗结核药物联合治疗小鼠耐药结核病的效果研究[J].中国防痨杂志,2007,29(5):382-385.
[12]梁艳,吴雪琼,李忠明,等.Ag85A/B嵌合DNA疫苗治疗小鼠敏感结核病疗效的实验研究[J].中国防痨杂志,2010,32(10):639-642.
[13]Malin A S,Huygen K,Content J,etal.Vaccinia expression of mycobacterium tuberculosis-secreted proteins:tissue plas minogen activator signal sequence enhances expression and immunogenicity of M.tuberculosis Ag85[J].Microbes Infect,2000,2(14):1677-1685.
[14]Lu J,Wang C,Zhou Z,etal.Immunogenicity and protective efficacy against murine tuberculosis of a prime-boost regimen with BCG and a DNA vaccine expressing ESAT-6 and Ag85A fusion protein[J].Clin Dev Immunol,2011,2:1-10.
[收稿2015-09-20修回2015-12-25]
(编辑许四平)
Construction and immunogenicity research on a therapeutic DNA vaccine of Mycobacterium Tuberculosis
RAOGui-Rong,ZHANGHuan-Jing,SHIYan-Fei,HUANGBin,YANGFu-Qiang,WANGHong-Min,CHENGuang-Ming.
InfectiousDiseaseCenter,the458thHospitalofPLA,Guangzhou510600,China
[Abstract]Objective:To develop effective therapeutic Mycobacterium Tuberculosis(TB) DNA vaccines and research their immune activity in vitro and in vivo.Methods: TB (H37Rv) antigen genes Ag85a,Ag85b,Ag85a-Esat6 and Ag85b-Esat6 fusion gene,whose 5′ terminal have gene encoding human granulocyte colony stimulating factor(GM-CSF),were amplified by PCR.Then these genes were subcloned into eukaryotic vector pVAX1,which were respectively named Ag85a/pVAX1,Ag85b/pVAX1,Ag85a-Esat6/pVAX1 and Ag85b-Esat6/pVAX1.The new plasmids were analyzed by restriction digestion and DNA sequencing.The plasmids were transfected into COS-7 cells in vitro with Lipofecta mineTM2000.At 48 h after trasfection,the supernatants were analysised by Western Blot and Elisa.The plasmids were injected into BALB/c mice by electroporation in situ and specific humoral and cellular immune responses were exa mined.Results: The four plasmids were constructed correctly by genetic analysis.At 48 h after transfection,Ag85a,Ag85b,Ag85a-Esat6 and Ag85b-Esat6 genes expressed respectively,and objestive proteins were detected by Western blot clearly specially.It was up to 10 ng/ml in supernatants detected by ELISA of Esat6.Experiment performed in BALB/c mice injected with only plasmids Ag85a-Esat6/pVAX1 or Ag85b/pVAX1 showed,protective antibodies of Ag85a or Ag85b were produced,and Ag85a or Ag85b specific killing response and Th1-type immune response with high level of IFN-γ were also induced.Positive ratios were both 100% in ELISA detecting anti-Ag85a or anti-Ag85b IgG and ELISPOT detecting specific spleenocytes secreting IFN-γ.The plasmid Ag85a-Esat6/pVAX1 had better immune efficacy than Ag85b/pVAX1 and significant deference from BCG.Conclusion: The TB DNA vaccines were constructed successfully,and Ag85a-Esat6/pVAX1 induced the most strong specific immune activity in vitro and in vivo.
[Key words]Mycobacterium Tuberculosis;DNA vaccine;Construction;Transfection;Immunity
doi:10.3969/j.issn.1000-484X.2016.05.018
作者简介:饶桂荣(1974年-),女,硕士,副主任药师,主要从事免疫治疗机理研究和及生物新药研发工作,E-mail:raogr@126.com。指导教师:杨富强(1965年-),男,博士,主任医师,主要从事免疫治疗机理研究和肿瘤生物治疗研究,E-mail:yangfq23@163.com。
中图分类号R392.33
文献标志码A
文章编号1000-484X(2016)05-0682-06
①本文为广东省科技计划项目(No.2015A010107011)。