花生AhFUSCA3基因的原核表达及在非生物胁迫下的表达分析
2016-06-05潘丽娟刘风珍万勇善迟晓元陈明娜禹山林
潘丽娟,梁 丹,刘风珍,万勇善,迟晓元,陈 娜,陈明娜,王 通,王 冕,杨 珍,禹山林*
(1.山东省花生研究所,山东 青岛 266100;2.作物生物学国家重点实验室/山东农业大学农学院,山东 泰安 271018)
花生AhFUSCA3基因的原核表达及在非生物胁迫下的表达分析
潘丽娟1,2,梁 丹1,刘风珍2,万勇善2,迟晓元1,陈 娜1,陈明娜1,王 通1,王 冕1,杨 珍1,禹山林1*
(1.山东省花生研究所,山东 青岛 266100;2.作物生物学国家重点实验室/山东农业大学农学院,山东 泰安 271018)
根据本实验室已获得的花生AhFUSCA3基因(NCBI登录号JX420284)序列,设计特异引物,构建原核表达载体,进行了重组蛋白表达分析,获得了分子量为42 KD左右的目的蛋白条带;利用荧光定量PCR(Quantitative Real-time RT-PCR)方法,检测了AhFUSCA3基因在低温、高盐和干旱胁迫条件下的表达情况。结果显示,AhFUSCA3基因在低温和高盐处理的花生叶片中表达量明显上调,但在干旱处理的叶片中表达量则有明显下降。以上结果表明AhFUSCA3基因可能参与了花生对低温、高盐和干旱的抗性调控。
花生;AhFUSCA3基因;原核表达;非生物胁迫;荧光定量PCR
干旱、盐碱、低温等非生物逆境是影响植物生长发育的主要因素,植物受到逆境胁迫时会产生形态、生理、基因表达等适应性调节反应以降低或消除危害[1-2]。转录因子(反式作用因子)基因是植物中最重要的一类调节基因,其在植物体内构成复杂的调节网络,在时间和空间上协同控制基因的表达。转录因子是能够与真核基因启动子区域中顺式作用元件发生特异性作用的DNA 结合蛋白,通过它们之间以及与其他相关蛋白之间的相互作用,激活或抑制基因转录。FUSCA3(FUS3)编码一个含有B3结构域的转录因子[3]。实验证明 FUS3 蛋白通过 B3 结构域直接结合到靶基因的 RY 基序上[4]。FUSCA3(FUS3)是在拟南芥中筛选突变体时首次被鉴定的[5],fus3突变体比野生型植株表现出花青素的过度累积和干旱耐受性减弱等特征,积累了更少的种子储藏蛋白[3,6]。
花生是重要的油料作物,不利的生长环境对其产量有很大影响。然而花生中有关非生物胁迫调控的分子生物学研究较少,处于刚刚起步的阶段。目前一些基因已经被证明可能参与了花生非生物胁迫的调控并得到了克隆[7-11]。Wan和Wang等通过将花生基因转化拟南芥证明花生中泛素连接酶和Germin-like家族蛋白可能参与了拟南芥对干旱或高盐胁迫的调控[12-13]。 除了以上报导,花生非生物胁迫的分子机理研究未见更深入的报导,花生抗逆基因的挖掘还有许多工作要做。本实验室前期从花生中分离克隆了FUSCA3全长基因,并对其进行了基本的生物信息学分析和表达特性研究[14]。本研究在前期试验基础上,进一步分析了FUSCA3基因在原核生物中的表达情况,以及通过荧光定量PCR分析发现,花生FUSCA3基因对低温、高盐和干旱胁迫均有响应,表明该基因可能参与了花生对以上胁迫的抗性调节。本研究为花生抗性分子调控研究提供了新的基因资源。
1 材料与方法
1.1 试 剂
载体pET-28b购自Novagen,T4DNA连接酶购自宝生物工程(大连)有限公司,总RNA提取试剂盒和E.coliBL21感受态购自天根生化科技有限公司,M-MLV反转录酶购自Promega,荧光定量PCR用SYBR Green PreMix 试剂盒购自台湾生工。
1.2 植物材料
本研究所用花生材料为花育33,花生种子在营养土与蛭石(2∶1)的混合土中萌发,之后在16h光照/8h黑暗(28°C/22°C)的光照培养箱中生长,待花生幼苗生长到三叶期后进行低温、高盐和干旱胁迫处理实验。
低温处理时,将生长于土中的花生幼苗置于光照培养箱中,温度设定为4°C。用NaCl和 PEG6000进行处理时,将花生幼苗从土中拔出,将根部土冲洗干净后直接浸泡到200mmol/L NaCl或20% PEG6000溶液中。所有处理均在处理的0h,4h,8h,12h,24h和72h分别取叶片,液氮冷冻保存,作为后续实验材料。
1.3 RNA提取与cDNA合成
样品总RNA的提取用天根的RNeasy Mini Kit,详细方法参考其使用说明。合成cDNA前要将提取的RNA用DNaseI处理以去除DNA污染。用M-MLV反转录酶进行cDNA的合成,每25-μL反应体系中加入2μg RNA;反转录反应体系在42°C进行1h,之后置于冰上冷却5min。
1.4 原核表达载体的构建
根据已报道的AhFUSCA3基因(登录号JX420284)序列,设计特异性引物,5'端引物加了Nde I酶切位点:5'- CATATG ATGATGATGGATCAGGGACA-3',3'端引物加了XhoI酶切位点:5'- CTCGAG TTAGTAGAAGTCATCAAGTG-3'。
将获得的目的片段PCR 产物纯化后用NdeI和XhoI双酶切,在T4DNA连接酶作用下连接到以相同酶切后回收的pET-28b载体上,16℃连接过夜。将连接产物转入DH5α 感受态细胞,在卡那霉素抗性的 LB 平板上挑取重组质粒,通过PCR、双酶切筛选阳性克隆,并对阳性克隆测序验证。构建成功的表达质粒命名为pET-28b-AhFUSCA3,将测序正确的质粒转化BL21感受态细胞。
1.5 重组质粒在大肠杆菌中的诱导表达及SDS-PAGE分析
挑测序正确的单克隆接种到4mL LB(30μg/mL卡那霉素)培养基中,震荡培养(200r/min, 37℃)12h后,将菌液按1∶100加到100mL LB(30μg/mL卡那霉素)培养基中200r/min 37℃震荡培养至OD600为约0.6时,加入 IPTG(使终浓度为0.5 mmol/L)进行诱导表达,分别在诱导0h,2h,6h,10h,16h后收集菌液,4℃保存备用。未加IPTG诱导的pET-28b-AhFUSCA3收集作为阴性对照。诱导全部完成后,收集50 mL 菌液离心收集菌体后用1×PBS缓冲液悬浮,超声裂解细菌,10 000 r/min 离心10 min 分离上清与沉淀,上清和沉淀样品中分别加入SDS上样缓冲液,混匀,沸水浴,取上清和沉淀分别进行SDS-PAGE(5%浓缩胶,12%分离胶),然后分析蛋白表达结果。
1.6 荧光定量RT-PCR
进行荧光定量PCR时,先将cDNA样品稀释到8 ng/μL,每反应体系中加2μL稀释后的cDNA。荧光定量PCR仪采用Roche的LightCycler 2.0 instrument system。反应条件:(1)预变性:95℃,10s;(2)扩增:95℃,5s;60℃,30s;72℃,10s;40个循环;(3)绘制溶解曲线:温度每10s升高0.5℃。本实验所用的内参基因为β-actin,每个样品重复三次,采用delta-delta Cp方法分析数据。荧光定量所用引物如下:β-actin为5'-TTGGAAT GGGTCAGAAGGATGC-3'和5'-AGTGGTGCCTCAGTAAGAAGC-3';AhFUSCA3为5'-CTTCTTCCCTCTTCTGTCAC-3'和5'-CTAGCCATTCTCCTCTTCCT-3'。
2 结果与分析
2.1AhFUSCA3基因原核表达产物的检测
用带有酶切位点的引物进行PCR 扩增,得到AhFUSCA3基因的cDNA编码区序列。将目的片段回收纯化后,用NdeI和XhoI 酶切,连接到相同酶切回收后的原核表达载体pET-28b上,获得pET-28b-AhFUSCA3原核表达载体,转化大肠杆菌DH5α。将目的条带测序,序列比对结果正确,表明pET-28b-AhFUSCA3原核表达载体已构建成功。
重组质粒pET-28b-AhFUSCA3转化感受态细胞BL21后,用IPTG诱导重组蛋白的表达,分别在诱导0h,2h,6h,10h,16h后收集菌液,分别对上清和沉淀进行SDS-PAGE电泳检测。结果表明,在分子量35KD和45KD之间出现明显的特异性目的条带(图1),与AhFUSCA3蛋白分子量预测值42KD一致。目测目的蛋白大部分以包涵体形式存在,在诱导10h时表达量最高(图1)。
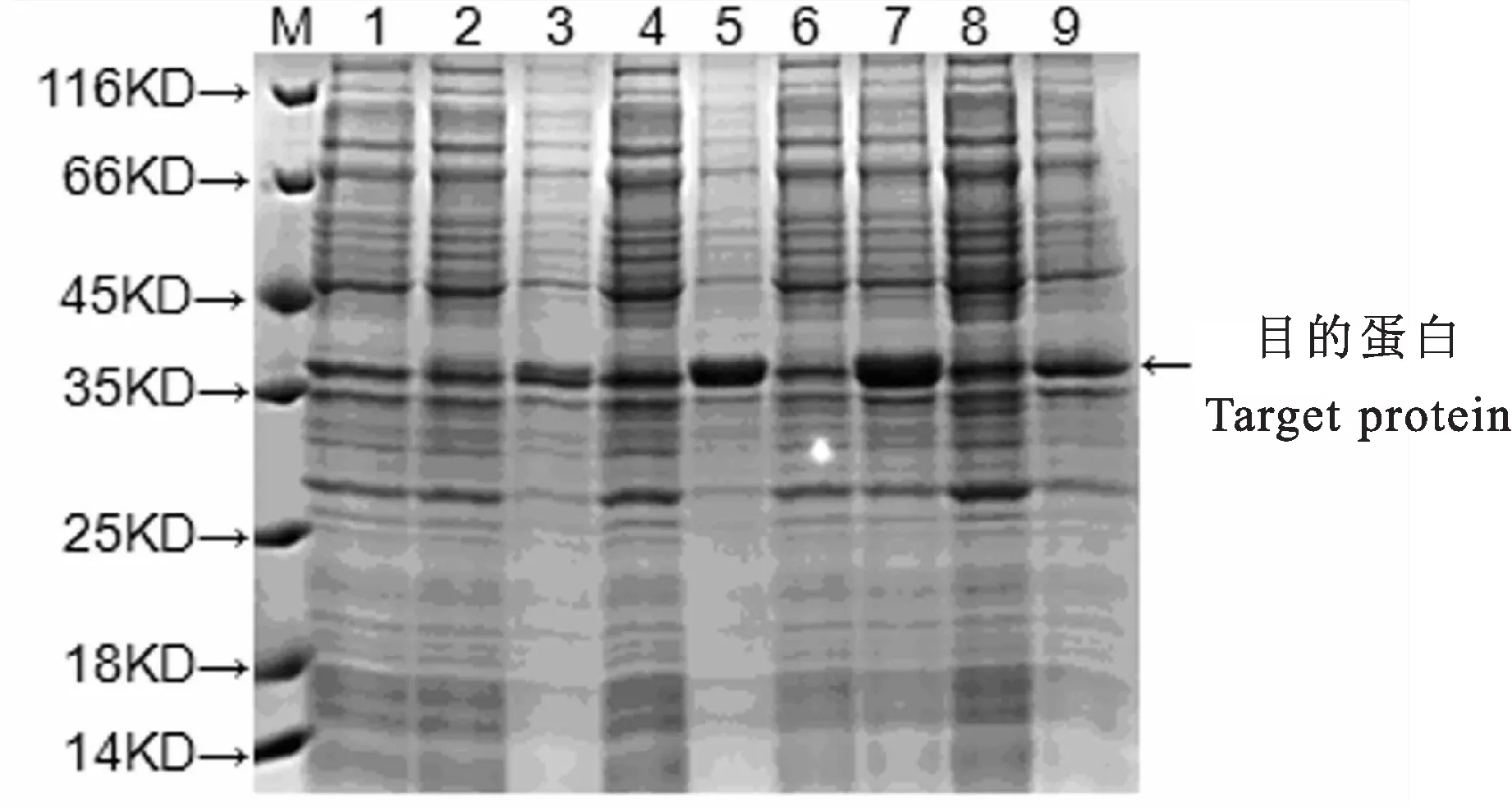
图1 AhFUSCA3基因重组蛋白在大肠杆菌中的表达Fig.1 Expression of recombinant pET-28b-AhFUSCA3 protein in BL21注:M:蛋白 Marker;1:诱导前全菌;2、4、6、8依次:诱导2h、6h、10h、16h后上清;3、5、7、9依次:诱导2h、6h、10h、16h后沉淀。Note:M:Protein Marker; Lane 1,total proteins of E.coli BL21/pET-28b-AhFUSCA3 before induction.Lanes 2,4,6 and 8,supernatant fractions after being induced 2,6,10 and 16 h,respectively; Lanes 3,5,7 and 9,precipitates after being induced 2,6,10 and 16 h,respectively.
2.2AhFUSCA3基因在非生物胁迫下的表达分析
通过荧光定量PCR分别检测了花生叶中AhFUSCA3基因在低温、高盐及干旱胁迫下的表达情况(图2)。从图2可以看出,AhFUSCA3基因在转录水平上的表达对低温、高盐及干旱胁迫均有响应,但响应模式有所差异。在花生叶中AhFUSCA3基因对低温有明显响应,在低温处理4h后表达量上调15倍左右,随后表达量逐渐下降(图2-A)。在花生叶中AhFUSCA3基因对高盐胁迫也有明显响应,盐处理8h后表达量最高,最高上调倍数约13倍(图2-B),随后表达量骤降。AhFUSCA3基因在PEG6000模拟的干旱处理条件下,其表达量在花生叶中明显下调,峰值出现在处理8h后,表达量下降约5倍(图2-C)。
总的来说,荧光定量PCR结果表明AhFUSCA3基因对三种非生物胁迫均有响应,在低温和高盐胁迫下其表达量明显上调,然而其表达量在干旱胁迫下明显下调。说明该基因可能参与了花生对低温、高盐和干旱胁迫的抗性调控,而与干旱胁迫可能是负调控。
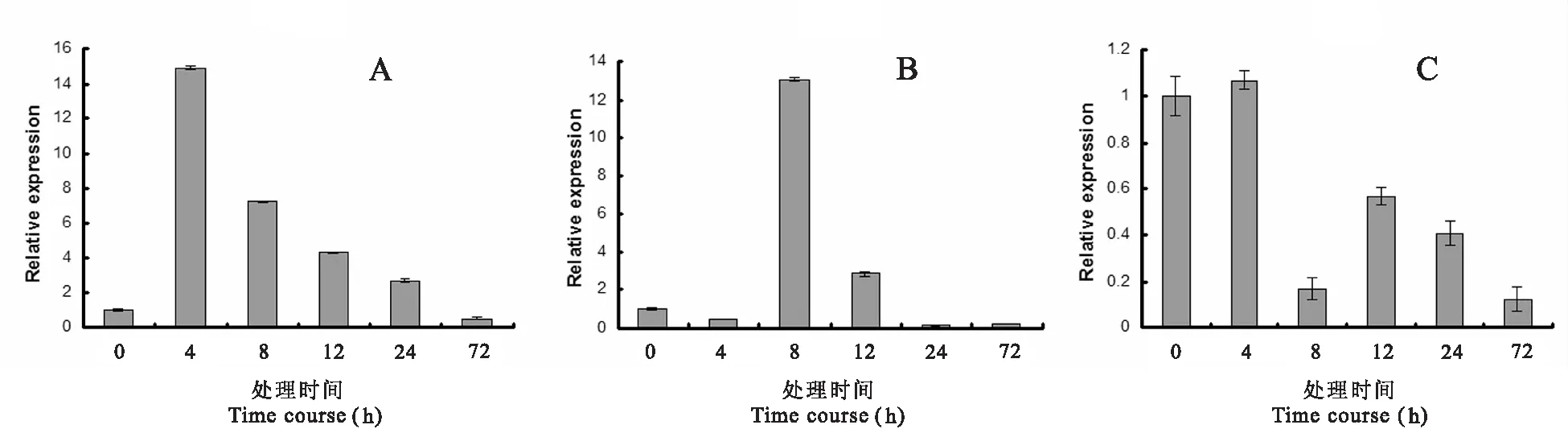
图2 AhFUSCA3基因在花生叶片中在非生物胁迫下的表达分析Fig.2 Expression analysis of AhFUSCA3 in abiotic stress treated leaves注:(A)AhFUSCA3基因在低温胁迫处理不同时间的表达;(B)AhFUSCA3基因在盐胁迫处理不同时间的表达;(C)AhFUSCA3基因在干旱胁迫处理不同时间的表达。数据为三次重复平均值,误差线代表标准偏差。Note:(A) AhFUSCA3 expression under cold stress condition; (B) AhFUSCA3 expression under salt stress condition; (C) AhFUSCA3 expression under drought stress condition.Data represent means of three replicates.Error bars are SD.
3 讨 论
花生是我国重要的油料作物,低温、高盐和干旱等非生物胁迫可以影响其萌发、生长、开花、产量等[15-16]。鉴定参与花生非生物胁迫调控的关键基因,是通过基因工程技术培育高产抗逆花生种质的基础。目前,花生基因组测序工作虽已完成,但大量的功能基因仍未获得全长,因此功能基因的克隆与鉴定仍是花生非生物胁迫研究工作的重要组成部分。
本研究在前期试验的基础上,进一步分析了花生AhFUSCA3基因在原核生物中的表达情况,获得了与理论分子量一致的目标蛋白。利用荧光定量PCR方法,对AhFUSCA3基因在非生物胁迫下的表达模式进行了详细研究。研究结果表明,该基因在转录水平上的表达对低温、高盐和干旱三种非生物胁迫均有响应(图2)。在低温和高盐胁迫下,AhFUSCA3基因在花生叶片中受到胁迫明显地诱导表达,表明该基因在这两种非生物胁迫下对花生抗逆性具有正调控作用。然而,在干旱胁迫下,AhFUSCA3基因在花生叶片中受到胁迫下调,表明该基因在干旱胁迫下对花生抗逆性可能具有负调控作用,这需要进一步研究。FUSCA3(FUS3)是在拟南芥中筛选突变体时首次被鉴定的[5],fus3突变体比野生型植株表现出花青素的过度累积和干旱耐受性减弱等特征[3,6]。FUSCA3基因对干旱胁迫的响应模式在花生和拟南芥中不同,可能是检测的植物组织部位不同引起的,我们将进一步研究在干旱胁迫下FUSCA3基因在花生其他组织中的表达情况。
总之,我们的研究结果表明AhFUSCA3蛋白在花生对低温、高盐和干旱等非生物胁迫的适应性中可能具有重要作用,这为该基因的功能研究提供了新的证据,为花生非生物胁迫转基因工程研究提供了新的基因资源。下一步将通过转基因技术将该基因导入花生中,研究该基因在花生非生物胁迫抗性调控中的生理功能,最终阐明该基因在花生中的作用机理。
[1] Hsieh T H,Lee J T,Yang P T,et al.Heterology expression of theArabidopsisC-repeat/dehydration response element binding factor 1 gene confers elevated tolerance to chilling and oxidative stresses in transgenic tomato [J].Plant Physiology,2004,129:1086-1094.
[2] Zhu J H,Dong C H,Zhu J K.Interplay between cold-responsive gene regulation,metabolism and RNA processing during plant cold acclimation [J].Current Opinion of Plant Biology,2007,10:290-295.
[3] Luerssen H,Kirik V,Herrmann P,et al.FUSCA3 encodes a protein with a conserved VP1/AB13-like B3 domain which is of functional importance for the regulation of seed maturation inArabidopsisthaliana[J].Plant J,1998,15:755-764.
[4] Monke G,Altschmied L,Tewes A,et al.Seed-specific transcription factors ABI3 and FUS3:molecular interaction with DNA [J].Planta,2004,219:158-166.
[5] Müller A J.Embryonentest zum Nachweis rezessiver Letalfaktoren beiArabidopsisthaliana[J].Biol Zentrabl,1963,82:113-163.
[6] Fankhauser C,Chory J.Light control of plant development [J].Annu Rev Cell Dev Biol,1997,13:201-229.
[7] Dave R S,Mitra R K.A low temperature induced apoplastic protein isolated fromArachishypogaea[J].Phytochemistry,1998,49:2207-2213.
[8] Rudrabhatla P,Rajasekharan R.Developmentally regulated dual-specificity kinase from peanut that is induced by abiotic stresses [J].Plant Physiology,2002,130:380-390.[9] Jain S,Srivastava S,Sarin N B,et al.Proteomics reveals elevated levels of PR 10 proteins in saline-tolerant peanut (Arachishypogaea) calli [J].Plant Physiology and Biochemistry,2006,44:253-259.
[10] Chen N,Yang Q,Su M,et al.Cloning of six ERF family transcription factor genes from peanut and analysis of their expression during abiotic stress [J].Plant Molecular Biology Reporter,2012,30:1415-1425.
[11] Dramé K N,Passaquet C,Repellin A,et al.Cloning,characterization and differential expression of a Bowman-Birk inhibitor during progressive water deficit and subsequent recovery in peanut (Arachishypogaea) leaves [J].Journal of Plant Physiology,2013,170:225-229.
[12] Wan X,Mo A,Liu S,et al.Constitutive expression of a peanut ubiquitin-conjugating enzyme gene inArabidopsisconfers improved water-stress tolerance through regulation of stress-responsive gene expression [J].Journal of Bioscience and Bioengineering,2011,111:478-84.
[13] Wang T,Chen X,Zhu F,et al.Characterization of peanut germin-like proteins,AhGLPsin plant development and defense [J].PLoS One,2013,8(4):e61722.
[14] 潘丽娟,刘风珍,万勇善,等.花生FUSCA3基因的克隆与表达分析[J].核农学报,2015,29(6):1044-1051.
[15] 万书波.中国花生栽培学 [M].上海:上海科学技术出版社,2003.
[16] 胡晓辉,孙令强,苗华荣,等.不同盐浓度对花生品种耐盐性鉴定指标的影响 [J].山东农业科学,2011,11:35-37.
Prokaryotic Expression ofAhFUSCA3 Gene and Its Expression Analysis under Abiotic Stresses in Peanut
PAN Li-juan1,2,LIANG Dan1,LIU Feng-zhen2,WAN Yong-shan2,CHI Xiao-yuan1,CHEN Na1, CHEN Ming-na1,WANG Tong1,WANG Mian1,YANG Zhen1,YU Shan-lin1*
(1.ShandongPeanutResearchInstitute,Qingdao266100;2.NationalKeyLaboratoryofCropBiology/CollegeofAgronomy,ShandongAgriculturalUniversity,Tai'an271018)
In this study,according to the sequence ofAhFUSCA3 gene (GenBank accession number JX420284),specific primers were designed to construct prokaryotic expression vector.The recombinant protein was induced and the molecular weight of the target protein was about 42 KD.Expression analysis indicated that theAhFUSCA3 gene was induced in peanut leaves under either cold or salt conditions.However,the expression of theAhFUSCA3 gene was decreased in leaves under drought treatment.The results suggested that theAhFUSCA3 gene may be involved in abiotic stress regulation of peanut.
peanut;AhFUSCA3 gene; prokaryotic expression; abiotic stresses; real-time PCR
10.14001/j.issn.1002-4093.2016.04.001
2016-07-29
2014年国家“万人计划”青年拔尖人才;国家花生产业技术体系项目(CARS-14);山东省自然科学基金项目(ZR2011CQ036;ZR2012CQ031;ZR2014YL011;ZR2014YL012);国家自然科学基金项目(31000728;31200211);青岛市科技计划应用基础研究项目(11-2-4-9-(3)-jch; 12-1-4-11-(2)-jch);青岛市民生计划项目(14-2-3-34-nsh);山东省农业科学院青年科研基金项目(2016YQN14);农业部油料作物生物学与遗传育种重点实验室开放课题基金(2014010);山东省农业科学院青年英才培养计划
潘丽娟(1980-),女,山东潍坊人,山东省花生研究所助理研究员,在读博士,主要从事花生遗传育种研究。
*通讯作者:禹山林(1956-),男,研究员,主要从事花生遗传育种研究。E-mail:yshanlin1956@163.com
S565.2; Q786
A
