甘遂半夏汤加减甘遂及不同品种甘草对腹水模型大鼠肝脏CYP450m RNA的影响
2016-05-25许皖柳海艳钟赣生于雪张建美郭岩松王思睿修琳琳
许皖 柳海艳 钟赣生 于雪 张建美 郭岩松 王思睿 修琳琳
100029 北京中医药大学基础医学院[许皖(硕士研究生)、张建美(硕士研究生)、郭岩松(硕士研究生)、修琳琳(博士研究生)、王思睿(硕士研究生)],基础医学院方药系(钟赣生、柳海艳),科研实验中心(于雪)
甘遂半夏汤加减甘遂及不同品种甘草对腹水模型大鼠肝脏CYP450m RNA的影响
许皖柳海艳钟赣生于雪张建美郭岩松王思睿修琳琳
100029北京中医药大学基础医学院[许皖(硕士研究生)、张建美(硕士研究生)、郭岩松(硕士研究生)、修琳琳(博士研究生)、王思睿(硕士研究生)],基础医学院方药系(钟赣生、柳海艳),科研实验中心(于雪)
【摘要】目的观察含不同品种甘草的甘遂半夏汤加减甘遂甘草反药组合对腹水模型大鼠肝脏CYP450 mRNA的影响。方法采用Walker-256细胞制造癌性腹水模型,将Wistar大鼠按体质量随机分为空白组、模型组、阳性对照组、全方炙甘草组、全方炙光果甘草组、全方炙胀果甘草组、去遂炙甘草组、去遂炙光果甘草组、去遂炙胀果甘草组、去炙甘草组、去炙甘草醋甘遂组,共计11组。空白组和模型组灌胃蒸馏水,其余各给药组灌胃相应药物。给药11天后,摘取肝脏,液氮保存,进行PCR实验。结果在CYP2E1 mRNA表达方面,全方炙甘草组、全方炙胀果甘草表达下调,且优于全方去掉一味或两味反药。三个甘草品种的甘遂半夏汤的CYP3A1 mRNA、CYP3A2 mRNA表达上调,且优于全方去掉一味或两味反药。结论(1)全方炙甘草组、全方炙胀果甘草组在CYP450表达方面表现出一定的药效作用,其中全方炙甘草组优于全方炙胀果甘草,且均优于全方去掉一味或两味反药组。(2)全方炙光果甘草组则未表现出一定的药效作用,但也未表现出毒性作用,弱于去掉一味或两味反药。
【关键词】反药组合;甘遂;炙甘草;炙光果甘草;炙胀果甘草;CYP450 mRNA
“藻戟遂芫俱战草”属中药“十八反”配伍禁忌的范畴,是古人临床实践的经验总结。一些医家认为反药同用相反相激,可以治疗沉疾,但另有一些医家认为反药同用会对人体造成伤害,应避免使用。那么,反药到底能否同用至今尚无统一的定论,有待于去进一步研究。鉴于临床应用中,“相反”药物配伍多用于特定的病理条件下,因此,本实验选择有临床应用基础的经方甘遂半夏汤(含甘遂与甘草反药组合),针对特定的病理条件,即腹水模型进行相关研究。课题前期已经对含甘遂甘草反药组合对不同剂量,不同炮制品种,不同配伍比例,不同给药次数以及不同入药方式等方面进行了初步的探讨。鉴于《中华人民共和国药典》中记载甘草为豆科植物甘草GlycyrrhizauralensisFisch.、胀果甘草GlycyrrhizainflateBat.或光果甘草GlycyrrhizaglabraL.的干燥根和根茎,且甘遂半夏汤原方中未明确标明甘草的具体品种。因此,本实验拟以此为切入点,从甘草不同品种的角度进行拆方研究探讨反药能否同用及是否与其品种相关。本文选取与肝脏药物代谢密切相关的CYP2E1、CYP3A1、CYP3A2指标进行探讨,其中药物会诱导或抑制肝脏中CYP2E1酶活性的表达,对药物的代谢产生影响,可能导致不良反应的产生和药物毒性的加重[1-2]。药物在联合应用时是CYP3A1、CYP3A2代谢酶的诱导剂和抑制剂,可能导致某种药物的药效或毒性增强或减弱[3-4]
1材料与方法
1.1材料
1.1.1动物Wistar大鼠220只,SPF级,体质量(210~230) g,雄性。由维通利华(北京)实验动物科技有限公司提供,许可证号:SCXK(京)2012-0001。
1.1.2药物醋甘遂(由安徽丰原铜陵中药饮片厂提供,批号120301)为大戟科植物甘遂EuphorbiakansuiT.N.Liou ex T.P.Wang的干燥块根、炙甘草(由安徽丰原铜陵中药饮片厂提供,批号120201)为豆科植物甘草GlycyrrhizauralensisFisch.的干燥根和根茎;炙光果甘草(由安徽丰原铜陵中药饮片厂提供,批号120201)为豆科植物甘草GlycyrrhizaglabraL.的干燥根和根茎;炙胀果甘草(由安徽丰原铜陵中药饮片厂提供,批号120201)为豆科植物甘草GlycyrrhizainflateBat.的干燥根和根茎;法半夏(由安徽丰原铜陵中药饮片厂提供,批号100701)为天南星科植物半夏Pinellia ternate(Thunb) Breit.的块茎,经甘草和石灰炮制的炮制品;白芍(安徽丰原铜陵中药饮片厂提供)为毛莨科植物芍药PaeonialactifloraPall.的根;呋塞米片(江苏亚邦爱普森药业有限公司,批号H32021428)。
1.1.3试剂与仪器Trizol RNA提取试剂(美国Invitrogen公司,批号66014);RNA逆转录试剂盒(赛默飞世尔科技(中国)有限公司,批号00169216);蛋白酶抑制剂混合物(北京康为世纪生物科技有限公司,批号2614H);OligdT(生工生物工程(上海)股份有限公司,批号109302I);Light Cycler2.0实时荧光定量PCR仪(德国Roche诊断公司);image system凝胶成像系统(美国Alpha Inn tech 公司);Implen超微量分光光度计(德国IMPLEN公司)。
1.2模型复制
将冻存于-70℃冰箱中的Walker-256癌性细胞于37℃水浴复苏,分为0.6、0.8、1.0 mL剂量注入大鼠体内,长出腹水后再以每只1 mL的剂量注入大鼠体内进行2次传代,2次传代的大鼠长出腹水后,选取淡黄色的腹水进行细胞计数,以1.68×109/L注入正式实验的大鼠体内,每只注射1 mL。
1.3分组及给药
将Wistar大鼠按体质量随机分为空白组、模型组、阳性药组(呋塞米)、甘遂半夏汤全方炙甘草组(简称全方炙甘草组)、甘遂半夏汤全方炙甘草汤去醋甘遂组(简称全方炙甘草去遂组)、甘遂半夏汤全方炙光果甘草组(简称全方炙光果甘草组)、甘遂半夏汤全方炙光果甘草汤去醋甘遂组(简称全方炙光果甘草去遂组)、甘遂半夏汤全方炙胀果甘草组(简称全方炙胀果甘草组)、甘遂半夏汤全方炙胀果甘草汤去醋甘遂组(简称全方炙胀果甘草去遂组)、甘遂半夏汤全方去甘草组(简称全方去草组)、甘遂半夏汤全方去炙甘草醋甘遂组(简称全方去草遂组),共11组,每组20只。正常喂养,每天上午除空白组外,模型组灌胃蒸馏水,各给药组的给药剂量分别为阳性药组(呋塞米4.2 g/kg),甘遂半夏汤全方组(5.68 g/kg),全方去醋甘遂组(5.57 g/kg),全方去炙甘草组(4.01 g/kg),全方去草遂组(3.9 g/kg),均灌胃给药。
1.4药物制备方法
课题组前期已经对含甘遂与甘草反药组合以1∶15配比的高、中、低剂量的甘遂半夏汤全方进行了探讨,结果表明低剂量组有效且未显示出明显毒性,较适合配伍应用[5]。因此本实验所拟定的甘遂半夏汤处方即为低剂量条件下的:醋甘遂0.11 g(研末)、法半夏0.9 g、白芍1.5 g、炙甘草1.67 g、蜂蜜1.5 g。
甘遂半夏汤药液的制备:将法半夏、白芍、炙甘草加10倍量水浸泡1小时,煮沸后小火继续煎煮1小时,第2次加8倍量水煎煮,沸腾后小火继续煎煮1小时,将两次煎煮的药液合并,加入蜂蜜,放至水浴锅上浓缩至1.14 g/mL,临用时按比例加入醋甘遂粉末,加入适量水至0.568 g/mL。
甘遂半夏汤去醋甘遂药液的制备:同甘遂半夏汤药液的制备,临用时不加入醋甘遂,加水稀释至0.557 g/mL。
甘遂半夏汤去炙甘草药液的制备:将法半夏、白芍加10倍量水浸泡1小时,煮沸后小火继续煎煮1小时,第2次加8倍量水煎煮,沸腾后小火继续煎煮1小时,将两次煎煮的药液合并,加入蜂蜜,放至水浴锅上浓缩至0.78 g/mL,临用时按比例加入适量醋甘遂,加水稀释至0.401 g/mL。
甘遂半夏汤去炙甘草醋甘遂药液的制备:同甘遂半夏汤去炙甘草药液的制备,临用时不加入醋甘遂,加水稀释至0.39 g/mL。
1.5样本采集及指标检测
腹主动脉取血后,迅速剖开腹腔取出肝脏,在同一部位选取约黄豆大小一块肝组织,置于冻存管中,液氮冻存。
1.5.1提取肝组织RNA(1)剪取50~100 mg组织,放入已加入1 mL预冷Trizol的研磨器中匀浆;(2)加0.2 mL(1/5体积)氯仿,先混匀后剧烈振荡15秒,室温放置5~10分钟;(3)4℃离心,15000 rpm,15分钟;(4)吸取约400 μL液体加等体积异丙醇,颠倒混匀,放置10分钟。(5)4℃离心,15000 rpm,15分钟;(6)加1 mL 75%乙醇重悬,4℃离心,12000 rpm,8分钟。(7)弃上清,超净台内室温干燥5~10分钟。(8)加200 μL DEPC水溶解RNA样品。
1.5.2超微量分光光度法检测RNA样品的浓度并计算纯度加1 μL去离子水在检测窗口上调零。擦拭盖子,加入1 μLRNA样品,盖上盖子开始检测,并读取260 nm、280 nm处OD比值及RNA浓度值。
1.5.3结果分析用记录的样品RNA浓度计算RNA体积,计算公式为:RNA体积(μL)=3 g×1000/RNA浓度值
1.5.4mRNA反转录为cDNA5×逆转录酶缓冲液:4 μL;dNTP Mixture:2 μL;Oligo(DT):2 μL;RNA酶抑制剂1 μL;MLV逆转录酶1 μL;RNA样品3 μg;TotalRNA Add to 20 μL,按以下条件进行反转录反应:37℃ 60分钟。
1.5.5PCR引物合成引物由生工生物工程(上海)股份有限公司提供,具体碱基序列如表1所示。
1.5.6cDNA扩增方法取各组RT反应产物按表2、3、4所示配制PCR扩增反应液。
1.5.7cDNA扩增反应条件(1)2E1 Stage 1:预变性,循环1次,94℃3分钟;Stage 2:PCR反应循环33次,94℃30秒,55℃30秒,72℃1分钟,72℃延伸8分钟。(2)3A1 Stage 1:预变性,循环1次,94℃3分钟;Stage 2:PCR反应循环34次,94℃30秒,55℃40秒,72℃1分钟,72℃延伸8分钟。(3)3A2 Stage 1:预变性,循环1次,94℃3分钟;Stage 2:PCR反应循环32次,94℃30秒,55℃30秒,72℃1分钟,72℃延伸8分钟。
1.5.8数据采集取PCR反应液5 μL进行琼脂糖凝胶电泳(CYP2E1为1.2%的胶,CYP3A1和CYP3A2为2%的胶),取RNA样品各5 μL,加入6×Lording buffer 1 μL,混匀,将所有液体加入凝胶加样孔中。以600 bp DNA Ladder marker作为参照,120 V电压下电泳25分钟。跑胶结束后应用BIO IMAGING SYSTEM (Gene Snap)照像,AlphViea SA收集数据,以GAPDH或β-actin作为内标,计算公式:RNA含量=目的基因/GAPDH或β-actin。

表1 PCR引物信息

表2 CYP2E1反应体系
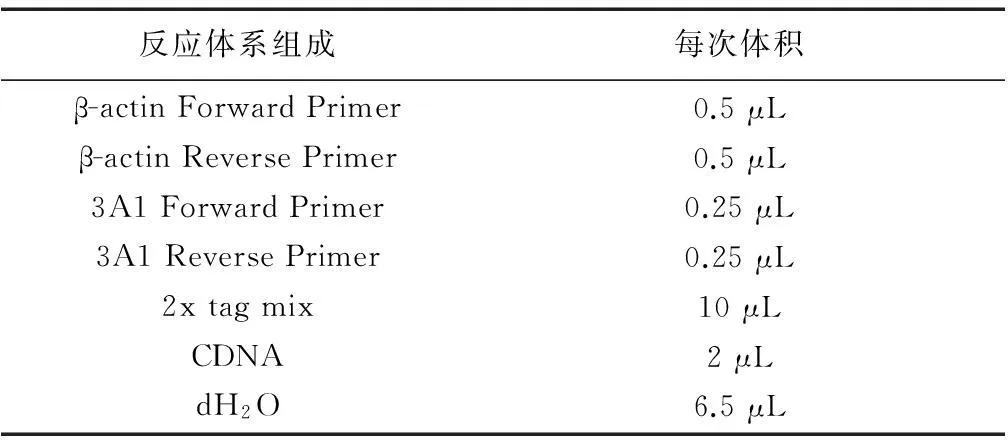
表3 CYP3A1反应体系
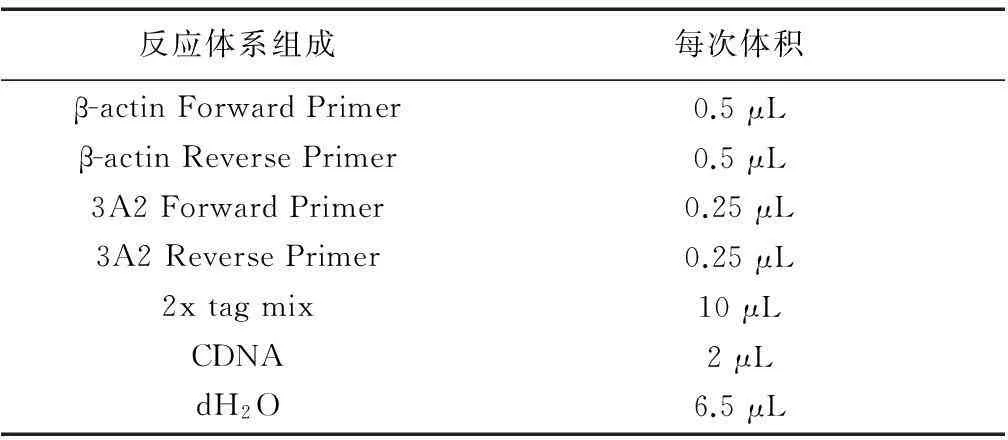
表4 CYP3A2反应体系
1.6统计学处理
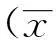
2结果
2.1各组大鼠肝脏CYP2E1 mRNA比较
与空白组比较,全方炙甘草组的大鼠肝脏CYP2E1 mRNA表达下调,具有统计学差异(P<0.05);全方炙光果甘草组、全方炙胀果甘草组呈现出表达下调的趋势。
与模型组比较,全方炙甘草组、全方炙胀果甘草组的大鼠肝CYP2E1 mRNA表达下调,但不具有统计学差异(P>0.05);全方炙光果甘草组及其余给药组的大鼠肝脏CYP2E1 mRNA表达上调,但不具有统计学差异(P>0.05)。
与全方炙甘草组比较,全方炙光果甘草组、全方胀果炙甘草组的大鼠肝脏CYP2E1 mRNA表达上调,但不具有统计学差异(P>0.05)。去遂(剩炙甘草)组、去遂(剩炙光果甘草)组、去草组、去草遂组较相应的全方组在大鼠肝脏CYP2E1 mRNA表达上调,但不具有统计学差异(P>0.05)。见表5和图1。
2.2各组大鼠肝脏CYP3A1 mRNA比较
与空白组比较,模型组、阳性药组、全方炙光果甘草组、全方炙胀果甘草组、去遂炙甘草组大鼠肝脏CYP3A1 mRNA表达下调,有统计学差异(P<0.05或P<0.01)。其余各给药组的大鼠肝脏CYP3A1 mRNA表达上调,但无统计学差异(P>0.05)。
与模型组比较,各给药组的大鼠肝脏CYP3A1 mRNA表达上调,其中全方炙甘草组、全方炙胀果甘草组、遂炙光果甘草组、去遂炙胀果甘草组、去草组、去草遂组的上调具有统计学差异(P<0.05或P<0.01)。
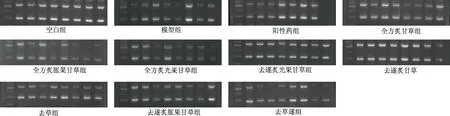
图1 各组大鼠CYP2E1 mRNA电泳结果
图2 各组大鼠CYP3A1 mRNA电泳结果

图3 各组大鼠CYP3A2 mRNA电泳结果
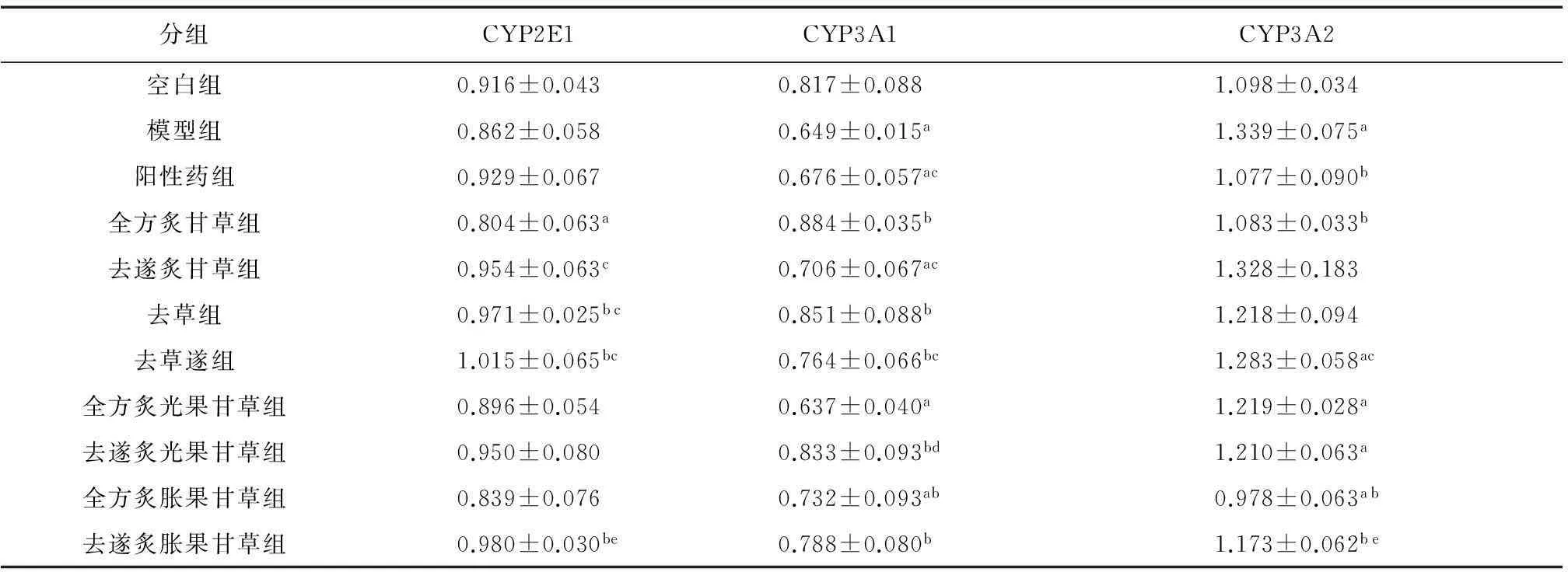
分组CYP2E1CYP3A1CYP3A2空白组0.916±0.0430.817±0.0881.098±0.034模型组0.862±0.0580.649±0.015a1.339±0.075a阳性药组0.929±0.0670.676±0.057ac1.077±0.090b全方炙甘草组0.804±0.063a0.884±0.035b1.083±0.033b去遂炙甘草组0.954±0.063c0.706±0.067ac1.328±0.183去草组0.971±0.025bc0.851±0.088b1.218±0.094去草遂组1.015±0.065bc0.764±0.066bc1.283±0.058ac全方炙光果甘草组0.896±0.0540.637±0.040a1.219±0.028a去遂炙光果甘草组0.950±0.0800.833±0.093bd1.210±0.063a全方炙胀果甘草组0.839±0.0760.732±0.093ab0.978±0.063ab去遂炙胀果甘草组0.980±0.030be0.788±0.080b1.173±0.062be
注: 与空白组比较,aP<0.05;与模型组比较,bP<0.05;与全方炙甘草组比较,cP<0.05;与全方炙光果甘草组比较,dP<0.05;与全方炙胀果甘草组比较,eP<0.05;
与全方炙甘草组比较,全方炙光果甘草、全方胀果炙甘草组大鼠肝脏CYP3A1 mRNA表达下调,有统计学差异(P<0.05或P<0.01)。其中全方胀果炙甘草组的的大鼠肝脏CYP3A1 mRNA表达较全方炙光果甘草组有上调的趋势(P<0.05)。去遂炙光果甘草组、去遂炙胀果甘草组、去草组、去草遂组较相应的全方在CYP3A1 mRNA表达方面呈现上调的趋势(P<0.05)。见表5和图2。
2.3各组大鼠肝脏CYP3A2 mRNA比较
与空白组比较,全方炙胀果甘草组的大鼠肝CYP3A2 mRNA表达下调,有统计学差异(P<0.05),其余各给药组显现出上调的趋势,其中模型组、全方炙光果甘草组、去遂(剩炙光果甘草)组、去草遂组的上调,有统计学差异(P<0.01)。
与模型组比较,阳性药组、全方炙甘草组、全方炙胀果甘草组、去遂(剩炙胀果甘草)组的大鼠肝CYP3A2 mRNA表达下调,具有统计学的差异(P<0.01)。其余给药组显现出上调的趋势,但不具有统计学差异(P>0.05)。
与全方炙甘草组比较,全方炙光果甘草组的大鼠肝脏CYP3A2 mRNA表达上调,有统计学差异(P<0.01)。全方胀果炙甘草组较全方炙光果甘草的大鼠肝脏CYP3A2 mRNA表达下调,有统计学差异(P<0.01)。去遂(剩炙甘草)组、去遂(剩炙胀果甘草)组、去草组、去草遂组较相应的全方组的大鼠肝脏CYP3A2 mRNA表达略有上调,但不具有统计学差异。见表5和图3。
3讨论
现有的研究发现,单味中药甘遂或甘草以及两药组合均可诱导CYP2E1活性的增强,进而促使甘遂中的前致癌物质和毒物转化为致癌物和毒物,其中甘草对CYP2E1活性的诱导作用强于甘遂,而两药组合的诱导作用强于单味药。在对CYP3A2的研究中,甘遂对CYP3A2活性的诱导作用最强,甘草可以抑制CYP3A2的活性从而减慢甘遂中毒性成分的代谢速度[6]。以上研究说明甘遂与甘草反药组合存在基于药物代谢的相互作用。现有的实验研究表明,甘遂甘草反药组合的使用并不是完全禁忌的,而是受不同条件限制的,与肝药酶存在密切联系[7]。
从肝脏CYP2E1 mRNA表达方面的实验结果来看,含炙甘草醋甘遂反药组合的甘遂半夏汤全方在降低CYP2E1 mRNA表达方面均优于全方去掉其中一味或两味反药。同样,含炙胀果甘草醋甘遂反药组合的甘遂半夏汤全方在降低CYP2E1 mRNA表达方面优于全方去掉其中一味或两味反药。由此说明,这两个全方组具有一定的降低恶性腹水大鼠肝脏CYP2E1 mRNA表达,这可能是其降低恶性腹水模型大鼠进一步增多恶化的途径之一,从而表现出一定的药效作用。而含炙光果甘草醋甘遂反药组合的甘遂半夏汤全方在降低CYP2E1 mRNA表达方面均弱于全方去掉其中一味或两味反药,未表现出一定的药效作用,也未表现出毒性。
在肝脏CYP3A1 mRNA表达方面的实验结果来看,与模型组比较,全方炙甘草组、全方炙光果甘草组、全方炙胀果甘草组对大鼠肝脏CYP3A1 mRNA表达有所上调,说明三个全方组对中药中有毒物质的代谢有一定的促进作用。其中全方炙甘草组在促进毒性物质代谢方面优于全方炙光果甘草组及全方炙胀果甘草组。从甘草不同品种的拆方实验来看,含炙甘草醋甘遂反药组合的甘遂半夏汤全方在升高CYP3A1 mRNA及CYP3A2 mRNA表达方面均优于全方去掉其中一味或两味反药。同样,含炙胀果甘草醋甘遂反药组合的甘遂半夏汤全方在升高CYP3A1 mRNA及CYP3A2 mRNA表达方面均优于全方去掉其中一味或两味反药。由此说明,两个全方均表现出一定的药效作用。而含炙光果甘草醋甘遂反药组合的甘遂半夏汤全方在升高CYP2E1 mRNA表达方面弱于全方去掉其中一味或两味反药,即未表现出一定的药效作用,也未表现出毒性。
综上所述,在全方条件下,全方炙甘草组、全方炙胀果甘草组在CYP450表达方面表现出一定的药效作用,可能表现出一定的肝保护作用,且全方炙甘草组优于全方炙胀果甘草。而全方炙光果甘草组则未表现出一定的药效作用,但也未表现出毒性作用。在拆方条件下,全方炙甘草组、全方炙胀果甘草组在CYP450表达方面均优于去掉一味或两味反药,而全方炙光果甘草组弱于去掉一味或两味反药,未表现出一定的药效。
参考文献
[1]代方国,罗仁,王宇光,等.甘遂配伍甘草对大鼠肝脏CYP2E1表达及活性的影响[J].第三军医大学学报,2005,27(8):742-744.
[2]年华,马明华,徐玲玲,等.细胞色素P450酶与药物代谢的研究进展与评价[J].中国医院用药评价与分析,2010,10(11):964-967.
[3]周淑娟,李强,刘卫红,等.栀子苷对大鼠肝指数、肝功能及肝脏微粒体中CYP3A2的影响[J].中医研究,2010,23(3):20-22.
[4]Tong L,Edward T.Down-regulation of phenol barbital induced CYP2BmRNA and protein by endotoxin in mice[J].Bio M Pharm,2001,(64):1703-1711.
[5]王茜.甘遂半夏汤中甘遂甘草反药组合的配伍宜忌条件实验研究[D].北京:北京中医药大学,2012:85.
[6]代方国,罗仁,王宇光,等.甘遂配伍甘草对大鼠肝脏CYP3A2影响[J].第四军医大学学报,2005,26(10):951-953.
[7]张建美,许皖,钟赣生,等.甘遂甘草反药组合宜忌条件的实验研究回顾与评价[J].环球中医药,2015,8(9):25-30.
(本文编辑: 董历华)
Comparing the effect ofGansuiBanxiadecoction plus or reduce kansui and varieties of glycyrrhiza on the CYP450 mRNA of liver of ascites model rats
XUWan,LIUHai-yan,ZHONGGan-sheng,etal.
SchoolofBasicMedicalSciences,BeijingUniversityofChineseMedicine,Beijing100029,China
【Abstract】ObjectiveTo observe the effect of different varieties of glycyrrhiza and kansui incompatible herbs in Gansui Banxia decoction on liver CYP450 mRNA ascites model rat. MethodsThe Walker-256 cell was used to manufacture carcinomatous ascites model. The Wistar rats were randomly divided into blank group, model group, positive control group, complete formula with Glycyrrhiza uralensis Fisch. group, complete formula with Glycyrrhiza glabra L.group, complete formula with Glycyrrhiza inflata Bat. group, the Glycyrrhiza uralensis Fisch. Without kansui group , the Glycyrrhiza glabra L.without kansui group, the Glycyrrhiza inflata Bat. without kansui group, prescription without glycyrrhiza group, prescription without glycyrrhiza and kansui group, a total of 11 group. The blank control group and model group were given distilled water, the rest of the drug group were given corresponding drugs. After 11 days of treatment, the liver was removed and stored in liquid nitrogen and saved for PCR experiment. ResultsThe expression of CYP2E1 mRNA in complete formula with Glycyrrhiza uralensis Fisch. group and complete formula with Glycyrrhiza glabra L. Group were down-regulation and superior to add and subtract the prescription. CYP3A1 and CYP3A2 mRNA expression in the three complete formula groups with three species of glycyrrhiza were up-regulated, and better than add and subtract the prescription. Conclusion(1) CYP450 expression in complete formula with Glycyrrhiza uralensis Fisch. group and complete formula Glycyrrhiza inflata Bat. group showed certain effect, which Glycyrrhiza uralensis Fisch. group is better than the roast Glycyrrhiza inflata Bat., and was better than the group which was added and subtracted the prescription. (2) The complete formula with Glycyrrhiza glabra L.group did not show a certain effect, but also did not show toxic effects, the effect was weak than the group which was added and subtracted the prescription.
【Keywords】Incompatible herbs;Kansui;Glycyrrhiza uralensis Fisch.;Glycyrrhiza glabra L.;Glycyrrhiza inflate Bat.;CYP450 mRNA
(收稿日期:2016-01-05)
Corresponding author:ZHONG Gan-sheng, E-mail: zhonggansheng@sohu.com
【中图分类号】R285.5
【文献标识码】A
doi:10.3969/j.issn.1674-1749.2016.05.002
作者简介:许皖(1990- ),女,2013级在读硕士研究生。研究方向:中药药性理论研究。E-mail:1043855021@qq.com通讯作者: 钟赣生(1961- ),硕士,教授,博士生导师。研究方向:中药药性理论研究。E-mail:zhonggansheng@sohu.com
基金项目:国家重点基础研究发展计划(973计划)(2011CB505306); 北京中医药大学2016年度基本科研业务费项目(中青年教师类)(2016-JYB-JSMS-005)
·甘遂甘草反药研究专题·
