芪精愈消胶囊薄层鉴别及含量测定研究
2016-05-23许广华李小伟
许广华,王 虎,李小伟,陈 刚
(太和县中医院药剂科,安徽 太和 236600)
芪精愈消胶囊薄层鉴别及含量测定研究
许广华,王虎,李小伟,陈刚
(太和县中医院药剂科,安徽 太和236600)
摘要:目的 制定芪精愈消胶囊的质量标准。方法 采用TLC法鉴别处方中的黄芪、五味子;采用HPLC法测定葛根中葛根素的含量,Agilent C(18)色谱柱(4.6 mm×250 mm,5 μm),流动相为甲醇—0.4%磷酸溶液(25∶75),检测波长250 nm。结果黄芪、五味子薄层鉴别斑点清晰,阴性无干扰,可作为定性鉴别;含量测定中葛根素在0.169 4~0.846 8 μg范围内,与峰面积线性关系良好,回归方程为A=4375 947C+1 708(r=0.999 9),回收率平均为99.36%,RSD=0.98%(n=5)。 结论该方法操作简单,专属性和重现性良好,可作为该制剂的质量控制方法。
关键词:芪精愈消胶囊;五味子;黄芪;葛根;葛根素
芪精愈消胶囊为太和县中医院制剂,由黄芪、五味子、葛根、黄精等七味中药制成。具有益气养阴、扶正固本的功效,用于口渴、多饮、多尿、乏力、多汗诸症。处方中所用药材,化学成分比较清楚,主要有黄芪甲苷、葛根素、五味子乙素等。为了更好的控制药品质量,保证用药安全有效,本文对处方中的黄芪和五味子进行了薄层鉴别,同时采用HPLC法测定了葛根中葛根素的含量。
1仪器与试药
1.1 仪器LC-1220型高效液相色谱仪(安捷伦);ZF-2型三用紫外仪(上海安亭电子仪器厂);HS-180型超声波清洗机(安徽金尼克机械有限公司);HH型水浴锅(江苏金坛中大仪器厂);101-1A型数显恒温干燥箱(沪粤科学仪器厂);硅胶G板、硅胶GF254板(50 mm×100 mm,青岛海洋化工厂分厂)。
1.2试药 葛根素对照品(中国食品药品检定研究院,批号110752-200209);五味子乙素对照品(中国食品药品检定研究院,批号110765-200407);五味子对照药材(中国食品药品检定研究院,批号120922-201108);黄芪对照药材(中国食品药品检定研究院,批号121462-201003);芪精愈消胶囊(太和县中医院,批号:20140603、20140606、20140609);甲醇为色谱纯,水为重蒸水;其余试剂均为分析纯。
2薄层鉴别
2.1黄芪薄层鉴别 取本品混匀的内容物2 g,加乙酸乙酯20 mL,加热回流1 h,放冷,滤过,滤液浓缩至1 mL,作为样品溶液。再取按芪精愈消胶囊制备工艺生产的不含黄芪的样品,同法制成阴性对照溶液。另取黄芪对照药材1 g,照样品溶液的制备方法制成药材对照溶液。按《中国药典》2015版四部0502薄层色谱法,分别吸取以上三种溶液各10 μL,点于同一硅胶G薄层板(105℃活化30 min)上,展开剂为三氯甲烷—甲醇(17∶1)[1],展开,取出,晾干,喷以碳酸钠试液,置紫外灯365 nm下检视。样品色谱在与对照色谱相对应的位置上,显颜色相同的荧光斑点。而阴性对照在此位置处无斑点,方法专属性强,可作为本品中黄芪的鉴别,见图1。
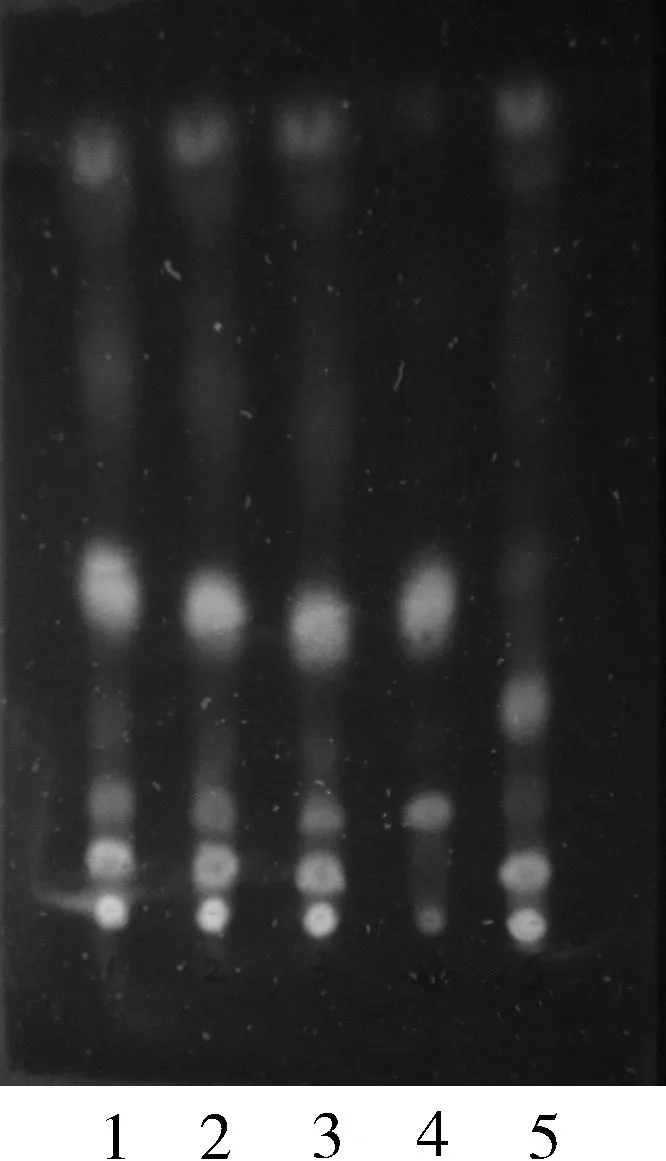
图1 黄芪TLC图
注:1.批号20140603样品;2.批号20140606样品;3.批号20140609样品;4.黄芪对照药材;5.阴性对照样品 。
2.2五味子薄层鉴别[2]取本品混匀的内容物4 g,加三氯甲烷30 mL,浸泡1 h,超声30 min,过滤,滤液蒸干,残渣用1 mL乙酸乙酯使溶解,作为样品溶液。再取按芪精愈消胶囊制备工艺生产的不含五味子的样品,同法制成阴性对照溶液。另取五味子乙素对照品,加甲醇制成1 g·L-1的溶液,作为对照品溶液。按《中国药典》2015版四部0502薄层色谱法,分别吸取以上样品溶液与阴性对照溶液各5 μL、对照品溶液2 μL,点于同一硅胶GF254薄层板(105℃活化30 min)上,展开剂为石油醚(30~60℃)—甲酸乙酯—甲酸(15∶5∶1)的上层溶液,展开,取出,晾干,置紫外灯254 nm下检视。样品色谱在与对照品色谱相对应的位置上,显颜色相同的荧光斑点。而阴性对照在此位置处无干扰,方法专属性强,可作为本品中五味子的鉴别,见图2。
3含量测定
3.1波长的选择 以甲醇为空白对照,对葛根素在200~400 nm范围内进行波长扫描。结果葛根素在250.05 nm波长处有最大吸收(见图3)。参照药典中葛根药材的含量测定条件,故选择250 nm作为检测波长[3]。

图2 五味子TLC图
注:1.批号20140603样品;2.批号20140606样品;3.批号20140609样品;4.五味子乙素对照品;5.五味子对照药材;6.阴性对照样品。
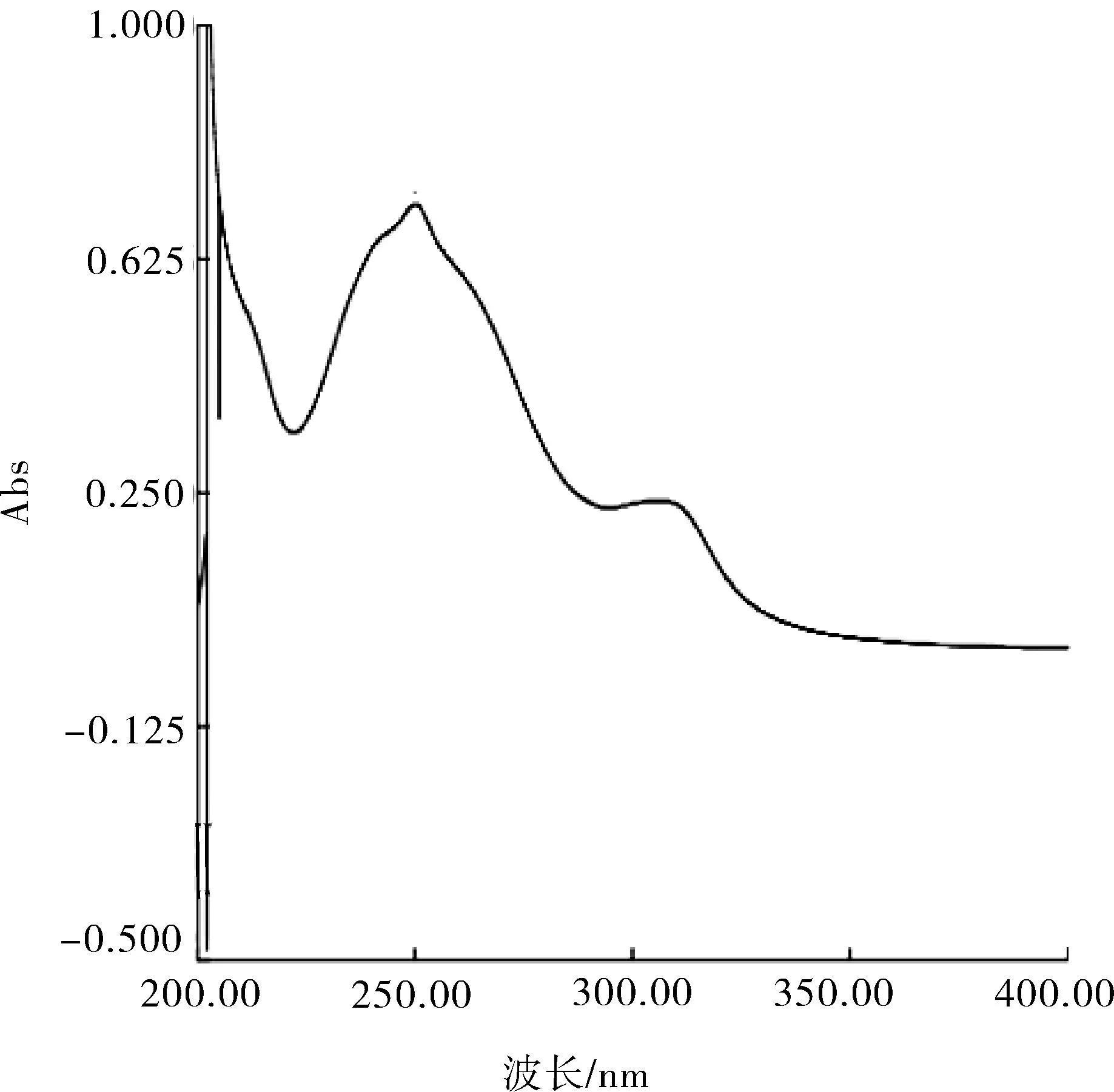
图3 葛根素波长扫描
3.2 色谱条件及系统适用性试验 色谱柱为Agilent C18柱(4.6 mm×250 mm,5 μm);流动相为甲醇—0.4%磷酸溶液(25∶75)[4-8];检测波为250 nm。理论板数以葛根素峰计算应不低于5 000,分离度为1.8,拖尾因子为0.99。
3.3溶液的制备
3.3.1对照品溶液的制备精密称定葛根素对照品若干,加甲醇制成每1 mL含80 μg的溶液,即得。
3.3.2供试品溶液的制备[9]取装量差异项下混匀的胶囊内容物,取约0.35 g,精密称定,置25 mL容量瓶中,加甲醇适量,超声20 min,取出,放冷后,加甲醇定容。摇匀,滤过,取续滤液,即得。
3.4缺葛根阴性样品测定取按芪精愈消胶囊制备工艺生产的不含葛根的样品,按“3.3.2”法制成阴性样品溶液,进样测定。结果表明:阴性样品的HPLC图谱中在与对照品葛根素HPLC图谱中相同的保留时间处无吸收峰,阴性无干扰,方法专属性较强,见图4。
3.5标准曲线的制备精密称取葛根素对照品2.117 mg,甲醇超声溶解,定容至25 mL。照“3.2”色谱条件,分别进样2、4、6、8、10 μL,测得峰面积并绘制标准曲线(以进样量为横坐标,峰面积为纵坐标)。其回归方程:A=4 375 947C+1 708,r=0.999 9。由图5知,葛根素在0.169 36~0.846 8 μg范围内线性良好。
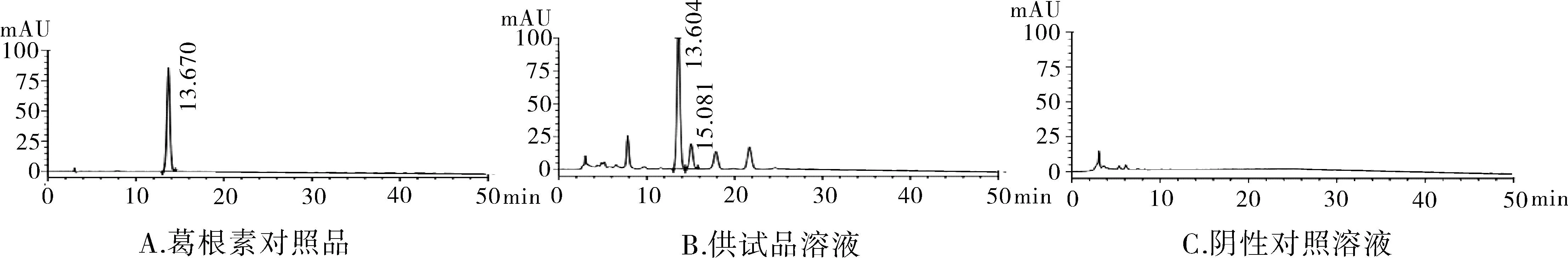
图4 专属性试验
。
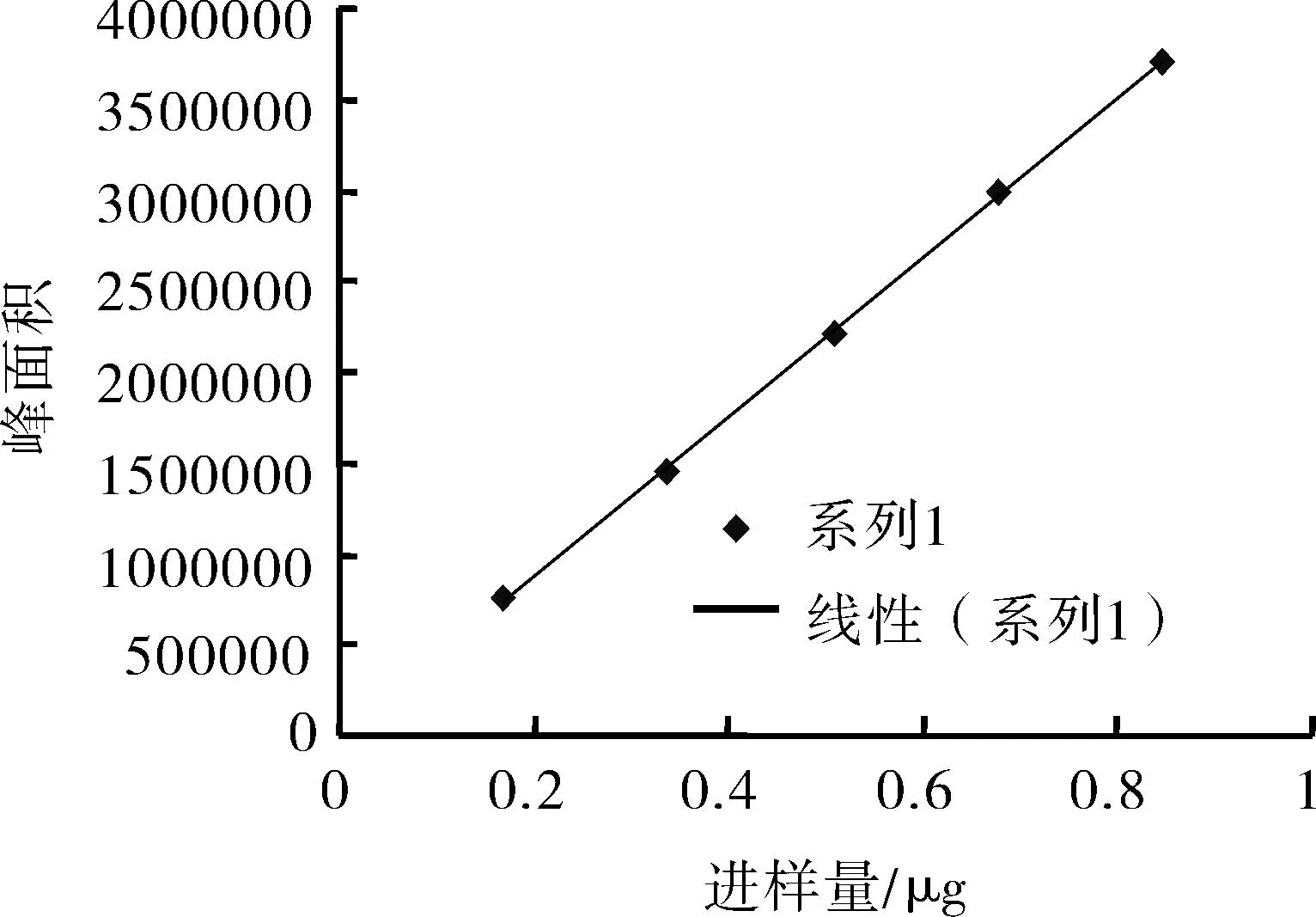
图5 葛根素标准曲线图
3.6稳定性试验取芪精愈消胶囊(批号:20140603),按“3.3.2”法制成供试液。分别在配制后0、4、8、12、24 h进样,测得葛根素的峰面积。结果葛根素平均峰面积2 921 813,RSD=1.49%,表明在24 h内样品较稳定。
3.7精密度试验取浓度为0.084 68 g·L-1的对照品溶液,连续进样6次,每次5 μL,记录峰面积值。结果葛根素的平均峰面积为1 849 360,RSD=1.56%,表明该仪器精密度能满足试验要求。
3.8重复性试验取芪精愈消胶囊(批号:20140603)样品6份,按“3.2”条件进样测定。由标准曲线求得葛根素的含量。结果样品平均含量为每粒3.54 mg,RSD=1.36%,表明方法重现性较好。
3.9加样回收试验取芪精愈消胶囊(批号:20140603,含量:0.962 0%)样品适量,精密加入一定量的葛根素对照品,按“3.3.2”法制成供试品溶液,再按“3.2”条件测定[10-13],结果见表1。样品的平均回收率为99.36%,RSD=0.98%。表明样品回收率良好,方法准确度较高。
3.10样品测定及含量限度的确定 对投料的葛根药材及三批成品制剂进行含量测定,计算转移率,结果见表2。
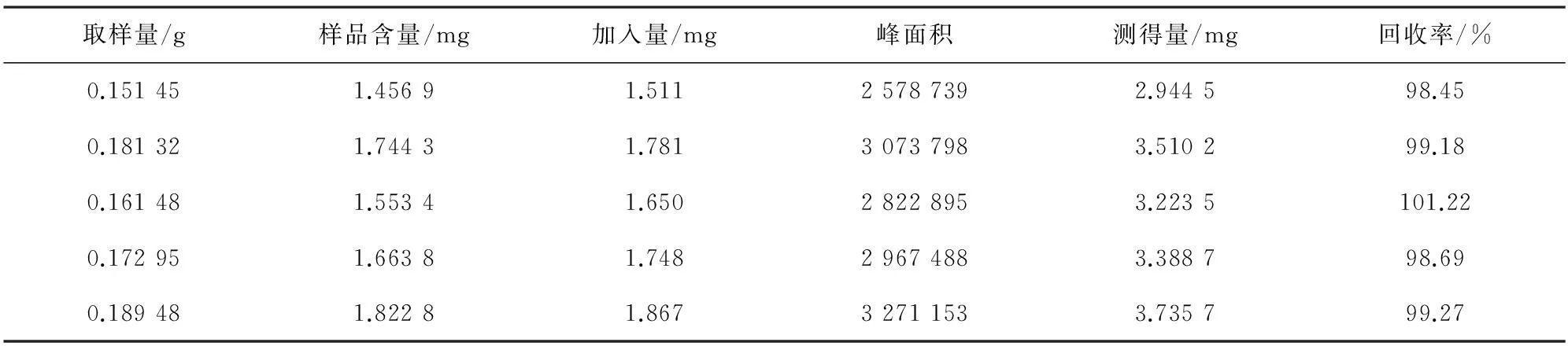
表1 加样回收试验
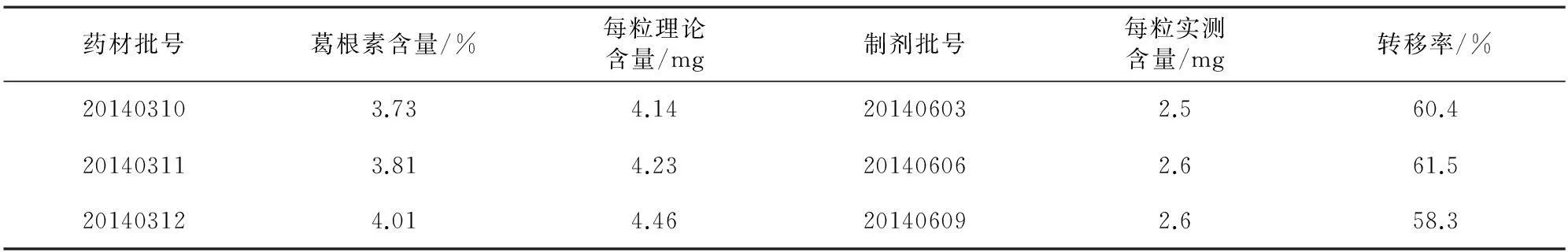
表2 葛根素转移率试验
不同批次药材含量测定结果表明,葛根素含量分别为3.73%、3.81%、4.01%,处方中每粒含葛根生药0.111 1 g,则制剂中理论葛根素含量分别为每粒4.14、4.23、4.46 mg,葛根素转移率分别为60.4%、61.5%、58.3%。《中国药典》2015年版一部葛根含量限度为2.4%(24 mg·g-1),则成品理论最低含量为每粒2.67 mg。根据转移率计算,制成制剂后成品含量限度为每粒1.57~1.64 mg。经多批制剂含量测定结果及生产实际,葛根素含量限度暂定为不少于每粒2.0 mg。
4结果与讨论
试验对处方中葛根、黄精等药味进行了鉴别研究。但葛根素阴性有干扰,黄精供试品分离效果较差,故质量标准暂仅收录了黄芪与五味子的薄层鉴别,其他鉴别有待进一步研究。
在含量测定供试品溶液的制备中,为了充分提取样品中的葛根素,采取同一批样品,分别超声和回流提取处理。测定结果表明二者含量相差不大,而超声更方便,故选择超声提取。而在超声提取的过程中,又考察了提取溶剂甲醇、乙醇和处理时间10、20、30 min的影响。结果表明以甲醇为溶剂,超声处理20 min,提取效果最佳。
试验中进行了系统适用性与耐用性考察。薄层鉴别分别考察了不同厂家薄层板、不同人员及不同实验室的影响,结果方法重现性较好,耐用性强。含量测定分别考察了分离度、重复性、流动相比例的变化、不同色谱柱及柱温的影响。结果分离度均>1.5,重复性RSD=0.69%,故流动相比例的变化、柱温对含量测定的影响不大;不同色谱柱仅保留时间有所不同,分离度、不对称性均符合要求。表明方法分离度高,重复性好,耐用性较强。
试验中以甲醇—水系统为流动相时,峰形拖尾严重。而在水相中加入适量磷酸后,峰形改善明显,拖尾因子在合适的范围内,说明pH值对测定有一定的影响。通过对不同浓度的磷酸溶液的考察,最终选择甲醇—0.4%磷酸系统作为流动相。
试验中的鉴别及含量测定方法简便快速,重现性好,可用于本制剂的质量控制,为新制剂的注册提供试验依据及质量标准。
参考文献:
[1]高辉,李晓燕,李冰,等.归脾丸质量标准研究[J].药学研究,2015,34(5):276-279.
[2]郑永萍,江先合,施文平.丹参五味子片的薄层色谱鉴别[J].中国现代药物应用,2014,8(5):3-4.
[3]国家药典委员会.中国药典(一部)[S].北京:中国医药科技出版社,2015:333.
[4]任少伟,张文成,李兵,等.HPLC法测定葛根超细粉葛根素含量[J].包装与食品机械,2014,32(3):67-69.
[5]李晓娟.反相高效液相色谱法测定护肝胶囊中葛根素含量[J].中国药业,2014,23(23):53-54.
[6]刘丽,李军,訾慧,等.保肝颗粒中葛根素含量测定方法研究[J].现代中医药,2015,35(5):186-187.
[7]李建华,胡倩,申庆亮,等.HPLC法测定升麻葛根颗粒中葛根素的含量[J].中医研究,2012,25(8):67-69.
[8]刘振东,段广珍.心血宁胶囊中葛根素含量测定[J].辽宁中医药大学学报,2014,16(4):46-47.
[9]刘利敏,胡译方.HPLC法同时测定葛根芩连片中黄芩苷和葛根素的含量[J].安徽医药,2012,16(11):1598-1600.
[10] 温金莲,郭丽冰,周清,等.保济丸中葛根素的含量测定及灭菌方法评价[J].中国实验方剂学杂志,2011,17(23):1-4.
[11] 崔明超,程斌,陈宏降,等.玉涎胶囊的质量标准研究[J].安徽医药,2014,18(5):815-819.
[12] 孙丹丹,闫雪生,李岩.菊葛天麻颗粒质量标准研究[J].中国实验方剂学杂志,2012,18(8):86-88.
[13] 田崇梅,王磊,李晓双,等.高效液相色谱法测量醒酒泡腾片中葛根素的含量[J].牡丹江医学院学报,2013,36(1):38-40.
《安徽医药》为月刊,每期定价12.00元,全年144.00元
欢迎投稿,欢迎订阅,邮发代号:26-175
Study on TLC identification and content determination of qijing yuxiao capsules
XU Guang-hua,WANG Hu,LI Xiao-wei,et al
(DepartmentofPharmacy,TaiheTraditionalChineseMedicineHospital,Taihe,Anhui236600,China)
Abstract:ObjectiveTo establish the quality standard of qijing yuxiao capsules. MethodsThe TLC method was used to identify schisandra chinensis,and astragalus membranaceus.HPLC method was used to determine the contents of puerarin. The optimal conditions of the separation and detection were achieved on a Agilent C18 column with a mobile phase consisting of methanol-0.4% phosphoric acid solution(25∶75) at the detective wavelength of 250 nm. Results TLC spots of radix astragalus and schisandra chinensis were clear and negative without interference, which can be used as qualitative method. The contents of puerarin had a good linear relation with peak area(r=0.999 9), when ranging from 0.169 4~0.846 8 μg. and equation was A=4375 947C+1 708.The average recovery of puerarin was 99.36% and RSD was 0.98%(n=5).Conclusion The method is simple,with good specificity and reproducibility,and can be used as the quality control for this preparation.
Key words:qijing yuxiao capsules;schisandra chinensis;astragalus membranaceus;root of kudzu vine;puerarin
(收稿日期:2015-09-30,修回日期:2016-02-10)
doi:10.3969/j.issn.1009-6469.2016.04.012
通信作者:陈刚,男,副主任中药师,研究方向:医院中药制剂的工艺和质量标准研究,E-mail:395522179@qq.com
