水处理提高MOF-199催化苯羟基化反应性能
2016-05-17刘艳凤张天永吴武斌李彬周政周浩浩海南大学材料与化工学院海南海口5708天津大学化工学院天津30007
刘艳凤,张天永,吴武斌,李彬,周政,周浩浩(海南大学材料与化工学院,海南 海口5708;天津大学化工学院,天津30007)
水处理提高MOF-199催化苯羟基化反应性能
刘艳凤1,2,张天永2,吴武斌2,李彬2,周政1,周浩浩1
(1海南大学材料与化工学院,海南 海口570228;2天津大学化工学院,天津300072)
摘要:以一水合乙酸铜和均苯三酸为原料,采用常温搅拌法合成金属有机框架化合物MOF-199,用XRD、IR、BET对其表征。将MOF-199用水处理后作为催化剂用于苯羟基化反应,考察了催化剂的用量、反应温度、反应时间、双氧水添加量对催化反应的影响。较优反应条件为:MOF-199(140mg,0.23mmol)、乙腈4mL、苯1.1mL、H2O23.3mL,在60℃的水浴中反应30min,所得苯的氧化物的产率为23.3%,苯酚的选择性为53.1%,转化频率(TOF值)为25.0h−1。水处理显著提高了MOF-199的催化活性,并形成了一种新的氧化模式,在一定程度上保护了MOF-199的框架结构。
关键词:金属有机框架化合物; MOF-199; 水合物; 苯; 催化
第一作者:刘艳凤(1980—),女,实验师,从事工业催化的研究。E-mail lyfvip@tju.edu.cn。联系人:李彬,副教授,从事工业催化和精细化工的研究。E-mail libin@tju.edu.cn。
苯的不饱和碳碳键的氧化在有机化工中间体合成中起着重要的作用。苯的稳定性高,难以活化,苯环中C—H键活化解离能(111kcal/mol,1kcal/mol=4.18kJ/mol)比一般烷烃(90~101kcal/mol)高,甚至比甲烷(105kcal/mol)还高[1],故常导致芳烃原料转化率低;同时,产物过氧化引起副反应,会导致反应选择性降低。以H2O2、O2为氧化剂由苯一步合成苯的氧化产物受到广泛关注[2],而此过程的关键是寻找催化性能优良、原子经济性高的催化剂。目前,含有铁、锰、钒、铜的金属复合物[3-7]、载有金属的分子筛[8-9]、杂多酸[10]等作为催化剂或催化剂载体用于苯羟基化反应中取得了不同的进展。其中,含有铜的催化剂,如Cu2(OH)PO4、[CuICuICuI(L)]1+簇合物(L为多齿型配基)表现出了良好的催化性能[11-12]。
金属有机框架配合物(metal-organic frameworks,MOFs)是一类有机-无机杂化材料,是由金属离子或金属簇[13]和芳香族及其衍生物或氮的杂环化合物等有机配体[14-17]通过配位键及其他弱的作用方式形成的具有高度规整的网状结构的新型多孔配位化合物。与传统的催化剂相比,MOFs具有多种多样的骨架结构、更大的比表面积和较高的热化学稳定性,同时,它兼具了金属离子和有机配体的两者功能性特点,适用于多种催化反应。目前,MOFs材料已经用于氧化[18]、氢化[19]、克脑文盖尔缩合[20]、Suzuki偶联反应[21]、酯交换反应[22]、催化裂化[23]和醛醇缩合[24]等许多催化反应。
金属有机框架化合物MOF-199又称为HKUST-1,其化学式为Cu3(C9H3O6)2或Cu3(BTC)2,BTC-H3为均苯三酸;它是由铜离子和多齿型有机配体均苯三酸通过配位反应制备的具有面心立方晶体结构的配位聚合物,包含轮桨式次级结构单元[Cu2(O2CR)4](R是一个芳环),这些次级结构单元相互交错连接形成三维网状结构[25]。MOF-199结构中的金属活性位点与易离去的客体小分子或配体离子作用处于饱和状态,经活化后,可除去这些小分子,使得活性位点裸露,实现不饱和金属活性位点催化反应。因此,含有不饱和铜Lewis酸活性位点的MOF-199是催化芳烃的氧化反应[26-27]、Aza-Michael反应[28]、乌尔曼缩合反应[29]的有效催化剂。在本论文中,将MOF-199样品分散在水中,在超声波作用下使其对水充分吸附直至变成浅蓝色的絮状,离心去水后用于苯的羟基化反应;相比于直接将MOF-199用于此反应,水处理过后的MOF-199表现出更高的催化活性。水分子在MOF-199孔道及表面的吸附避免了催化剂活性位点与双氧水的直接接触,使得催化剂在苯的催化过程中不易被破坏。
1 实验部分
1.1主要仪器和试剂
仪器:D8 Advance 多晶衍射仪器(德国Bruker公司),S-4800扫描电子显微镜(日本Hitachi公司),TENSOR27傅里叶变换红外光谱仪器(德国Bruker公司),KQ3200B超声清洗机(昆山市超声仪器有限公司),GC9890气相色谱仪(上海灵华仪器有限公司)。
原料及试剂:均苯三酸(BTC,纯度98%)购买于萨恩化学技术(上海)有限公司;乙酸铜[Cu(OAc)2·H2O]、苯、三乙胺、N,N-二甲基甲酰胺(DMF)、乙醇、二氯甲烷、氯苯全部为分析纯,乙腈(色谱纯)购买于天津市光复科技发展有限公司;H2O2(质量分数30%)购于天津市江天化工技术有限公司。
1.2催化剂的制备
依照参考文献[30]的合成方法制备催化剂:均苯三酸(500mg,2.38mmol)溶解在12mL体积比为1∶1∶1的DMF、乙醇和H2O的混合溶液中。Cu(OAc)2·H2O(860mg,4.31mmol)溶解在12mL同样的溶剂中。将均苯三酸溶液加到乙酸铜溶液中,边加边搅拌,再加0.5mL三乙胺后继续搅拌23h。过滤,用2×25mL的DMF洗涤,收集样品,将样品浸泡在50mL的DMF过夜。第二天,用3×50mL的二氯甲烷洗涤,再用50mL二氯甲烷浸泡过夜,抽滤,所得样品在真空干燥箱中干燥。对所得产物进行XRD、IR、BET表征。
1.3催化剂的表征
X射线粉末衍射(XRD)在德国Bruker公司 D8 ADVANCE 多晶粉末衍射仪上进行,测试条件为Cu靶(λ=1.5418Å,1Å=0.1nm),在室温条件下,以2θ步长为0.01°/min的扫描速度在3°~50°范围内进行扫描。红外光谱(IR)测试采用溴化钾压片法在德国Bruker公司TENSOR27型傅里叶变换红外光谱仪器上进行。样品的比表面积和孔径分布在美国Quantachrome 公司Autosorb-1 型吸附分析仪上测定,测量前样品在200℃真空脱气6h,利用BET法计算比表面积,BJH法计算平均孔径。
1.4催化性能评价
催化剂MOF-199(140mg,0.23mmol)加入到50mL的离心管中,加水24mL,超声1h(超声功率:150W),离心除水,所得催化剂命名为MOF-199(H2O);用4mL乙腈将MOF-199(H2O)移入50mL单口瓶中,向单口瓶依次加入苯1.1mL,双氧水3.3mL,冰水浴中搅拌2~5min,再将单口瓶置于60℃水浴中进行反应,冰水回流冷凝,反应30min,冰水冷却5~10min,加入氯苯作为内标。产物在6000r/min下离心后,收集上层清液,用气相色谱仪进行苯氧化产物含量的测定[见式(1)、式(2)]。检测条件:色谱柱OV-1701(30m×0.25mm)毛细管柱;程序升温:80~160℃,升温速率10℃/min,160~280℃,升温速率30℃/min,在280℃保留3min;氢火焰(FID)检测器,进样口温度300℃,检测器温度320℃。产物中各组分含量采用内标法计算。

2 结果与讨论
2.1催化剂的表征
2.1.1MOF-199 的XRD图谱
MOF-199粉末XRD分析数据见图1。在室温条件下,以2θ步长为0.01°/min的扫描速度得到衍射数据:光谱用晶面距d值表示在约3.042Å、3.109Å、3.428Å、3.687Å、3.802Å、4.397Å、4.654Å、5.068Å、5.392Å、6.043Å、6.601Å、7.609Å、9.438Å、13.219Å、15.303Å处有衍射峰。有文献[25]报道MOF-199约在3.037Å、3.108Å、3.429Å、3.694Å、3.797Å、4.383Å、4.650Å、5.067Å、5.379Å、6.051Å、6.602Å、7.614Å、9.333Å、13.261Å、15.247Å处有衍射峰,用室温搅拌法得到的化合物与文献[31]一致,可以确定合成的产品为MOF-199。
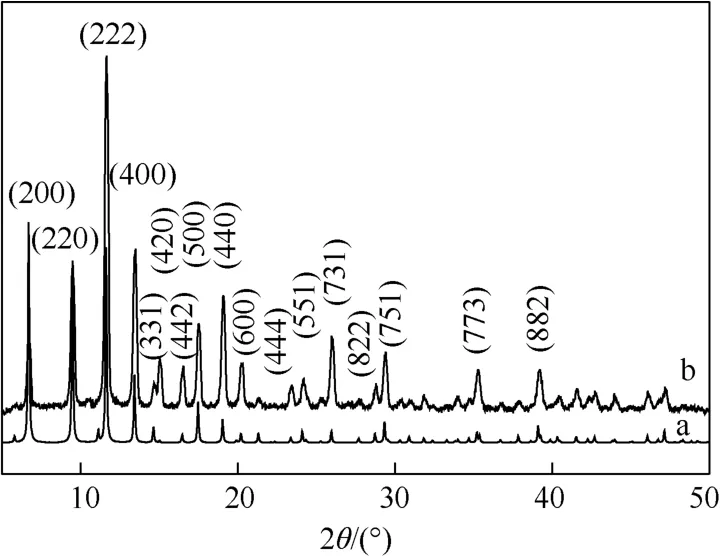
图1 MOF-199的XRD图谱
2.1.2红外检测MOF-199 的IR图谱
从图2中BTC的谱图可以看出,在1607cm−1和1454cm−1处的吸收峰为苯环骨架上C=C的伸缩振动吸收峰;而在3086cm−1和3003cm−1处的吸收峰为苯环上=C—H的伸缩振动吸收峰。在1722cm−1、1193cm−1和919cm−1处的吸收峰,分别为C=O、C—O、O—H的伸缩振动吸收峰,说明BTC中确实有羧基基团。在3200~2500cm−1处出现大而宽的吸收峰,为BTC中的羧基基团形成氢键的缘故。与BTC相比,图2中,MOF-199在1632cm−1处有O=C—O的反对称伸缩振动吸收峰,在1374cm−1处有O=C—O的对称伸缩振动吸收峰[28,32]。另外,760cm−1吸收峰的出现是因为苯环上链接的铜氧取代基团,而1110cm−1弱吸收峰的出现是因为C—O—Cu的伸缩振动[33]。

图2 BTC和MOF-199的红外图谱
2.1.3MOF-199的比表面积及孔径分布
室温搅拌合成的MOF-199不属于典型的IV型,在p/p0接近0的低压区有明显的吸附,证明有微孔存在;在相对压力大于0.7时出现一个滞后环,表明MOF-199有中孔结构,见图3(a)。由图3(b)可见,除了微孔外,脱附曲线得到的孔径分布较窄,孔径主要分布在5~7nm范围内,进一步证明了MOF-199具有介孔结构。常温搅拌合成的MOF-199,BET比表面积为927.8m2/g,朗格缪尔比表面积为1424m2/g,在p/p0= 0.9956时其总孔体积为1.182cm3/g;而采用溶剂热法合成[25]的MOF-199的BET比表面积为692.2m2/g,朗格缪尔比表面积为917.6m2/g,单点总孔体积为0.333cm3/g。显然,MOF-199的比表面积和孔体积的大小受到合成方法的影响,相比于溶剂热合成法,室温搅拌法更有利于合成比表面和孔体积都较大的MOF-199。
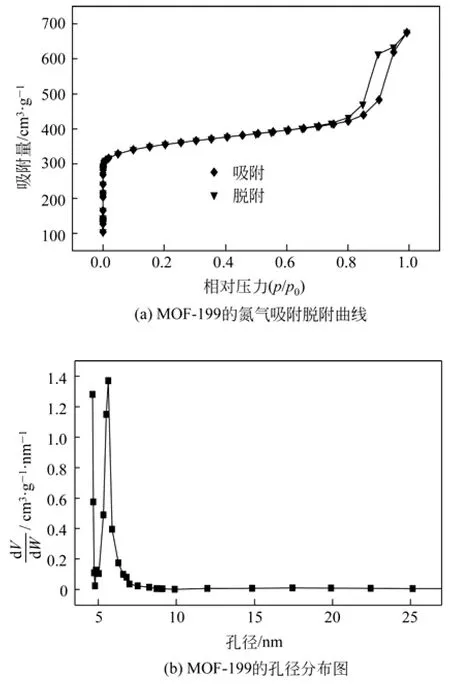
图3 MOF-199的氮气吸附脱附曲线与孔径分布图
2.2不同因素对苯羟基化反应的影响
2.2.1催化剂添加量的影响
将不同量的催化剂用水超声处理1h后,除水用于苯羟基化反应。乙腈4mL、苯添加量为1.1mL,、双氧水3.3mL、60℃水浴中进行反应30min。从表1可以看出,催化剂添加量为80mg时,苯酚和苯醌的选择性最高,分别为61.5%和28.7%;随着催化剂用量的增加,苯酚和苯醌的选择性逐渐降低,与此同时邻苯二酚和对苯二酚的选择性逐渐增加,当催化剂用量增加到140mg时,苯酚和苯醌的选择性分别下降到53.1%和3.5%,对苯二酚的选择性增加到25.3%,此时苯氧化物的产率最高为23.3%;继续增加催化剂的用量到160mg,苯氧化物的产率反而降低,可能是催化剂添加量过高使得产物进一步分解。综合考察苯氧化物的产率和苯酚的选择性,其中当催化剂用量为140mg时,整个体系催化效果较好。
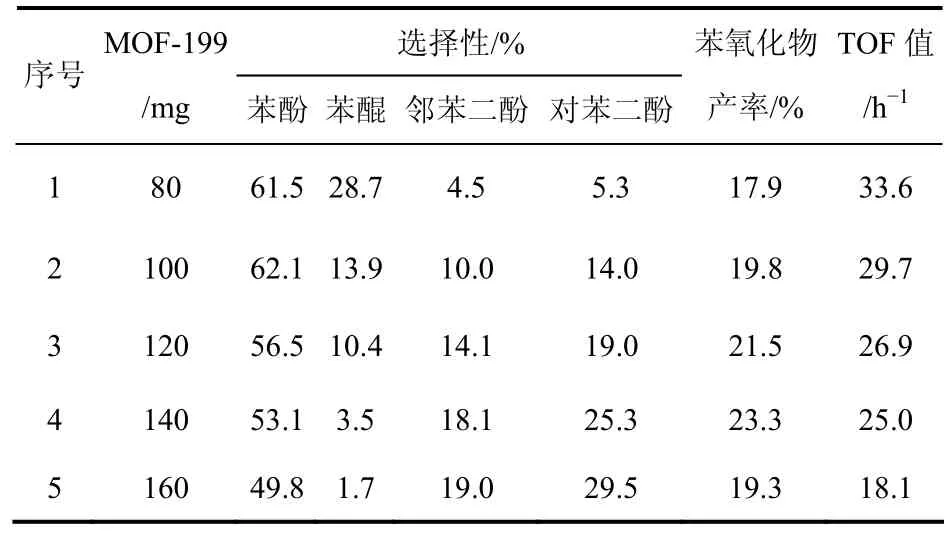
表1 催化剂添加量对苯的羟基化反应的影响
2.2.2反应时间的影响
考察反应时间对目标产物收率的影响。140mg的催化剂水处理后用于催化反应,乙腈4mL,苯添加量为1.1mL,双氧水3.3mL,60℃水浴中进行反应,反应时间分别为15min、30min、45min、60min进行反应。由表2可见,反应进行15min时,苯氧化物的产率为20.8%,苯酚的选择性为62.1%,此时反应后的混合物可以使得淀粉碘化钾试纸变为淡蓝色,说明反应体系中还有微量的H2O2。延长反应时间至30min,苯氧化物的产率为23.3%,苯酚的选择性为53.1%,此时反应后的混合物不能使淀粉碘化钾试纸变蓝,说明H2O2已经在反应过程中消耗完了。继续延长反应时间至45min、60min,苯氧化物的产率基本不变,而产物中苯醌、对苯二酚的选择性明显增加。可见,反应时间过短,反应进行得不彻底;反应时间过长,可能使得产物中的苯酚进一步氧化,不利于提高苯酚的选择性。当反应时间为30min时,苯氧化物的产率较高,苯酚的选择性相对也较高。

表2 反应时间对苯羟基化反应的影响
2.2.3反应温度的影响
考察反应温度对苯羟基化反应的影响,140mg的催化剂水处理后用于催化反应,乙腈4mL,苯添加量为1.1mL、双氧水3.3mL、水浴温度分别为30℃、40℃、50℃、60℃、70℃,反应30min,结果如表3所示。
由表3可以看出,苯氧化物的产率随反应温度的提高呈上升趋势,当反应温度为60℃时苯氧化物的产率最高为23.3%,此时TOF值为25.0h−1;继续增加反应温度到70℃,此时苯氧化物的产率降低到13.4%,相应的TOF值为14.4h−1。造成这种现象的原因是,较高的反应温度有利于苯的催化反应,但当温度过高时,剧烈的化学反应和较高的温度加速了H2O2的降解,H2O2的快速降解不利于苯氧化物的生成。在30℃时苯醌的选择性较高,可达66.1%,随着反应温度的升高,苯醌的选择性逐渐降低,邻苯二酚和对苯二酚的选择性逐渐增加,苯酚的选择性先增加后降低,造成这种现象的原因需要进一步进行分析验证。当反应温度为60℃时,苯氧化物的产率和苯酚的选择性相对都较高。

表3 反应温度对苯羟基化反应的影响
2.2.4双氧水添加量的影响
考察双氧水用量对苯羟基化反应的影响。MOF-199催化剂140mg,经过水处理后用于催化反应。4mL乙腈为溶剂,苯1.1mL,在60℃水浴中分别与1.1mL、2.2mL、3.3mL、4.4mL、5.5mL、6.6mL、7.7mL、8.8mL、9.9mL的H2O2(质量分数30%)反应30min,结果如表4所示。
由表4可见,随着双氧水用量增多,苯氧化物的产率缓慢增加,苯酚的选择性逐渐降低,双氧水
添加量为3.3mL、4.4mL、5.5mL、6.6mL时苯氧化物的产率较高,分别为23.3%、23.6%、23.5%、23.7%,其相应苯酚的选择性依次为53.1%、47.8%、47.3%、41.5%;当双氧水用量达到7.7mL时,苯氧化物的产率陡然下降为6.8%,而苯酚的选择性相比双氧水用量6.6mL时有所增加,由41.5%增加到51.9%。继续增加双氧水的用量到8.8mL、9.9mL,其苯氧化物的产率相对较低,分别为6.4%、6.2%。由此可见,双氧水的添加量对苯羟基化反应有一定的影响,当添加量过多时,反应剧烈,一方面双氧水快速分解,而另外一方面剧烈的化学反应促使产物中有效成分苯酚、苯醌、邻苯二酚、对苯二酚的分解。综合苯的转化率与苯酚的选择性考虑,苯和双氧水的最佳体积比为1.1∶3.3。

表4 双氧水添加量对苯的羟基化反应的影响
2.2.5水处理对催化剂性能的影响
将MOF-199和水处理的MOF-199(H2O)作为催化剂用于苯羟基化反应的效果,两种催化剂都反复使用三次,比较其催化效果。催化剂140mg,4mL乙腈为溶剂,苯1.1mL、H2O2(质量分数30%)5.5mL,60℃水浴反应30min,用气相色谱检测产物中有效成分的含量,收集催化剂用乙腈洗涤后再次循环利用。
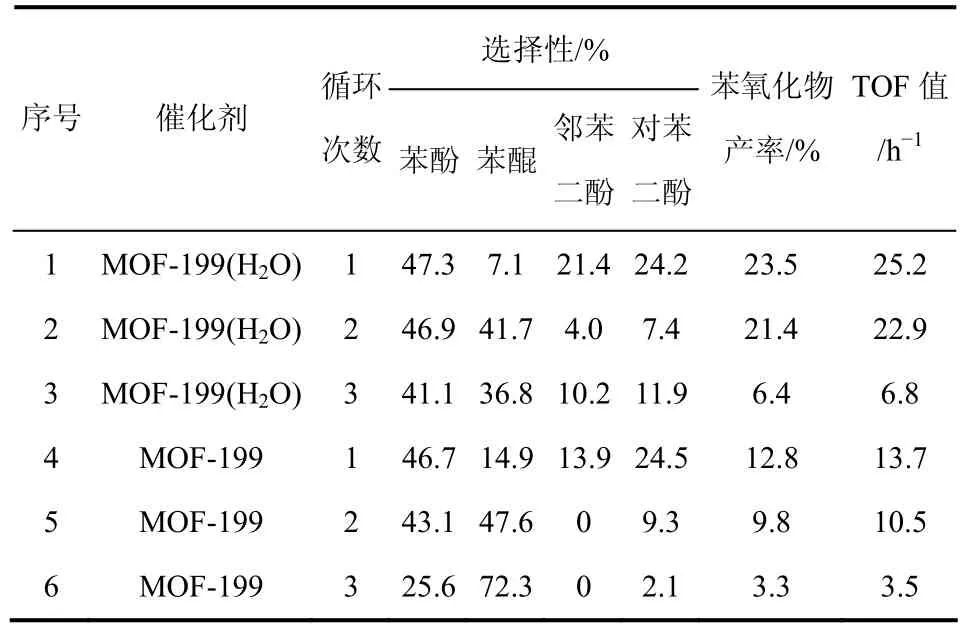
表5 水处理对MOF-199催化性能的影响
为了证实水处理对MOF-199的催化活性有促进作用和催化剂的稳定性有保护作用,在两种催化剂进行循环实验时,加大双氧水添加量至5.5mL。由表5可见,MOF-199(H2O)的催化活性显然高于MOF-199。MOF-199(H2O) 为催化剂时,第一次循环时苯氧化物的产率为23.5%;MOF-199为催化剂时,第一次循环时苯氧化物的产率为12.8%;同样,在每次催化循环过程中,MOF-199(H2O)为催化剂得到的苯氧化物的产率总是高于以MOF-199为催化剂的苯氧化物的产率,可见MOF-199(H2O)催化活性都远高于MOF-199。MOF-199(H2O)第一次催化后仅有微量的催化剂转化为草酸铜,而MOF-199第一次催化后全部转化为草酸铜,见图4(a)中曲线c和图4(b) 中曲线c。MOF-199(H2O)第二催化后仍有大部分催化剂保持原有的晶体结构,MOF-199(H2O)第三催化后才全部转化为草酸铜。相比于MOF-199用于苯羟基化反应,水处理明显提高了MOF-199催化活性和稳定性。若反应体系中减少H2O2的添加量,MOF-199(H2O)的循环利用次数明显增加。
2.2.6催化机理的探讨
MOF-199暴露在空气中一段时间,其裸露的铜金属活性位点即可与水结合。为了加快水与MOF-199的作用,将MOF-199浸泡在水中,并对其进行超声处理,水处理过的催化剂活性明显增强。水处理后,MOF-199由原来的颗粒状变为絮状,其孔道及表面都充满了水。水处理后的MOF-199在苯氧化反应中活性明显增强的原因可能为:一方面,与MOF-199通过物理吸附或化学吸附的水可能会与反应物苯形成O—H··π 键[34-35],此键的形成加速了苯与金属活性位点的接触;另一方面,在苯催化反应过程中,双氧水更容易取代与MOF-199铜活性位点结合的水,双氧水与金属活性位点结合后迅速形成Cu=O键,苯通过图5中a或b的一条途径与Cu=O键作用而生成苯酚,具体可能的反应路径见图5。
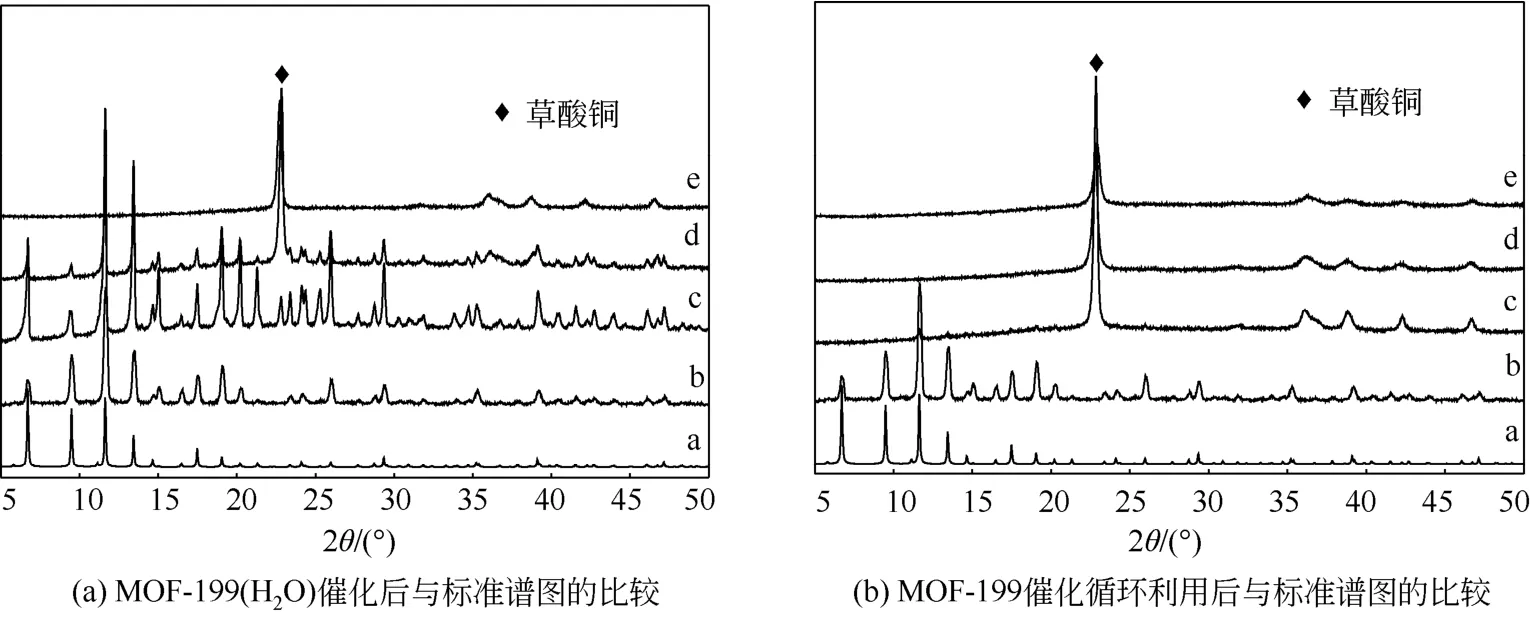
图4 MOF-199的XRD图谱
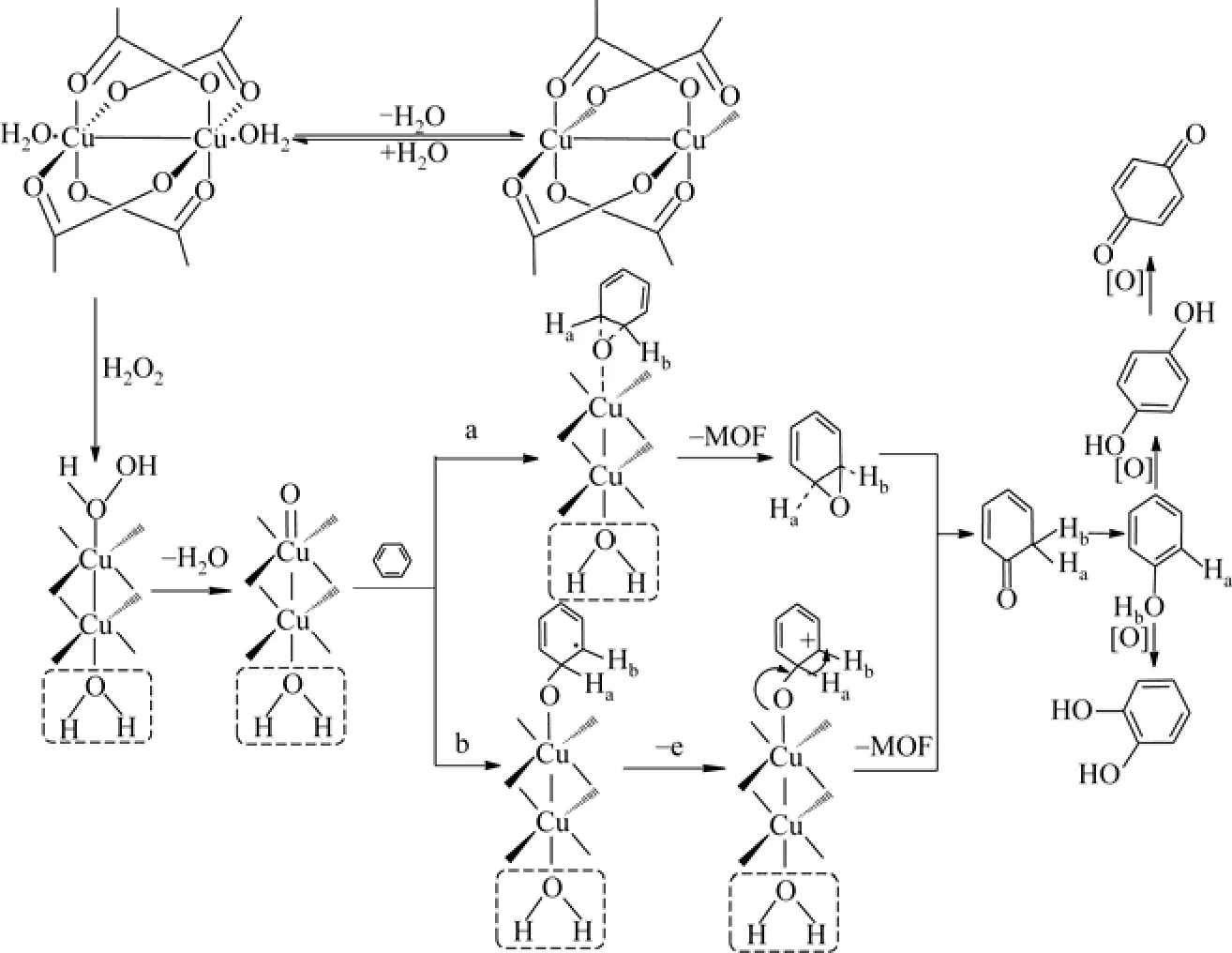
图5 水处理后的MOF-199用于苯氧化反应的可能路径
3 结论
MOF-199经过水处理后,将其用于催化苯制备苯的氧化物的反应中表现出了较高的催化活性。较优的反应条件为:140mg的MOF-199经过水处理后加入到4mL乙腈中,再与1.1mL苯和3.3mL双氧水混合后,60℃反应30min,得到苯的氧化物的产率为23.3%,苯酚的选择性为53.1%。实验还表明,水处理后的MOF-199用于催化反应中其催化活性和结构稳定性明显增强。可能的原因是反应物苯与吸附在MOF-199的水形成O—H··π 键,此键的形成加速了苯与金属活性位点的接触;在苯催化反应过程中双氧水更容易取代与MOF-199铜活性位点结合的水,双氧水与金属活性位点结合后迅速形成Cu=O键,加速了苯酚的生成。
参考文献
[1]MAYER J M. In biomimetic oxidations catalyzed by transition metal complexes[M]. London:Imperial College Press,2000.
[2]NIWA S I,ESWARAMOORTHY M,NAIR J,et al. A one-step conversion of benzene to phenol with a palladium membrane[J]. Science,2002,295(5552):105-107.
[3]RABA A,COKOJA M,HERRMANN W A,et al. Catalytic hydroxylation of benzene and toluene by an iron complex bearing a chelating di-pyridyl-di-NHC ligand[J]. Chemical Communications,2014,50:11454-11457.
[4]ZHAO L M,LIU Z C,GUO W Y,et al. Theoretical investigation of the gas-phase Mn+- and Co+-catalyzed oxidation of benzene by N2O[J]. Physical Chemistry Chemical Physics,2009,11(21):4219-4229.
[5]YANG H,WU Q,LI J,et al. Direct synthesis of phenol from benzene catalyzed by multi-V-POMs complex[J]. Applied Catalysis A:General,2013,457:21-25.
[6]WANG X,ZHANG T Y,YANG Q,et al. Synthesis and characterization of bio-inspired diiron complexes and their catalytic activity for direct hydroxylation of aromatic compounds[J]. European Journal of Inorganic Chemistry,2015,5:817-825.
[7]WANG Y H,ZHANG T Y,LI B,et al. Synthesis,characterization,electrochemical properties and catalytic reactivity of N-heterocyclic carbene-containing diiron complexes[J]. RSC Advances,2015,5:29022-29031.
[8]ENE A B,ARCHIPOV T,RODUNER E. Competitive adsorption and interaction of benzene and oxygen on Cu/HZSM5 zeolites[J]. The Journal of Physical Chemistry C,2011,115(9):3688-3694.
[9]HU L,YUE B,CHEN X,et al. Direct hydroxylation of benzene to phenol on Cu-V bimetal modified HMS catalysts[J]. Catalysis Communications,2014,43:179-183.
[10]ALEKAR N A,INDIRA V,HALLIGUDI S B,et al. Kinetics and mechanism of selective hydroxylation of benzene catalysed by vanadium substituted heteropolymolybdates[J]. Journal of Molecular Catalysis A:Chemical,2000,164(1/2):181-189.
[11]XIAO F S,SUN J M,MENG X J,et al. A novel catalyst of copper hydroxyphosphate with high activity in wet oxidation of aromatics[J]. Applied Catalysis A:General,2001,207(1/2):267-271.
[12]NAGABABU P,MAJI S,KUMAR M P,et al. Efficient room-temperature oxidation of hydrocarbons mediated by tricopper cluster complexes with different ligands[J]. Advanced Synthesis & Catalysis,2012,354(17):3275-3282.
[13]FURUKAWA H,CORDOVA K E,O’KEEFFE M,et al. The chemistry and applications of metal-organic frameworks[J]. Science,2013,341:974-986.
[14]陈恒,陈绍云,苑兴洲,等.咪唑衍生物辅助合成金属有机骨架MI L-101及 CO2吸附性能[J]. 化工进展,2014,33( 7):1808-1815.
[15]AN J,GEIB S J,ROSI N L. High and selective CO2uptake in a cobalt adeninate metal-organic framework exhibiting pyrimidine- and amino-decorated pores[J]. Journal of the American Chemical Society,2010,132(1):38-39.
[16]农洁静,赵文波,覃显业,等.金属有机骨架(MOFs)为壳的核壳结构材料研究进展[J]. 化工进展,2015,34( 3):774-783.
[17]MORRIS W,VOLOSSKIY B,DEMIR S,et al. Synthesis,structure,and metalation of two new highly porous zirconium metal-organic frameworks[J]. Inorganic Chemistry,2012,51 (12):6443-6445.
[18]LONG J L,WANG L M,GAO X F,et al. Activation of molecular oxygen by a metal-organic framework with open 2,2'-bipyridine for selective oxidation of saturated hydrocarbons[J]. Chemical Communications,2012,48:12109-12111.
[19]SCHUSTER S,KLEMM E,BAUER M. The role of Pd2+/Pd0in hydrogenation by[Pd(2-pymo)2]n:an X-ray absorption and IR spectroscopic study[J]. Chemistry:A European Journal,2012,18 (45):15831-15837.
[20]HWANG Y K,HONG D Y,CHANG J S,et al. Selective sulfoxidation of aryl sulfides by coordinatively unsaturated metal centers in chromium carboxylate MIL-101[J]. Applied Catalysis A:General,2009,358(2):249-253.
[21]PASCANU V,YAO Q X,GÓMEZ A B,et al. Sustainable catalysis:rational Pd loading on MIL-101Cr-NH2for more efficient and recyclable Suzuki-Miyaura reactions[J]. Chemistry:A European Journal,2013,19(51):17483-17493.
[22]CHIZALLET C,LAZARE S,BAZER-BACHI D,et al. Catalysis of transesterification by a nonfunctionalized metal-organic framework:acido-basicity at the external surface of ZIF-8 probed by FTIR and ab initio calculations[J]. Journal of America Chemistry Society,2010,132(35):12365-12377.
[23]CORMA A,DIAZ-CABANAS M J,JORDA J L,et al. High-throughput synthesis and catalytic properties of a molecular sieve with 18- and 10-member rings[J].Nature,2006,443(7113):842-845.
[24]HORIKE S,DINCǍ M,TAMAKI K,et al. Size-selective Lewis acid catalysis in a microporous metal-organic framework with exposed Mn2+coordination sites[J]. Journal of America Chemistry Society,2008,130(18):5854-5855.
[25]CHUI S S Y,LO S M F,CHARMANT J P H,et al. A chemically functionalizable nanoporous material[Cu3(TMA)2(H2O)]n[J]. Science,1999,283(5405):1148-1150.
[26]YANG H,LI J,WANG L Y,et al. Exceptional activity for direct synthesis of phenol from benzene over PMoV@MOF with O2[J]. Catalysis Communications,2013,35:101-104.
[27]MARX S,KLEIST W,BAIKER A. Synthesis,structural properties,and catalytic behavior of Cu-BTC and mixed-linker Cu-BTC-PyDC in the oxidation of benzene derivatives[J]. Journal of Catalysis,2011,281(1):76-87.
[28]NGUYEN L T L,NGUYEN T T,NGUYEN K D,et al. Metal-organic framework MOF-199 as an efficient heterogeneous catalyst for the aza-Michael reaction[J]. Applied Catalysis A:General,2012,425-426:44-52.
[29]PHAN N T S,NGUYEN T T,NGUYEN C V,et al. Ullmann-type coupling reaction using metal-organic framework MOF-199 as an efficient recyclable solid catalyst[J]. Applied Catalysis A:General,2013,457:69-77.
[30]TRANCHEMONTAGNE D J,HUNT J R,YAGHI O M. Room temperature synthesis of metal-organic frameworks:MOF-5,MOF-74,MOF-177,MOF-199,and IRMOF-0[J]. Tetrahedron,2008,64:8553-8557.
[31]LOERA-SERNA S,OLIVER-TOLENTINO M A,LÓPEZ- NÚŇEZ M L,et al. Electrochemical behavior of[Cu3(BTC)2]metal-organic framework:the effect of the method of synthesis[J]. Journal of Alloys and Compounds,2012,540(5):113-120.
[32]SPECHT C H,FRIMMEL F H. An in situ ATR-FTIR study on the adsorption of dicarboxylic acids onto kaolinite in aqueous suspensions[J]. Physical Chemistry Chemical Physics,2001,3:5444-5449.
[33]HU J,CAI H,REN H,et al. Mixed-matrix membrane hollow fibers of Cu3(BTC)2MOF and polyimide for gas separation and adsorption[J]. Industrial & Engineering Chemistry Research,2010,49(24):12605-12612.
[34]GIERSZAL K P,DAVIS J G,HANDS M D,et al. π-Hydrogen bonding in liquid water[J]. The Journal of Physical Chemistry Letters,2011,2(22):2930-2933.
[35]LIU Y F,ZHANG T Y,WU W B,et al. Water-mediated promotion of direct oxidation of benzene over metal-organic framework HKUST-1[J]. RSC Advances,2015,5:56020-56027.
Enhanced catalytic properties of MOF-199 with water treatment in the direct hydroxylation of benzene
LIU Yanfeng1,2,ZHANG Tianyong2,WU Wubin2,LI Bin2,ZHOU Zheng1,ZHOU Haohao1
(1School of Materials and Chemical Engineering,Hainan University,Haikou 570228,Hainan,China;2School of Chemical Engineering and Technology,Tianjin University,Tianjin 300072,China)
Abstract:Cu(OAc)2·H2O was treated with benzenetricarboxylic acid under stirring to form metal-organic framework MOF-199,which was then characterized by XRD,IR and BET. The obtained MOF-199 was treated with water and then applied for the hydroxylation of benzene as catalyst. The effect factors of MOF-199 amount,reaction temperature,reaction time,H2O2amount on the yield and the selectivity of benzene oxygenates were investigated. Results indicated suitable conditions for the preparation of benzene oxygenates,were that the water-treated MOF-199 (140mg,0.23mmol),acetonitrile (4mL),benzene (1.1mL) and H2O2(3.3mL) were mixed together,and then reacted for 30min at 60℃ in a water bath. The corresponding oxygenates had a yield of 23.3%,the selectivity to phenol of 53.1%,and the turnover frequency(TOF) was 25.0h−1. Pretreatment of MOF-199 catalyst with water significantly accelerated the catalytic oxidation of benzene to the corresponding oxygenates and preserved the metal-organic framework of MOF-199 due to the formation of a new reaction mode.
Key words:metal-organic framework; MOF-199; hydrate; benzene; catalysis
中图分类号:O 625.1
文献标志码:A
文章编号:1000–6613(2016)04–1113–08
DOI:10.16085/j.issn.1000-6613.2016.04.023
收稿日期:2015-07-27;修改稿日期:2015-10-16。
基金项目:国家自然科学基金(21103121,21276187)及海南大学本科生创新创业课题项目。
