最简单的有机化合物——甲烷考点分析
2016-05-14曹东
曹东


考点1甲烷的分子结构
考点说明该考点主要考查甲烷分子的立体结构以及甲烷取代产物分子的立体结构.甲烷是正四面体结构,分子中4个C—H长度、强度相同,夹角相同,分子结构示意图表示为
注意有机化合物的结构式只表示原子之间的连接方式,不表示真实的空间结构.
例1下列有机化合物的分子中,不是正四面体结构的是
A.CH4B.NH+4C.CCl4D.CH2C12
解析根据有机化合的概念,排除B项;正四面体结构中4个共价键的长度、强度相同,夹角相同,CH4是正四面体结构,类比甲烷,推出CCl4是正四面体结构.由于C—H与C—Cl键的长度、强度都相同,因此CH2C12是四面体结构,但不是正四面体结构.
答案D
解法指津甲烷是正四面体结构,甲烷分子中4个H若被4个相同的原子或原子团取代后,其取代产物的结构仍然是正四面体结构,否则只属于四面体结构.
考点2甲烷的化学性质
考点说明该考点主要考查甲烷的化学性质.甲烷的主要反应类型为氧化反应和取代反应.甲烷的氧化反应是指甲烷的燃烧反应:CH4+2O2[FY=]CO2+2H2O,燃烧火焰呈淡蓝色,根据燃烧方程式可以进行简单计算,注意燃烧前后气体体积的变化情况.甲烷的取代反应是指光照条件下甲烷与Cl2发生的反应,简单表示为:CH4+Cl2[FY=]CH3Cl+HCl,进一步反应又生成了二氯甲烷、三氯甲烷和四氯化碳.注意取代反应发生的条件、反应规律以及取代产物的结构与取代产物的某些物理特性.
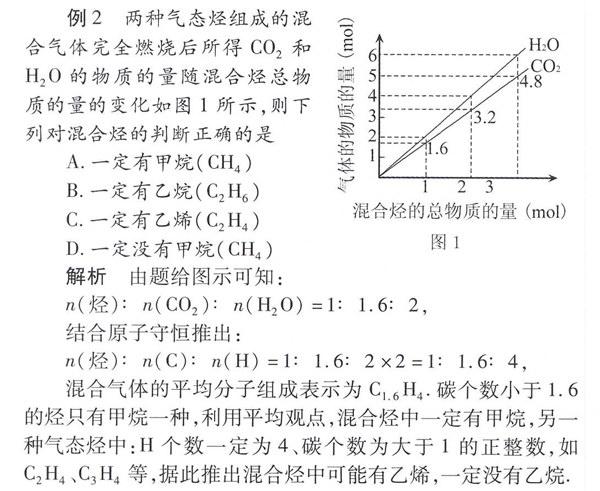
例2两种气态烃组成的混合气体完全燃烧后所得CO2和H2O的物质的量随混合烃总物质的量的变化如图1所示,则下列对混合烃的判断正确的是
A.一定有甲烷(CH4)
B.一定有乙烷(C2H6)
C.一定有乙烯(C2H4)
D.一定没有甲烷(CH4)
解析由题给图示可知:
n(烃)∶n(CO2)∶n(H2O)=1∶1.6∶2,
结合原子守恒推出:
n(烃)∶n(C)∶n(H)=1∶1.6∶2×2=1∶1.6∶4,
混合气体的平均分子组成表示为C1.6H4.碳个数小于1.6的烃只有甲烷一种,利用平均观点,混合烃中一定有甲烷,另一种气态烃中:H个数一定为4、碳个数为大于1的正整数,如C2H4、C3H4等,据此推出混合烃中可能有乙烯,一定没有乙烷.
答案A
解法指津气态烃(设其分子式为CxHy)完全燃烧,反应前后气体体积的变化都只与烃分子中氢原子的数目有关,而与碳原子的数目无关.在水为气态时:
①当y=4时,ΔV=0,反应后气体的体积不变.符合要求的烃有:CH4、C2H4和C3H4.
②当y>4时,ΔV>0,反应后气体的体积增大,分子中氢原子数大于4的气态烃都符合要求.如C2H6、C3H8等.
③当y<4时,ΔV<0,反应后气体的体积减小.气态烃中只有C2H2符合要求.
例3若要将0.6 mol甲烷完全和氯气发生取代反应,并且生成相同物质的量的四种取代物,则需要氯气的物质的量为
A.2.5 molB.4.5 molC.0.6 molD.1.5 mol
解析光照下,甲烷与氯气发生多次取代反应,分别生成CH3Cl、CH2Cl2、CHCl3和CCl4,根据取代反应规律得出每生成1 mol上述有机物消耗氯气依次为1 mol、2 mol、3 mol、4 mol.题知四种取代物的物质的量相等,假设四种取代物的物质的量都为x mol,根据碳原子守恒:
0.6 mol×1=x mol+x mol+x mol+x mol,
解得x=0.15,则发生取代反应的
n(Cl2)=0.15mol×1+0.15mol×2+0.15 mol×3+0.15mol×4=1.5 mol.
答案D
解法指津Cl2与CH4的取代反应,1 mol Cl2只能取代甲烷分子中的1 mol H原子,生成1 mol取代产物和1 mol HCl.结合原子守恒(如C、Cl)能快速解题.
考点3烷烃的性质
考点说明该考点主要考查烷烃的物理性质与化学性质.烷烃的物理性质随分子中碳原子数的增加,其状态、熔点、沸点、相对密度均呈现规律性的变化.烷烃的化学性质与甲烷类似,能发生燃烧反应和取代反应.
例4丁烷广泛应用于家用液化石油气,也用于打火机中作燃料,下列关于丁烷叙述正确的是
A.丁烷的分子式为C4H10,常温下是液体
B.丁烷的沸点小于CH4的沸点
C.丁烷能被酸性高锰酸钾溶液氧化
D.光照下丁烷与氯气发生取代反应,会生成多种不同的取代产物
解析丁烷的分子式为C4H10,常温下是气体,A错误;随烷烃分子中碳个数增加,沸点升高,丁烷的沸点大于CH4的沸点,B错误;根据甲烷不能被酸性高锰酸钾溶液氧化,推出丁烷也不能被酸性高锰酸钾溶液氧化,C错误;丁烷分子中氢原子数目较多,发生取代反应后会生成多种不同的取代产物,D正确.
答案D
解法指津根据烷烃物理性质的递变规律来解答烷烃物理性质的有关问题,类比甲烷的化学性质解答烷烃化学性质的有关问题.注意烷烃的物理性质特点及其递变规律:①烷烃均难溶于水,且密度比水小.②随着碳原子数的增多,熔、沸点逐渐升高,密度逐渐增大.③碳原子数为1~4时,烷烃为气态,当碳原子数≥5时,烷烃为非气态.
考点4同分异构体
考点说明该考点主要考查烷烃同分异构数目的判断以及一元取代产物同分异构体数目的判断.考查丁烷、戊烷、己烷同分异构体的数目,考查烷烃(碳个数小于或等于5)一元取代产物的数目等.
例5现有甲、乙、丙三种烷烃,甲:CH3(CH2)3CH3,乙:CH3CH(CH3)CH2CH3,丙:C(CH3)4,下列相关叙述正确的是
A.甲、乙、丙三者属于同系物关系
B.甲、乙、丙互为同分异构体
C.C4H10有3种同分异构体
D.C5H12表示一种纯净物
解析甲、乙、丙的分子式相同,不符合同系物概念,A错误;甲、乙、丙的分子式相同,碳原子的连接方式(或结构)不同,三者符合同分异构体概念,B 正确;C4H10有2种同分异构体,C错误;C5H12是分子式,它有3种同分异构体,即甲、乙、丙,因此C5H12不能表示一种纯净物,D错误.
答案B
解法指津烷烃从丁烷开始出现了同分异构体现象,烷烃同分异构体数目的判断方法采用记忆法,丁烷、戊烷、己烷同分异构体的数目分别为2种、3种、5种.
例6分子式为C4H9Cl的同分异构体共有(不考虑立体异构)
A.2种B.3种C.4种D.5种
解析C4H9Cl可以看做是C4H10分子中的一个H原子被一个Cl原子取代后的产物.C4H10有CH3CH2CH2CH3、CH3CH(CH3)CH3两种同分异构体,CH3CH2CH2CH3分子中的氢是2种类型,一个H原子被一个Cl原子取代后得到2种同分异构体,CH3CH(CH3)CH3分子中的氢也是2种类型,一个H原子被一个Cl取代后得到2种同分异构体,因此C4H9Cl的同分异构体共有4种.
答案C
解法指津烷烃一元取代物的种类一般根据等效氢法去判断,烷烃分子中若有n种不同的等效氢,其一元取代物就有n种.利用等效氢法判断氢类型时注意:①同一碳原子上的氢为等效氢;②同一碳原子上所连甲基(甲烷分子去掉一个氢原子后剩余部分为甲基,简单表示为—CH3)为等效甲基,等效甲基中的所有氢为等效氢;③处于对称位置的碳原子上的氢原子也为等效氢原子.
