超高效液相色谱串联质谱同时测定雷公藤药材中5个有效成分
2016-05-14胡峻刘超郭兰萍郝庆秀康利平南铁贵刘勇詹志来黄璐琦
胡峻 刘超 郭兰萍 郝庆秀 康利平 南铁贵 刘勇 詹志来 黄璐琦

[摘要]该文建立了超高效液相色谱电喷雾串联三重四级杆质谱同时测定雷公藤药材中5种有效成分的方法,并比较了不同产地及来源的雷公藤药材中5种有效成分的含量差别。以乙腈2%甲酸铵水为流动相洗脱,Waters ACQUITY UPLCCSHC18S柱(21 mm×100 mm,17 μm),以电喷雾离子源为接口, 正离子模式扫描,质谱多反应监测(MRM)模式检测。结果表明,5种有效成分在各自线性范围内线性关系良好(r>0997 8),加样回收率在9672%~1032%,RSD为10%~24%。该研究所建立的方法稳定性、精密度、重复性良好,适用于雷公藤中有效成分的含量测定;不同来源的雷公藤药材中成分含量差异显著,雷公藤药材的质量和安全性亟待提高,而对雷公藤药材实施多指标的含量控制是保证其临床药用安全可控的必要途径。
[关键词]超高效液相色谱电喷雾串联三重四级杆质谱;雷公藤;昆明山海棠;有效成分;含量测定
[Abstracts]This paper is aimed to develop a method for the determination of five effective components in medicinal material of Tripterygium using ultra performance liquid chromalography coupled withelectrospray ionization tandem mass spectrometry(UPLCESIMS/MS), which then was used to study their contents in raw materials from different areas and different sourcesThe separation was performed on a Waters ACQUITY UPLCCSHC18S column(21 mm×100 mm,17 μm), usingacetonitrile02% ammonium formateaqueous solutionas mobile phase The target components were detected in multiplereactionmonitoring(MRM) mode by mass spectrometry with electrospray ionization (ESI) source operated in positive ionization mode The quantitative results showed that good linearity wasachievedin their respective linear ranges and fine determination coefficient (r>0997 8),and the overall recoveries ranged from 9672%1032% with the RSD ranging from 10%24%The methodissensitive and accurate,and suitable for the effective components quantification in medicinal material of Tripterygium; contents of five effective components from different sources vary significantly, so the quality and safety of medicinal material of Tripterygium needs to be improved It is very important to control the quality with multiindex for clinic safety
[Key words]UPLCESIMS/MS; Tripterygium wilfordii; Tripterygium hypoglaucum; effective components; content determination
doi:10.4268/cjcmm20160817
雷公藤属植物是重要的药用植物,民间多做杀虫剂使用,20世纪60年代因试用其治疗麻风反应效果显著,引起广泛关注,并相继开展了系统的研究,发现其有强大的抗炎、免疫抑制、抗肿瘤、抗生育等多种药理作用,目前被广泛在应用于难治的类风湿关节炎、肾病综合症、红斑狼疮、皮肌炎、大疱性皮肤病等,同样对各型银屑病也有显著的疗效[13]。雷公藤与昆明山海棠由于形态特征相近,在民间均做为药用雷公藤的主要来源[45],且两者所含主要的化学成分均为三萜类、生物碱类、二萜内酯类、倍半萜类、有机酸类、蒽醌类、黄酮类、木脂素等[68],其中二萜内酯类成分如雷公藤甲素、雷公藤内酯酮是最主要的活性成分,生物碱类成分如雷公藤晋碱、雷公藤定碱、雷公藤次碱是含量最高的成分。但这些成分既是活性成分,也是有毒成分,时有报道其引起的不良反应[916]。
目前对其质量的评价主要采用单一指标性成分,如斯金平等[17]以雷公藤甲素的含量来评价雷公藤药材的质量;高旋等[18]以雷公藤内酯醇来评价不同药材部位及产地的雷公藤药材质量,但单一化学成分不能全面反映药材的质量。而多指标评价主要采用液相色谱法,如张茹萍等[19]运用HPLC同时定量测定雷公藤药材中6种有效成分并结合主成分分析法(PCA)评价不同产地的雷公藤药材质量,但HPLC耗时长,且其灵敏度低,尤其对于没有紫外吸收的成分以及含量较低的萜类等成分检测存在困难,此外雷公藤药材中几个指标性生物碱的含量较低,加上与其极性相近的结构类似物较多,导致液相检测峰型、分离度均较差,存在误差较大的问题。
近年来兴起的超高效液相色谱电喷雾串联三重四级杆质谱由于其分离速度快、灵敏度高、测定准确性强已广泛用于中药及复方的分析中,尤其是微量成分的研究[20]。本实验基于超高效液相色谱电喷雾串联三重四级杆质谱建立了对雷公藤药材根中5种有效成分进行定量分析的方法,并对不同产地的雷公藤药材中5种成分测定,比较其含量差异,以对雷公藤药材的质量进行多指标的控制,保证其用药的安全。
1材料
ACQUITY IClass 超高效液相色谱仪(美国Waters 公司);AB QTRAP 6500 三重四级杆质谱仪(美国ABsciex公司,数据采集Analyst ABsciex;数据分析Multiquant 30),BSA224S型1/1万分析天平(德国Sartorius公司),Centrifuge 5415D型离心机(德国Eppendorf公司),SB800DTD型超声清洗机,超声功率500W(宁波新芝生物科技股份有限公司),Pacific TⅡ型超纯水仪(美国Thermo公司)。
化学对照品雷公藤甲素(批号PS14030304),雷公藤晋碱(批号PS07250010),雷公藤定碱(批号PS07250005)购于成都普思生物科技股份有限公司,纯度均>98%,雷公藤次碱(批号4001165865)购于上海远慕生物科技有限公司,纯度>98%,雷公藤内酯酮(批号MUST14092810)购于成都曼斯特生物科技有限公司,纯度>98%。水为超纯水,甲醇,乙腈为色谱纯(Fishier Scientific公司),其余试剂均为分析纯。
试验所用的为雷公藤及昆明山海棠的根,分别采自江西、湖南、云南、浙江等,均经中国中医科学院中药资源中心郝近大研究员鉴定,留样凭证存放于中国中医科学院中药资源中心,药材来源见表1。
2方法与结果
21色谱分析条件
色谱条件为色谱柱Waters ACQUITY UPLCCSHC18S(21 mm×100 mm,17 μm);流动相为2%甲酸铵(A)乙腈(B),梯度洗脱;0~5 min,40%~70% B;51~7 min,100% B;71~9 min,40% B;流速05 mL·min-1;柱温40 ℃;进样量1 μL。
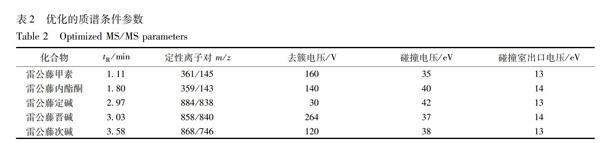
质谱条件为离子源Turbo V,电离模式:(ESI+);采集方式多反应监测(MRM);离子化温度(TEM) 550 ℃;喷雾电压5 500 V;雾化气(Gas 1) 55 kPa;辅助气(Gas 2):55 kPa;气帘气(CUR): 30 kPa;碰撞气(CAD)Medium;优化的各离子对质谱参数值, 见表2。
22对照品溶液的制备
精密称取对照品雷公藤甲素,雷公藤内酯酮,雷公藤次碱,雷公藤定碱,雷公藤晋碱对照品适量,置10 mL量瓶中,加适量甲醇超声使其溶解,再加甲醇至刻度,摇匀,制得质量浓度为23×102 mg·L-1的雷公藤甲素,14×102 mg·L-1雷公藤内酯酮,09×102 mg·L-1的雷公藤次碱,17×102 mg·L-1的雷公藤定碱,17×102 mg·L-1的雷公藤晋碱对照品供试液。
23供试品溶液的制备
13批雷公藤药材粉碎,过筛,精密称取药材粉末020 g置2 mL Ep管中,加入80%甲醇15 mL,超声(功率500 W)提取1h,放置室温,12 000 r·s-1离心10 min,取上清液,过022 μm的微孔滤膜,供UPLCQTRAP 分析。
24方法学考察
241方法专属性
在上述色谱质谱条件下, 混合对照品和样品5种有效成分MRM定量离子图见图1。5种成分分离良好, 而空白基质加标样品的分析表明基质成分不干扰被测5种有效成分的检测。
242线性范围、检测限、定量限
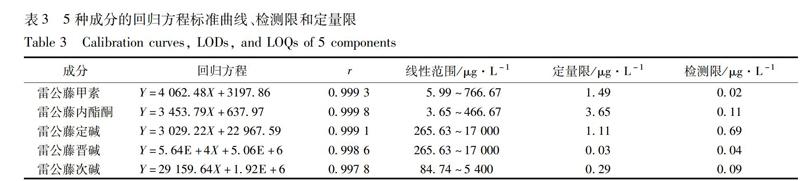
精密量取制备好的对照品溶液适量,稀释到一定的浓度,再分别用甲醇稀释配置成7个梯度浓度的对照品溶液,按已有色谱条件进行分析。以峰面积为纵坐标(Y),对照品溶液的浓度为横坐标(X),
243精密度、稳定性、重复性和回收率试验
2431精密度试验取一定浓度的混合对照品溶液,按照21项的色谱条件,重复进样6次,分别计算各成分面积的RSD在17%~26%,结果表明仪器精密度良好。
2432重复性试验按照上述供试品溶液制备方法,取同一样品平行制备6 份供试品溶液,按21项的色谱条件进样分析,测定各成分含量的RSD在13%~29%,表明方法重复性良好。
2433稳定性试验取重复性试验中的同一份供试品溶液,按21项的色谱条件分别于0, 2, 4, 8, 12, 24 h 进样分析,分别计算各成分含量的RSD在25%~42%,结果表明供试品溶液室温下在24 h内稳定。
2434回收率试验精密称取已知含量的同一样品6份,约020 g,精密加入低、中、高3个浓度的 5种对照品,按照供试品制备方法制备供试品溶液,按21项的色谱条件进样分析,计算5个成分的平均加样回收率在9672%~1032%,其RSD在10%~24%,表明方法回收率良好,结果见表4。
25样品测定
分别精密称取13批的雷公藤样品粉末约020 g,按供试品制备方法制备供试品溶液, 按21项的色谱条件进样分析, 分别计算各成分的含量,见表5。
3讨论
在样品分析过程中,本研究比较了不同粒径色谱柱对雷公藤中5种成分的分离效果,考察了Waters HSS T3 C18(21 mm×100 mm,17 μm), Waters CSHC18S(21 mm×100 mm,17 μm),Waters BEH C18(21 mm×100 mm,17 μm),Waters BEH C18(21 mm×50 mm,17 μm)4根色谱柱,最终选择Waters CSHC18S(21 mm×100 mm,17 μm)柱,因其分离度和灵敏度均明显高于其他超高效液相色谱柱。对于流动相的选择,考察了乙腈01%甲酸水、乙腈01%甲酸铵水、乙腈02%甲酸铵水,乙腈02%甲酸铵水最佳。另外,色谱分离上雷公藤定碱和雷公藤次碱无法有效分离,但在质谱通道上2个化合的离子对不相互干扰,可以准确定量。
对13个批次的雷公藤及昆明山海棠样品进行定量分析,在选定的色谱条件下,经方法学考察,方法的重复性、稳定性、精密度均符合有关规定,方法准确可靠、简便快速。但是,不同批次的雷公藤药材中雷公藤甲素、雷公藤内酯酮、雷公藤定碱、雷公藤晋碱、雷公藤次碱含量差异较大。
从表5中可以看出,雷公藤定碱含量在江西萍乡、湖南岳阳、浙江兰溪的雷公藤中,江西遂川的昆明山海棠中含量较高;雷公藤内酯酮含量在湖南岳阳、浙江新昌的雷公藤中,贵州剑河、福建泰宁的昆明山海棠中较高,且其都为栽培品;雷公藤甲素含量在浙江新昌,浙江兰溪的雷公藤中,贵州剑河的昆明山海棠中含量较高。福建泰宁为雷公藤的道地产区,从表5中可以看出产地为福建泰宁的2个雷公藤样品中雷公藤晋碱,雷公藤次碱含量较高。整体来说昆明山海棠中5个成分含量低于雷公藤。
综上,本研究建立的UPLCESIMS/MS同时测定雷公藤中雷公藤甲素、雷公藤内酯酮、雷公藤定碱、雷公藤晋碱、雷公藤次碱5种活性成分的定量方法简单、快捷、准确,为综合评价雷公藤药材的质量,保证其用药的安全提供参考。
[参考文献]
[1]刘玉凤,潘丽,南丽红,等. 雷公藤药理作用研究进展[J]. 亚太传统医药,2014,10(9):37.
[2]汪群红,胡敏. 雷公藤的药理作用与毒副作用[J]. 中国药业,2010,19(19):85.
[3]肖廷超,朱必越. 雷公藤片的临床应用及不良反应文献分析[J]. 重庆医学,2013, 42(9):1007.
[4]斯金平,阮秀春,郭宝林,等. 雷公藤资源现状及可持续利用的研究[J]. 中药材,2015, 28(1):10.
[5]黄文华,郭宝林,斯金平,等. 雷公藤属3种植物不同群体和个体中雷公藤甲素的研究[J]. 中草药, 2005, 36(7):1065.
[6]万大武. 雷公藤化学成分研究[D]. 昆明: 昆明理工大学, 2013.
[7]谢富贵,李创军,杨敬芝,等. 昆明山海棠根皮化学成分研究[J]. 中药材,2012,35(7):1083.
[8]王芳,张瑜,赵余庆. 昆明山海棠化学成分的研究[J]. 中草药,2011,42(1):46.
[9]刘劝,王友群. 雷公藤甲素的药理作用研究[J]. 药学进展, 2005,29 (4):156.
[10]林绥,阙慧卿,彭华毅,等. 雷公藤中二萜内酯类成分的研究(Ⅱ) [J]. 药学学报, 2011, 46 (8): 942.
[11]褚克丹,陈立典,倪峰,等. 雷公藤总生物碱的药效实验研究[J]. 中药药理与临床,2011,27(1):33.
[12]张贺,王芳,葛平,等. 雷公藤不良反应及其配伍减毒增效研究进展[J]. 中国中医药信息杂志,2014,21(8): 126.
[13]运乃茹,甘井山. 雷公藤及其制剂临床不良反应概述[J]. 天津药学,2012,24(1):18.
[14]李文英. 雷公藤及其制剂的不良反应与防治措施[J]. 首都医药,2008,8:47.
[15]Carter B Z, Mak D H, Schober W D, et al. Triptolide induces caspase dependent cell death mediated via the mitochondrial pathway in leukemic cells[J]. Blood, 2006,108(2): 630.
[16]黄思行. 昆明山海棠雄性生殖毒性及作用机制研究[D]. 重庆: 重庆医科大学,2014.
[17]斯金平,黄文华,郭宝林,等. 雷公藤药材中雷公藤甲素变异规律[J]. 中国中药杂志,2006,31(24):2016.
[18]高旋,宋敏,庄莹 雷公藤药材及制剂的HPLC特征图谱研究[J]. 药物分析杂志,2009, 29(5):702.
[19]张茹萍,何昱,石森林,等. HPLC 指纹图谱结合主成分分析评价不同产地雷公藤药材质量[J]. 中国现代应用药学, 2014, 31(11):1338.
[20]Yang Y, Wang H J, JianY, et al.Chemical profiling and quantification of Chinese medicinal formula HuangLianJieDu decoction,a systematic quality control strategy using ultrahigh performance liquid chromatography combined with hybridquadrupoleorbitrap and triple quadrupole mass spectrometers[J]. J Chromatogr A, 2013(1321):88.
[责任编辑丁广治]
