栽培尼泊尔菊三七中的木脂素类化合物
2016-05-14张志辉陆瑶邓安珺马林吴丰李志宏秦海林
张志辉 陆瑶 邓安珺 马林 吴丰 李志宏 秦海林
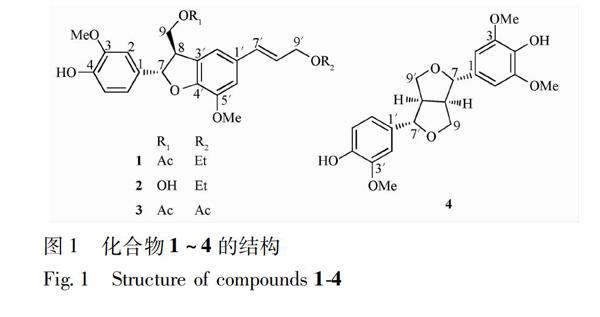

[摘要]采用溶剂提取、萃取粗分离、硅胶和Sephadex LH20凝胶柱色谱以及制备HPLC等纯化技术,从采自北京郊区的尼泊尔菊三七栽培品中分离得到4个化合物,通过波谱分析并参考文献数据鉴定其结构分别为7S,8R9′O乙基去氢双松柏醇9乙酸酯(1)、9′O乙基去氢双松柏醇(2)、去氢双松柏醇9,9′二乙酸酯(3)和(+)梣皮树脂醇(4)。1为新的2,3二氢苯并呋喃8,3′新木脂素型化合物,2~4均为首次从尼泊尔菊三七中分离得到的木脂素类化合物。对4个化合物在DMSOd6溶剂中的1H和13CNMR数据进行了全归属。
[关键词]尼泊尔菊三七;菊科;木脂素;7S,8R9′O乙基去氢双松柏醇9乙酸酯;结构鉴定
[Abstract]Taking application of some isolation and purification technologies, including solvent extraction, rude solvent isolation, column chromatographies on silica gel and Sephadex LH20 , and preparative HPLC , 4 compounds were obtained from Gynuranepalensiscultivated in a suburban area of Beijing. Their structures were identified by spectroscopic methods in conjunction with comparison of the NMR data with literature values as 7S,8R9′Oethyldehydrodiconiferyl9acetate (1), 9′Oethyldehydrodiconiferyl alcohol (2), dehydrodiconiferyl9,9′diacetate(3), and (+)medioresinol(4), respectively. 1 is a new 2,3dihydrobenzofuran8,3′neolignane type compound, and 24 were isolated from G.nepalensis for the first time. The complete assignment of the 1H and 13CNMR spectroscopic data of the four compounds recorded in DMSOd6 was achieved.
[Key words]Gynuranepalensis; Compositae; lignans; 7S,8R9′Oethyldehydrodiconiferyl9acetate; structure elucidation
doi:10.4268/cjcmm20160815
尼泊尔菊三七Gynura nepalensis DC为菊科Compositae菊三七属多年生草本植物,在国内西南个别地区有零星野生分布,偶有栽培品[12]。据文献记载,包括尼泊尔菊三七在内的菊三七属植物有药用功效,民间用其治疗支气管炎、肺结核、崩漏、臃肿、烫伤、跌打损伤、刀伤出血、身体创伤等多种疾病[35]。虽然已有一些文献报道了从菊三七属植物中分离鉴定了生物碱、黄酮、氨基酸、挥发油、萜烯等多种类型化合物[68],但有关尼泊尔菊三七的化学成分研究还很少,仅有本课题组报道从其地上部分分离鉴定了10个化合物,主要为7个增碳环香叶烷型单萜(其中6个化合物也可分类为大柱香波龙烷型C13降倍半萜),其他3个化合物分属有机酸酯和吲哚生物碱[2]。鉴于这些化合物的较丰富的结构多样性以及文献对尼泊尔菊三七的民间药用记载等,本课题组继续开展了对该植物化学成分的研究。从采自北京郊区的栽培尼泊尔菊三七的地上部分进一步获得4个化合物,包括1个新的苯并呋喃型新木脂素和3个首次从尼泊尔菊三七中分离得到的木脂素类化合物。本文报道这些化合物的分离和结构鉴定。
1材料
Varian Mercury400型和Bruker AvanceⅢ600型核磁共振波谱仪;Nicolet 5700型傅里叶变换红外光谱仪;PerkinElmer 241型旋光测定仪;JASCO J810型CD光谱仪;Agilent 1100 LC/MSD Trap SL型液相色谱质谱联用仪;LC6AD制备型高效液相色谱仪(配有SPD20A紫外检测器, 20 mm×250 mm PRCODS色谱柱);柱色谱硅胶(200~300目)和薄层色谱用硅胶预制板均为青岛海洋化工厂产品;Sephadex LH20为Pharmacia公司产品;色谱纯试剂为Fisher公司产品;水为市售纯净水;其他试剂均为分析纯产品。
实验用尼泊尔菊三七的植物原料采集、基原鉴定和标本保存见文献[2]。
2提取分离
干燥的尼泊尔菊三七茎和叶67 kg的前处理、溶剂提取、溶剂萃取粗分离和乙酸乙酯萃取物的硅胶柱色谱法粗分离见文献描述[2]。前文硅胶柱色谱分离后获得的Fr3 (15 g,石油醚乙酸乙酯4∶1)洗脱组分再经硅胶柱色谱,以石油醚乙酸乙酯混合洗脱剂系统梯度洗脱分成3个洗脱组分(Fr31~Fr33),Fr32(297 mg,石油醚乙酸乙酯10∶1)经凝胶柱色谱,以甲醇洗脱分成3个洗脱组分(Fr321~Fr323);Fr323 (98 mg)经制备高效液相色谱分离(以水甲醇 20∶80为流动相,流速6 mL·min-1,以210 nm作为UV检测波长)得到化合物1(4 mg)和3(3 mg)。前文Fr4洗脱组分(1 g,石油醚乙酸乙酯3∶1)再经硅胶柱色谱,以石油醚乙酸乙酯混合洗脱剂系统梯度洗脱分成7个洗脱组分(Fr41~Fr47);Fr45 (163 mg,石油醚乙酸乙酯5∶1)经凝胶柱色谱,以甲醇洗脱分成4个洗脱组分(Fr451~Fr454);Fr452 (62 mg)用制备高效液相色谱(以水甲醇 20∶80为流动相,流速6 mL·min-1,以210 nm作为UV检测波长)分离得到化合物2(4 mg)和4(3 mg)(图1)。
3结构鉴定
化合物1白色无定形粉末,[α]20D-385
化合物2白色无定形粉末;其正离子模式高分辨ESIMS给出质子加合的准分子离子峰m/z 387180 3(C22H27O6计算值为387180 2)、钠加合的准分子离子峰m/z 409163 1(C22H26NaO6计算值为409162 2),结合其13CNMR数据,确定其分子式为C22H26O6,不饱和度为10。对化合物2进行了1HNMR,13CNMR,DEPT,1H1H COSY,HSQC,HMBC和1D NOE差谱等波谱学实验,其1H和13CNMR数据与化合物1非常相似,主要区别在于化合物2中不存在化合物1的乙酰基信号δH197 (3H,s),δC1703 (s)和206 (q),且H9a,H9b和H8的化学位移分别向高场位移了Δδ-066,-064和-028,C9的化学位移向高场位移了Δδ-19,C8的化学位移向低场位移了Δδ+37。经深入的数据分析及归属,鉴定其为已知化合物9′O乙基去氢双松柏醇[11]。鉴于文献已报道了丙酮为测试溶剂的数据归属,本研究中化合物2以DMSOd6为测试溶剂的1H和13CNMR数据见表1。
化合物3白色无定形粉末;其正离子模式高分辨ESIMS给出钠加合的准分子离子峰m/z 465156 2(C24H26NaO8计算值为465152 0),结合其13CNMR数据,确定其分子式为C24H26O8,不饱和度为12。对化合物3进行了1HNMR,13CNMR,DEPT,1H1H COSY,HSQC,HMBC和1D NOE差谱等波谱学实验,经深入的数据分析及归属,鉴定其为已知化合物去氢双松柏醇9,9′二乙酸酯。鉴于文献已报道了氯仿为测试溶剂的数据归属,本研究中化合物3以DMSOd6为测试溶剂的1H和13CNMR数据见表1。
化合物4淡黄色粉末;1HNMR(DMSOd6,400 MHz)δ:889(1H,s,OH4′),824(1H,s,OH4),688(1H,d,J=18 Hz,H2′),674(1H,dd,J=84,18 Hz,H6′),671(1H,d,J=84 Hz,H5′),658(2H,s,H2,6),459(2H,m,H7,7′),412(2H,m,H9a,9′a),375(3H,s,OMe3′),374(6H,s,OMe3,5),373(2H,m,H9b,9′b),303(2H,m,H8,8′);13CNMR(DMSOd6,150 MHz)δ:1478(s,C3,5),1474(s,C3′),1458(s,C4′),1347(s,C4),1321(s,C1′),1313(s,C1),1185(d,C6′),1150(d,C5′),1103(d,C2′),1035(d,C2,6),852(d,C7),850(d,C7′),709(t,C9′),708(t,C9),559(q,OMe3,5),555(q,OMe3′),536(d,C8),534(d,C8′)。ESIMS m/z 389[M+H]+。数据与文献[1213]报道的(+)梣皮树脂醇一致。
[参考文献]
[1]中国科学院中国植物志编委会. 中国植物志. 第77卷 [M]. 北京:科学出版社,1999:314.
[2]陆瑶,李志宏,马林,等. 栽培尼泊尔菊三七化学成分的研究[J]. 中国中药杂志,2014,39(19):3777.
[3]Zhang X F, Tan B K H. Effects of an ethanolic extract of Gynura procumbens on serum glucose, cholesterol and triglyceride levels in normal and streptozotocininduced diabetic rats[J]. Singapore Med J, 2000, 41(1):9.
[4]胡勇,李维林,林厚文,等. 白背三七地上部分降血糖作用研究[J]. 西南林学院学报,2007,27(1):55.
[5]刘杭,俞坚,童芬美. 菊三七不同提取部位体外抗肿瘤实验研究[J]. 医学研究杂志,2006,35(5):66.
[6]袁珊琴,顾国明,魏同泰. 菊叶三七生物碱成分的研究[J]. 药学学报,1990,25(3):191.
[7]蒋娟娟,徐德然,濮社班,等. 菊三七地下部分的化学成分[J]. 药学与临床研究,2008,16(3):178.
[8]胡勇,李维林,林厚文,等. 白背三七地上部分的化学成分[J]. 中国天然药物,2006,4(2):156.
[9]Duarte N, Lage H, Ferreira M J U. Three new Jatrophane polyesters and antiproliferative constituents from Euphorbia tuckeyana[J]. Planta Med, 2008,74(1):61.
[10]Yoshikawa M, Morikawa T, Xu F, et al. (7R,8S)and(7S,8R)85′ linked neolignans from Egyptian herbal medicine Anastatica hierochuntica and inhibitory activities of lignans on nitric oxide production[J]. Heterocycles, 2003, 60(8):1787.
[11]Xiong L, Zhu C, Li Y. Lignans and neolignans from Sinocalamus affinis and their absolute configurations[J]. J Nat Prod, 2011, 74:1188.
[12]Tsukamoto H, Hisada S, Nishibe S. Lignans from bark of Fraxinus mandshurica var. japonica and F. japonica[J]. Chem Pharm Bull, 1984, 32(11):4482.
[13]张修朋,秦辉,杨芳,等. 黄素馨化学成分及其抗氧化活性[J]. 中国中药杂志, 2014, 39(11):2029.
[责任编辑丁广治]
