蛇葡萄素混合纳米胶束的制备及体外评价お
2016-05-11黄仁杰鄢雪梨陈虎彪
黄仁杰 鄢雪梨 陈虎彪
[摘要]为了提高蛇葡萄素的溶解性和抗肿瘤活性,以普朗尼克F127和Dα维生素E聚乙二醇1000琥珀酸酯为复合载体材料,采用薄膜水化法制备蛇葡萄素纳米胶束,考察蛇葡萄素纳米胶束的最佳工艺条件和理化参数。采用MTT法,比较原料及纳米胶束制剂对MCF7细胞增殖的抑制作用。结果表明,蛇葡萄素纳米胶束平均粒径为(226±05) nm,包封率为(8042±113)%,载药量为(441±026)%。所制得的蛇葡萄素混合纳米胶束比蛇葡萄素原料的溶解度增加16倍,且在不同释放介质中8 h可累积释放药物90%以上,并能够显著抑制MCF7细胞的增殖(P<001)。该混合纳米胶束可作为蛇葡萄素新的药物传递系统。
[关键词]蛇葡萄素;纳米胶束;普朗尼克F127;Dα维生素E聚乙二醇1000琥珀酸酯;薄膜水化法;抗肿瘤
蛇葡萄素(ampelopsin)又名二氢杨梅素,系藤茶的最主要活性成分。现代药理学研究表明,蛇葡萄素具有抑菌[1]、抗肿瘤[25]、抗炎镇痛、降血脂、抗氧化[6]等作用,因此极具开发潜力。但蛇葡萄素水溶性差,生物半衰期短[78],从而影响其在体内的生物利用度。有研究报道通过将蛇葡萄素制备成固体分散体、环糊精包合物等来提高其溶解度,但存在载药量低、增溶倍数低[9],且不能达到延长体内生物半衰期的目的。
纳米胶束作为新的药物载体是解决上述问题的有效手段,其不但可以提高药物的水溶性,还可以降低药物被网状内皮系统识别和摄取的机会达到体内长循环,通过增强渗透滞留效应(EPR)实现被动靶向[1012]。因此,本课题组用普朗尼克F127(Pluronic F127)和Dα维生素E聚乙二醇1000琥珀酸酯(TPGS1000 )为复合载体,采用薄膜水化法制备蛇葡萄素纳米胶束,对其制剂学性质及体外抗肿瘤活性进行考察,为蛇葡萄素新剂型的研究奠定基础。
1材料
LC2010A高效液相色谱仪(日本岛津公司);LCsolution色谱工作站(日本岛津公司);EL2042C型电子分析天平(梅特勒勒托利多仪器有限公司);Nicomp 380ZLS粒度及Zeta电位检测分析仪(美国PSS公司);Tecnai G2 20ST型透射电镜(美国FEI 公司),RE5230旋转蒸发仪(上海亚荣生化仪器厂);SHAA水浴恒温振荡器(江苏金坛市环宇科学仪器厂);SB5200DT超声波清洗机(宁波新芝科技股份有限公司);BioRAD680 酶标仪(美国BioRAD 公司);透析袋(8 000~14 000 Da,北京拜尔迪生物技术有限公司)。
蛇葡萄素对照品(纯度>98%,张家界生力生物有限公司,批号130926);Dα维生素E聚乙二醇1000维生素E琥珀酸酯(TPGS1000,Sigma公司,批号130610);普朗尼克F127(Sigma公司,批号130117);人乳腺癌细胞系(MCF7细胞,南京凯基生物技术有限公司);胎牛血清、胰蛋白酶、1640 培养基、磷酸盐缓冲液(PBS)均购自美国Hyclone 公司;甲醇为色谱纯,水为超纯水,其他试剂均为分析纯。
2方法与结果
21纳米胶束的制备
分别精密称取聚乙二醇1000维生素E琥珀酸酯(TPGS1000)和普朗尼克F127(5∶15)适量,按药载比为1∶20称取蛇葡萄素置于茄形瓶中,加入适量甲醇经超声波振荡溶解,于37 ℃下旋转蒸发除去甲醇,待茄形瓶底部及内壁形成一层均匀的薄膜,加入纯化水50 mL,37 ℃下超声波(240 W,40 kHz)振荡水化至薄膜溶解,依次分别用孔径02, 01 μm的聚碳酸酯膜过滤,各重复3次,即得蛇葡萄素混合纳米胶束制剂。
22HPLC测定纳米胶束中蛇葡萄素含量
221色谱条件采用Wondasil C18 (46 mm×250 mm, 5 μm)色谱柱,以甲醇水磷酸 (35∶65∶02)为流动相,流速10 mL·min-1,检测波长292 nm,柱温25 ℃,进样量20 μL[13]。
222含量测定按文献[13]方法,精密量取蛇葡萄素纳米胶束各01 mL,置10 mL量瓶中,加甲醇超声波(240 W,40 kHz)处理10 min,甲醇稀释至刻度,摇匀,按上述色谱条件测定峰面积,计算。测得质量浓度为(327±004) g·L-1。
23包封率及载药量的测定
按文献[13]方法,精密量取已知含量的蛇葡萄素纳米胶束溶液50 mL置于烧杯中,将装有2 mL纯化水的透析袋两端扎紧后置于其中进行反透析,4 h后取袋内的溶液05 mL,以甲醇稀释定容至10 mL,按上述色谱条件进样检测,记录峰面积,计算得游离蛇葡萄素浓度Cfree,按包封率=(50Ctotal-52Cfree)/50Ctotal×100%,计算包封率[13],Ctotal为蛇葡萄素纳米胶束溶液中的蛇葡萄素含量。结果表明,蛇葡萄素纳米胶束的包封率为(8042±113)%。
同时将经反透析后的胶束溶液进行冷冻干燥,称其质量M,按载药量=(50Ctotal-52Cfree)/(M-Cfree)×100%计算载药量。结果表明蛇葡萄素纳米胶束的载药量为(441±026) %。
24渗漏率的测定
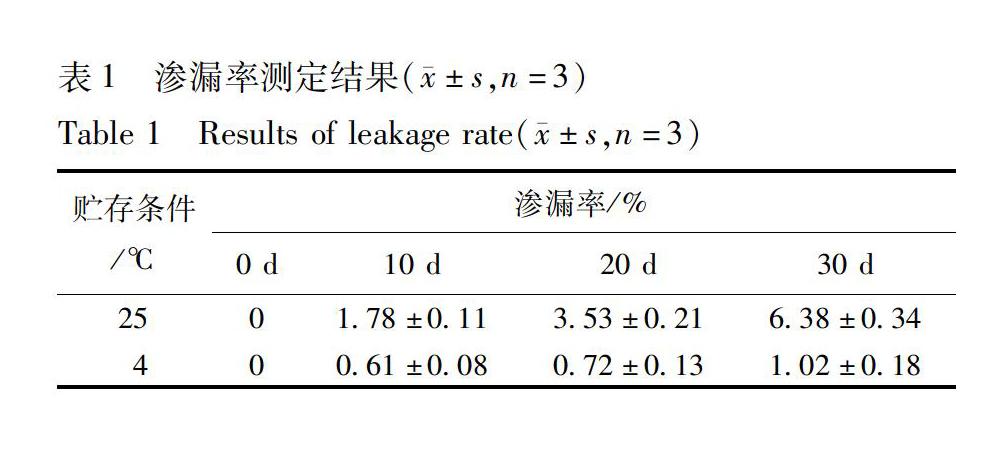
将蛇葡萄素纳米胶束溶液灌封于安瓿中,分别于室温(25 ℃) 、冷藏条件(4 ℃)放置,于0,5,15,30 d 取样,测定放置前后的游离药物量,按渗漏率=(Mt-M0)/(M-M0)×100%计算,结果见表1。式中Mt为贮存一段时间后测得游离药物的量,M0为贮存前游离药物的量,M为纳米胶束中药物总量。
结果表明,在冷藏条件(4 ℃)下,蛇葡萄素纳米胶束渗漏率未见明显变化,稳定性较好;而在室温(25 ℃)下,渗漏率随时间延长呈逐渐增长趋势,提示该胶束在常温下溶液稳定性较差,可通过冻干处理成固体粉末以解决渗漏稳定性问题,该部分研究将在后续进一步开展。
25制剂工艺优化
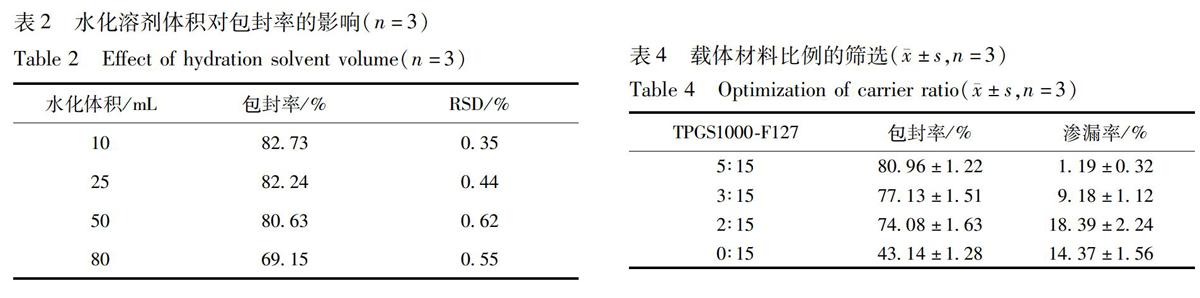
251水化溶剂体积的筛选固定其他工艺条件,分别考察不同体积的水化溶剂对所制备蛇葡萄素纳米胶束包封率的影响,结果见表2。当水化溶剂体积从10 mL增加至50 mL时,胶束的包封率呈微弱下降;当增加至80 mL时,包封率出现明显的下降。综合考虑到水化过程及包封率测定的可操作性,选择50 mL。
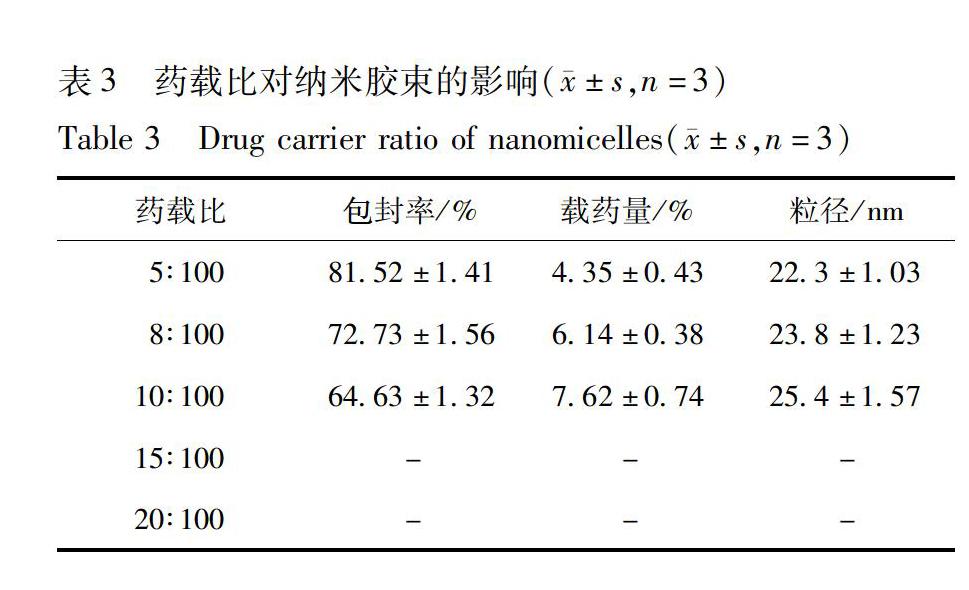
252药载比的影响选取5个不同的药物与载体比例,分别制备蛇葡萄素纳米胶束,并对其载药量、包封率、粒径进行考察,结果见表3。固定载体质量为100 mg 时,当药物质量为5 mg时,药物包封率最高,达到80%以上,但随着药物质量的增加,包封率随之降低,当药物质量为15 mg以上时,由于疏水性内核中的药物达到过饱和,在水化过程中即出现药物析出而导致包封率等参数无法准确测定。此外从稳定性方面考察,当药物质量为10 mg时,在4 ℃存放第5天即出白色药物析出,而药物为5 mg的样品可存放30 d以上且包封率未出现明显下降。综合考虑,优选药载比为5∶100。
253TPGS1000与F127的比例筛选固定其他工艺参数,选取4种不同质量比例的复合载体制备蛇葡萄素纳米胶束,考察包封率及渗漏率进行评价,结果见表4。当TPGS1000的添加量为0时,纳米胶束的包封率偏低(40%),随着TPGS1000的开始加入,纳米胶束的包封率出现明显增大(>70%),但随着TPGS1000加入比例继续提高,其包封率并未出现相应的增大。此外,从稳定性角度考虑,同样在4 ℃条件下贮存30 d,5∶15载体比例的纳米胶束的渗漏率最低,故选择该比例作为最佳载体比例。
26胶束的粒径、电位与形态
取适量蛇葡萄素纳米胶束,用纯化水稀释10倍,混匀,经022 μm的微孔滤膜过滤。使用激光粒度仪测定胶束的粒径和Zeta电位。每个样品测定20个循环时间,测定温度设定为25 ℃。实验结果表明,蛇葡萄素纳米胶束的平均粒径为(226±05)nm,Zeta电位为(-2073±013)mV,多分散系数为023,表明分散度良好,胶束的粒径较小且分布较窄,见图1。
取适量蛇葡萄素纳米胶束,用纯化水进行稀释,经022 μm微孔滤膜过滤后,将铺有碳膜的铜网漂放在纳米胶束溶液上,1~2 min后取出铜网,用滤纸从铜网边缘吸干多余液体。将俘获有纳米胶束粒子的铜网漂放在1%醋酸双氧铀染液上约1 min,取出,同样用滤纸吸干多余液体。室温放置过夜后,将晾干的铜网放入透射电镜仪,在加速电压160 kV下观察纳米胶束外部形态,见图1。纳米胶束均为球形,外观圆整,粒径均一,约20~30 nm,粒径大小与激光粒度仪测得的结果一致。
27表观溶解度测定
分别将过量的蛇葡萄素、蛇葡萄素纳米胶束冻干粉加入一定量纯化水中,于25 ℃恒温水浴振荡器中振荡,待平衡后分别取样适,置于10 mL量瓶中加甲醇稀释定容。经022 μm微孔滤膜滤过后,按22项下方法测定,计算表观溶解度。结果显示,制成纳米胶束后,蛇葡萄素溶解度由0486 g·L-1提高至7744 g·L-1,提高16倍左右。说明此纳米胶束对蛇葡萄素有很强的增溶能力。
28体外释放研究
分别取已知含量的胶束溶液剂及蛇葡萄素原料药混悬液2 mL放入到预先处理好的透析袋中,并将透析袋置于100 mL释放介质中,即pH 65 磷酸盐缓冲液(PBS)及pH 74 PBS,于(370±05)℃恒温水浴振荡(100 r·min-1),分别定时取样1 mL,并补充同温等量释放介质。样品用022 μm 微孔滤膜滤过,按22项下方法测定,计算累计释放率,绘制释药曲线,结果见图2,3。由于蛇葡萄素的水溶性差,在12 h内仅释放30%左右。蛇葡萄素纳米胶束在模拟血液(pH 74)和肿瘤细胞外液(pH 65)的环境下,释放行为基本一致,在前2 h仅累积释放药物10%左右,随后释放加速,8 h释放达90%左右,12 h释放达100%。
29细胞毒性实验
采用MTT法,取对数生长期的MCF7 细胞用胰酶消化,接种于96孔板, 调整细胞浓度使每孔104个,置培养箱中孵育24 h使其贴壁。次日加入适当浓度的蛇葡萄素,每组设3个复孔,继续培养72 h,吸弃各孔液体,加入5 g·L-1 MTT溶液20 μL,置培养箱中(37 ℃,5% CO2)孵育4 h,吸弃各孔液体,加入150 μL 的DMSO,混匀后使用酶标仪在492 nm 处测定各孔调零后的吸光度。计算细胞增殖抑制率=(1-A实验/A对照)×100%,结果见表5。
结果表明,蛇葡萄素纳米胶束对乳腺癌细胞MCF7的抑制率明显高于蛇葡萄素原料组,两者具有显著差异(P<00l)。通过GraphPad prism 50 软件拟合数据计算蛇葡萄素与蛇葡萄素纳米胶束对MCF7 细胞的IC50分别为2328,776 mg·L-1,可知,经过72 h干预,混合纳米胶束的IC50明显低于蛇葡萄素原料药的IC50,综上表明蛇葡萄素包裹于混合纳米胶束中能显著提高其对乳腺癌细胞MCF7的抑制率。
3讨论
普郎尼克F127在水溶液中能自发聚集形成胶束使难溶性药物被包裹在其中,从而提高药物的溶解度,增加稳定性,延长药物体内循环时间。但普郎尼克F127的临界胶束浓度比较大,当用溶液稀释时很容易导致胶束不稳定。加入TPGS1000构成混合体系能降低胶束的临界胶束浓度,同时其结构中含有芳香环,可使胶束疏水核体积增大,从而使更多的难溶药物进入胶束的疏水核,提高胶束的包封率和载药量[14]。基于此,本课题组选择普郎尼克F127和TPGS1000共同构建蛇葡萄素混合胶束体系,并得到很好的验证。
制备胶束的水化条件包括水化溶剂种类、体积、水化时间、水化温度等,这些均可能不同程度地影响胶束的包封率与粒径等重要质量指标。实验中发现某些常用试剂(如 Hepes缓冲液)对胶束的形成及含量测定均产生不利影响,为减少干扰,采用纯化水为水化溶剂。经初步比较,水化时间及温度对本处方工艺制备的胶束影响不大,同时考虑到对药物稳定性影响,故在37 ℃下水化溶解后即直接用02,01 μm的聚碳酸酯膜对胶束进行挤压过滤。水化溶剂体积越大,溶解药物越多,导致胶束包封率下降明显。
细胞毒性结果表明,对于MCF7细胞,载药胶束的细胞毒性远远高于原料药。这是由于蛇葡萄素包入胶束后溶解度增大,亦更容易进入细胞内所造成的。在高浓度时,空白胶束与原料药相比,也显示出一定的细胞毒性。这与文献报道的TPGS在较高浓度对特定细胞具有一定的细胞毒性相一致。关于该胶束在动物体内的药物动力学过程与药效将在后续研究中进一步开展。
[参考文献]
[1]刘吉华,高山林,朱丹妮,等蛇葡萄素的抑菌作用研究[J]中国药科大学学报,2002,33(5): 439
[2]刘德育,丘明祺,梁婷韵无莿根中蛇葡萄素的提取及其对黑色素瘤的抑制作用[J]中山医科大学学报,1999,20(2): 127
[3]刘德育,郑宏强,罗高琴蛇葡萄素体内外对小鼠B16黑色素瘤侵袭和转移的抑制作用[J]中国中药杂志,2003,28(10): 957
[4]邹静,王小琴,郑作文.蛇葡萄素对大鼠肝星状细胞增殖及胶原蛋白、细胞因子生成的影响[J].中国实验方剂学杂志,2014,20(8):163.
[5]郑作文,吕林艳,王小琴,等蛇葡萄素诱导人胃癌细胞凋亡的研究[J]中国实验方剂学杂志,2012,18(24): 292
[6]张友胜,宁正祥,胡闫勇黄酮类化合物二氢杨梅素的研究利用现状[J]中成药,2002,24(12): 970
[7]何志峰,刘德育,曾飒,等蛇葡萄素脂质体的制备研究[J]中国中药杂志,2008,39(1): 27
[8]黄仁杰,邓元荣荧光分析法测定兔血浆中蛇葡萄素浓度[J]中国现代应用药学,2011,28(1): 70
[9]Ruan L P, Yu B Y, Fu G M, et al Improving the solubility of ampelopsin by solid dispersions and inclusion complexes[J] J Pharm Biomed, 2005, 38(3): 457
[10]Mikhail A S, Allen C Block copolymer micelles for delivery of cancer therapy: transport at the whole body, tissue and cellular levels [J] J Control Release, 2009, 138(3): 214
[11]Nishiyama N, Kataoka K Current state, achievements, and future prospects of polymeric micelles as nanocarriers for drug and gene delivery [J] Pharmacol Therapeut, 2006, 112(3): 630
[12]Guo M, Yan Y, Liu X, et al Multilayer nanoparticles with a magnetite core and a olycation inner shell as pHresponsive carriers for drug delivery [J] Nanoscale, 2009, 2(3): 434
[13]黄仁杰,鄢雪梨,狄万鹏,等蛇葡萄素纳米胶束含量与包封率的测定[J]药物分析杂志,2015, 35(2): 261
[14]杨兴国,李凌冰 Pluronic P105/PEGPE/TPGS混合胶束系统对喜树碱的增溶[J]中国药学杂志,2009, 44(10): 762
[责任编辑孔晶晶]
