核-壳结构磁性金属有机骨架材料Fe3O4@UiO-66-NH2的合成、表征及催化性能
2016-05-03戴田霖张艳梅储刚张
戴田霖张艳梅储 刚张 静
(1辽宁石油化工大学化学与材料科学学院,抚顺 113001) (2大连民族大学生命科学学院,大连 116600)
核-壳结构磁性金属有机骨架材料Fe3O4@UiO-66-NH2的合成、表征及催化性能
戴田霖1,2张艳梅*,2储刚*,1张静1
(1辽宁石油化工大学化学与材料科学学院,抚顺113001) (2大连民族大学生命科学学院,大连116600)
摘要:UiO-66-NH2是以Zr(4+)为金属,以2-氨基对苯二甲酸为配体制备得到的金属有机骨架材料,它是目前报道中具有较高热稳定性和化学稳定性的材料之一。本文以Fe3O4为核,以UiO-66-NH2为壳,采用层层自组装方法制备了核-壳结构的磁性金属有机骨架材料Fe3O4@UiO-66-NH2。利用X射线衍射(XRD)、傅里叶变换红外光谱(FTIR)、透射电子显微镜(TEM)、扫描电子显微镜(SEM)和氮气吸附等对其进行了表征,并考察了该磁性材料在克脑文盖尔(Knoevenagel)缩合反应中的催化性能。结果表明,该磁性材料Fe3O4@UiO-66-NH2为核-壳结构,壳层厚度约为100 nm,氨基含量为1.70 mmol·g(-1)。该磁性复合材料具有Fe3O4和UiO-66-NH2的双重功能,既可以磁性分离,又具有UiO-66-NH2的孔结构和催化性能。由于壳层材料中Lewis酸性位(Zr(4+))和碱性基团(-NH2)的协同催化能力及其壳层的纳米尺寸效应,该磁性材料在Knoevenagel缩合反应中表现出和UiO-66-NH2纳米粒子相当的催化活性。而且,通过磁性分离实现催化剂的多次循环使用后,其结构没有明显变化。
关键词:四氧化三铁;金属有机骨架材料;核-壳结构;克脑文盖尔缩合反应;磁性分离
国家自然科学基金(No.21203017)、国家重点实验室开放基金(No.N-11-03)、辽宁省高等学校优秀人才支持计划、中央高校基本研究业务费专项资金(No.DC201502020304)资助项目。
*通信联系人。E-mail:ymzhang@dlnu.edu.cn
0引 言
含有活泼亚甲基的化合物与醛或酮在弱碱催化下,发生失水缩合生成,α,β-不饱和羰基化合物及其类似物的反应称为克脑文盖尔(Knoevenagel)缩合反应,通过此反应可以制备许多重要的药物中间体。发展至今,已有多种均相和多相催化剂被应用于该反应。相对于均相催化剂,多相催化剂具有易分离和回收,简化操作步骤,减少环境污染和资源浪费等优势[1]。因此,开发高效、环境友好的新型多相催化剂具有重要意义。基于上述原因,近年来分子筛[2]、介孔碳[3]、有机功能化的介孔硅材料[4]和金属有机骨架材料[5]等材料被开发应用于克脑文盖尔(Knoevenagel)缩合反应中。
金属有机骨架材料(MOFs)是一种由金属离子或金属簇与有机桥联配体通过配位作用组装形成的新型多孔晶体材料,已成为现代多孔材料研究的热点领域之一[6-7]。MOFs具有大比表面积、高孔隙率、热稳定性好、规整且可调控的孔结构、易于功能化的骨架金属离子和有机配体等优点,是制备多相催化剂的重要平台材料之一[5-8]。多相催化剂的分离和回收使用是评价其性能的重要指标之一。对于多孔固体催化剂,减小催化剂的粒径尺寸可以减少底物的扩散限制,提高反应效率。但是,纳米催化剂的彻底分离和回收困难。为了解决纳米金属有机骨架材料分离困难的问题,柯飞等研究者通过层层自组装技术制备了核-壳结构的磁性金属有机骨架材料,并考察了Fe3O4@MIL-100(Fe)在克莱森缩合反应中的催化反应性能[9-12]。研究表明,核-壳结构的磁性金属有机骨架材料不仅可以表现出较好的催化活性,而且可以实现催化剂的简单磁性分离。在前期研究中,我们通过层层自组装技术分别制备了核-壳结构的磁性金属有机骨架材料Fe3O4@Cu3(BTC)2-NH2和Fe3O4@IRMOF-3,并考察了上述材料在Knoevenagel缩合反应中的催化性能[13-14]。结果表明,由于壳层材料的尺寸效应,位于复合材料壳层的金属有机骨架材料在反应中表现出比体相金属有机骨架材料更高的催化活性,并且可以通过简单的磁性分离实现催化剂的分离和循环使用。但是上述两种金属有机骨架材料在反应中的稳定性不高,磁性复合材料在反应后结构遭到部分破坏。
UiO-66及其氨基化材料是以Zr4+为金属,以对苯二甲酸或2-氨基对苯二甲酸为配体制备得到的金属有机骨架材料。UiO-66及其氨基化材料是目前报道中具有较高热稳定性和化学稳定性的材料之一[15-16]。而且,UiO-66-NH2材料中具有Lewis酸(Zr4+)和弱碱(-NH2)的协同催化作用,已经被证实在Knoevenagel缩合反应中及交叉缩合反应中表现出优异的催化性能[1,17-18]。因此,设计合成基于UiO-66及其氨基化材料的磁性金属有机骨架材料是开发高活性和高稳定性固体碱催化剂的有效途径。目前关于核-壳结构的磁性金属有机骨架材料的合成及其应用研究还处于初级阶段,关于核-壳结构的磁性UiO-66-NH2复合材料的设计合成及应用还未见报道。如图1所示,本研究通过层层自组装方法制备了核-壳结构的Fe3O4@UiO-66-NH2复合材料,并考察了其在克脑文盖尔(Knoevenagel)缩合反应中的活性、选择性和循环稳定性。
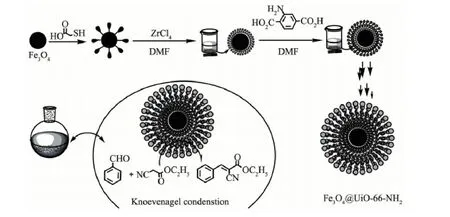
图1 核-壳结构磁性金属骨架材料Fe3O4@UiO-66-NH2的合成及其在Knoevenagel缩合反应中的应用Fig.1 Preparation procedure for core-shell magnetic microsphere Fe3O4@UiO-66-NH2and its catalytic application in Knoevenagel condensation
1 实验部分
1.1 Fe3O4@UiO-66-NH2材料的合成
首先按照文献方法制备巯基乙酸修饰的Fe3O4纳米粒子[13]。将1.00 g巯基乙酸修饰的Fe3O4样品分散到80 mL ZrCl4(10 mmol·L-1)的DMF溶液中,在120℃搅拌2 h后磁性分离。将固体再分散到80 mL 2-氨基对苯二甲酸(10 mmol·L-1)的DMF溶液中,120℃反应2 h。上述每一步骤都磁性分离,并用DMF洗3次。重复上述操作10次,固体在150℃真空干燥,制备得到Fe3O4@UiO-66-NH2。
1.2 Knoevenagel缩合反应
将0.05 g催化剂和0.745 mL(7 mmol)氰基乙酸乙酯加入到5 mL DMF中,搅拌下将混合物升温到80℃后再加入0.815 mL (8 mmol)的苯甲醛启动反应,间隔30 min取样,用TLC监测反应过程,离心后用气相分析产率和选择性。反应结束后将催化剂磁性分离,用DMF洗3次后,直接用于下次循环反应。
1.3材料的表征
利用岛津XRD-6000型X射线衍射仪(XRD)测定材料的XRD图,Cu Kα靶作为发射源,电压为40 kV,电流为30 mA,扫描范围2θ=5°~80°;利用FEI Quanta 200F型扫描电子显微镜(SEM)对样品形貌进行表征,加速电压为20 kV,将样品固定在导电胶上并喷金60s后测试;利用JEM-2010型透射电子显微镜(TEM)对样品结构进行表征,加速电压为200 kV,将样品分散到乙醇中,然后滴加到铜网上后进行测试;利用Prestige-21型傅里叶变换红外光谱仪在波数400~4 000 cm-1范围内对材料进行红外光谱扫描;利用配备Rxi@-1毛细管柱(30 m×0.25 mm×0.5 μm)和FID检测器的岛津2010气相色谱仪对反应后的混合物进行分析;利用化学吸附仪ASAP2020对样品的孔结构进行分析,样品测试前先在120℃真空处理6 h,测定温度为77 K。
2 结果与讨论
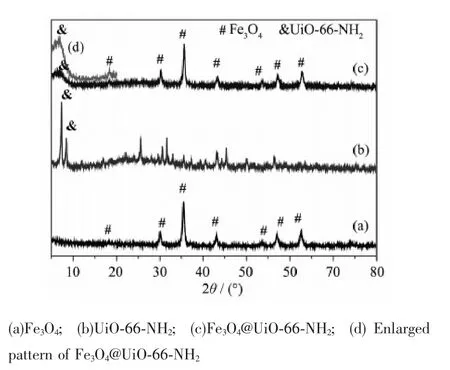
图2 材料的XRD图Fig.2 XRD patterns of materials
2.1材料的表征
2.1.1材料的XRD表征
图2a是Fe3O4的XRD图,在30.1°、35.5°、43.1°、53.4°、57.0°、62.6°出现对应Fe3O4的220、311、400、422、511、440晶面的特征衍射峰。图2b是根据文献方法合成的UiO-66-NH2的XRD图,在5°~80°范围内出现了一系列特征衍射峰,与文献报道结果一致[1]。图2c是通过层层自组装方法制备得到的复合材料Fe3O4@UiO-66-NH2的XRD图。相对于Fe3O4的XRD图,壳层材料的引入使其在5~10之间出现了对应于UiO-66-NH2的特征衍射峰(Fig.2c)。虽然XRD结果表明壳层材料UiO-66-NH2的结晶度较低,但上述结果表明通过该方法成功在Fe3O4表面引入了UiO-66-NH2材料。其核-壳结构有待进一步通过扫描电镜(SEM)和透射电镜(TEM)确认。
2.1.2材料的形貌和结构的表征
虽然XRD结果表明通过层层自组装方法成功制备了UiO-66-NH2和Fe3O4复合材料,但是该复合材料的微观结构是两种材料的简单混合还是核-壳结构还有待进一步确认。首先采用扫描电子显微镜(SEM)观测材料的形貌。如图3a所示,合成的Fe3O4为球形结构,粒径大小约为300~600 nm。而通过XRD结果计算得到Fe3O4的晶体粒子大小为17 nm,这说明此磁性微球是Fe3O4纳米颗粒的聚集体。图3b是采用层层自组装方法制备得到的Fe3O4@UiO-66-NH2的SEM图,可以看出材料依然保持球形形貌,但球形颗粒的粒径变大,表面形貌发生了变化,通过与Fe3O4的SEM图对比,可以推断在Fe3O4的球形颗粒上包覆上一层UiO-66-NH2材料。进一步利用SEM-EDS测定了该磁性复合材料的元素组成。Fe3O4中(Fig.S2a)主要含有Fe、O元素,通过自组装方法引入UiO-66-NH2壳层之后,SEM-EDS谱图中(Fig.S2b)出现了Zr元素的谱峰。通过积分得到的原子比例结果综合在表1中。根据Fe和Zr的原子比计算得到此该磁性复合材料上UiO-66-NH2的质量百分含量为60%,氨基的含量为1.70 mmol· g-1。进一步采用透射电子显微镜(TEM)表征材料的微观结构。图3d是Fe3O4的TEM图,可以看出Fe3O4为球形结构,粒径大小与扫描电镜结果一致。图3e 是Fe3O4@UiO-66-NH2的TEM图,可以明显观察到材料的核-壳结构,壳层材料厚度大约为100 nm。

图3 材料的扫描电镜图和透射电镜图Fig.3 SEM and TEM images of materials
2.1.3材料的红外光谱表征
图4是材料的红外谱图。图4a是Fe3O4的红外谱图,在580 cm-1附近出现了Fe-O-Fe的典型吸收峰。图4b是Fe3O4@UiO-66-NH2的红外谱图,在1 654 cm-1出现了羧基-C=O的伸缩振动峰,在1 620、1 560、1 420和1 370 cm-1分别出现了苯环骨架的伸缩振动峰,在3 350和3 440 cm-1分别出现了伯胺的对称和不对称伸缩振动峰,说明磁性材料上自由氨基的存在[19-20]。通过与图4a和图4c(UiO-66-NH2的红外谱图)对比,可知复合材料中同时含有Fe3O4和UiO-66-NH2两种物质。
2.1.4材料的孔结构表征
图5是材料的氮气吸附-脱附等温曲线,据此计算得出的比表面积和孔容数据综合在表1中。图5a是Fe3O4的氮气吸附-脱附等温曲线,在较高压力范围内(P/P0>0.8),曲线上存在一个明显的滞后环,这是由于纳米粒子的堆积造成的介孔孔道以及磁球内部的空心对氮气的吸附作用。图5c是Fe3O4@UiO-66-NH2的氮气吸附-脱附等温线,此等温线同时具有I型和IV型吸附等温线的部分特征,在较高压力范围内(0.4<P/P0<1.0),曲线上存在一个明显的滞后环,说明样品中存在介孔孔道。采用BJH方法计算材料的孔径分布,结果显示最可几孔径为8.3 nm (Fig.S3);同时,在较低压力范围内(P/P0<0.1),曲线上也存在一个明显的台阶,表明样品中存在着微孔孔道。Qiu等设计合成的介孔金属有机骨架材料具有类似的氮气吸附等温线[21]。由上述结果可知,材料中同时存在来源于金属有机骨架材料的微孔孔道和来源于粒子堆积产生的介孔孔道,这对反应底物在材料中的扩散是非常有利的。从表1中数据可知,Fe3O4的BET比表面积和孔容分别为129 m2·g-1和 0.28 cm3·g-1,主要来源于Fe3O4纳米粒子的外表面和粒子堆积产生的介孔孔道。Fe3O4@UiO-66-NH2的BET比表面积为121 m2·g-1,单点法计算得到总孔容为0.11 cm3·g-1。由t-plot方法计算得到来自微孔的比表面积为68 m2·g-1;微孔孔容为0.04 cm3·g-1。从XRD计算得到的粒径、以及透射电镜及扫描电镜图中部分破裂的球可知,本文采用的磁性纳米球是由纳米粒子组成的空心球。因此具有较大的比表面积和孔容。合成核壳结构的材料后,由于UiO-66-NH2材料占据了磁性纳米粒子之间的空隙以及磁性微球的空心;且复合材料中UiO-66-NH2材料的质量百分比仅为60%,因此虽然单纯UiO-66-NH2的比表面积较大,但是复合材料体现出的总比表面积和孔容反而小于原始的磁性纳米球。材料中微孔和介孔共存的性质有利于催化反应中底物的扩散和传输。
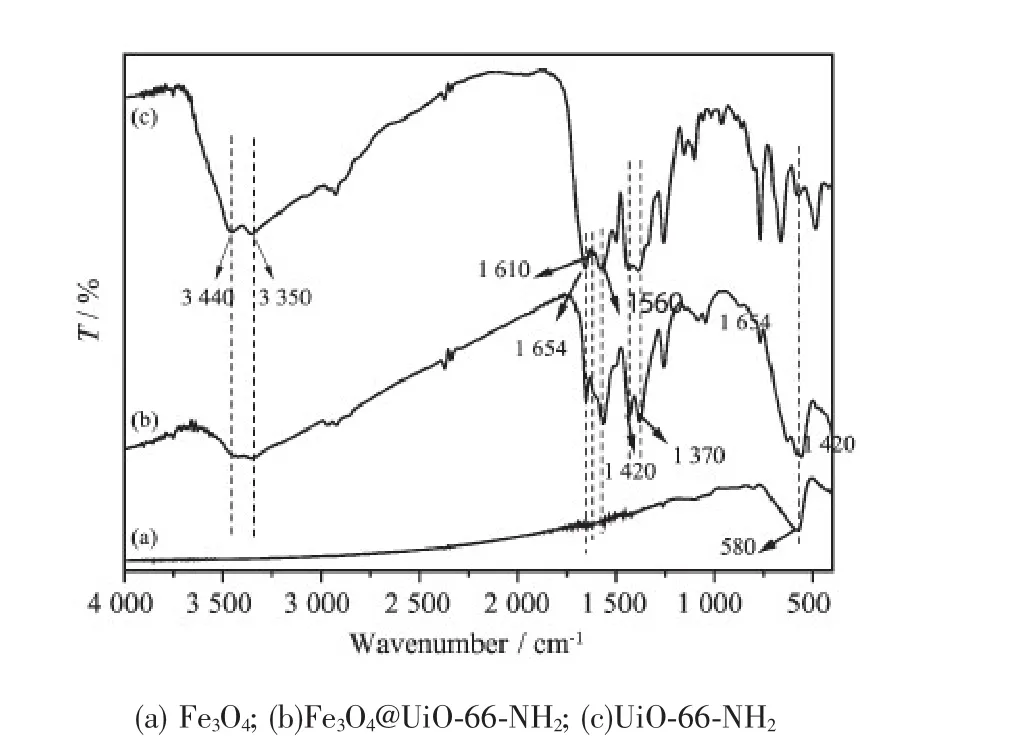
图4 材料的红外光谱图Fig.4 IR spectra of materials

图5 材料的氮气吸附-脱附等温曲线Fig.5 N2adsorption-desorption isotherms of materials
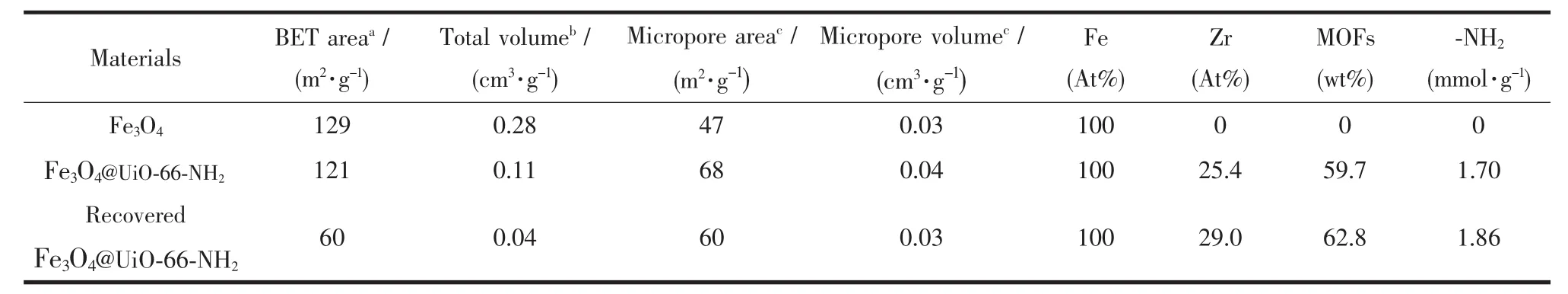
表1 材料的物理参数Table1 Physical properties of materials
2.2材料的催化反应
2.2.1催化反应活性
据文献报道,UiO-66-NH2中存在Lewis酸性位(Zr4+)和碱位(-NH2)的协同催化作用,是一类优秀的固体碱催化剂[1,17-18]。本文以苯甲醛和氰基乙酸乙酯的Knoevenagel缩合反应作为模型反应,考察了制备的磁性材料Fe3O4@UiO-66-NH2作为固体碱催化剂的催化性能。结果如表2所示,在80℃,没有催化剂或采用Fe3O4作为催化剂的条件下,反应缓慢进行,反应2 h后产率仅为20.3%和21.4%。采用1%粒径约为100 nm的UiO-66-NH2纳米粒子作为催化剂,反应1 h的产率为80.3%。采用含有相同氨基含量的Fe3O4@UiO-66-NH2作为催化剂,得到和UiO-66-NH2纳米粒子相当的反应活性和选择性,在相同的条件下产率为82.9%,选择性为96.9%。随后考察了反应温度对反应性能的影响,从表2数据可知,随着温度升高,单位时间内的产率逐渐提高。但在较高的温度下反应,催化剂结构遭到部分破坏的几率增加,因此后面的实验采用80℃作为最佳反应温度。前期的研究结果表明,极性溶剂有利于Knoevenagel缩合反应的进行[1,19-23]。因此本文继续考察了反应的溶剂效应。从表2中数据可知,催化剂在极性溶剂DMF、DMSO、THF中表现出较好的活性和选择性,而在非极性溶剂中如甲苯、正己烷中活性较低,这和文献报道结果是一致的[1,19-23]。
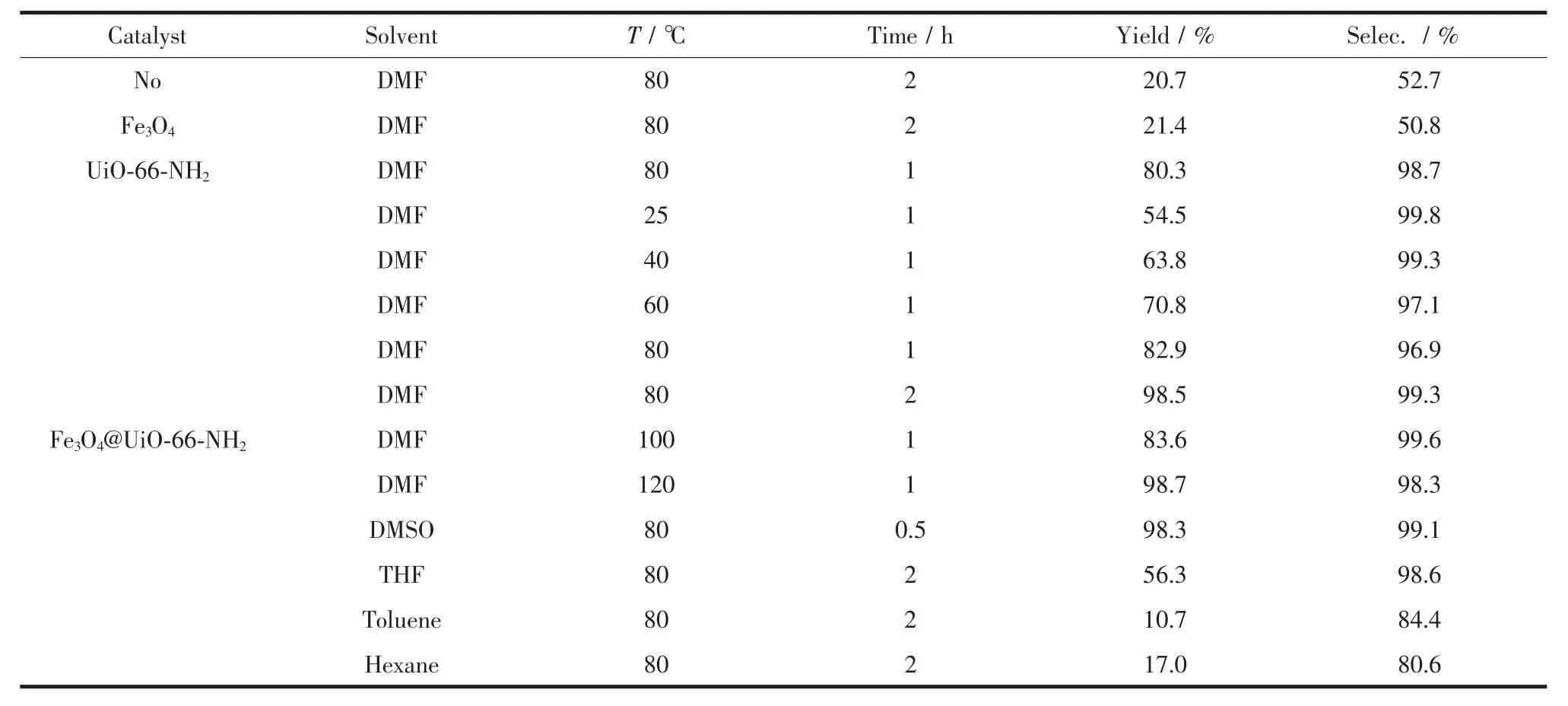
表2 Fe3O4@UiO-66-NH2催化的Knoevenagel缩合反应结果Table2 Results of Knoevenagel condensations in different organic solvents byFe3O4@UiO-66-NH2
为了验证该磁性材料催化反应为多相催化,进行了热过滤实验,结果如图6所示。在热过滤实验中,反应30 min后,转化率为64%。将催化剂通过磁性分离去除后,液体继续搅拌3.5 h,发现转化率几乎没有变化,说明滤液中无活性中心存在。此结果证实此反应是多相催化反应,活性中心主要来源于磁性材料上的UiO-66-NH2,且反应过程中没有活性中心的流失。

图6 Fe3O4@UiO-66-NH2催化的热过滤实验Fig.6 Hot filtration reaction catalyzed by Fe3O4@UiO-66 -NH2
催化剂的循环稳定性是多相催化剂的重要评价指标之一,因此本文进一步考察了该材料在Knoevenagel缩合反应中的循环稳定性。结果如图7 和Fig.S6所示,随着循环次数的增加,产率逐渐降低,从第一次的98%降低到第四次的80%。而且,如图8所示,催化剂在反应过程中均匀分散于反应溶液中。反应完毕后,通过外加磁场,可以实现催化剂的简单磁性分离。
图9是反应前后材料的XRD图,虽然在DMSO中反应后材料的XRD中特征峰的强度明显降低,但在DMF中反应后材料的XRD图中特征峰的位置和强度均无明显变化,说明材料结构在以DMF为溶剂的反应体系中比较稳定。而且,扫描电镜结果(图3c 和Fig.S2)和透射电镜(图3f)也表明,材料的元素组成、形貌和粒径大小也未发现明显变化,进一步说明材料在反应过程中结构稳定。采用氮气吸附-脱附等温线进一步考察材料部分失活的原因。发现反应后材料对氮气吸附量明显减少(图5c),大部分介孔孔道被堵塞或者坍塌,这可能是催化剂部分失活的主要原因。
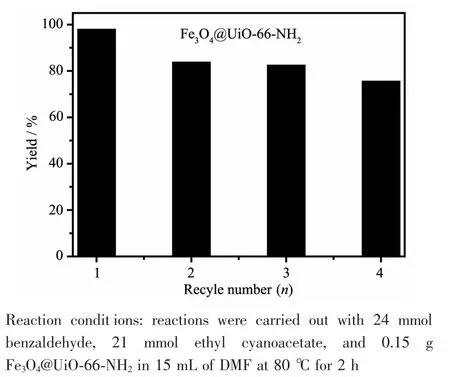
图7 Fe3O4@UiO-66-NH2催化的循环反应结果Fig.7 Recycle results of reactions catalyzed by Fe3O4@UiO-66-NH2

图8 催化剂Fe3O4@UiO-66-NH2的磁性分离Fig.8 Magnetic seperation of Fe3O4@UiO-66-NH2

图9 Fe3O4@UiO-66-NH2反应前后的XRD图Fig.9 XRD patterns of Fe3O4@UiO-66-NH2before and after reaction
3结 论
本文首次报道了核-壳结构的磁性金属有机骨架材料Fe3O4@UiO-66-NH2的合成、表征及其在克脑文盖尔(Knoevenagel)缩合反应中的催化性能。此磁性材料采用层层自组装方法合成,利用此方法可以实现壳层厚度可控。在催化过程中,UiO-66-NH2材料骨架上的路易斯酸Zr4+和碱性基团-NH2具有协同催化效应,同时纳米壳层有利于反应物的扩散和传输。因此,Fe3O4@UiO-66-NH2在苯甲醛和氰基乙酸乙酯的Knoevenagel缩合反应表现出和UiO-66-NH2纳米粒子相当的反应活性和选择性;而且,该磁性催化剂可以通过简单的磁性分离实现催化剂的分离和循环。这类催化剂的制备方法简单、无毒,是一类经济环保的固体多相催化剂。
Supporting information is available at http://www.wjhxxb.cn
参考文献:
[1] Yang Y, Yao H F, Xi F G, et al. J. Mol. Catal. A: Chem., 2014,390:198-205
[2] Opanasenko M, Dhakshinamoorthy A, Shamzhy M, et al. J. Catal. Sci. Technol., 2013,3:500-507
[3] Rong X, Zheng H F. J. Chin. Chem. Soc., 2014,61:1093-1100
[4] Mahmoudi H, Malakooti R. J. React. Kinet. Mech. Catal., 2014,113:241-255
[5] Burgoyne A R, Meijboom R. J. Catal. Lett., 2013,143:563-571
[6] Zhu Q L, Xu Q. J. Chem. Soc. Rev., 2014,43:5468-5512
[7] Lee J, Farha O K, Roberts J, et al. Chem. Soc. Rev., 2009, 38:1450-1459
[8] Dhakshinamoorthy A, Garcia H. ChemSusChem, 2014,7: 2392-2410
[9] Ke F, Yuan Y P, Qiu L G, et al. J. Mater. Chem., 2011,21: 3843-3848
[10]Ke F, Qiu L G, Yuan Y P, et al. J. Mater. Chem., 2012,22: 9497-9500
[11]Ke F, Qiu L G, Yuan Y P, et al. J. Hazard. Mater., 2011, 196:36-43
[12]Ke F, Qiu L G, Zhu J F. Nanoscale, 2014,6:1596-1601
[13]ZHANG Yan- Mei(张艳梅), ZHANG Jing(张静), TIAN Miao-Miao(田苗苗), et al. Chin. J. Catal.(催化学报), 2016, 37(3):420-427
[14]LI Xiao-Fang(李晓芳), ZHANG Yan-Mei(张艳梅), ZHANG Jing(张静), et al. J. Funct. Mater.(功能材料), 2015,46: 06039-06041
[15]SONG Xiao- Kai(宋肖锴), ZHOU Ya-Jing(周雅静), LI Liang(李亮). Prog. Chem.(化学进展), 2014,26:424-435
[16]Cheetham A K, Rao C N R, Feller R K. Chem. Commun., 2006:4780-4795
[17]Panchenko V N, Matrosova M M, Jeon J, et al. J. Catal., 2014:316:251-259
[18]Vermoortele F, Ameloot R, Vimont A, et al. Chem. Commun., 2011,47:1521-1523
[19]Gascon J, Aktay U, Hernandez A M D, et al. J. Catal., 2009,261:75-87
[20]Kandiah M, Nilsen M H, Usseglio S, et al. Chem. Mater., 2010,22:6632-6640
[21]Qiu LG, Xu T, Li Z Q, et al. Angew. Chem. Int. Ed., 2008, 47:9487-9491
[22]GAO Jin-Bao(高金宝),WANG Li-Bing(王丽冰), LIU Xiu-Li(刘秀丽), et al. J. Mol. Catal.(China) (分子催化), 2008, 22(2):117-122
[23]Nguyen L T L, Le K K A, Truong H X, et al. Catal. Sci. Technol., 2012,2:521-528
Core-Shell Magnetic Microsphere Fe3O4@UiO-66-NH2: Characterization and Application as Heterogeneous Catalyst
DAI Tian-Lin1,2ZHANG Yan-Mei*,2CHU Gang*,1ZHANG Jing1
(1School of Chemistry and Material Science, Liaoning ShiHua University, Fushun, Liaoning 113001, China)
(2College of Life Science, Dalian Nationalities University, Dalian, Liaoning 116600, China)
Abstract:Magnetic metal organic frameworks exhibit both magnetic characteristics and catalytic properties. However, their applications as heterogeneous catalysts are still very limited. Herein, a novel kind of core-shell structured Fe3O4@UiO-66-NH2has been successfully fabricated by a layer-by-layer self assembly method which could be used as an active basic catalyst for Knoevenagel condensation. In a typical synthesis, Fe3O4nanoparticals were synthesized by a solvothermal method and then surface modified with mercaptoacetic acid (MAA). Dispersing the MAA-modified Fe3O4microspheres alternately in DMF solutions of ZrCl4(10 mmol·L(-1)) and 2-aminobenzenetricarboxylic acid DMF solution (10 mmol·L(-1)) at 120℃for 2 h, Fe3O4@UiO-66-NH2core-shell structured microspheres were successfully prepared as expected. Its core-shell structure was confirmed by XRD and TEM techniques, composition by SEM-EDS and the amine functionality proven by IR spectroscopy. The shell thickness is about 100 nm and its weight content is about 60%. Correspondingly, the amino content was calculated to be 1.7 mmol·g(-1). The core-shell Fe3O4@UiO-66-NH2is an ideal recyclable catalyst for Knoevenagel conden-book=610,ebook=59sation that derive from a combination of a superparamagnetic core for efficient magnetic separation and a thin porous MOF shell for high catalytic activity. The remarkable activities for Knoevenagel condensation reactions are thanks to the cooperative action of amino groups and Lewis acid Zr(4+)ions in UiO-66-NH2. Obvious solvents effect on the activity and stability was observed, and DMF was selected as good medium for recyclability for a sacrificial balance between activity and recyclability. The catalyst could be easily separated from the reaction mixture and reused without significant change in the catalytic activity after four reaction cycles. Furthermore, its structure and morphology was not changed after the reaction in DMF, confirmed by the XRD, SEM and TEM techniques. Therefore, such kind of MOF-based core-shell magnetic catalysts is expected to be used in large scale industrial applications, where separation and recycling are critically required to reduce the cost as well as waste production. Moreover, the catalyst preparation procedure is fairly simple and the catalysts contain no toxic materials, thus this catalyst is green and cheap.
Keywords:Fe3O4; metal organic frameworks; core-shell structure; Knoevenagel condensation; magnetic separation
收稿日期:2015-11-17。收修改稿日期:2016-02-01。
DOI:10.11862/CJIC.2016.078
中图分类号:O643.3
文献标识码:A
文章编号:1001-4861(2016)04-609-08
