关于硫酸性质与应用的系列问题(1)———透过硫酸分子结构理解其物理性质
2016-04-28王笃年
关于硫酸性质与应用的系列问题(1)———透过硫酸分子结构理解其物理性质
◇北京王笃年
硫酸在现代社会生产和生活中有着重要的地位,从科学研究到工业生产,从中学化学教科书、实验室到大众文化,都不断出现它的身影.硫酸产量是一个国家化学工业发展水平的重要标志.关于硫酸的性质与应用,是中学化学的基础知识,但仅仅记住这些知识是不够的;作为高中理科学生,应该根据硫酸的分子结构,深入理解硫酸的性质和应用.
1) 如何根据硫酸的分子结构理解其物理性质?
硫酸作为一种液态物质(熔点10.4 ℃,沸点337℃),其物理性质和一般的液体相比有很大的不同.黏稠、油状、沸点极高、以任意比例溶解于水、溶解过程中释放大量的热……结构决定性质,让我们先看看硫酸分子具有怎样的结构,如图1,2,3所示.
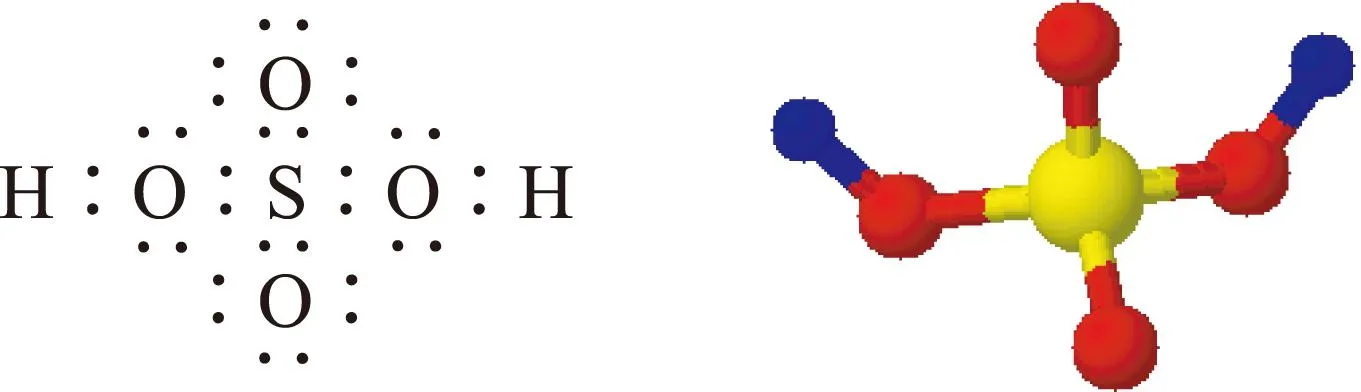
图1 电子式 图2 分子结构模型

图3 结构式
硫酸分子内有4个氧原子以及2个和氧原子直接相连的氢原子(羟基氢原子),具备形成分子间氢键的条件,所以,硫酸自身分子之间存在大量的氢键作用,故沸点和一般的液体物质相比显得非常高(相对分子质量接近的烷烃C7H16,熔点90.6℃,沸点98.4℃).由于硫酸分子之间作用力太强,以至于流动性减弱,显得黏稠.
硫酸分子与水分子之间也可以形成大量氢键,故硫酸与水可以以任意比例混溶.由于形成氢键的过程释放能量,所以硫酸溶于水的过程中会释放大量的热(该过程也包含破坏原来的“硫酸—硫酸”“水—水”分子间氢键,这2个过程会吸收能量,从实验事实看,“硫酸—水”分子间形成氢键释放的能量多于破坏原来的氢键所吸收的能量).硫酸具有强吸水性的原因,也和它容易与水分子间形成氢键有关.
纯硫酸的密度为1.81g·cm-3,相对较大(相对分子质量接近的烷烃C7H16密度为0.7g·cm-3),显然也与其分子间作用力强,彼此结合更紧密有关.
这里需要说明的是,油状、黏稠的性状和密度大小并无直接关联.比如CCl4,它的密度很大(密度1.6g·cm-3),但并不黏稠,用滴管取用CCl4时可以看到,CCl4液滴比水滴小得多,又由于其密度大且与玻璃不易浸润,一不小心很容易滴落到桌面上.
2) 硫酸的吸水性和脱水性有何区别与联系?胆矾遇浓硫酸变白过程中,硫酸表现了吸水性还是脱水性?
一般认为,吸水性属于硫酸的物理性质,而脱水性则属于硫酸的化学性质,但又很难说清楚硫酸是如何表现其化学作用的,因为吸水、脱水前后,硫酸似乎都还是硫酸,只是浓度有所降低而已.宏观上,从硫酸的角度看,似乎二者并无本质区别.其实不然,硫酸吸水虽然不能说就是简单的物理过程(形成氢键属于物理变化还是化学变化?这个问题存在争议),但毕竟硫酸分子结合的是原本就独立存在的H2O分子.相比而言,硫酸脱水的过程就很复杂了,比如硫酸使蔗糖脱水,硫酸一定参与了蔗糖脱水的反应过程,只是最终又恢复了原来的成分而已.蔗糖结构比较复杂,让我们以乙醇脱水过程为例加以说明:
C2H5OH+HO—SO2—OH→
C2H5—O—SO2—OH(硫酸氢乙酯)+H2O,

在硫酸催化乙醇脱水反应中,硫酸的作用就是催化剂,其催化的本质就是脱水,所以传统说法“催化剂、脱水剂”属于重复叙述.
把胆矾加入浓硫酸中搅拌,蓝色固体逐渐变白的过程中,硫酸表现了吸水性还是脱水性呢?让我们借助如图4所示实验加以说明.

图4
实验表明,图4所示密闭系统内,左侧容器内的蓝色的胆矾晶体经过很长一段时间后会变白,而右侧容器内硫酸的浓度则会降低.那么此实验中硫酸表现了吸水性还是脱水性呢?显然是吸水性.若把硫酸和胆矾直接混合,胆矾变白的原理与这个实验并无不同.
3) 何谓发烟硫酸?发烟硫酸发出的是烟吗?
纯硫酸具有吸收、溶解SO3的能力,硫酸工业正是根据这一点,利用98.3%的浓硫酸吸收SO3的,因为该溶解过程放热少,且硫酸沸点高,不易导致硫酸沸腾产生酸雾.
吸收了过多SO3的硫酸就是发烟硫酸,吸收了过多SO3的发烟硫酸因SO3挥发,与空气中的水蒸气作用形成大量硫酸酸雾,肉眼难以辨别是烟还是雾,被称为“发烟硫酸”.
(作者单位:北京十一学校)
