HPLC法测定注射用丹参多酚酸盐中丹参乙酸镁的含量
2016-04-19时荣同张清文叶小虎
时荣同,张清文,姚 惠,叶小虎
(皖北煤电集团总医院药剂科,安徽 宿州 234011)
HPLC法测定注射用丹参多酚酸盐中丹参乙酸镁的含量
时荣同,张清文,姚惠,叶小虎
(皖北煤电集团总医院药剂科,安徽 宿州234011)
摘要:目的研究合适的分离方法分离注射用丹参多酚酸盐中丹参乙酸镁,采用HPLC法检测丹参乙酸镁含量,观察HPLC法的应用效果。 方法采用正交试验进行方法优选。采用Zorbax-SB-C(18) (250 mm×4.6 mm,5 μm)色谱柱,以乙腈—四氢呋喃(26∶74)为流动相;流速:1.0 mL·min(-1);检测波长:以 ELSD 检测器进行检测,波长为290 nm;参数为:增益 10,气压 25 psi,漂移管65℃,Neb heater 60%;柱温:25℃;进样量:10 μL。 结果丹参乙酸镁峰面积的自然对数值与浓度的自然对数值呈良好的线性关系,丹参乙酸镁的标准曲线方程为:Y = -2.006X + 7.355,R2 = 0.999 3,线性范围为59.79~597.90 mg·L(-1);丹参乙酸镁的平均回收率为 98.02%,RSD 为6.87%。 结论HPLC法测定注射用丹参多酚酸盐中丹参乙酸镁的含量操作简单,且可重复性好,可用于注射用丹参多酚酸中丹参乙酸镁的含量测定。
关键词:丹参多酚酸盐;丹参乙酸镁;HPLC法
丹参为唇形科鼠尾草属植物丹参(SalviamiltiorrhizaBge)的干燥根及根茎,临床多用于活血化瘀[1]。据《神农本草经》记载,丹参具有祛瘀止痛、活血通经支功效[2]。现代药理学分析发现[3],丹参中的有效成分之一的水溶性成分具有抑制血小板聚集、防治动脉粥样硬化、抗肝损伤抗肝纤维化和诱导细胞凋亡等功效。
丹参多酚酸盐是从丹参中提取的以丹参乙酸镁为主要成分的丹参多酚酸盐类化合物,具有活血化瘀作用,目前临床已应用于冠心病的治疗[4]。但丹参多酚酸盐成分较为复杂,目前对其质量和工艺有着诸多的研究,但如何测定丹参多酚酸盐中各成分的含量及其对其质量的控制存在一定的难度,也具有重要的意义[4-5]。本研究采用高效液相色谱法(high performance liquid chromatography,HPLC)检测丹参多酚酸盐中丹参乙酸镁含量,对方法进行优化,以观察HPLC法的检测效果。现将结果报道如下。
1仪器和试药
1.1实验仪器高效液相色谱仪:Agilent 1100,配Agilent 1200ELSD 检测器,美国Agilent公司生产;电子天平:XP型十万分之一电子分析天平,Mettler Toledo 公司生产。SPE-C18固相萃取柱,规格6 mL。
1.2实验药品注射用丹参多酚酸盐,批号分别为20150912、20150920;规格:每瓶160 mg(丹参乙酸镁),上海绿谷制药有限公司产;丹参乙酸镁对照品,超纯水。
2方法和结果
2.1色谱条件参数的研究和结果
2.1.1优化后的色谱条件参数色谱柱:Zorbax-SB-C18(250 mm×4.6 mm,5 μm);流动相:以乙腈—四氢呋喃(26∶74)为流动相(为正交试验优化所得);流速:1.0 mL·min-1(为正交试验优化所得);检测波长:290 nm。
具体参数设置为[6-7]:增益 10,气压 25 psi,漂移管64℃,Neb heater 60%;柱温:25℃;进样量10 μL;外标法。其中漂移管温度为正交试验优化所得。
在此条件下,丹参乙酸镁的出峰时间tR=(23.7±0.1) min。峰型对称良好,前后无干扰组分峰。参见图1图2。
2.1.2色谱条件参数的研究实验 正交试验委托安徽医科大学公共卫生学院实验中心进行。根据此前预试验的结果,决定重点筛选4个色谱条件参数(表1),设计为4因素3水平的正交试验,使用L9(34)正交表,进行优化选择。
正交试验效应量(判断指标)由HPLC峰高(mV)和定量准确度(%)合并构建: 效应量=峰高(mV)×回收率(%),判断方向:以大为优。
所用样品为后述对照品溶液(No 5,0.16 g·L-1),进样量为20 μL。
正交试验因素水平设计见表1;正交试验结果见表2;方差分析结果见表3。
按正交试验结果,并进行最后的试验微调,最终得优化后的HPLC条件参数如“2.1.1”。

表1 正交试验因素及水平(色谱条件参数)选择
注:流动相配比做随机化处理。
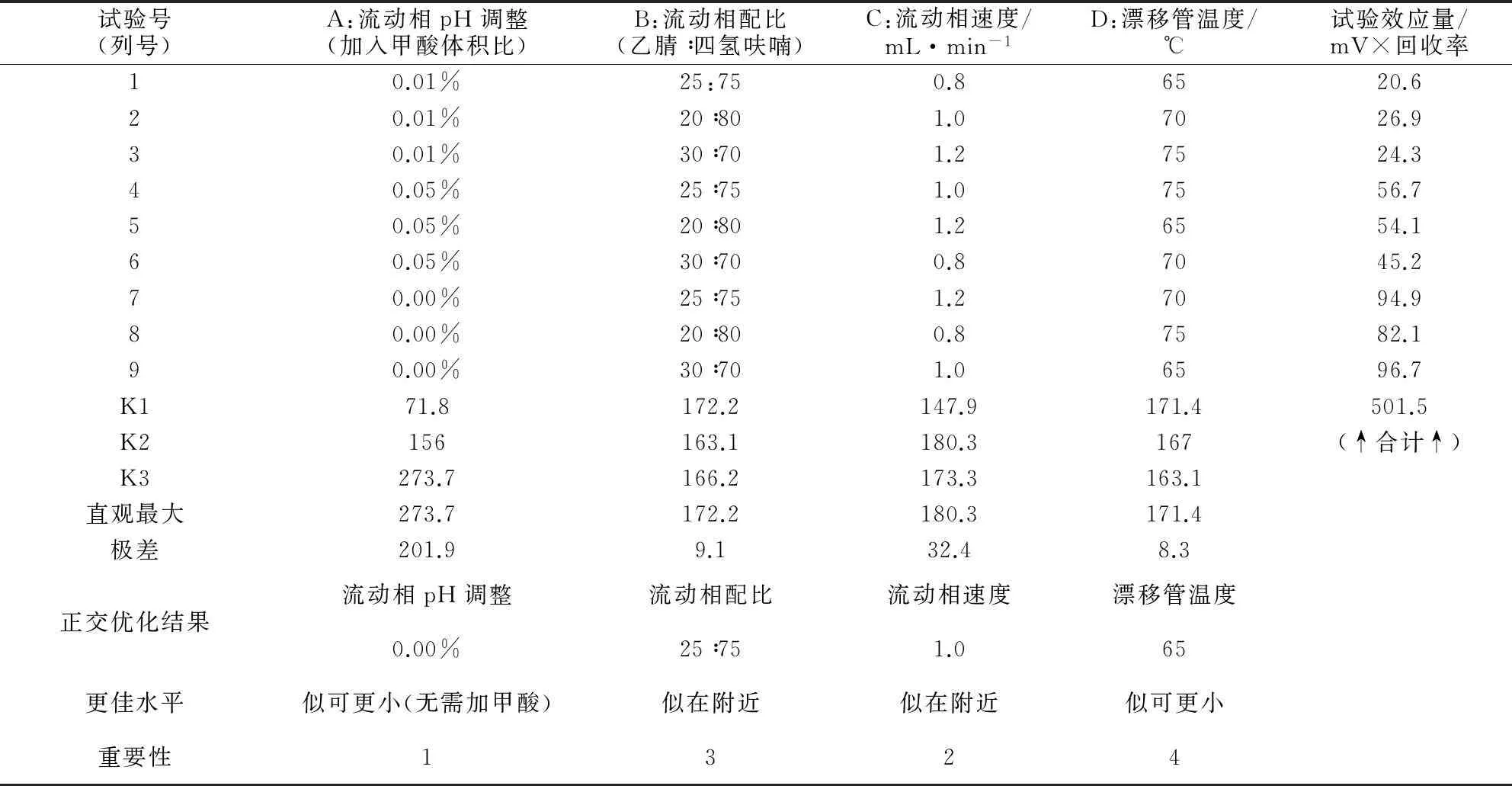
表2 正交试验结果及直观分析
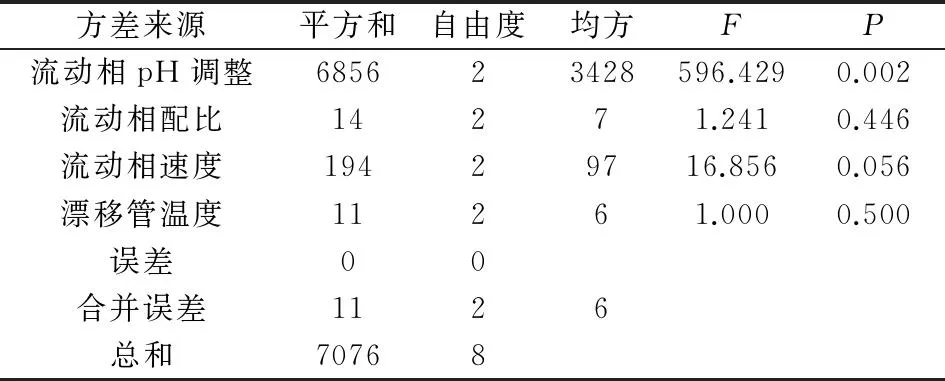
表3 方差分析结果
注:此为饱和正交试验,误差项实为0,且取平方和最小项为误差,以提高分析灵敏度。
2.2各种实验溶液的配制
2.2.1供试品溶液配制用精密天平称取干燥的注射用丹参多酚酸盐100.0 mg,用 5.0 mL 水溶解,滴加0.1%的醋酸溶液,调整 pH 至微酸性(pH5.5~6.5)。再加至SPE-C18过滤柱头(固相萃取小柱),过柱并水洗。过柱液体总量为20.0 mL,收集后再加约5 倍柱体积的进行洗脱(总约30 mL)。最后加水补至 100.0 mL,混匀。
2.2.2对照品溶液配制 用精密天平量取对照品丹参乙酸镁适量,加流动相溶解并定量稀释,制成1.0 g·L-1的对照品储备液。再精密量取对照品储备液2.0 mL,置 10 mL 量瓶中,加流动相稀释至刻度,摇匀,即得浓度为0.20 g·L-1的对照品溶液[8]。
2.3线性关系考察分别精密量取对照品溶液1、2、4、6、8、10 mL置 10 mL量瓶中,用超纯水定容至刻度,摇匀。分别取20 uL进行进样,记录峰面积A,以峰面积的自然对数值对质量浓度的自然对数值进行线性回归,绘制标准曲线。根据曲线所得丹参乙酸镁的标准曲线方程为:Y=-2.006X+7.355,R2= 0.999 3,线性范围为59.79~597.90 mg·L-1(按供试品取样方法折合)。数据见表4,HPLC谱图见图1。
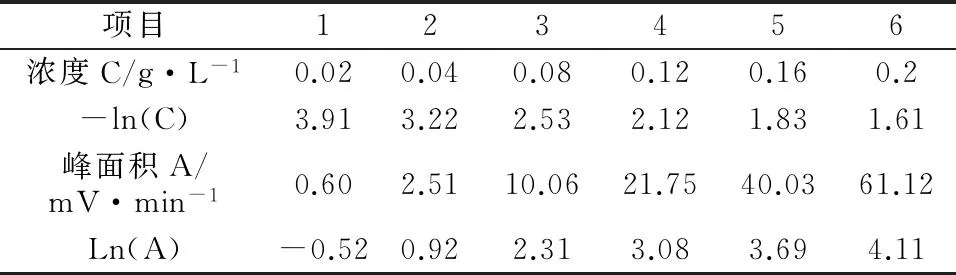
表4 标准曲线测定结果
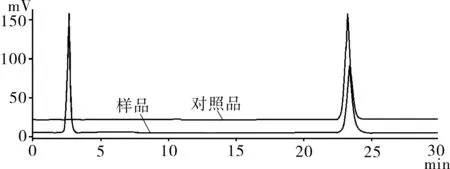
图1丹参乙酸镁对照品与注射用丹参多酚酸盐
样品 HPLC 色谱图
2.4精密度、重复性、准确度、稳定性试验
2.4.1精密度精密吸取某供试品溶液按上述色谱条件连续进样 6 次,进样量 20 μL,测定丹参乙酸镁的峰面积(mV·min-1)分别为38.96、38.94、38.63、40.05、40.72、39.14,平均(39.41±0.80)。测得丹参乙酸镁峰面积的 RSD为2.01%,结果表明仪器的精密度良好。
2.4.2准确度即加样回收率实验:精密称取 6 份已知含量的干燥的注射用丹参多酚酸盐,每份 50 mg,分别加入丹参乙酸镁对照品溶液适量,然后用超纯水定容至 5 mL,调整 pH 至酸性,过柱体积为20 mL,收集直接流出液和3 倍柱体积水洗液,加水补至75 mL,混匀,在上述色谱条件下进行测定,计算回收率和 RSD 值。回收率(%)分别为94.42、93.36、107.18、104.93、98.00、90.25,平均(98.02±6.73)。即丹参乙酸镁的平均回收率为 98.02%,RSD 为6.87%。
2.4.3稳定性取新配制低、中、高三种不同浓度的供试品溶液,室温静置0、4、6、8 h进行测定,结果其RSD均小于6.28%,表明样品在8 h内稳定性良好。
2.5样品测定从两个批次的注射用丹参多酚酸盐中随机抽出6瓶样品(标示量每瓶160 mg),采用本法进行HPLC测定,对应的HPLC谱图见图2。其每瓶丹参乙酸镁含量分别为167、164、157、145、134、134 mg,平均(150.19±14.44)mg。
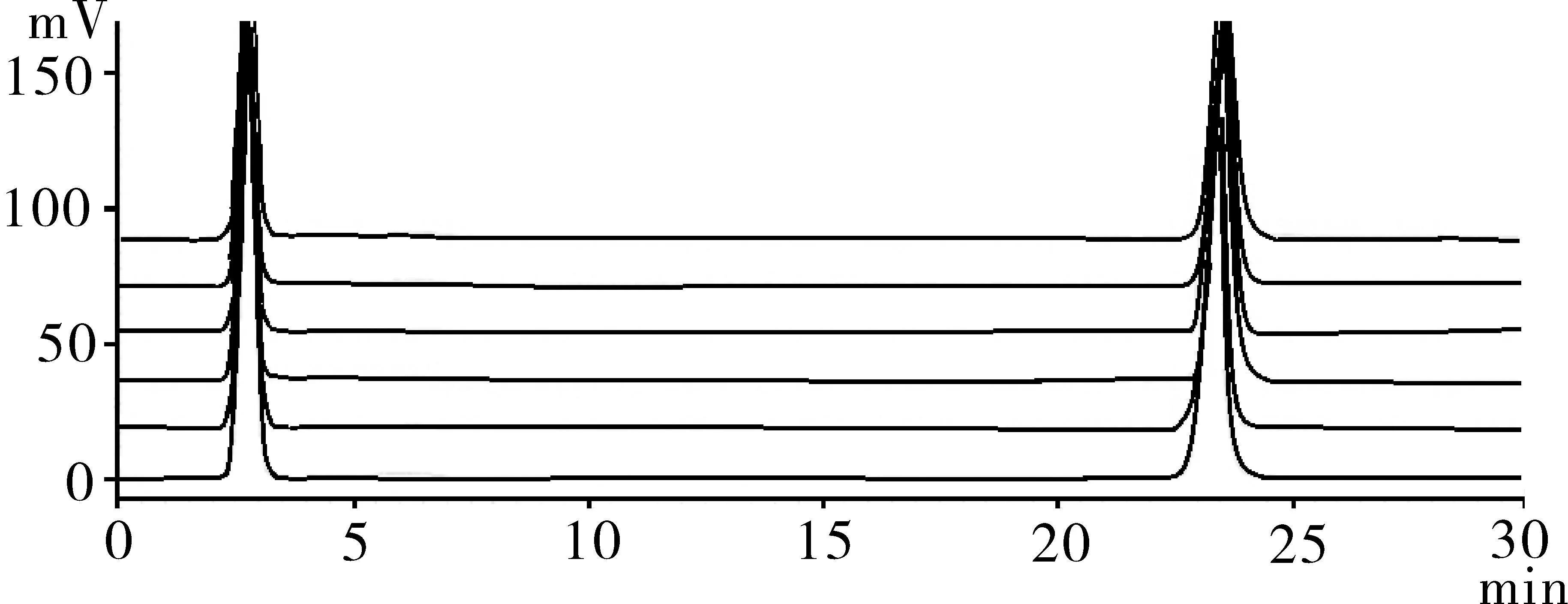
图2 6批次注射用丹参多酚酸盐样品的
3讨论
丹参是我国传统医药学中应用最早而且最广泛的药物之一,有“一味丹参功同四物”的说法,由于其含多种成分,因此对每组样品的不同测定对不同药物的制作及准确应用有着显著的效果[9]。
本组研究采用HPLC法检测丹参多酚酸盐中丹参乙酸镁含量,观察HPLC法的检测效果,结果显示:两个批次的多份丹参多酚盐样品中的丹参乙酸镁含量相对来说比较稳定,表明:采用HPLC方法检测简便易行,临床可用于监控和评价丹参多酚酸盐的质量。
有文献介绍:由于注射用的丹参多酚盐中的酚主要以钠盐形式存在,在HPLC方法进行测定时,也需要对流动相进行pH值的调节试验,以防多酚盐中物质因流动相中的水性组分影响致其结构转变[10]。在本试验中,由于所用流动相并不含有水,故加甲酸调节的效果未能体现(见正交试验的结果)。这是否对方法的性能及结果,例如含量为每瓶160 mg实测每瓶为(150.19±14.44)mg,存有一定的影响,有待今后的试验中继续探索。
综上所述,HPLC法测定注射用丹参多酚酸盐中丹参乙酸镁的含量操作简单,且重现性较好,可用于注射用丹参多酚酸中丹参乙酸镁的含量测定。
参考文献:
[1]国家药典委员会.中国药典(一部)[S]. 北京:中国医药科技出版社,2010:70.
[2]杨菲,王智民,张启伟,等.“一测多评”法测定丹参酚酸类成分的含量[J].中国中药杂志,2011,36(17):2372-2379.
[3]薛静,叶正良,李德坤,等.HPLC 同时测定注射用丹参多酚酸中丹酚酸 D,迷迭香酸,紫草酸,丹酚酸 B 的含量[J].中国实验方剂学杂志,2013,19(3):70-73.
[4]刘畅,刘玉强,张振秋,等.HPLC 波长切换法同时测定山楂丹参分散片中 6 个指标性成分的含量[J].中国新药杂志,2014,23(3):333-337.
[5]徐静瑶,刘小琳,佟玲,等.高效液相色谱法测定注射用丹参多酚酸中 6 种水溶性成分的含量[J].中国新药杂志,2015,24(14):1599-1604.
[6]盛少琴,褚红女,倪娟,等.高效液相色谱法测定孕羊羊水中丹参乙酸镁的含量[J]. 医学研究杂志,2011,40(9):73-75.
[7]厉瑶,郭正泰,龚行楚,等.丹参红花混煎液中丹参素,羟基红花黄色素 A,迷迭香酸,紫草酸和丹酚酸 B 的 HPLC 测定方法[J].中国中药杂志,2013,38(11):1653.
[8]吴笛,叶秋雄,李楚源.一测多评法测定复方丹参片中5 种酚酸类成分的含量[J].中国新药杂志,2013,22(18):2130-2135.
[9]赵琼,任大伟,杨瑞花,等.丹参不同产地加工方法对丹参多酚酸盐质量的影响[J]. 中华中医药杂志,2013,28(3):645-648.
[10] 詹雪艳,史新元,孙启生,等.基于组合相似度丹参样本质量稳定性评价[J].中华中医药杂志,2012,27(6):1650-1654.
(收稿日期:2015-11-09,修回日期:2016-01-15)
doi:10.3969/j.issn.1009-6469.2016.03.015
