乙醇木素纯化及其结构表征
2016-04-19丁子栋周景辉
赵 吉 丁子栋 王 兴 周景辉,*
(1.大连工业大学轻工与化学工程学院,辽宁大连,116034;
2.大连市供水有限公司,辽宁大连,116021)
·木素纯化·
乙醇木素纯化及其结构表征
赵吉1丁子栋2王兴1周景辉1,*
(1.大连工业大学轻工与化学工程学院,辽宁大连,116034;
2.大连市供水有限公司,辽宁大连,116021)
摘要:采用弱酸法及液液提纯法提纯杨木乙醇制浆黑液中分离的木素,通过离子色谱仪、红外光谱仪、碳核磁共振光谱仪及热重分析仪,分析纯化效果并对纯化后木素的结构及其热稳定性进行分析。结果表明,粗木素总含糖量为0.99%,木素纯度为98.67%;液液法纯化对糖类杂质的去除效果较好,纯化后总糖含量降低到0.36%,木素纯度提高至99.64%。液液法纯化后木素的热稳定性有一定的提高,最大失重峰由320℃提高至350℃。纯化前后乙醇木素结构有一定变化,木素缩合程度有一定的增加。纯化后乙醇木素富含游离羟基、甲氧基等功能基,更加有利于其利用。纯化后乙醇木素纯度较高有利于结构分析。
关键词:乙醇制浆;木素;提纯;结构分析
新能源、新材料的开发和利用备受关注,植物中的木素是自然界中唯一大量含有芳香类结构的可再生资源。木素含量视植物种类和品种不同稍有不同,针叶木一般为25%~35%;阔叶木一般为18%~22%;禾本科植物一般为16%~25%[1]。从制浆黑液中分离得到的粗木素杂质较多,尤其是碱法制浆中的木素含有较多的无机灰分、糖类等杂质,不利于木素的改性利用[2-3]。
乙醇制浆是有机溶剂法制浆中研究较为充分的制浆方法之一,具有制浆过程用药剂少、制浆得率较高、纸浆强度较高、乙醇易回收、木素易得等优点,且蒸煮所得黑液含有大量的糖类以及有机酸等有价值的副产物。此外,乙醇制浆分离所得木素含无机物灰分少、木素结构变化较小、有利于木素结构改性及应用的研究[4-7]。
针对木素含有大量芳香类结构的特点,众多的研究者致力于研究木素的热解、超临界解聚等,以得到用于生产生物质燃油和化工中间产物的低环、单环芳香化合物。但乙醇木素中含有的杂质影响木素解聚,增加了降解产物研究的难度[3,8]。为更好地研究和利用木素,去除乙醇木素中含有的灰分及糖类等杂质是非常必要的。本实验采用酶解-弱酸两步法中的弱酸段提纯法[9]和Lundquist液液提纯法[10]来提纯杨木乙醇制浆黑液中的木素,并对纯化后的木素结构进行初步表征,旨在考察不同提纯方法对杂质的去除效果及乙醇木素在提纯过程中结构的变化。
1实验
1.1原料与试剂
原料为三倍体毛白杨,由岳阳泰格林纸集团有限公司提供,经人工挑选除尘后,放入密封袋平衡水分备用。
阿拉伯糖、半乳糖、葡萄糖、木糖、甘露糖、果糖均为色谱纯,购自Sigma公司;浓盐酸、1,4-二氧六环、NaHCO3、NaOH、浓硫酸、吡啶、醋酸、三氯甲烷、乙醚等均为国药分析纯产品。
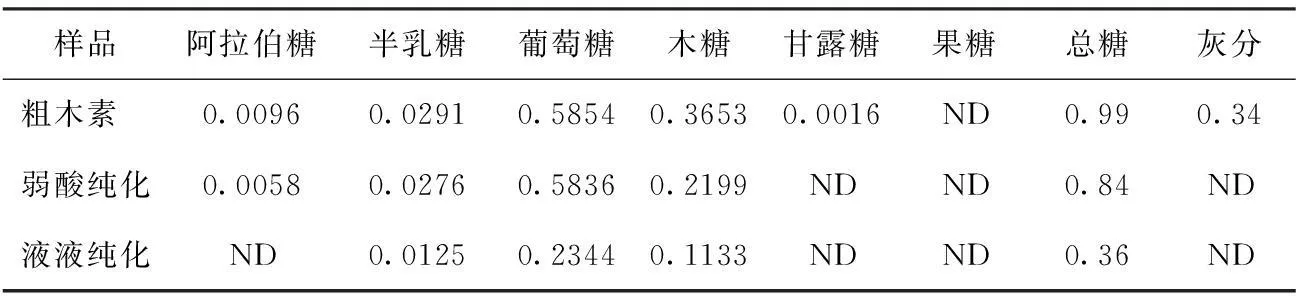
表1 粗木素和纯化后木素水解液单糖含量及灰分含量 %
注ND为未检测到。
1.2木素的制备与纯化
杨木乙醇制浆黑液由实验室制得,工艺条件为:乙醇浓度60%,液比1∶10,最高温度205℃,保温时间150 min[4]。制得的黑液过滤后加水沉淀,加入适量盐酸使木素沉淀较为完全,过滤并洗涤固体,冷冻后置于冷冻干燥机冻干,制得粗木素。
按照参考文献[9]对粗木素弱酸法进行纯化:将木素溶解到二氧六环-水溶液中(85∶15,体积比)中,木素浓度为5%,加酸调节溶液pH值至2,通入氮气,80℃左右加热回流2 h,过滤取滤液,杂质用二氧六环-水溶液洗涤,碳酸氢钠中和,滤液室温下由旋转蒸发浓缩后,缓慢滴加到pH值为2的酸水中,过滤沉淀木素,冷冻干燥后用色谱级正己烷洗涤,真空干燥后即为弱酸法纯化木素。
按照参考文献[10]对粗木素进行液液提纯法纯化:将1.5 g粗木素溶于42 mL吡啶-醋酸-水(9∶1∶4,体积比)混合溶液中,充分溶解后加入54 mL氯仿,充分混合后,至分液漏斗,分层后取下层三氯甲烷相,室温下旋转蒸发除去氯仿,加入乙醚中沉淀,过滤收集沉淀木素并在室温下干燥过夜即为液液提纯法纯化木素。
1.3木素糖含量及灰分含量测定
分别称取粗木素与纯化后的木素各0.1 g放于150 mL锥形瓶中,准确加入1.5 mL 72%的浓H2SO4,混合均匀后放入20℃的恒温摇床反应2 h后,加入42 mL 去离子水,在121℃的恒温油浴中水解1 h,用G3玻璃坩埚过滤,收集滤液。采用离子色谱分析仪进行糖含量的测定。
木素灰分含量测定参照GB/T2677.3—1993进行。
1.4分析方法
1.4.1离子色谱分析[11]
水解液稀释10倍,用0.45 μm水系过滤头过滤。滤液用美国戴安公司的ICS-5000离子色谱仪检测。色谱分离条件为:分析柱CarboPac TM PA20,150×3 mm;保护柱CarboPac TM PA20,30×3 mm;柱温30℃;流速0.5 mL/min;ED5000电化学检测器,Ag电极,淋洗液分别为0.2 mol/L NaOH、0.2 mol/L NaAc、2 mmol/L NaOH和超纯水。
1.4.2红外光谱分析
纯化后的木素红外灯干燥后与KBr晶体按质量比1∶100混合后研磨均匀,用压片机压片,压好的薄片用PE公司Frontier系列傅里叶变换红外光谱仪检测木素结构。
1.4.3核磁共振碳谱(13C-NMR)分析
以氘代二甲基亚砜为溶剂,将80 mg木素溶解于0.6 mL DMSO-d6溶剂中,在50℃下使用Bruker ADVANCE Ⅲ QNP探头核磁共振光谱仪,以75.5 MHz的频率扫描10000次,进行13C-NMR分析,进一步对木素精细结构进行检测。
1.4.4热稳定性分析
木素热稳定性分析实验在Q50-TGA热重分析仪上进行。取适量木素放入玛瑙研钵中研细后,将约10 mg木素均匀平铺于铂金称量盘面。以高纯氮气为载气,流速40 mL/min。升温速率20℃/min,升温区间30~700℃。
2结果与讨论
2.1糖含量及灰分分析
将粗木素和纯化后的木素进行水解,用离子色谱法测定各单糖含量。粗木素与纯化后木素的单糖含量及灰分含量测定结果见表1,单糖含量及灰分含量分别为对应原料的质量百分含量(%)。
从表1可知,两种提纯方法均有一定的效果,弱酸法纯化木素后甘露糖消失,其他单糖含量只有较少的降低;液液法纯化木素效果好于弱酸法的。液液法纯化木素后阿拉伯糖和甘露糖消失,与粗木素相比,其他单糖含量明显降低,液液法纯化木素后总糖含量由0.99%降低到0.36%,木素纯度由粗木素的98.67%提高至99.64%,纯化后木素纯度较高,更加有利于后续乙醇木素结构的研究及其改性利用。

图2 粗木素及纯化后木素13C-NMR谱图
2.2红外光谱分析
粗木素和纯化后木素的红外光谱图见图1,木素基团归属及其强度见表2。
由图1及表2可知,纯化后木素的结构变化不明显,部分基团强度存在一定的差异。3420 cm-1处附近均有羟基强烈的伸缩振动峰,吸收峰面积较大,说明粗木素中含有大量的游离羟基;2939、2842 cm-1处均有甲基、亚甲基C—H键明显的伸缩振动峰,表明粗木素中含有较多的烷基侧链;1328、1121 cm-1处附近均有较强的C—C键特征吸收峰,表明纯化后木素含有较多的紫丁香基和愈创木基。此外,从图2中还可以看出粗木素中含有较多的羰基、甲氧基等功能基团,可在一定程度上增加粗木素的活性,有利于其改性及利用[12]。
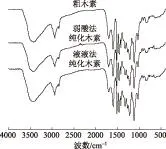
图1 粗木素和纯化后木素红外光谱图

波数/cm-1粗木素弱酸法纯化木素液液法纯化木素基团归属341934263426羟基O—H伸缩振动293829392939亚甲基C—H伸缩振动284228422842甲基C—H伸缩振动170417041702CO伸缩振动160616061596芳环振动151515151514芳环振动142514251424芳环振动132813281328紫丁香基127112711270C—O伸缩,愈创木基121712171219C—O伸缩,芳环111811181121紫丁香基和愈创木基C—C103210321032芳香核C—H面外弯曲振动
2.313C-NMR分析
采用核磁共振光谱仪对木素的精细结构进行进一步考察,粗木素及纯化后木素的13C-NMR谱图见图2。并对不同化学位移对应的木素结构进行图谱解析,结果见表3。按照参考文献[13-15]对粗木素进行13C-NMR处理,以木素芳香环δ=102~160为基准对其结构及基团进行积分,重点考察木素间连接键及部分官能团。
从表3可以看出,β-O- 4型连接是杨木木素结构单元的一个重要特征,此外,还有一定的β-β等连接,杨木粗木素中含有大量的愈创木基(G)、紫丁香基(S)及少量对羟苯基型(H)结构单元。两种纯化方法纯化后木素结构有一定差异,主要表现为纯化后木素有一定的缩合,甲氧基含量及部分连接键含量有所变化。对弱酸法纯化木素,其甲氧基含量较其余木素明显降低,而液液法纯化木素,其甲氧基含量与粗木素相比减少更加明显,β-O- 4、β-β连接均有较大幅度的增加,木素缩合程度更为明显。

表3 粗木素及纯化后木素13C-NMR谱图解析
弱酸法纯化过程中较高的温度可能使木素缩合,其甲氧基含量减少,木素芳环结构及主要连接键与粗木素相比变化较小,因而其缩合程度有限;而液液法纯化过程中使用醚类等有机溶剂较多,使得部分低分子质量醚键连接的木素结构在醚类等有机溶剂的溶解度增加,尤其是含有甲氧基较多的木素结构片段,纯化过程中该部分木素不易在醚类溶剂中析出,使得木素结构中甲氧基含量及苯环上的C—O链接大幅减少,小分子质量木素的去除使得木素的缩合程度有所提高。
2.4热稳定性分析
图3为粗木素及纯化木素的热重分析曲线。由图3可知,随着温度的升高,纯化前后木素的TG曲线快速下降,木素开始失重,失重速率DTG曲线开始增大。当TG曲线趋于平稳以及DTG速率几乎不变时,木素降解反应结束。从TG和DTG曲线上可以看出,木素在100℃前的失重应该是木素水分损失引起的。木素降解主要在140~460℃之间,大致可以分为4个阶段,第一阶段(140~200℃)主要是木素脂肪链上β-O- 4醚键中结合力较弱的化学键断裂;第二阶段(200~350℃)主要是木素中β-O- 4醚键断裂;第三阶段(350~400℃)主要是木素侧链氧化及其脱水;第四阶段(400~600℃)主要是木素C—C键断裂,芳环降解,以及芳环中甲氧基的脱除[16]。至700℃左右时,木素降解几乎停止,此时仍有约38%的木素未发生降解,木素最终的失重率约为62%。
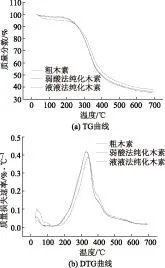
图3 粗木素和纯化木素热重分析曲线
由图3还可知,弱酸法纯化木素的TG、DTG曲线和粗木素的TG、DTG曲线差别很小,其最高降解速率温度为320℃左右,而液液法纯化木素的TG和DTG曲线总体上要比前两者有明显提高,木素降解温度有一定的上升,其最高降解速率在350℃左右。300℃左右主要是β-O- 4醚键的断裂,β-O- 4醚键的含量对木素的热稳定性有较大的影响。采用液液法纯化木素后其β-O- 4醚键含量增加较为明显,因此液液法纯化后木素的热稳定有一定的增加,此外,木素热稳定性还受较多因素的影响,如木素缩合程度、羟基含量等因素[16]。
3结论
3.1用液液提纯法提纯的乙醇木素对糖类杂质的去除率比用弱酸法提纯的高。纯化后木素总糖含量由粗木素的0.99%降低到0.36%,粗木素水解液中含有的单糖主要是半乳糖、葡萄糖和木糖。木素纯度由粗木素的98.67%提高到99.64%。
3.2纯化前后木素的红外光谱和核磁共振碳谱(13C-NMR)分析表明,乙醇木素纯化后结构发生一定的改变,纯化后乙醇木素均有一定的缩合,乙醇木素液液法纯化后β-O- 4及β-β型连接增加。纯化后的木素含有较多的游离羟基、羰基和甲氧基等功能基,乙醇木素活性较高。
3.3纯化前后木素的热稳定性分析表明,粗木素的降解温度主要在140~460℃之间,粗木素和弱酸法纯化木素在320℃左右出现最大失重峰。液液法纯化后的木素最高降解速率提高至350℃左右,比粗木素提高30℃左右,热稳定性有一定的提高。无论是粗木素还是纯化后木素降解至700℃左右时,木素降解均几乎停止,最终失重率约为62%。
参考文献
[1]Yang Shu-hui. Plant Fiber Chemical[M]. Beijing: China Light Industry Press, 2010.
杨淑蕙. 植物纤维化学[M]. 北京: 中国轻工业出版社, 2010.
[2]LI Zhong-zheng. Research on renewable biomass resource[J]. Joumal of Nanjing Forestry UniversiIy(Natural Science Edition), 2012, 36(1): 1.
李忠正. 可再生生物质资源-木质素的研究[J]. 南京林业大学学报:自然科学版, 2012, 36(1): 1.
[3]REN Miao-miao, LU Hui-hua, ZHANG Min-hua, et al. Research Progress on the Application of Lignin[J]. Polymer Bulletin, 2012(8): 44.
任苗苗, 吕惠生, 张敏华, 等. 木质素资源利用的研究进展[J]. 高分子通报, 2012(8): 44.
[4]ZHOU Jing-hui, SUI Xin-jin, PING Qing-wei. Change of Aspen Lignin Structure in Auto-catalyzed Ethanol-water Pulping[J]. Transactions of China Pulp and Paper, 2008, 23(3): 16.
周景辉, 隋鑫金, 平清伟. 杨木乙醇制浆中木素结构变化的研究[J]. 中国造纸学报, 2008, 23(3): 16.
[5]PU Wen-juan, XU Yong-jian, ZHANG Mei-yun. Outlook of Non-wood Fibrous Materials Ethanol Pulping[J]. China Pulp & Paper, 2007, 26(8): 52.
蒲文娟, 徐永建, 张美云. 非木材纤维原料乙醇制浆的发展前景与展望[J]. 中国造纸, 2007, 26(8): 52.
[6]AN Jie, ZHOU Jing-hui, SUN Guang-wei, et al. Analysis of the Organic Acids in the Waste-liquor of Aspen Auto-catalyzed Ethanol-water Pulping[J]. Transactions of China Pulp and Paper, 2011, 26(1): 41.
安洁, 周景辉, 孙广卫, 等.杨木自催化乙醇制浆废液中有机酸的分析[J]. 中国造纸学报, 2011, 26(1): 41.
[7]ZHANG Mei-yun,TAN Guo-ming. Auto-Catalyzed Ethanol-Water Pulping of Chinese Alpine Rush[J]. China Pulp & Paper, 2002, 21(4): 23.
张美云, 谭国民. 龙须草自催化乙醇法制浆工艺参数的优化[J]. 中国造纸, 2002, 21(4): 23.
[8]WANG Xing, ZHOU Jing-hui. The research progress on characteristics of lignin’s chemical depolymerization products and its depolymerization mechanism[J]. China Pulp & Paper Industry, 2014, 33(4): 32.
王兴, 周景辉. 木素化学解聚产物特征及机理研究进展[J]. 中华纸业, 2014, 33(4): 32.
[9]LIU Yu. The research of triploid Populus tomentosa EMCC pulping and TCF bleaching and change of lignin structure[D]. Guangzhou: South University of Technology, 2005.
刘玉. 三倍体毛白杨EMCC蒸煮和TCF漂白及其木素结构变化的研究[D]. 广州: 华南理工大学, 2005.
[10]Lundquist K, Ohlsson B, Simonson R. Isolation of lignin by means of liquid-liquid extraction[J]. Svensk Papperstidning, 1977, 80(5): 143.
[11]CUI Jin-long, LI Hai-ming, BI Jia-jie. Analysis of carbohydrates in papermaking materials by ion chromatography[J]. Journal of Dalian Polytechnic University. 2013, 32(6): 432.
崔金龙, 李海明, 毕佳捷. 离子色谱在造纸原料碳水化合物分析中的应用[J]. 大连工业大学学报, 2013, 32(6):432.
[12]Liu Chao, Wu Shu-bin, Zhou Jing-hui. Purification of Alcell Lignin from Aspen with Mild Acidolysis and Study on Its Physicochemical Properties[J]. Paper Science & Technology, 2014, 33(6): 7.
刘超, 武书彬, 周景辉. 杨木乙醇黑液木质素的温和酸解纯化及其理化特性研究[J]. 造纸科学与技术, 2014, 33(6): 7.
[13]Chum H L, Black S K, Johnson D K, et al. Organosolv pretreatment for enzymatic hydrolysis of poplars: isolation and quantitative structural studies of lignins[J]. Clean Products and Processes, 1999, 1(3): 187.
[14]Capanema E A, Balakshin M Y, Kadla J F.A comprehensive approach for quantitative ligin characterization by NMR apectroscopy[J]. Journal of Agricultural and Food Chemistry, 2004, 52(7): 1850.
[15]Capanema E A, Balakshin M Y, Kadla J F. Quantitative characterization of a hardwood milled wood lignin by nuclear magnetic resonance spectroscopy[J]. Journal of Agricultural and Food Chemistry, 2005, 53(25): 9639.
[16]Wen J L, Xue B L, Sun S L, et al. Quantitative structural characterization and thermal properties of birch lignins after auto-catalyzed organosolv pretreatment and enzymatic hydrolysis[J]. Journal of Chemical Technology and Biotechnology, 2013, 88(9): 1663.

(责任编辑:董凤霞)
Purification of Ethanol-organosolv Lignin and Characterization of Its Structure
ZHAO Ji1DING Zi-dong2WANG Xing1ZHOU Jing-hui1,*
(1.SchoolofLightIndustryandChemicalEngineering,DalianPolytechnicUniversity,Dalian,LiaoningProvince, 116034;2.DalianWaterCorporation,Dalian,LiaoningProvince, 116021) (*E-mail: zhoujh@dlpu.edu.cn)
Abstract:Lignin exiting in the black liquor of aspen ethanol-organosolv pulping was purified by the methods of mild acid hydrolysis and liquid-liquid extraction. The properties of purified lignin, including chemical structure and thermal stability, were analyzed by ion chromatography, FT-IR, (13)C-NMR and thermogravimetric analysis. Results showed that the method of liquid-liquid extraction was better than mild acid hydrolysis in terms of removing carbohydrates. The content of total sugar in crude lignin was 0.99% and the purity of lignin was 98.67%. After purification, the content of total sugar in lignin was decreased to 0.36% and the purity of lignin was increased to 99.64%. It was found that the thermal stability of purified lignin was better than crude lignin indicated by the fact that the maximum weight loss peak of lignin shifted from 320℃ to 350℃. However, the structure of lignin had little change after purification. The purified aspen ethanol-organosolv lignin was rich in functional groups such as hydroxyl groups, methoxy groups, which was more benefite to its utilization. The higher purity of lignin was beneficial for analyzing the structure of the ethanol-organosolv lignin.
Key words:ethanol-organosolv pulping; lignin; purification; structure analysis
中图分类号:TQ351.01
文献标识码:A
DOI:10.11980/j.issn.0254- 508X.2016.03.006
*通信作者:周景辉先生,E-mail:zhoujh@dlpu.edu.cn。
基金项目:国家自然科学基金资助项目(31470604)、(31170554)。
收稿日期:2015-10-28(修改稿)
作者简介:赵吉先生,在读硕士研究生;研究方向:制浆造纸清洁生产与植物资源高值化利用。
