祛风安脑口服液质量标准研究
2016-04-19蒋霞黄银妹王小洁兰丽华李
蒋霞 黄银妹 王小洁 兰丽华 李梅
【摘 要】 目的:建立祛风安脑口服液定性、定量分析方法。 方法:采用TLC对麻黄、黄芩、防风、川芎进行定性鉴别;采用HPLC测定阿魏酸含量,色谱条件:以Inertsil ODS-3(250mm×4.6nm,5μm)为色谱柱,甲醇-1%冰醋酸(30∶70)为流动相,检测波长为321nm,柱温为25℃。结果:薄层色谱斑点清晰,阴性对照无干扰;阿魏酸在1.824~10.940μg线性关系良好(r=0.9998),平均回收率为100.51%,RSD=1.94%。结论:本方法简便易行、结果准确,可作为该产品质量控制的方法。
【关键词】 祛风安脑口服液;阿魏酸;HPLC ;TLC
【中图分类号】R286 【文献标志码】 A 【文章编号】1007-8517(2016)06-0019-04
祛风安脑口服液是我院中药制剂,处方源于《备急千金要方》所载的续命汤,由麻黄、红参、黄芩、肉桂、甘草、川芎、苦杏仁、熟附子、防风、干姜、石膏、赤芍、当归这十三味药材加工制成,具有疏通经络、调和营卫、解表祛邪的功效,临床用于中风、身体不能自持、口不能言或拘急不得转侧等症。为保证制剂质量稳定可控,研究采用薄层色谱法(TLC)对该制剂主要成分麻黄、防风、川芎、黄芩进行薄层色谱鉴别,并参考相关文献[1-2],采用高效液相色谱法(HPLC)测定制剂中阿魏酸的含量,为制定祛风安脑口服液的质量标准提供依据。
1 仪器与材料
1.1 仪器 SIL-10AF高效液相(含SPD-15C紫外检测器,岛津国际贸易上海有限公司);XS205DU十万分之一天平(梅特勒-托利多仪器上海有限公司);R-1001N旋转蒸发仪(郑州长城科工贸有限公司);
1.2 材料 硅胶板(青岛海洋化工分厂);点样毛细管(泰州市北平贸易有限公司);黄芩苷对照品(批号110715-200212,中国药品生物制品鉴定所);阿魏酸对照品(批号110773-201313,中国食品药品检定研究院);甲醇为色谱纯,水为超纯水,其他试剂为分析纯。
2 方法与结果
2.1 祛风安脑口服液的制备 除肉桂、红参外,其他药材加10倍量水,加热煎煮两次,每次1.5h,合并2次煎液,滤过。滤液浓缩,加入乙醇至乙醇浓度为65%,静置24h,滤过,回收乙醇至无醇味。取红参,加10倍水,加热煎煮2次,每次1.5h,滤过,合并2次煎液,浓缩,与上述制得的浓缩液合并,再加入肉桂粉,煮10min,过滤,加入苯甲酸3g,加蒸馏水至900ml,静置24h,滤过,滤液调至总量为1000ml,灌装,即得。
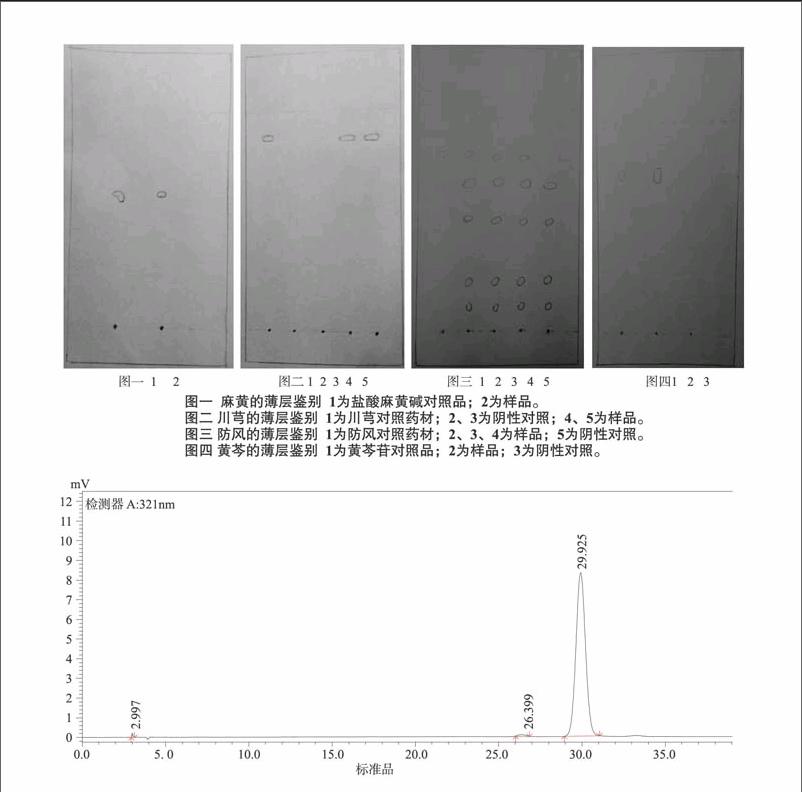
2.2 TLC定性鉴定
2.2.1 麻黄TLC 取样品20ml,加氨水调pH至1~2,用乙醚萃取2次,合并乙醚层,挥干乙醚,加盐酸乙醇(1∶20)10ml,摇匀,水浴蒸干,残渣加甲醇溶解,即为供试品溶液。另取盐酸麻黄碱对照品,加甲醇制成浓度为1mg/ml的溶液,作为对照品溶液。吸取上述溶液各5ml,分别点于硅胶G薄层板上,以正丁醇-冰醋酸-水=8∶2∶1为展开剂[3],展开,晾干,喷以茚三酮试液,105℃烘5min。供试品在与对照品的相应色谱位置上,均显相同紫红色斑点,Rf=0.62。
2.2.2 川芎TLC 取制剂样品10ml,加乙醚20ml萃取,超声10min,过滤,挥干乙醚,加乙酸乙酯1ml,即为供试品溶液。另取相同制备工艺制成的缺川芎的阴性样品,同法制成阴性对照品溶液。取川芎对照药材1g,加乙醚20ml,超声10min,滤过,挥干,加乙酸乙酯1ml,制成对照液。吸取上述溶液各5μl,分别点于同一硅胶G板,以氯仿-甲醇=8∶1为展开剂[4],展开,取出,晾干,置紫外光灯365nm下检视,供试品色谱中,在与对照药材相应的位置上,显相同颜色的斑点。阴性对照无干扰,Rf=0.857。
2.2.3 防风TLC 取制剂样品15ml,用乙酸乙酯萃取2次,每次20ml,合并乙酸乙酯层,水浴蒸干,残渣加甲醇1ml使溶解,作为供试品溶液。另取相同制备工艺制成的缺防风的阴性样品,同法制成阴性对照液,取防风对照药材1g,加甲醇10ml,回流30min,滤过,滤液蒸干,加水20ml使溶解,用乙酸乙酯萃取2次,每次15ml,合并乙酸乙酯层,水浴蒸干,残渣加甲醇1ml使溶解作为对照药材溶液。吸取上述溶液各5μl,分别点于同一硅胶G薄层板上,以氯仿-甲醇=4∶1为展开剂[5],展开,取出,晾干。置紫外光灯365nm下检视,供试品色谱中,在与对照药材相应的位置上,显相同颜色的斑点。阴性对照无干扰,Rf=0.758。
2.2.4 黄芩TLC 取制剂样品10ml,用乙酸乙酯萃取2次,合并乙酸乙酯层,水浴蒸干,加甲醇溶解,作为供试液。另取相同制备工艺制成的缺黄芩的阴性样品,同法制成阴性对照品溶液。另取黄芩苷对照品,加甲醇制成浓度为1mg/ml的溶液,作为对照品溶液。吸取上述溶液各5μl,分别点于硅胶G薄层板上,以乙酸乙酯-甲醇-甲酸-水=7∶2∶0.5∶0.5为展开剂[6],展开,取出,晾干。喷三氯化铁的乙醇溶液,晾干,供试品色谱中,在与对照品相应的位置上,显相同墨绿色的斑点,阴性对照无干扰,Rf=0.756。
2.3 HPLC含量测定
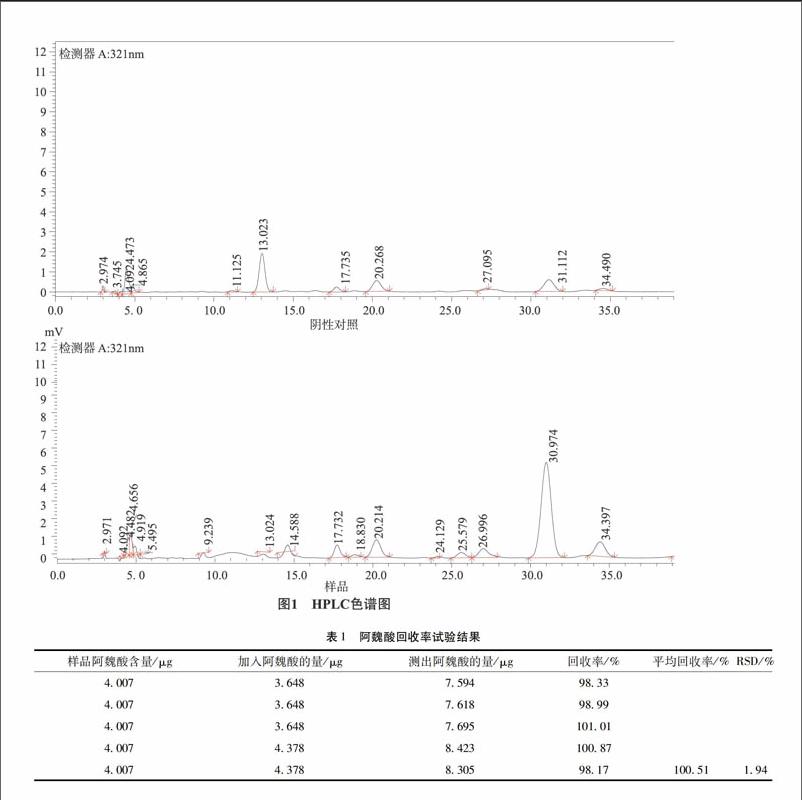
2.3.1 色谱条件 色谱柱:InertsilODS-3(250mm×4.6nm,5μm);流动相:甲醇-1%冰醋酸(30∶70);检测波长:321nm;柱温:25℃;流速:1ml/min;进样量:10μl。在上述色谱条件下,按阿魏酸峰计算,理论塔板数在4000以上[5];祛风安脑口服液中阿魏酸的色谱峰与其他成分的色谱峰分离良好,且阴性样品溶液无干扰。见图1。
2.3.2 对照品溶液的制备 精密称取阿魏酸4.56mg定容于25ml棕色容量瓶中,加甲醇配成182.40μg/ml对照品储备液,精密量取1ml对照品储备液,定容于10ml的棕色容量瓶中,制成含70%甲醇,浓度为18.24μg/ml的对照品溶液,用0.45μm微孔滤膜滤过,取续滤液,即得。
2.3.3 供试品溶液的制备 精密称取祛风安脑口服液10ml,用乙醚10ml萃取,萃取3次,挥干乙醚,用甲醇定容于100ml的容量瓶,制成供试品液,摇匀,用0.45μm微孔滤膜滤过,取续滤液,即得。
2.3.4 阴性对照品溶液的制备 按处方量制成缺当归及川芎的阴性样品,同供试品溶液的制备制成阴性对照液。
2.3.5 线性关系考察 分别精密吸取对照品溶液(18.24μg/ml)1、2、3、4、5、6ml置于10ml的容量瓶中,加甲醇至刻度,摇匀。按上述色谱条件,测定峰面积。以峰面积为纵坐标(Y),以进样量(μg)为横坐标(X),绘制标准曲线,计算得回归方程Y=58526X+11512,r=0.9998。结果表明:阿魏酸在1.824~10.940μg范围内呈良好的线性关系。
2.3.6 精密度试验 吸取对照品溶液10μl,在所选色谱条件下连续进样5次,测定阿魏酸峰面积值,RSD=1.11%。结果表明,仪器的精密度良好。
2.3.7 重复性试验 精密量取同一批样品5份,按供试品溶液制备方法项下方法操作,共配制5份供试液,各进样10μl,结果测定出的含量RSD为1.67%,表明实验重复性良好。
2.3.8 稳定性试验 取同一供试品溶液,分别于0、2、4、6、8、10h进样,测定阿魏酸色谱峰面积,比较10h内测得制剂含量RSD值。实验结果显示,RSD为2.00%,表明本供试品溶液在室温下放置10h内稳定。
2.3.9 加样回收率试验 采用加样回收法,取已知含量同一样品,分别加标0.8倍、1.0倍、1.2倍,每个水平重复3次。按上述的色谱条件进样,计算回收率,结果见表1。
2.3.10 样品测定 精密量取5批祛风安脑口服液,并按“2.3.3”项下制成供试品溶液,分别取10μl,注入高效液相色谱仪,在上述的色谱条件下记录峰面积,计算阿魏酸的含量。结果见表2。3 讨论
祛风安脑口服液为中药复方制剂,当归和川芎中的共有成分阿魏酸为有效成分之一,故实验选择阿魏酸的含量作为祛风安脑口服液质量控制的参考依据。
由于本品为中药复方制剂,成分复杂,故采用水提后,65%乙醇醇沉,除去水提液中的淀粉、树胶、多糖、粘液质色素等,而乙醇的上清液含有鞣质、生物碱、苷类等[7]。测定阿魏酸含量时,先用乙醚萃取3次,以减少其他成分干扰。报道阿魏酸对光和热不稳定[8],因此稀释后应置于棕色瓶中,于冰箱中保存。
实验结果表明,通过薄层色谱的定性鉴别,各检出成分不受处方中其他成分的干扰,方法简便、快速、专属性强、重复性好。通过阿魏酸的含量测定,可知祛风安脑口服液中阿魏酸在1.824~10.940g/ml范围内线性良好,方法的精密度实验、重复性试验均在合理的范围内,且本供试品溶液在10h内稳定,可见运用本方法测定祛风安脑口服液中阿魏酸的含量可行。
参考文献
[1] 顾民,张亮,张正行.HPLC测定逍遥散及当归中阿魏酸的含量[J].中成药,2000 ,22(5):32.
[2] 王卫锋,康阿龙,汤迎爽,等.HPLC测定妇月康胶囊中阿魏酸的含量[J].中成药,2004 ,26(6):8.
[3] 胡英,刘庆荣.感冒软胶囊中盐酸麻黄碱的薄层色谱鉴别方法探讨[J].中国药事,2006,20(9):573.
[4] 孙菲,丁莹,梁雪,等.川芎、当归的薄层鉴别[J].中国医药学报,2013,41(2):56-57.
[5] 国家药典委员会. 中华人民共和国药典(一部) [S]. 北京:中国医药科技出版社,2010.
[6] 陈菲菲.黄芩苷的提取及结构鉴定[J].天然药物化学实验开题报告,
[7] 王庆.浅谈中药的醇沉工艺及设备[J].中国制药装备,2009,11(11):38.
[8] 孙忠,彭康.HPLC法测定安阳还五汤中阿魏酸的含量研究[J].中医药学刊,2004,22(5) :833.
(收稿日期:2016.01.04)
