基于颜色主波长与补色波长的比色法定量检测
2016-04-13李海燕张校亮李晓春
李海燕,张校亮,李晓春*
(1.太原理工大学 新型传感器与智能控制教育部与山西省重点实验室,山西 太原 030024;2.太原理工大学 物理与光电工程学院,山西 太原 030024)
基于颜色主波长与补色波长的比色法定量检测
李海燕1,2,张校亮1,2,李晓春1,2*
(1.太原理工大学 新型传感器与智能控制教育部与山西省重点实验室,山西 太原 030024;2.太原理工大学 物理与光电工程学院,山西 太原 030024)
利用sRGB(Standard RGB)颜色空间与国际照明委员会(CIE)色度系统的转化关系以及CIE 1931色品图的性质,编写MATLAB程序实现了颜色的RGB信息到颜色主波长或补色波长的转化,并将此程序用于分析面光源下采集到的显色产物的图片。利用颜色的主波长实现了对pH值的定量检测,利用颜色的补色波长完成了对亚硝酸根离子的定量检测。当pH值分别在4.0~7.0和7.5~10.0范围内,pH值均与其显色产物颜色的主波长呈线性变化;亚硝酸根离子浓度在10~40 mg/L范围内与其显色产物颜色的补色波长有良好的线性关系,通过结合图片的G值分析,扩大了传统吸收光谱法的检测范围。
主波长;程序;pH值;亚硝酸盐;比色分析
比色法是以生成有色化合物的显色反应为基础,通过比较或测量有色物质溶液的颜色深度来确定待测组分含量的方法,广泛用于生物、医学、化学、环境等方面的检测。常用的比色法有目视比色法、光电比色法以及数字图片比色法。目视比色法的主要优点是设备简单和操作简便,但眼睛观察存在主观误差,准确度较低;而光电比色法如分光光度法消除了主观误差,提高了测量准确度。
近年来,在快速检测以及前期筛选的研究中,数字图片比色法的应用越来越广泛,其原理包括图像采集和图片处理两部分[1-3]。常用的图像采集工具有扫描仪、CCD 或CMOS成像仪、数码相机、智能手机等;而处理图片则根据显色产物的特点来选择不同的颜色模型,并由专业的图片处理软件或开发相关的手机APP来完成。对于显色色调单一的反应,通常采用图片处理软件Photoshop来分析颜色。 在检测中[4-5]先对样本进行成像,然后将图片从RGB模式转换为CMYK模式或灰度模式,建立Y值或灰度强度与待检测物浓度之间的关系。这类反应不需要进行模式转换,直接分析显色产物的RGB值即可完成定量检测。而对于色调明显变化的显色反应,此类方法不再适用。典型的如对pH值的检测,Shen等[6]建立了不同pH值与其显色产物的色品坐标之间的三维关系,但该方法相对比较复杂。Yetisen等[7]使用CIE 1931色品图,通过相关算法计算得到样品的pH值。Devadhasan等[8]发现不同pH值溶液各色品点的欧几里德距离与pH值之间呈一定的线性关系,但文中未直接给出欧几里德距离与pH值之间的拟合直线。除此之外,部分比色分析基于金纳米粒子,如Jing等[9]通过程序将单纳米粒子的RGB信息经CIE色度系统转化为颜色的波长,进而计算得到单个纳米金粒子的直径。但文献的程序中只提及绿色的金纳米粒子与其波长的转化,未说明程序的适用范围。Cheng等[10]通过改变成像光源,使得红移很小的金纳米粒子之间的色差信号放大,从而大大降低了三聚氰胺的检测限。
本文通过sRGB颜色空间与CIE色度系统的转换,以及CIE 1931色品图的性质,将图片的RGB颜色信息转化为颜色的主波长(或补色波长),并使用MATLAB软件编写程序实现了转化过程。同时,使用此程序处理LED面光源[11]下用智能手机采集到的显色产物的图片,从而利用颜色的主波长完成了pH 4.0~10.0范围的定量检测,利用颜色的G值和补色波长完成了浓度范围为0~40 mg/L的亚硝酸根离子的定量检测。
1 实验部分
1.1 试剂与仪器
亚硝酸钠(≥99.0%)、甲醇(≥99.5%)、无水乙醇(≥99.7%)、碳酸钠(≥99.8%l)、碳酸氢钠(≥99.5%)、溴百里香酚蓝(变色范围6.0~7.6),均为分析纯试剂,购于Kermel公司;磺胺(≥99%)、盐酸萘基乙二胺(98%),均为分析纯试剂,购于Aladdin公司;柠檬酸(≥99.5%,ACS,Sigma-Aldrich公司);无水磷酸氢二钠(≥99.5%,分子生物学级,Aladdin公司);甲基红(变色范围4.5~6.2)、百里酚蓝(变色范围1.2~2.8,8.0~9.6)、酚酞(变色范围8.0~10.0),购于Kermel公司;氢氧化钠(97%,ACS,Aladdin公司);喷墨打印机专用连供墨水(厦门亿色科技有限公司);实验用水为去离子水(电阻率18.2 MΩ·cm)。
UV-3100PC紫外-可见分光光度计(上海美普达仪器有限公司),pH计(奥豪斯STARTER 3100),LED 面光源(18 cm×18 cm,20 W,佛山飞力照明科技有限公司),智能手机(Coolpad Dazon F2),电子天平(奥豪斯先行者),Pipet-LiteXLS手动单道移液枪(美国梅特勒托利多公司),SK-1快速混匀器(金陵市科析仪器有限公司),10 mm×4 mm玻璃比色皿(山西誉兴盛实验设备有限公司),超纯水仪(美国赛默飞世尔科技公司)。
1.2 MATLAB程序的编写及验证
MATLAB程序主要包括:将采集到的图片RGB信息转化为D65照明体下CIE 1931色品图的色品坐标;通过色品坐标计算各种颜色的主波长(或补色波长)。
将青色、品红色和黄色3种墨水以不同比例两两混合,形成一系列有梯度的颜色,通过以下两种方法计算其主波长(或补色波长):①手机采集所有颜色的图片,并用MATLAB程序计算颜色的主波长(或补色波长);②使用紫外-可见分光光度计得到溶液的吸光谱或透射谱,并根据公式⑴~⑹计算颜色的主波长(或补色波长)。
1.3 溶液的配制
不同pH值溶液:0.1 mol/L柠檬酸溶液和0.2 mol/L磷酸氢二钠溶液以不同比例混合得到pH值4.0~8.5(pH值间隔0.5)的溶液,0.1 mol/L碳酸氢钠溶液和0.1 mol/L碳酸钠溶液以不同比例混合后分别得到pH值为9.0,9.5,10.0的溶液。所有溶液的pH值均由pH计测定。
pH显色剂:分别称取百里酚蓝0.01 g,甲基红0.32 g,溴百里香酚蓝1.20 g,酚酞1.20 g,混合并研匀后,用200 mL 浓度为95%的无水乙醇充分溶解,并加150 mL水稀释。用0.1 mol/L氢氧化钠溶液中和至刚好显绿色,并加水定容至400 mL。
亚硝酸钠溶液:称取0.025 g亚硝酸钠粉末,溶于25 mL水中,得到1 000 mg/L的亚硝酸钠溶液。以此为母液,分别配制浓度为0,1,2,5,10,12,15,20,25,30,40 mg/L的亚硝酸钠溶液。
显色剂:称取0.172 2 g磺胺、0.051 8 g盐酸萘乙二胺和0.317 g柠檬酸,溶于20 mL甲醇中,于低温下避光保存。
2 结果与讨论
2.1 MATLAB程序可行性的验证研究
输入设备(如扫描仪、数码相机)对颜色的响应为RGB数字控制值;显示设备(如显示器)在RGB数字值的控制下会显示一定的颜色,该颜色满足sRGB颜色空间。而当颜色信息从输入设备传递到显示设备时,先将满足输入设备特性的颜色值转化为表征人眼视觉的CIE色度值,再转化为满足显示设备特性的颜色值。因此,图片在显示器上显示时,图片的颜色信息既满足sRGB颜色空间,也满足sRGB颜色空间与CIE色度系统的转化关系。具体的转化关系如下所示[12-15]:
在8位编码的情况下,R,G,B取0~255整数,令:
(1)
当R′,G′,B′≤0.040 45时:
(2)
而当R′,G′,B′>0.040 45时:
(3)
则r,g,b3个因子与对应形成的混合色光在D65照明体下的CIE XYZ色度值有如下关系:
(4)
且对应的色品坐标为:
(5)
主波长是指某一种光谱色的波长,用符号λd表示,通过色品坐标可以计算颜色的主波长(或补色波长)。如图1所示,对于颜色点S1的主波长,可由白点O(如CIE标准光源D65)与S1连线的延长线与光谱轨迹的交点L代表的光谱色波长所决定。但并不是所有颜色都有主波长,色品图中连接白点与光谱轨迹两端点所形成的三角形区域内,各色品均无主波长,这是因为连接光谱轨迹两端点直线上所有的色光色,均由400 nm的蓝光和700 nm的红光混合而成。对于这部分颜色的波长可由其补色波长表示,用符号-λd或λc表示。 例如,对于三角形区域内的颜色点S2,其补色波长由点O与点S2连线的反向延长线与光谱轨迹的交点Q点代表的光谱色波长来决定。综上所述,具有相同波长的两个颜色点(如S1和L)或两个互补颜色点(如S2和Q),连接白点与这两个颜色点直线的斜率相同。对于色品图内所有的样品颜色点,可通过公式(6)[16]计算斜率,而光谱轨迹上所有光谱色的波长与斜率一一对应并且已知,因此计算出样品点的斜率,再通过查表方可求得该样品点的波长。
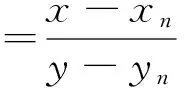
(6)
公式(6)中,x,y为样品点(如S1和S2)的色品坐标,xn,yn为白点O(如D65照明体)的色品坐标。
基于以上,编写了MATLAB程序,实现了颜色RGB信息到颜色主波长(或补色波长)的转化。为验证程序计算颜色主波长的准确性,与公式法计算颜色主波长(或补色波长)的结果进行了对比。由于程序以D65照明体为标准光源(即白点),而紫外-可见分光光度计内部使用的可见光源是卤钨灯,属于A类照明体。不同的光源会影响样本的色品,所以,需通过紫外-可见分光光度计结合公式(7)计算出D65照明体下的三刺激值,进而计算色品坐标与颜色主波长(或补色波长)。
当被测物体是非自发光物体时,透明体在D65照明体下的三刺激值计算公式如下[16]:
(7)

因此,通过一组不同颜色的样本溶液(图2A),将MATLAB程序计算的颜色主波长(或补色波长)与公式法计算的结果进行对比,如图2所示。图2B为样本溶液(除第7个样本外)颜色主波长的对比结果,图2C为样本溶液(除第4个样本外)补色波长的对比结果。由于第7个样本溶液的颜色色品位于图1中红色三角形区域内,因此它没有主波长,只能计算其补色波长。而第4个样本溶液的补色色品位于图1中红色三角形区域内,因此它只有主波长,没有补色波长。从图2B和图2C可以看出,不管是样本溶液颜色的主波长还是补色波长,通过两种方法计算的波长结果基本吻合。因此,本研究证实了程序计算颜色主波长(或补色波长)的准确性,以及程序用于提取图片波长信息的可行性。
2.2pH值的检测
在数字图片分析中,最直接简便的是分析图片颜色的RGB值,而对于色调发生明显变化的显色反应,分析颜色的RGB值与被测量参数之间并无明显的对应关系。如pH值的检测,图3A为采集到的不同pH值(4.0~10.0)溶液中加入显色剂后显色产物的颜色照片。图3B为pH值分别与其显色产物颜色的R,G,B值之间的关系,可以看出,R,G或B值与pH值之间无明显关系,因此,直接分析RGB值的方法对于这一类显色反应不适用。
将采集到的图片利用程序计算其主波长,主波长值与pH值关系如图4所示。图4A显示,在pH 4.0~7.0和7.5~10.0的范围内,pH值与其显色产物颜色的主波长均呈线性变化关系。但当pH值从7.0变化到7.5时,显色产物的颜色主波长从560 nm左右下降到510 nm左右。主波长骤降的原因可以用色品图解释。如图4B所示,图中红点代表不同pH值溶液显色后颜色的色品在CIE 1931色品图上的位置,两个箭头所指的方向代表pH 7.0和pH 7.5时显色产物的颜色对应的主波长。由于在色品图上颜色分布的不均匀性,尤其绿色的颜色范围较大,所以在此范围内,颜色变化很小时,波长会有很大的变化。因此,pH值从7.0变化到7.5时显色产物的颜色主波长变化较大。
2.3 亚硝酸根离子浓度的检测
亚硝酸根离子的比色分析是基于格里斯重氮化反应,最后的显色产物呈品红色,且随着亚硝酸根离子浓度的增加,显色产物的颜色逐渐加深。因此,可使用RGB颜色模型或CMYK颜色模型来直接分析显色产物。首先用稀释不同倍数的品红色墨水溶液模拟反应。采集稀释不同倍数的品红色溶液的图片,通过分析这些图片的RGB值,可以得出品红色墨水的稀释比例分别与其颜色的R,G,B值之间的关系。结果显示,随着品红色墨水溶液颜色的变化,G值的变化最大,且与品红色墨水溶液的比例呈很好的线性关系。
因此,将此方法用于亚硝酸根离子浓度的检测。检测了不同浓度亚硝酸根溶液在显色剂作用下显色产物的图片,分析了这些图片颜色的G值,结果如图5A所示,从插图中可以看出亚硝酸根离子浓度在0~10 mg/L范围内与G值存在较好的线性关系,相关系数为0.977 0,但当浓度超过10 mg/L后,G值达到饱和。由于显色产物为品红色,该颜色位于图1色品图中红色三角形区域内,因此使用程序计算这些颜色的补色波长,并分析其与亚硝酸根离子浓度的关系。结果显示,亚硝酸根离子浓度在10~40 mg/L范围内,显色产物的波长随浓度增大而减小,并呈良好的线性关系,相关系数为0.989 6。在亚硝酸根离子浓度较小的范围内,显色产物的补色波长与亚硝酸根离子浓度间并无明显关系,这也可以通过CIE 1931色品图来解释。如图5B所示,品红色的点代表不同浓度的亚硝酸盐溶液显色后颜色的色品在CIE 1931色品图上的位置。随着箭头的方向,亚硝酸根离子的浓度依次增大。由计算颜色波长的方法可知,在亚硝酸根离子浓度较小时,这些色品点与D65白点的连线几乎在一条直线上,即波长变化不明显;而在浓度较大的范围内,色品点与白点连线的斜率开始有明显变化,因此波长也有明显的区别。所以,在浓度较小的范围内,可使用G值分析亚硝酸盐溶液的显色产物,在浓度较大的范围内,使用波长进行分析。
与传统的分光光度法对比的结果显示,分光光度法在亚硝盐浓度为0~15 mg/L范围内有较好的线性关系,而浓度大于15 mg/L时,吸光度值已趋于饱和。因此,本实验结合分析亚硝酸盐显色产物的G值与其颜色的补色波长,增大了亚硝酸根离子的检测范围。
3 结 论
本文提出了基于颜色主波长或补色波长的比色分析方法。利用sRGB颜色空间与CIE色度系统的转化关系以及CIE 1931色品图的性质,编写MATLAB程序,实现了利用颜色的主波长或补色波长进行基于显色反应的物质的定量检测。通过分析显色反应的颜色主波长和补色波长信息,实现对不同色调的显色反应进行线性的拟合,并利用该方法提高了同一色调显色反应的检测范围。以pH值和亚硝酸根检测为例,验证了该方法的可行性与准确性。
[1] Sumriddetchkajorn S,Chaitavon K,Intaravanne Y.Sens.ActuatorsB,2013,182:592-597.
[2] Lopez-Ruiz N,Curto V F,Erenas M M,Benito-Lopez F,Diomand D,Palma A J,Capitan-Vallvey L F.Anal.Chem.,2014,86(19):9554-9562.
[3] Hong J I,Chang B Y.LabChip,2014,14(10):1725-1732.
[4] Meng X J,Schultz C W,Cui C E,Li X C,Yu H Z.Sens.ActuatorsB,2015,215:577-583.
[5] Li X,Tian J F,Shen W.Anal.Bioanal.Chem.,2010,396(1):495-501.
[6] Shen L,Hagen J A,Papautsky I.LabChip,2012,12(21):4240-4243.
[7] Yetisen A K,Martinez-Hurtado J L,Garcia-Melendrez A,Vasconcellos F D,Lowe C R.Sens.ActuatorsB,2014,196:156-160.
[8] Devadhasan J P,Kim S.Anal.Chim.Acta,2015,858:55-59.
[9] Jing C,Gu Z,Ying Y L,Li D W,Zhang L,Long Y T.Anal.Chem.,2012,84(10):4284-4291.
[10] Cheng X D,Dai D G,Yuan Z Q,Peng L,He Y,Yeung E S.Anal.Chem.,2014,86(15):7584-7592.
[11] Yang D D,Zhang X L,Cui C E,Tan K,Li X C.J.Instrum.Anal.(杨冬冬,张校亮,崔彩娥,谭慷,李晓春.分析测试学报),2015,34(10):1179-1184.
[12] Katoh N,Deguchi T,Berns R S.Opt.Rev.,2001,8(5):305-314.
[13] Katoh N,Deguchi T,Berns R S.Opt.Rev.,2001,8(5):397-408.
[14] Xu Y F,Huang M,Jin Y.Chin.J.Liq.Cryst.Disp.(徐艳芳,黄敏,金杨.液晶与显示),2008,23(6):771-777.[15] Xu Y F.ColorManagementPrinciplesandApplications.Beijing:Printing Industry Press(徐艳芳.色彩管理原理与应用.北京:印刷工业出版社),2011:1-91.
[16] Hu W J,Tang S Q,Zhu Z F.ModernColorScienceandApplication.Beijing:Beijing Institute of Technology Press(胡威捷,汤顺青,朱正芳.现代颜色技术原理及应用.北京:北京理工大学出版社),2007:31-97.
Colorimetric Analysis for Quantitative Detection Based on the Dominant Wavelength and the Complementary Wavelength of Colors
LI Hai-yan1,2,ZHANG Xiao-liang1,2,LI Xiao-chun1,2*
(1.Key Laboratory of Advanced Transducers and Intelligent Control System Ministry of Education and Shanxi Province,Taiyuan University of Technology,Shanxi Province,Taiyuan 030024;2.College of Physics and Optoelectronics,Taiyuan University of Technology,Shanxi Province,Taiyuan 030024,China)
According to the conversion of sRGB(Standard RGB) color space and CIE(Commission Internationale de L′Eclairage) colorimetric system and the character of the CIE 1931 chromaticity diagram,the MATLAB program was composed to achieve the conversion from the RGB information to the dominant wavelength or the complementary wavelength of one color,and then was utilized to analyze the images of the chromogenic products under the area light source.The quantitative detection of the pH value was realized with the color's dominant wavelength and the detection of the nitrite with the color's complementary wavelength.There are linear relationships between pH value and the color's dominant wavelength of its chromogenic products in the pH value ranges of 4.0-7.0 and 7.5-10.0,respectively.And there is a favorable linear relationship between concentration(10-40 mg/L) of nitrite and color's complementary wavelength of its chromogenic products.Combined with the Green value of the color,the range of detection by the traditional absorption spectrometry was enlarged.
dominant wavelength;program;pH value;nitrite;colorimetric analysis
2016-04-17;
2016-05-22
国家自然科学基金(21575098,21505098);山西省国际合作项目(2015081019);山西省回国留学人员科研资助项目(2013-038);山西省高等学校科技创新项目(2015123)
10.3969/j.issn.1004-4957.2016.11.006
O657.3;O433.4
A
1004-4957(2016)11-1403-06
*通讯作者:李晓春,博士,教授,研究方向:光电生物分子检测,Tel:0351-3176638,E-mail:lixiaochun@tyut.edu.cn
