二氟氨基类物质的合成应用现状及发展趋势
2016-04-09秦叶军郑文芳潘仁明王万军
梅 莹,李 欢,秦叶军,郑文芳,潘仁明,王万军,
(1.南京理工大学 化工学院,江苏 南京 210094;2.中国科学院 上海有机化学研究所,上海 200032)
二氟氨基类物质的合成应用现状及发展趋势
梅莹1,李欢1,秦叶军2,郑文芳1,潘仁明1,王万军1,2
(1.南京理工大学 化工学院,江苏 南京 210094;2.中国科学院 上海有机化学研究所,上海 200032)
摘要:二氟氨基由于含有较高的能量,是提高化合物能量密度最为理想的基团之一。其在推进剂和火炸药中具有广泛的应用前景,受到了普遍的关注,因此,对二氟氨基类物质进行详细的研究是很有必要的。根据所含官能团的不同,对二氟氨基类物质进行了分类,并综述了二氟氨基类物质的合成应用现状及发展趋势。
关键词:二氟氨基;合成;氧化剂;增塑剂;粘结剂
含二氟氨基的化合物和其他的含氟氮基团的化合物(如,氟亚氨基、二氟氨基和N-氟氧化偶氮基等)代表了一类具有高电负性的化合物,它们的氧化性均较强。19世纪60年代中期,二氟氨基类化合物得到了详细的研究。其中的一些化合物很快就被申请专利,用作药物、杀菌剂、合成中间体以及杀虫剂等,如,二氟氨基金刚烷已被申请专利用作抗病毒制剂[1-2]。
将二氟氨基引入含能材料中,能够提高材料的能量密度。本文根据二氟氨基类化合物结构中其他主要官能团的不同,将其分为二氟氨基烷烃类、醇类、醚类、腈类、酯类和硝铵类等。
1二氟氨基烷烃类
首例公开报道的二氟氨基化合物是二氟氨基三氟甲烷[3]。此后,科学家们对二氟氨基三氟甲烷的合成又进行了一系列的探索。C. J. Schack[4]报道了一种全新的制备二氟氨基三氟甲烷的方法,在70~80 ℃条件下通过叠氮三氟甲烷的直接氟化制得,同时指出用氟化钾作催化剂可以加快反应速率,并可提高产率(高达90%~95%)。其合成路线为:
(1)
R. D. Chapman等[5]通过相应的偕二乙酰氨基的直接氟化,成功制备了环状和链状偕二氟氨基烷烃。式2和式3分别以1,1-偕二乙酰氨基丙烷和1,1-偕二乙酰氨基环己烷为原料,制得了相应的二氟氨基烷烃。以这种方法合成偕二氟氨基环己烷及1,1-偕二氟氨基丙烷的收率分别为10%和40%,虽然较传统工艺收率的提高不明显,但合成过程使用F2而规避了易爆的N2F4和HNF2,合成过程更为安全绿色,利于工艺放大及应用。

(2)

(3)
式2和式3中对应的试剂与反应条件为:i. 5%~10%F2/N2,CH3CN,-40 ℃,25%;ii. 5%~10%F2/N2,CH3CN,-40 ℃,31%;iii. 5%~10%F2/N2,CH3CN,-40 ℃;iv. 5%~10%F2/N2,CH3CN,-40 ℃,40%。
2二氟氨基醇类
C. L. Coon等[6]设计并合成了一种同时含有二氟氨基和硝基的醇类化合物——2,2-双(二氟氨基)-5-氟-5,5-二硝基-1-戊醇,合成路线见式4。其以2-丁炔-1,4-二醇为原料,经过氧化、硝化、磺酰化和酯化等4步反应得到化合物4。化合物4在双基推进剂中可作为增塑剂来使用,化合物结构中羟基的存在提高了其增塑性能,同时,其含能特性能进一步增大双基推进剂的比冲和燃速。

(4)
式4中对应的试剂与反应条件为:i. HgSO4/H2SO4,FC(NO2)2H,24 h,50%;ii. CH2Cl2,Na2CO3,(CF3CO)2O,3 h,0~5 ℃,82%;iii. F2NSO3H,CH2Cl2,0~5 ℃,3 h,61%;iv. CH3OH,1 h,81%。
二氟氨基醇类不仅可以通过酯的水解而制得,还可以由酮的二氟氨基化制得。A. V. Fokin等[7]总结了一些典型的二氟氨基化反应,其中,通过二氟甲胺与脂肪族或脂环族的醛或酮进行反应,可以制得α-二氟氨基醇,当二氟甲胺过量时,可进一步得到偕二氟氨基烷烃。反应式如下:

(5)
式中,R是H、烷基和亚烷基等。
3二氟氨基腈类
合成二氟氨基腈类化合物最简单的反应即是3-丁炔腈与四氟肼的反应,生成3,4-双(二氟氨基)丁烯腈(7),反应式如下:

(6)
由于二氟氨基腈类化合物具有较高的能量,不会降低硝化棉的爆炸威力,具备用作硝化棉增塑剂的可能。R. C. Petry[8]报道了一批含二氟氨基腈类增塑剂的合成方法及其用途。这些增塑剂可以提高以硝化棉为粘合剂体系的固体推进剂标准理论比冲,添加此类增塑剂后,固体推进剂的理论比冲均>250 s,其中,以1,2,3-三(二氟氨基)丙烯腈为增塑剂的推进剂的理论比冲高达271 s。
4二氟氨基硝基类
M. W. Lerom等[9]通过芳烃硝化衍生物的偶联反应得到三联苯,然后经胺化、氟化等过程,获得硝基二氟氨基三联苯(见式7)。该化合物具备较多的含能基团,能量较高,可用作炸药,尤其是桥式爆发器的雷管。式7中对应的试剂与反应条件为:i. KNO3,30%H2SO4,125 ℃,4 h,95%;ii. HNO3/H2SO4,CH3OH;iii. Cu,硝基苯,135 ℃,5 h 53%;iv. THF/甲醇,NH3·H2O,RT,1 h,60%;v. 10% F2,-35 ℃,5 h,2%。

(7)
5二氟氨基酯类
H. G. Adolph等[10]设计并合成了3,3-双(二氟氨基)-1,5-戊二硝酸酯(BFDNP,9),一种同时含有二氟氨基和硝酸酯基的含能增塑剂,该增塑剂可用于醋酸丁基纤维素和硝酸酯纤维素粘合剂体系。该增塑剂主要是通过酮的二氟氨基化以及醇的硝化来制备,反应式如下:

(8)
式8中对应的试剂与反应条件为:i. NaOCOCF3,75 ℃,64 h,68%;ii. HNF2,Oleum,0 ℃,3 h,62.6%;iii. CH3OH,65 ℃,48 h,50.6%;iv. 100%HNO3/H2SO4,0 ℃,2 h,90%.。
BFDNP在常温下呈液态,通过DSC扫描测试可知,BFDNP的玻璃化转变温度为-87 ℃,分解温度为186 ℃,在196 ℃时达到峰值。密度为1.56 g/cm3,NF含量高达26%。大多数含有α-H的二氟氨基化合物热力学上不稳定,易分解,但是,BFDNP中-NF2与叔碳原子相连,空间位阻很大,且不含α-H,所以分子较稳定。经计算可知,其生成焓为-76 kcal/mol。基于这些数据,通过Kamlet Short Method方法,计算得出含BFDNP的推进剂比冲为278.9 s,与BTTN、SYFO和SYEP相比,BFDNP具有更优秀的性能。
T. G. Archibald等[11-12]发现,当二氟氨基基团直接联结在新戊基碳,即(CH3)2CCH2—上时,由于新戊基的空间位阻很大,能够稳定二氟氨基,阻止HF气体的放出。同时,直接氟化带保护基团的新戊基胺很容易获得新戊基二氟氨基类化合物。在此基础上, 他们通过3,3-不对称氨基取代甲基环氧丁烷与氯代甲酸乙酯反应,得到相应的氨基甲酸酯中间体,然后进一步在惰性溶剂中用经过氮气稀释的氟气对其进行氟化[13],率先合成了3-二氟氨基甲基-3-甲基氧杂环丁烷(DFAMO)和3,3-偕(二氟氨基甲基)氧杂环丁烷(BDFAO)。
在此基础上,以二氯甲烷为溶剂,将DFAMO和BDFAO分别与100%的硝酸反应,得到相应的硝酸酯,可用作增塑剂。其合成过程如下:

(9)

(10)
式9和式10中对应的试剂与反应条件为:i. 98%HNO3,CH2Cl2,RT,71%;ii. 98%HNO3,CH2Cl2,RT,54%。
部分新戊基二氟氨基硝酸酯的性能见表1。由表1可知,随着分子中-NF2逐个取代-ONO2,化合物的热焓逐渐增大,推进剂体系的比冲也逐渐增大。
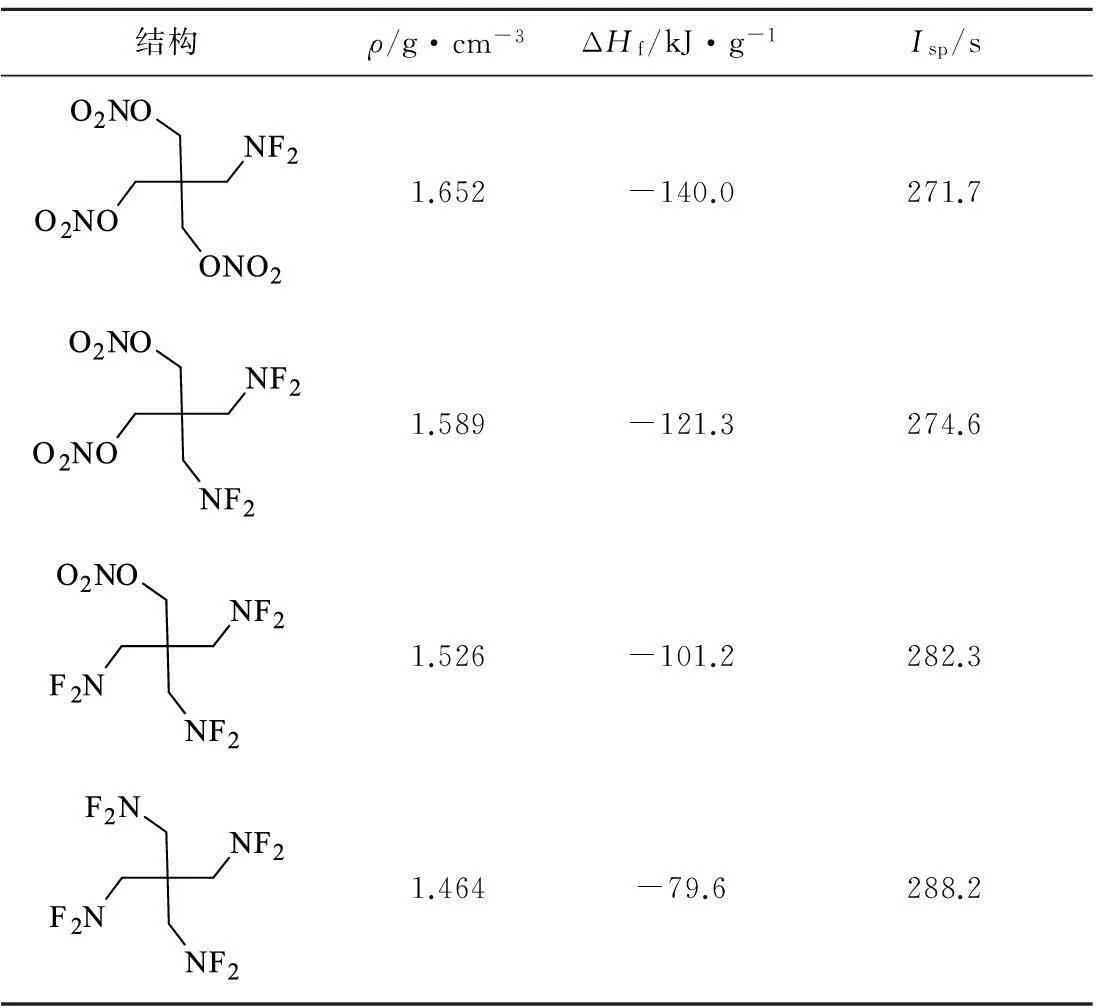
表1 新戊基二氟氨基硝酸酯预估性能
注:比冲为计算值,密度为实测值。
另外,二氟氨基酯类除了二氟氨基硝酸酯,还有二氟氨基碳酸酯、丙烯酸酯和聚氨酯等。如A. L. Rocklin[14]报道了一种二氟氨基碳酸酯,可作为增塑剂使用,C. T. Camilli等[15]报道了一种二氟氨基丙烯酸酯,可用作粘结剂,A. H. Muenker等[16]合成了一种二氟氨基聚氨酯,可用作固体火箭推进剂的粘结剂。
6二氟氨基硝铵类
尽管早在1963年二氟氨基取代的硝铵化合物就被合成出来[17-18],但这些化合物都是双二氟氨基取代的初级硝铵和N-烷基-N-二氟氨基甲基硝铵,由于其结构稳定性差,无法用于推进剂配方中。随后,偕-双(二氟氨基)取代的环状硝胺被设计出来,其结构稳定,且具备较高的密度。然而,传统方法合成偕-双二氟氨基烷烃需要强酸体系(如无水硫酸、发烟硫酸和氟磺酸等),而在此条件下大部分硝铵类以及氮杂环类化合物是极不稳定的,因此,需要寻求此类二氟氨基化合物的稳定合成工艺。
6.1HNFX
R. S. Miller和R. D. Chapman等[19-20]成功合成了3,3,7,7-四(二氟氨基)八氢化-1,5-二硝基-1,5-二氮芳辛(HNFX,12)。最初的合成方法中,通过典型的二氟氨基化反应(二氟甲胺-氟磺酸-硫酸)就可制得HNFX,其合成过程如下:

(11)
试剂与反应条件:1)HNF2, H2SO4, 53%;2)a. HNO3-(CF3CO)2O,CH2Cl2, -27℃,b. NO2消除, 50%;3)F2NSO3H-H2SO4, -23 ℃, 约1%。
不过上述反应最后一步产率极低,仅约为1%,因此,该合成方法仅具有理论研究价值[21]。R. D. Chapman等[22]通过将保护基团换为对硝基苯磺酰基(Ns),以及将氮上的磺酰基在强酸的作用下脱去,成为双氢取代的季铵正离子,再通过硝化作用合成HNFX,最终将总收率提高到75%。反应式如下:

(12)
式12中对应的试剂与反应条件为:i. HNF2,H2SO4(53%),F2NSO3H,CFCl3,-15 ℃;ii. F2NSO3H,H2SO4,CF3SO3H;iii. HNO3,H2SO4,CF3SO3H。
6.2RNFX
R. D. Chapman等[23]制备了RNFX,即5,5-双(二氟氨基)八氢化-1,3-二硝基嘧啶(14)。合成RNFX的一个关键步骤与合成HNFX的过程很相似:都使用四氢化-1,3-双(4-硝基-苯磺酰基)嘧啶-5(4H)-基团作为二氟氨基化中N的保护基团。然而,杂环硝铵上取代基的转化过程却与HNFX的合成过程差别很大,八氢化嘧啶中间体是在硝酰阳离子或者超强酸的作用下开环,而四氢化嘧啶是在溶剂二氯甲烷中用98%的硝酸进行硝化开环。简单来说,RNFX的合成方法主要包括二氟氨基化、硝化开环及其去质子化保护关环等,详细的合成过程反应式如下:

(13)
除了合成方法的明确说明,RNFX的性能暂时还没有得到实验性的总结。
6.3TNFX
早期的一种比较有潜力的二氟氨基硝铵类化合物是TNFX(15),它是HMX上2个硝铵基团被偕二氟氨基和偕二硝基取代,氧平衡值比HNFX高,同时还含有二氟氨基基团。T. Axenrod等[24]成功合成了这种二氟氨基硝铵类化合物,其合成过程反应式如下:

(14)
式14中对应的试剂与反应条件为:i. 邻、对硝基苯磺酰氯, THF-H2O, K2CO3, RT; ii. CrO3,H2SO4,丙酮,RT;iii. 聚乙烯,对甲苯磺酰氯,甲苯;iv CH2=C(CH2Br)2,K2CO3,丙酮,回流;v(i) O3,CH2Cl2,-78 ℃;v(ii) Me2S;vi. NH2OH·HCl,NaOAc,EtOH,回流;vii. HNO3,NH4NO3;viii. H2SO4,RT;ix. HNF2-F2NSO3H-H2SO4-CFCl3,-15 ℃;x. HNO3-CF3SO3H-SbF5。
TNFX的结构被证明存在2种结晶:1)低密度的三方晶系结构,ρ=1.712 g·cm-3;2)高密度的斜方晶系结构,ρ=1.904 g·cm-3。与HNFX的低密度(ρ=1.807 g·cm-3)三方晶系结构相比,偕二硝基取代偕二氟氨基后,密度稍有降低。
7结语
二氟氨基类物质的合成主要集中在二氟氨基化试剂的选择以及工艺优化上,二氟氨基类物质的用途非常广泛,可用作增塑剂、粘结剂或氧化剂,加入到高能推进剂中,以提高推进剂的能量特性及其他物理化学性能。同时,由于氟的存在,在医学或药学方面的研究与应用也将是一个新的发展方向。
参考文献
[1] Barton D H R, Hesse R H. Preparation of N,N-difluoroamines: US, 4234515[P].1980-11-18.
[2] Barton D H R, Hesse R H. Process for the preparation of N-monofluoro-acid amides, N-monofluoro and N,N-difluoro-tertiary amines: US, 3917688 [P].1975-11-04.
[3] Ruff O, Giese M. Die fluorierung des silbercyanids [J]. Ber. Dtsch. Chem. Ges. B, 1936, 69(3):598-603.
[4] Schack C J. Novel method for the preparation of CF3NF2: US, 4430514 [P].1984-02-07.
[5] Chapman R D, Davis M C, Gilardi R. A new preparation of gem-bis(difluoroamino)-alkanes via direct fluorination of germinal bisacetanides[J]. Synth. Commun., 2003, 33(23):4173-4184.
[6] Coon C L, Hill M E, Ross D L. 2,2-bis(difluoroamino)-5-fluoro-5,5-dinitro-1-pentanol: US, 3759998 [P].1973-09-18.
[7] Fokin A V, Kosyrev Y M, Shevchenko V I. Certain examples of difluoroamine alkylation reactions [J]. Bull. Acad. Sci. USSR, Div. Chem. Sci., 1982, 31(8):1626-1632.
[8] Petry R C. Nitrogen-and fluorine-containing compounds: US, 4001059[P].1977-01-04.
[9] Lerom M W, Peters H M. Nitrodifluoroaminoterphenyl compounds and processes: US, 3894086[P].1975-07-08.
[10] Adolph H G, Trivedi N J. Energetic plasticizers containing 3,3-bis(difluoroamino)-1,5-dinitratopentane and method of preparation: US, 6325876 [P].2001-12-04.
[11] Archibald T G, Manser G E, Immoos J E. Difluoroamino oxetanes and polymers formed therefrom for use in energetic formulations: US, 5272249 [P].1993-12-21.
[12] Archibald T G, Manser G E. Neopentyl difluoroamino compounds for use in energetic formulations: US, 5789617[P].1998-08-04.
[13] 冯增国. 重新唤起人们兴趣的二氟氨基及其化合物[J]. 化学进展, 2000, 12(2): 171-178.
[14] Rocklin A L. Fluorine-containing organic carbonate: US, 3856589[P].1974-12-24.
[15] Camilli C T, Engel L J. Propellant binder and synthesis: US, 3708358[P].1973-1-2.
[16] Muenker A H, Beach L K, Engel L J. Highly plasticized binder for solid propellants: US, 3745075[P].1973-07-10.
[17] Sayles D C. Method of preparing bis-difluoroamino-bis-nitroamino-alkanes: US, 3636154 [P].1972-01-18.
[18] Tyler W E, Lovett J R. Certain difluoramino compounds: US, 3687954 [P].1972-08-29.
[19] Miller R S. Research on new energetic materials[C]//MRS Proceeding. London: Cambridge University Press,1995.
[20] Chapman R D, Welker M F, Kreutzberger C B. Difluoramination of heterocyclic ketones: control of microbasicity[J]. J. Org. Chem., 1998, 63(5):1566-1570.
[21] 李欢, 秦叶军, 李金华, 等. 二氟氨基化合物的合成研究进展[J]. 化学通报, 2013, 75(12): 1076-1080.
[22] Chapman R D, Groshens T J. Method for making 3,3,7,7-tetrakis(difluoramino) octahydro-1,5-dinitro-1,5-diazocine(HNFX): US, 7632943[P].2009-12-15.
[23] Chapman R D, Nguyen B V. 5,5-bis(difluoramino)hexahydro-1,3-dinitropyrimidine(RNFX) and certain electronegatively substituted pyrimidines: US, 6310204[P]. 2001-10-30.
[24] Axenrod T, Guan X P, Chapman R D, et al. Synthesis of 3,3-bis(difluoramino)octahydro-1,5,7,7-tetro-1,5-diazocine(TNFX),a diversified energetic heterocycle[J]. Tetrahedron Lett, 2001, 42(14):2621-2623.
责任编辑郑练

Synthetic Application Status and Development of Difluoroamino Materials
MEI Ying1, LI Huan1, QIN Yejun2, ZHENG Wenfang1, PAN Renming1, WANG Wanjun1,2
(1.School of Chemical and Engineering, Nanjing University of Science and Technology, Nanjing, 210094, China;2.Shanghai Institute of Organic Chemistry, Chinese Academy of Sciences, Shanghai 200032, China)
Abstract:Due to the high energy property, difluoramino group becomes one of the most ideal groups to improve the energy density of compounds. Since difluoramino materials has wide application prospect in propellant and explosives, it has received widespread attention. So it is very necessary for the detailed study of difluoramino materials. Difluoramino materials are classified according to the content of different functional groups,and the synthetic application status and development trend of difluoramino materials are reviewed.
Key words:difluoroamino, synthesis, oxidizer, plasticizer, binder
收稿日期:2015-08-31
作者简介:梅莹(1990-),女,硕士研究生,主要从事含能增塑剂的合成及应用等方面的研究。
中图分类号:O 622.2
文献标志码:A
