维药制剂药渣中蛋白质及游离氨基酸的含量测定
2016-04-06张凤雪文娥李柯翱季志红田树革
张凤雪文 娥李柯翱季志红田树革
(1新疆医科大学中医学院,乌鲁木齐,830054;2新疆奇康哈博维药股份有限公司,乌鲁木齐,830026;3新疆医科大学中心实验室,乌鲁木齐,830054)
维药制剂药渣中蛋白质及游离氨基酸的含量测定
张凤雪1文 娥1李柯翱2季志红2田树革3
(1新疆医科大学中医学院,乌鲁木齐,830054;2新疆奇康哈博维药股份有限公司,乌鲁木齐,830026;3新疆医科大学中心实验室,乌鲁木齐,830054)
摘要目的:测定药渣中蛋白质及氨基酸的含量。方法:用考马斯亮蓝G-250、茚三酮显色,分光光度法测定蛋白质及氨基酸的含量。结果:CBB G-250显色测定蛋白质线性范围0. 081~0. 202 mg,加样回收率102. 06%、RSD为0. 99%;茚三酮显色测定氨基酸的线性范围0. 016~0. 029 mg/mL,加样回收率99. 83%、RSD为1. 82%。结论:CBB G-250和茚三酮显色,均具有简便、快速、灵敏度高、成本低、重现性好等特点。
关键词药渣;蛋白质;氨基酸;茚三酮;考马斯亮蓝;分光光度法;含量测定
Determlnatlon of Proteln and Free Amlno Acld wlthln the Resldues of Uygur Medlclne
Zhang Fengxue1,Wen E1Li Ke'ao2,Ji Zhihong2,Tian Shuge3
(1 College of Traditional Chinese Medicine,Xinjiang Medical University,Urumqi 830054,China;2 Xinjiang Qikang Habo Uygur Medicine Limited Liability Company,Urumqi 830026,China;3 The Central Laboratory of Xinjiang Medical University,Urumqi 830054,China)
Abstract Objectlve:To determine the content of protein and free amino acid within the residues of the Uygur medicine. Methods:The protein and amino acid content were determined by spectrophotometry with colored by coomassie brilliant blue G-250 and inhydrin. Results:The linear range of protein determined by CBB G-250 chromogenic assay was 0. 081~0. 202mg,recovery was 102. 06%,RSD was 0. 99%;the linear range of free amino acid by Ninhydrin chromogenic assay was 0. 016-0. 029mg/mL,recovery was 99. 83%,RSD was 1. 82%. Concluslon:CBB G-250 and ninhydrin chromogenic assay is simple,rapid with high sensitivity,low cost,fine reproducible characteristics and so on.
Key Words Residues of medicine;Protein;Free amino acid;Ninhydrin;Coomassie brilliant blue;Spectrophotometry;Content determination
我国药渣根据原料来源,类型主要有中药渣、生物制药药渣、藏药渣、抗生素类药渣等,其中中药渣所占的比例最大。据统计,中药渣在我国的排放量逐渐增加,平均年排放量已达3千万吨[1]。药渣中含有丰富的粗蛋白、碳水化合物、粗纤维、无机物和粗脂肪等[2-5],这些药渣若被丢弃会对环境造成严重的污染,这些药渣的处理将是刻不容缓的问题。本实验测定蛋白质及氨基酸的含量,有效的解决药渣的处理难题,易污染等问题,并为后期如何利用药渣栽培食用菌[6-7]、制成有机肥[8-9]提供理论依据和数据。
1 仪器与试剂
1. 1 仪器 KQ-5200DE型数控超声波清洗器(昆山市超声仪器有限公司),AL04型万分之一电子天平(德国梅特勒-托利多仪器有限公司),752紫外可见分光光度计(上海菁华科技仪器有限公司),B-260型水浴锅(上海亚荣生化仪器厂),TDL-40B低速台式离心机(上海安亭科学仪器厂)。
1. 2 试剂 牛血清白蛋白(批号:0332-201304,上海励瑞科技有限公司),精氨基酸(批号:100080-200908,中国药品生物制品检定所),CBB G-250 (Fluka进口分装,中国医药集团上海化学试剂公司),茚三酮(批号:20140216,上海科丰实业有限公司),磷酸,乙醇等均为分析纯。
2 方法与结果
2. 1 游离氨基酸的含量测定
2. 1. 1 测定波长的选择 取样品溶液和对照品溶液适量,在紫外分光光度计中进行400~800 nm波长扫描,二者均在567 nm附近有最大吸收,因此选择567 nm为测定波长[10-11]。
2. 1. 2 标准溶液的配制 精密称取10 mg精氨酸对照品,加蒸馏水溶解于50 mL容量瓶中,摇匀,得精氨酸对照品溶液的浓度为0. 2 mg/mL的。
2. 1. 3 供试品溶液的制备 精密称取药渣粗粉1 g,加25 mL蒸馏水超声30 min,离心,过滤,滤液备用。
2. 1. 4 显色剂的配制 2%的茚三酮的配制:精密称取4 g茚三酮放入200 mL容量瓶中,用乙醇溶解并定容至刻度,备用。pH=6. 8的磷酸缓冲液的配制:精密称取磷酸二氢钾3. 4 g,氢氧化钠0. 472 5 g,加蒸馏水并稀释至500 mL,备用[11-12]。
2. 1. 5 标准曲线的绘制 精密吸取上述对照品溶液0. 0、0. 8、1. 0、1. 1、1. 3、1. 4 mL分别置于10 mL具塞试管中,各加入2%的茚三酮乙醇溶液2 mL,摇匀,再加pH=6. 8的磷酸缓冲液1 mL,摇匀,在沸水浴中加热15 min,取出,在冷水中迅速放凉,用蒸馏水补足至10 mL,摇匀,在567 nm处用分光光度计测量其吸光度值。横坐标为精氨酸对照品溶液的浓度(mg/mL)纵坐标为吸光度值A,绘制标准曲线图,得回归方程:A=42. 523C-0. 453 9(R2=0. 999 5),在所测量的游离氨基酸浓度范围内浓度与吸光度呈良好的线性关系。
2. 1. 6 方法学考察
2. 1. 6. 1 精密度 分别精密吸取6份精氨酸对照品溶液各1. 1 mL于10 mL具塞试管中,按照“2. 1. 5”项下实验方法操作,测定其在567 nm处吸光度值,RSD为1. 02%(n=6)。
2. 1. 6. 2 重复性 取3号样品1 g,按“2. 1. 3”项下实验方法操作,得滤液,精密吸取提取液0. 8 mL,按照“2. 1. 5”项下实验方法操作,测定样品中氨基酸吸光度值,并计算,RSD为0. 92%(n=6)。
2. 1. 6. 3 稳定性试验 分别精密量取精氨酸对照品溶液1. 1 mL,按照“2. 1. 5”项下实验方法操作,每隔2 h测定吸光度值,RSD为2. 27%(n=6)。试验表明在10 h内测定稳定。
2. 1. 6. 4 加样回收率试验 利用加标回收法,分别吸取已知氨基酸含量已知的药渣提取液0. 3 mL,共6份,各加入对照品溶液0. 6 mL,按照“2. 1. 5”项下实验方法操作,测定吸光度值,并计算其回收率,结果见表1。
2. 1. 6. 5 样品含量测定 取样品1 g,按“2. 1. 3”项下实验方法方法操作,得滤液,精密吸取一定量的提取液,按照“2. 1. 5”项下实验方法操作,测定吸光度值,并计算样品中游离氨基酸的含量,结果见表3。
2. 2 蛋白质的含量测定
2. 2. 1 测定波长的选择 取样品溶液和对照品溶液适量,在紫外分光光度计中进行400~800 nm波长扫描,二者均在595 nm附近有最大吸收,因此选择595 nm为测定波长[13-14]。
2. 2. 2 标准溶液的配制 精密称取牛血清白蛋白(BSA)对照品10 mg置于100 mL容量瓶中,加蒸馏水溶解并稀释至刻度,摇匀,得浓度为0. 1 mg/mL的BSA对照品溶液。
2. 2. 3 供试品溶液的制备 精密称取药渣粗粉1 g,加25 mL蒸馏水超声30 min,离心,过滤,滤液备用。
2. 2. 4 显色剂的配制 CBB G-250染料试剂:称50 mg CBB G-250,溶于25 mL 95%的乙醇后,再加入50 mL 85%的磷酸,用水稀释至500 mL[15]。
2. 2. 5 标准曲线的绘制 精密吸取上述溶液0. 0、0. 8、1. 0、1. 2、1. 4、1. 6、1. 8、2 mL分别置于10 mL具塞试管中,各加入CBB G-250染料5 mL,用蒸馏水补足至10 mL,轻微振摇,混匀,在595 nm处用分光光度计测量其吸光度值。横坐标为BSA对照品溶液的含量(mg),纵坐标为吸光度值A,绘制标准曲线图,得回归方程:A=3. 410 1C+0. 097 5(R2=0. 999 5),在所测量的游离氨基酸浓度范围内浓度与吸光度呈良好的线性关系。
2. 2. 6 方法学考察
2. 2. 6. 1 精密度 精密量取BSA对照品溶液6份,各1. 2 mL于10 mL具塞试管中,按“2. 2. 5”项下方法操作,测定其在595 nm处吸光度值,RSD为0. 97%(n=6)。
2. 2. 6. 2 重复性 取3号样品1 g,按“2. 2. 3”项下实验方法操作,得滤液,精密量取0. 8 mL提取液,按照“2. 2. 5”项下方法操作,测定蛋白质在样品中吸光度值,并计算,1. 63%(n=6)。
2. 2. 6. 3 稳定性试验 分别精密量取BSA对照品溶液1. 4 mL,按照“2. 2. 5”项下实验方法操作,每隔5 min测定吸光度值,RSD为2. 02%(n=6)。试验表明在15 min内测定稳定。
2. 2. 6. 4 加样回收率试验 利用加标回收法,分别吸取已知蛋白质含量的药渣提取液0. 3 mL,共6份,各加入对照品溶液0. 8 mL,按照“2. 2. 5”项下实验方法操作,测定吸光度值,并计算其回收率,结果见表2。
2. 2. 6. 5 样品含量测定 取样品1 g,按“2. 2. 3”项下实验方法方法操作,得滤液,精密吸取一定量的提取液,按照“2. 2. 5”项下实验方法操作,测定吸光度值,并计算样品中总蛋白质的含量,结果见表3。

表1 药渣中总游离氨基酸回收率试验结果(n=6)

表2 药渣中总蛋白质回收率试验结果(n=6)
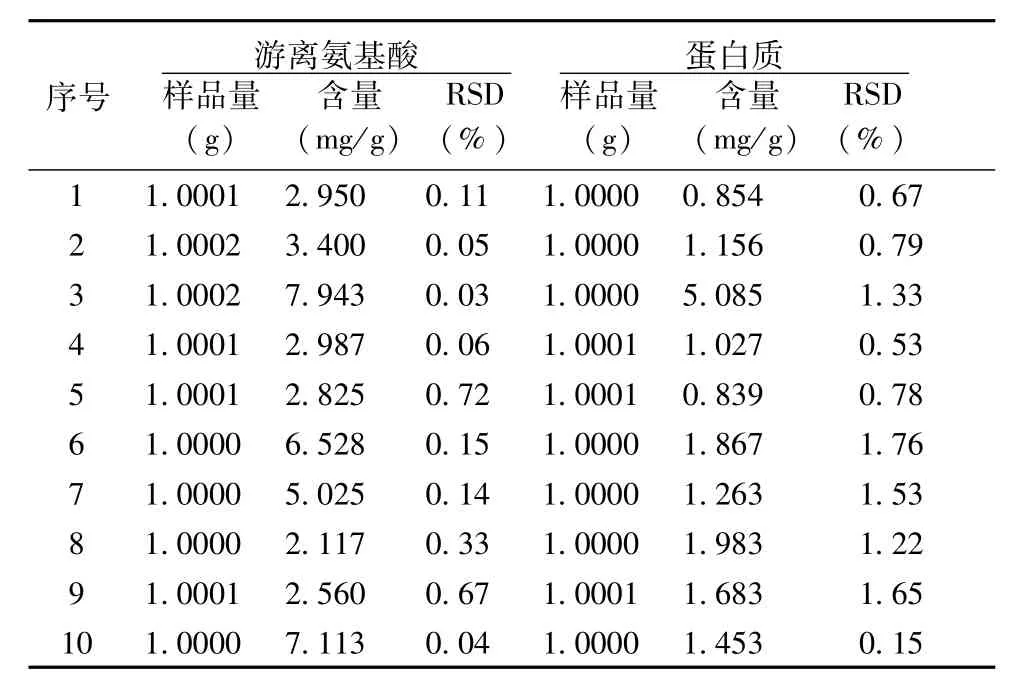
表3 游离氨基酸及蛋白质含量测定试验结果(n=5)
3 小结
3. 1 用茚三酮显色法测定药渣中游离氨基酸的含量的原理 弱酸性溶液中茚三酮与氨基酸共热,可引起氨基酸的脱氨、脱羧反应,最终与还原性茚三酮发生作用,生成紫色物质,颜色深浅与氨基酸含量成正比。该方法简便、快捷、灵敏度高、检测成本低,可用于大样本的检测。
3. 2 用考马斯亮蓝法测定蛋白质含量的基本原理考马斯亮蓝与蛋白质直接结合,颜色深浅与蛋白质含量成正比,因此,测定结果不受样品中非蛋白氮的影响,结果更准确[15]。用考马斯亮蓝G-250,作为蛋白质的显色剂,灵敏度高、简便、快速等优点。与古老的经典的测定蛋白质的方法相比,考马斯亮蓝法,不需要消化且用时用时较短,加入显色剂后立刻就能测定,可用于蛋白质的检识,灵敏度高,且迅速而简便。
4 讨论
在检测氨基酸过程中,混匀时轻微的震荡,使混合均匀,剧烈震荡会产生气泡,不易定容;水浴温度每次做要保持一致,温度对显色影响较大。在测定蛋白质过程中,加入CBB G-250后,立即轻微震荡混匀,再定容,若剧烈震荡会产生大量的气泡,干扰定容。测定时要迅速,该显色反应随时间增长,吸光度值在逐渐降低。
参考文献
[1]蔡景义,周安国.中草药渣在动物生产中的应用[J].黑龙江畜牧兽医,2009(1):56-57.
[2]曹德宾,王广来,李艳秋,等.中药废渣栽培平菇试验初报[J].中国食菌,2008,27(4):17-18.
[3]王小晶,邓宇,方德华.急支糖浆药渣栽培野生平菇的效应研究[J].食用菌学报,2008,16(3):36-38.
[4]潘华峰,邓乔丹,冯毅种,等.中药渣综合利用的可行性分析[J].时珍国医国药,2011,22(8):2026-2027.
[5]陆景伟,王远会,张远陵,等.中药渣在农业上的综合利用研究进展[J].南方农业,2013,7(12):64-67.
[6]吴焱鑫,冀彦锡,任昂,等.中药渣栽培食(药)用真菌研究的概述[J].中国食用菌,2011,30(4):3-6.
[7]谭永忠,陈今朝,韩宗先,等.中药渣栽培平菇试验[J].北方园艺,2012(9):168-170.
[8]王茂,郭鑫,韩峰,等.中药渣有氧发酵有机肥中试及田间肥效试验研究[J].现代农业科技,2014(18):217-218.
[9]唐懋华,成维东.中药渣基质对蔬菜育苗及产量的影响[J].江苏农业科学,2005,33(4):81-82.
[10]胡京枝,董小海,余大杰,等.紫外分光光度法测定含乳饮料中游离氨基酸含量[J].中国食品添加剂,2007(6):164-166,64.
[11]张永芳,张琪,王润梅,等.茚三酮呈色法测定谷子种子中的游离氨基酸含量[J].种子,2014,33(1):111-113,126.
[12]梁英丽,李艳,高孟婷,等.西归中总氨基酸含量测定方法研究[J].大理学院学报,2009,8(10):7-9.
[13]李娟,张耀庭,曾伟,等.应用考马斯亮蓝法测定总蛋白含量[J].中国生物制品学杂志,2000,13(2):118-120.
[14]王孝平,邢树礼.考马斯亮蓝法测定蛋白含量的研究[J].天津化工,2009,23(3):40-42.
[15]王艾平,周丽明.考马斯亮蓝法测定茶籽多糖中蛋白质含量条件的优化[J].河南农业科学,2014,43(3):150-153.
(2015-06-17收稿 责任编辑:王明)
中图分类号:R284. 1
文献标识码:A dol:10. 3969/j. issn. 1673-7202. 2016. 02. 039
通信作者:田树革(1968. 05—),男,博士,教授,博士研究生导师,研究方向:中药化学与质量标准,E-mail:tsgyz@sina. com
作者简介:张凤雪(1990. 01—),女,2014级在读硕士研究生,中药化学与中药分析学,E-mail:1165025478@qq. com
基金项目:新疆医科大学中药化学教学团队专项资助(编号:JXTD2013-3)
