Zr添加对V2.1TiNi0.3贮氢合金结构和电化学性能的影响
2016-03-30宋茂成张荣华张雪峰赵朝勇同艳维
宋茂成,张荣华,张雪峰,赵朝勇,同艳维
Zr添加对V2.1TiNi0.3贮氢合金结构和电化学性能的影响
宋茂成1,2,张荣华1,2,张雪峰3,赵朝勇2,同艳维3
(1. 西华大学 材料科学与工程学院,四川 成都 610039;2. 攀枝花学院 材料工程学院,四川 攀枝花 617000;3. 攀枝花学院 生物与化学工程学院,四川 攀枝花 617000)
利用电弧熔炼法制备了V2.1TiNi0.3Zr(=0~0.12)贮氢合金,系统研究了该系列合金的相结构和电化学性能。显微组织及X射线衍射(XRD)分析表明:无Zr合金由体心立方结构的V基固溶体主相和TiNi基第二相组成,当加入Zr后,合金第二相变为具有六方结构的C14型Laves相而主相不变,所有第二相均呈网状分布于主相晶界附近。随着Zr添加量的增加,合金主相的晶胞参数和晶胞体积呈增大趋势。电化学测试表明:添加一定量的Zr既能提高其活化性能,又能提高其最大放电比容量;同时,随着Zr添加量的增加,合金电极的高倍率放电能力及交换电流密度均有所提高。通过比较发现,V2.1TiNi0.3Zr0.06合金电极具有较好的综合性能。
钒基贮氢电极合金;镍氢电池;Zr添加;显微结构;电化学性能;循环稳定性
钒基固溶体贮氢合金由于具有相对高的贮氢量及放电比容量,用作Ni-MH电池负极材料,被誉为高能绿色环保型能源电池材料。Tsukahara等[1]对V基固溶体贮氢合金V-Ti-Ni三元合金材料进行研究,发现V3TiNi0.56具有相对较高的放电比容量(420 mAh·g–1)。从此,这类合金开始得到广泛研究。Iwakura等[2]的研究表明,在放电电流密度为25 mA·g–1时,V0.9TiNi0.5合金具有最高放电比容量430 mAh·g–1,对其进行深入研究发现该合金组织主要由V2.1TiNi0.3固溶体主相、起导电集流和催化作用的TiNi基第二相(V0.2TiNi0.8)及少量的Ti2Ni基相组成,其中V2.1TiNi0.3与上述V3TiNi0.56合金的组织结构特征近乎一样,其合金结构均由两相结构组成:主要吸氢相V基固溶体主相及具有导电集流作用的TiNi基第二相。在相同放电条件下,其放电比容量最大可达540 mAh·g–1。该合金具有高容量的重要原因是V2.1TiNi0.3合金中形成了与主相比例最合适,且最有利于电化学吸放氢的呈网状结构分布于主相周围的第二相,但该合金的最大缺点是循环寿命和高倍率放电能力差,这严重阻碍了Ni-MH电池在实际中的应用。
大量研究表明多元合金化是提高贮氢合金电极综合性能最有效的方法之一[3-13]。在V3TiNi0.56合金的基础上通过添加元素Zr、Hf,合金中第二相开始出现C14型Laves相,由于该相本身具有一定的可逆吸放氢性能、较好的导电集流及电催化活性,最终使合金电极的综合性能得到很好的改善[8-10]。因而,本研究在V2.1TiNi0.3合金的基础上,选择Zr作为添加元素,系统地研究其对V2.1TiNi0.3Zr(=0~0.12)贮氢合金结构及电化学性能的影响。
1 实验
1.1 合金电极的制备
V2.1TiNi0.3Zr(=0~0.12)合金均采用质量分数大于99.9%的V、Ti、Ni、Zr金属作为原料,在型号为WS-3的非自耗真空电弧炉中熔炼。为防止合金氧化,先反复清洗炉体3次,再向电弧炉中通入适量的氩气进行熔炼。为使得到的合金成分均匀,将其反复翻身熔炼5次。打磨掉炼制后合金的氧化皮,将其放入氢化装置反应器中,在773 K温度下经4次充放氢,最后在抽真空的条件下冷却至室温得到氢化合金。将合金在玛瑙研钵中研磨并过75mm(200目)筛,之后取合金粉120 mg并以1:4的质量比与羟基镍粉混合均匀,然后将其注入模具中,再以12 MPa的压力将其冷压在大小适中的泡沫镍上,成型后获得直径为10 mm的电极片。
1.2 电化学性能测试
采用开口式三电极体系对合金电极的电化学性能进行测试。其中,合金电极作为研究电极,烧结式Ni(OH)2/NiOOH片作为辅助电极,正负极用隔膜分开,氧化汞(Hg/HgO)作为参比电极,7 mol·L–1的KOH纯水溶液作为电解液。用LANHE蓝电电池测试系统测试合金电极的充放性能,测试温度均设定为303 K。充放电机制为:充电电流密度均为100 mA·g–1,充电时间为320 min,静置5 min后,以60 mA·g–1的放电电流密度进行放电性能测试,截止电位0.6 V。进行高倍率放电测试时,用相同的充放电机制使合金电极完全活化后,再分别以60,100,200,400,600 mAh·g–1的放电电流密度进行放电,截止电压均为0.6 V,最后再均以60 mAh·g–1的放电电流密度放电至0.6 V。进行极化曲线测试时,待合金电极完全活化后,将其放电至放电深度(DOD)为50%,再在CHI600E型电化学工作站上以1 mV·s–1的扫描速率,在–0.5~+0.5 mV范围内对合金进行极化曲线测试。
1.3 合金的显微结构分析
将熔炼出的铸态合金样品打磨出两个面。其中一面抛光,将其在HF,HCl,乙醇的体积分数分别为10%,10%,80%的混合液中浸渍5~7 min,经冲洗和吹干后,再在DMM-440C型金相显微镜下观察,并拍摄金相组织图片。另一面采用型号为DX-2700的X射线衍射仪进行相结构分析,45 kV和30 mA的CuKa靶辐射,角度扫描范围2为30°~100°,步长为0.03°。
2 结果与分析
2.1 电极合金的结构
图1为V2.1TiNi0.3Zr(=0~0.12)电极合金的铸态XRD谱。由图可知无Zr电极合金由体心立方(BCC)结构的V基固溶体主相与TiNi基第二相组成。加入Zr后,合金中的第二相变为C14型Laves相,这与文献[14]的结论类似。随着Zr添加量的增多,合金中的C14型Laves相逐渐增多,体心立方结构的V基固溶体主相衍射峰向小角度方向逐渐偏移,这表明主相的晶胞体积随Zr含量的增多有所增大。V基固溶体主相的晶胞参数及体积经XRD分析计算后的结果如表1所示。由表可知,随着合金中Zr含量的增加,主相的晶胞参数和体积均呈增大的趋势。从原子半径方面看,V、Ti、Ni、Zr的原子半径分别为0.135,0.145,0.124,0.160 nm,其中Zr的原子半径最大。当向合金中添加Zr时,该原子可能以原子取代的形式存在于合金中,从而导致合金主相晶胞体积的增大。

图1 V2.1TiNi0.3Zrx(x=0~0.12)合金的XRD谱
表1 V2.1TiNi0.3Zr(=0~0.12)合金中主相的晶胞参数和晶胞体积
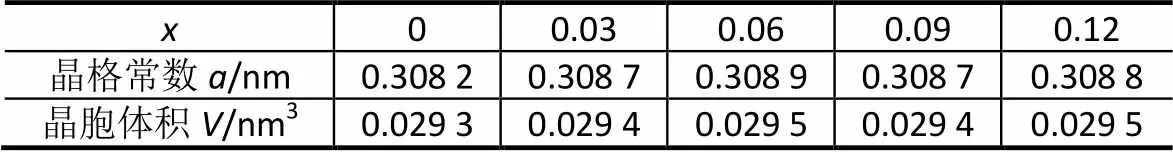
Tab.1 Cell parameters and volume of the main phase in the V2.1TiNi0.3Zrx (x=0-0.12) alloys
图2为V2.1TiNi0.3Zr(=0~0.12)合金的显微组织图。根据图2与文献[15]可得知,在=0时,合金组织中呈浅灰色的为V基固溶体主相,呈深灰色的三维网状结构为TiNi基二次相。在=0.03~0.12时,合金主相不变,但二次相变为C14型Laves相。从图中还可得知,随着的增大合金中的组织逐渐细化,二次相网状结构逐渐密集,这有利于提高Laves在电解液中的稳定性及催化活性。

(a) x=0;(b) x=0.03;(c) x=0.06;(d) x=0.09;(e) x=0.12
2.2 合金电极的电化学性能
2.2.1 电极的活化性能与最大放电比容量
在充电电流密度为100 mA·g–1、放电电流密度为60 mA·g–1、温度为303 K的条件下,V2.1TiNi0.3Zr(=0~0.12)合金电极最大放电比容量与活化性能曲线图如图3所示。由图3中可得知,在≤0.03时,合金电极需经2次充放电活化后才可达到最大放电比容量;而在≥0.06时,合金首次充放电活化就可达到其最大放电比容量。在=0时,合金电极的最大放电比容量为454.30 mAh·g–1。随着合金中Zr含量的增加,其最大放电比容量先降低后升高再降低,在=0.03时,合金电极的最大放电比容量降低到435.20 mAh·g–1,=0.06最大放电比容量在所有合金电极中达到最大值为483.70 mAh·g–1。但当Zr加入量=0.09和0.12时,其最大放电比容量分别降低到468.90,449.90 mAh·g–1。据报道实验中C14型Laves相在合金电极中既具有催化和导电集流作用,又具有较高的可逆充放电能力[14],这是合金电极的活化性得到改善的原因,也是V2.1TiNi0.3Zr(=0.06, 0.09)最大放电比容量高于对照组合金的原因之一。另一原因是Zr的加入使原合金的晶胞体积增大从而使合金的吸氢量增大,最终使其放电比容量增大。V2.1TiNi0.3Zr0.03合金电极具有的最大放电比容量比对照组合金低的原因可能是Zr的加入量较少,从而使C14型Laves相的形成少,同时V基固溶体主要吸氢相有微量减少。V2.1TiNi0.3Zr0.12合金电极的容量降低是因为Zr添加量增多使C14型Laves相增多而主要吸氢相减少,增加的Laves相吸氢能力比V基固溶体主相弱,因此Zr添加量增加到一定程度时会导致合金电极放电比容量的降低。
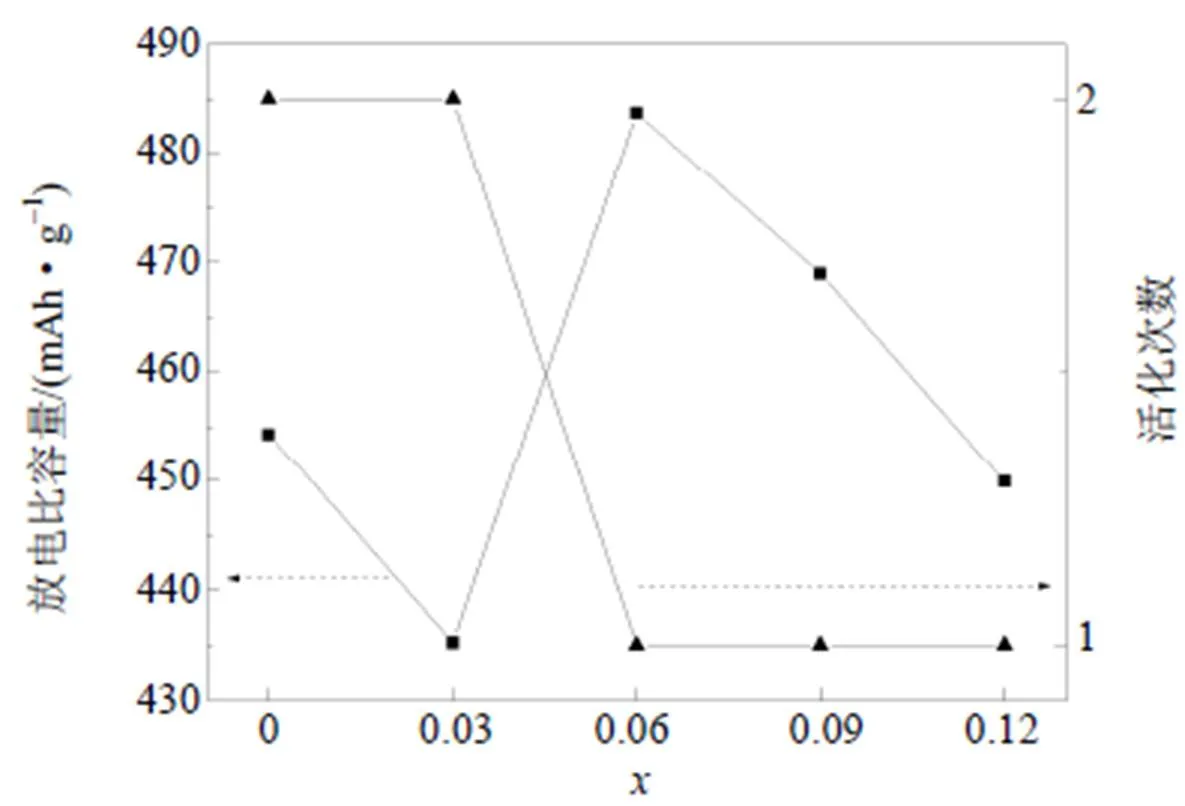
图3 V2.1TiNi0.3Zrx(x=0~0.12)合金电极的活化次数与最大放电比容量曲线
综上所述,添加适量的Zr控制合金中主相与第二相的比例是提高合金放电比容量的主要措施之一。本实验中V2.1TiNi0.3Zr0.06合金的主相与第二相比例最佳,所以具有最大的放电比容量。
2.2.2 合金电极的循环稳定性
图4是V2.1TiNi0.3Zr(=0~0.12)合金电极在303 K时的循环稳定性曲线,图5为该合金电极的容量保持率及第20次放电比容量与Zr添加量的关系曲线。由图4和图5可知,随Zr含量的增加,合金电极的循环稳定性、容量保持率及其第20次放电比容量均先降低后升高,但相对无Zr合金电极均有所降低。其中,V2.1TiNi0.3合金电极具有最好的循环稳定性和最高的容量保持率,第20次放电比容量最大为104 mAh·g–1,而V2.1TiNi0.3Zr0.06循环稳定性最差,容量保持率仅有14.53%,第20次放电比容量只有70.30 mAh·g–1。向合金中添加Zr元素其循环稳定性降低,可能是因为添加Zr元素之后,在合金电极表面形成一层ZrO2薄膜,这种膜会加速合金电极内部吸氢元素在KOH电解液中的腐蚀,在进行充放电过程中该膜的厚度和致密度都得到一定程度的加强,充放电时氢原子很难穿过该薄膜,这会使活性物质颗粒间的接触电阻增大。此外,合金电极在充放电循环过程中,贮氢元素V会被腐蚀溶解于电解液中,进而使合金电极抗腐蚀能力降低,再加上具有催化性能的第二相网状结构遭到破坏,所以在V2.1TiNi0.3合金中添加Zr对其循环稳定性具有不利影响。
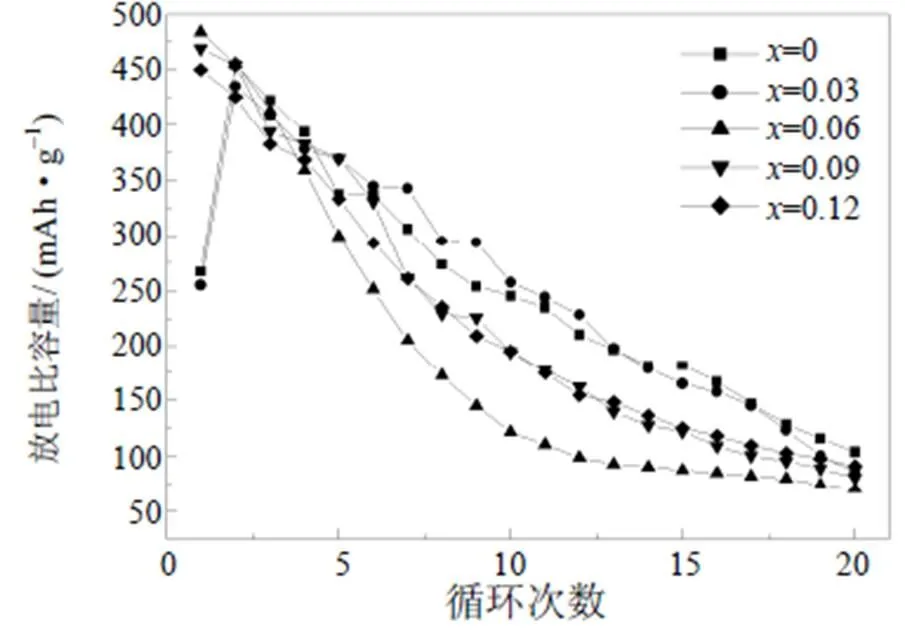
图4 V2.1TiNi0.3Zrx(x=0~0.08)合金电极的循环稳定性曲线
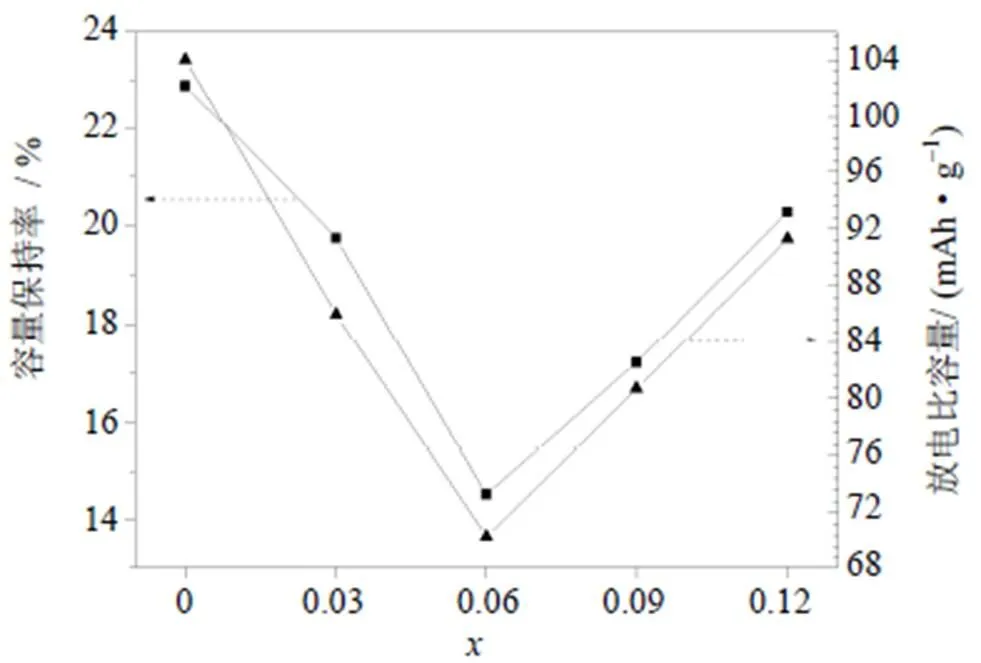
图5 V2.1TiNi0.3Zrx(x=0~0.12)合金电极的容量保持率和第20次放电比容量曲线
2.2.3 合金电极的放电性能
图6为V2.1TiNi0.3Zr(=0~0.12)合金电极在303 K的温度下达到最大放电比容量所对应的放电电位曲线。从图中可知,电极电势随着放电过程的进行均逐渐降低,这是由于在充电过程中电极吸收的氢逐渐被氧化所致。随着Zr的加入,合金电极出现两个放电平台,且其放电平台的宽度和放电比容量正相关。第一个较高的放电平台是V基固溶体氢化物放电所致,而第二个放电平台则是C14型Laves相的氢化物放电所引起的。在放电过程中,随Zr添加量的增加,合金放电平台宽度先减小后增大再减小。这是因为在≤0.03时,合金中不仅V基固溶体主要吸氢相有所减少,而且没能形成既具有较强可逆吸放氢能力又具有催化及导电集流作用的C14型Laves相,最终使合金的放电比容量有所减小。当Zr添加量适当时,即在=0.06时,C14型Laves第二相与合金的吸氢主相达到最佳比例,从而使其放电比容量达到最大。但当≥0.06时,合金中C14型Laves相增多,同时主要吸放氢相含量进一步减少,从而使其放电比容量减小。
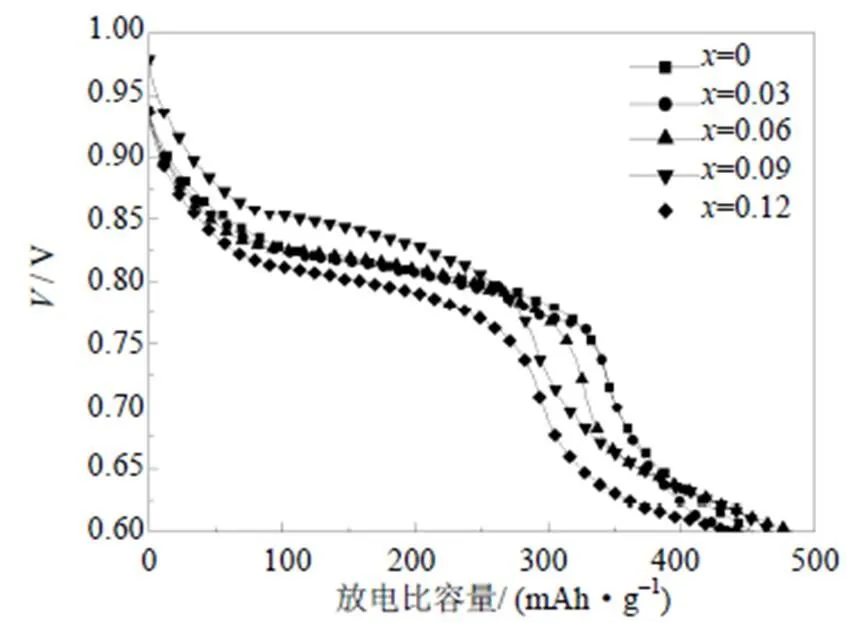
图6 V2.1TiNi0.3Zrx(x=0~0.12)合金电极的放电性能曲线
2.3 合金电极的动力学性能
2.3.1 合金电极的高倍率放电性能
图7是V2.1TiNi0.3Zr(=0~0.12)合金电极以放电电流密度分别为60,100,200,400,600 mA·g–1放电时的高倍率放电性能曲线。图8为V2.1TiNi0.3Zr(=0~0.12)合金电极在不同放电电流密度下的放电比容量曲线。表2列出了放电电流密度为200 mA·g–1时各合金对应的高倍率放电能力(HRD200)。由图7和表2可知,随着放电电流密度的增加,合金电极的高倍率放电性能均逐渐降低。随Zr添加量的增加,合金电极的高倍率放电能力均得到提高,呈现出先增加后减小的趋势。在200 mA·g–1的放电电流密度下,对照组合金(V2.1TiNi0.3)HRD200只有22.50%。当=0.03~0.12时,合金的HRD200由59.70%提高到最大,达71.70%,之后再降低到49.20%。由图8可看出,随放电电流密度的增大,合金的放电比容量逐渐降低。在同等大小的放电电流密度下,随合金中Zr含量的增加放电比容量先增加后降低。

图7 V2.1TiNi0.3Zrx(x=0~0.12)合金电极高倍率放电性能曲线

图8 V2.1TiNi0.3Zrx(x=0~0.12)合金电极不同放电电流密度下的放电比容量
表2 V2.1TiNi0.3Zr(=0~0.12)合金电极的电化学动力学参数

Tab.2 Electrochemical kinetic parameters of the V2.1TiNi0.3Zrx(x=0-0.12) alloy electrodes
2.3.2 合金电极的交换电流密度
图9为V2.1TiNi0.3Zr(=0~0.12)合金电极在303 K及放电深度DOD=50%时的线性极化曲线。合金电极的极化曲线在极化电位为–0.5~+0.5 mV时,其极化电位和极化电流之间具有较好的线性关系。文献[16]报道,根据线性极化曲线的斜率可估算出电化学反应的交换电流密度(0),其公式如下所示:
式中:为气体常数;为热力学温度;为法拉第常数;/是极化曲线斜率。
图9 303 K时V2.1TiNi0.3Zr(=0~0.12)合金电极50% DOD的线性极化曲线
Fig.9 Linear polarization curves of V2.1TiNi0.3Zr(=0-0.12) alloy electrodes measured at 50% DODand 303 K
合金的0经计算列于表2中。由表可知,合金电极的交换电流密度0随Zr添加量的增加,由=0时的54.80 mA·g–1增大到=0.06时的125.90 mA·g–1,而后降低到=0.12时的111.10 mA·g–1。因为反映电极表面的电化学反应速率的基本指标是交换电流密度,所以表2的结果表明Zr添加到合金中可以有效提高合金电极的电化学反应速率。随Zr含量增加,合金电极高倍率放电性能与交换电流密度具有一致的规律。
3 结论
(1) V2.1TiNi0.3Zr(=0.03~0.12)合金均由体心立方结构的V基固溶体主相和第二相组成,且第二相呈网状结构分布于主相晶界附近。在=0时合金的第二相为TiNi基相。当≥0.03时,合金中的第二相变为具有六方结构的C14型Laves相。合金主相的晶胞参数和晶胞体积随着Zr添加量的增加呈增大趋势。
(2) 添加Zr可以改善V2.1TiNi0.3合金电极的活化性能,其最大放电比容量随Zr含量的增加先降低后升高再降低。在=0.06时,合金电极的放电比容量达到最大483.70 mAh·g–1。
(3) 随着Zr添加量的增加,合金电极的高倍率放电能力及交换电流密度均有所提高。其中,高倍率放电能力呈现出先增大后减小的趋势,合金电极的交换电流密度具有先升高后降低的规律。
(4) 在所研究的电极合金中,V2.1TiNi0.3Zr0.06具有相对较好的综合电化学性能,经过1次活化达到最大放电比容量483.70 mAh·g–1,20次充放电比容量保持率为14.53%,在放电电流密度为200 mA·g–1的条件下,其高倍率放电能力(HRD200)达到71.70%。
[1] TSUKAHARA M, TAKAHASHI K, MISHIMA T, et al. An improvement in the properties of hydrogen storage alloy by copper microencapsulation [J]. J Alloy Compd, 1995, 224: 162-169.
[2] IWAKURA C, CHOI W K, MIYAUEHI R, et al. Electrochemical and structural characterization of Ti-V-Ni hydrogen storage alloys with BCC structure [J]. J Electrochem Soc, 2000, 147: 2503-2506.
[3] 刘守平, 徐安莲, 田卫国, 等. V3TiNi0.56Al贮氢合金充放电性能和吸放氢性能研究[J]. 材料导报, 2007, 21(5): 278-280.
[4] TSUKAHARA M, TAKAHASHI K, MISHIMA T, et al. Influence of various additives in vanadium-based alloys V3TiNi0.56on secondary phase formation, hydrogen storage properties and electrode properties [J]. J Alloy Compd, 1996, 245(1): 59-65.
[5] TSUKAHARA M, TAKAHASHI K, ISOMURA A, et al. Improvement of the cycle stability of vanadium-based alloy for nickel metal hydride(Ni-MH)battery [J]. J Alloy Compd, 1999, 287: 215-220.
[6] ZHANG Q A, LEI Y Q, WANG Q D, et al. Influence of Mn on phase structures and electrochemical properties of V3TiNi0.56Hf0.24alloy [J]. Int J Hydrogen Energy, 2000, 25(7): 657-662.
[7] 李荣, 周上祺, 刘守平, 等. V3TiNi0.56Al0.2Cr(=0–0.3)贮氢合金的微结构及电化学性能[J]. 中国有色金属学报, 2010, 20(4): 706-711.
[8] TSUKAHARA M, TAKAHASHI K, MISHIMA T, et al. Vanadium-based solid solution alloys with three-dimensional network structure for high capacity metal hydride electrodes [J]. J Alloy Compd, 1997, 253: 583-586.
[9] 刘守平, 徐安莲, 田中青, 等. 贮氢合金V3TiNi0.56Cr的充放电性能和吸放氢性能研究[J]. 功能材料, 2007, 38(2): 286-288.
[10] TSUKAHARA M, TAKAHASHI K, MISHIMA T, et al. V-based solid solution alloys With Laves phase network: hydrogen absorption properties and microstructure [J]. J Alloy Compd, 1996, 236: 151-155.
[11] 周怀营, 钟燕. V2.1TiNi0.4Gd贮氢合金的结构和电化学性能研究[J]. 广西大学学报(自然科学版), 2008, 33(3): 275-279.
[12] ZHANG Q A, LEI Y Q, YANG X G, et al. Phase struetures and electrochemical properties of Cr-added V3TiNi0.56Hf0.24Mn0.15alloys [J]. Int J Hydrogen Energy, 2000, 25: 977-981.
[13] 董玉臻. 合金元素对钒基固溶体储氢合金组织与电化学性能的影响[J]. 钢铁钒钛, 2015, 36(4): 43-47.
[14] PAN H G, ZHU Y F, GAO M X, et al. A study on the cycling stability of the Ti-V-based hydrogen storage electrode alloys [J]. J Alloy Compd, 2004, 364(1): 271-279.
[15] 陈立新, 李露, 王新华, 等. V2.1TiNi0.4Zr(0–0.06)储氢合金电极的相结构及电化学性能[J]. 物理化学学报, 2006, 22(5): 523-527.
[16] NOTTEN P H L, HOKKELING P. Double-phase hydride forming compounds: A new class of highly electrocatalytic materials [J]. J Electrochem Soc, 1991, 138(7): 1877-1885.
(编辑:曾革)
Effect of zirconium addition on microstructure and electrochemical properties of V2.1TiNi0.3alloy
SONG Maocheng1,2,ZHANG Ronghua1,2,ZHANG Xuefeng3, ZHAO Chaoyong2,TONG Yanwei3
(1. College of Materials Science and Engineering, Xihua University, Chengdu 610039, China; 2. College of Materials Engineering, Panzhihua University, Panzhihua 617000, Sichuan Province, China; 3. College of Biological and Chemical Engineering, Panzhihua University, Panzhihua 617000, Sichuan Province, China)
V2.1TiNi0.3Zr(=0-0.12) hydrogen storage alloys were synthesized by vacuum arc melting method, and the phase structure and electrochemical properties were systematically investigated. The microstructure and XRD analysis show that the V2.1TiNi0.3alloy consists of V-based solid solution main phases with a bcc structure and TiNi-based secondary phases. The secondary phase of the V2.1TiNi0.3Zr(=0.03-0.12) alloy changes into a C14-type Laves phase with hexagonal structure after the Zr element is added, and the main phases remain. The secondary phases of all alloys distribute near the grain boundaries of the main phase in a network structure. In addition, the cell parameters and volumes of the main phase show a increasing tendency with increasing Zr content. According to the electrochemical measurements, not only the activation ability but also the maximum discharge capacity is improved by adding moderate Zr content into the V2.1TiNi0.3alloy. Moreover, the high-rate dischargeability and the exchange current density of the alloys are both improved. It is found that the alloy electrode of V2.1TiNi0.3Zr0.06has better comprehensive performance in the investigated alloys.
V-based hydrogen storage alloy; Ni-MH battery; Zr addition; microstructure; electrochemical property; cycling stability
10.14106/j.cnki.1001-2028.2016.07.009
TM912
A
1001-2028(2016)07-0037-05
2016-03-23
张雪峰
四川省科技支撑计划项目(No. 2012GZX0089);四川省重点实验室项目(No. VTZ-2015003)
张雪峰(1965-),男,四川仁寿人,教授,主要从事钒钛功能材料领域的研究与开发,E-mail: wzyzxf@163.com;
宋茂成(1988-),男,湖南保靖人,研究生,主要从事新能源电极材料的研究,E-mail: 15281206625@163.com 。
2016-07-01 10:47:57
http://www.cnki.net/kcms/detail/51.1241.TN.20160701.1047.008.html
