玻璃体腔注射地塞米松植入物与抗血管内皮生长因子药物治疗视网膜静脉阻塞并发黄斑水肿比较的Meta分析
2016-03-30刘从威董方田
许 妮,刘从威,董方田
1中国医学科学院 北京协和医学院 北京协和医院眼科,北京100730
2中南大学湘雅二医院骨科,长沙410011
玻璃体腔注射地塞米松植入物与抗血管内皮生长因子药物治疗视网膜静脉阻塞并发黄斑水肿比较的Meta分析
许 妮1,刘从威2,董方田1
1中国医学科学院 北京协和医学院 北京协和医院眼科,北京100730
2中南大学湘雅二医院骨科,长沙410011
目的 比较玻璃体腔注射地塞米松植入物 (dexamethasone implant,DEX)与抗血管内皮生长因子 (anti-vascular epithelial growth factor,anti-VEGF)药物在治疗视网膜静脉阻塞 (retinal vein occlusion,RVO)并发黄斑水肿 (macular edema,ME)时的有效性及安全性。方法 以“retinal vein occlusion”、“macular edema”、“anti-VEGF”、“pegaptanib”、“Macugen”、“bevacizumab”、“Avastin”、“ranibizumab”、“Lucentis”、“aflibercept”、“Trap-eye”、“Ozurdex”、“dexamethasone invitreal implant”、“clinical trial”为关键词,检索1948年1月至2015年6月外文生物医学数据库Cochrane图书馆、Pubmed、EMBASE、Ovid Medline及ClinicalTrials.gov关于两种药物对RVO并发ME比较治疗的临床试验。采用Cochrane或Newcastle-Ottawa scale评价方法评价所纳入研究的文献质量,并提取有效数据后用RevMan 5.3软件进行Meta分析。结果 随访1个月时,玻璃体腔注射DEX与anti-VEGF治疗前后最佳矫正视力差值的差异无统计学意义[MD=0.04糖尿病视网膜病变早期治疗研究字母视力表(Early Treatment Diabetic Retinopathy Study,ETDRS)字母,95%CI: -2.07~2.15 ETDRS字母,P=0.97]。但在随访3、4、6个月时,anti-VEGF药物能获得更好的治疗前后最佳矫正视力差值,两组间差异有统计学意义 (MD=-6.98,-12.18,-11.84 ETDRS字母,95%CI: -10.39~-3.58,-20.34~-4.03,-19.66~-4.02 ETDRS字母,P<0.0001,P=0.003,P=0.003)。随访6个月时,anti-VEGF药物较DEX能更有效地降低中央视网膜厚度变化值 (MD=135.86 μm,95%CI:57.07~214.64 μm,P=0.0007)。anti-VEGF组眼压升高的人数比例也较DEX组低 (OR=3.54,95%CI:1.64~7.66,P=0.001)。结论 在治疗RVO引起的ME时,anti-VEGF药物较DEX可更有效改善最佳矫正视力、减少ME,同时对眼内压的影响较小,其有效性及安全性均优于DEX。
视网膜静脉阻塞;黄斑水肿;玻璃体腔地塞米松植入物;抗血管内皮生长因子药物;Meta分析
Med J PUMCH,2016,7(3):168-175
视网膜静脉阻塞 (retinal vein occlusion,RVO)是临床上常见的威胁视力的视网膜血管疾病之一[1]。中央或分支静脉阻塞所致视力丧失的最主要并发症为黄斑缺血以及黄斑水肿 (macular edema,ME)。一直以来RVO并发ME的治疗比较困难。随着对眼内注射治疗的探索发展,曲安萘德以及抗血管内皮生长因子(anti-vascular epithelial growth factor,anti-VEGF)药物在临床得到广泛使用[2-8]。近年来,越来越多的研究报道长效皮质类固醇玻璃体腔植入药物缓释系统如地塞米松植入物 (dexamethasone implant,DEX)在治疗RVO并发ME中的有效性[9-15]。本研究首次采用循证医学的研究方法,对anti-VEGF药物与DEX在RVO并发ME治疗中的有效性及安全性进行比较,以期为临床应用提供参考依据。
资料和方法
检索策略
以“retinal vein occlusion”、“macular edema”、“anti-VEGF”、“pegaptanib”、“Macugen”、“bevacizumab”、“Avastin”、“ranibizumab”、“Lucentis”、“aflibercept”、“Trap-eye”、“Ozurdex”、“dexamethasone intravitreal implant”、“clinical trial”为关键词,电子检索了1948年1月至2015年6月外文生物医学数据库Cochrane图书馆、PubMed、EMBASE、Ovid Medline及 ClinicalTrials.gov中的临床试验。
纳入与排除标准
纳入标准:(1)研究设计:临床试验;(2)研究人群:继发于RVO的ME;(3)干预措施为试验组采用DEX治疗,对照组给予anti-VEGF治疗;(4)需包含以下任一项患者结局指标如:治疗前后最佳矫正视力差值、视力提高≥15个糖尿病视网膜病变早期治疗研究字母视力表 (Early Treatment Diabetic Retinopathy Study,ETDRS)字母的人数比例、视力下降≥15个ETDRS字母的人数比例、中央视网膜厚度 (central retinal thickness,CRT)变化值和眼内压升高的人数比例。排除标准:(1)无对照试验组;(2)个案报道; (3)提供信息不完整或重复发表的文献;(4)摘要或会议摘要;(5)动物实验研究。
文献筛选和资料提取
根据纳入和排除标准筛选文献,阅读所获文献题目和摘要,排除明显不符合纳入标准的文献后,对可能符合纳入标准的文献阅读全文,以确定是否符合纳入标准并提取相关资料,核对纳入文献的结果,对有分歧而难以确定其是否纳入的文献通过第三方决定。提取资料包括:(1)一般资料:题目、第一作者、发表日期、研究地点等; (2)研究特征:研究设计类型、研究人群的平均年龄和性别比、研究眼睛数量、不同的治疗方法及随访时间点等;(3)结局指标:治疗前后最佳矫正视力差值、视力提高≥15个ETDRS字母的人数比例、视力下降≥15个ETDRS字母的人数比例、CTR变化值及眼内压升高的人数比例。文献筛选和资料提取先行预实验以保证准确性,整个过程由两名评价员独立操作并交叉核对。由评价员提取资料,整个过程实施盲法,以保证研究的客观性,尽量减少人为偏倚。
文献质量评估
随机对照试验按照Cochrane评价手册提供的评价标准[16]进行质量评价:(1)随机分配方法; (2)分配方案隐藏;(3)是否采用盲法;(4)结果数据的完整性、随访情况;(5)基线是否可比。用Jadad评分进行说明,分数1~2分为低质量,3~5分为高质量。非随机对照试验按照改良版Newcastle-Ottawa Scale[17]评价纳入文献的质量: (1)病例组和对照组的选择(4颗星);(2)可比性 (2颗星); (3)暴露 (4颗星)。评价后星数越多表明质量越好,最好为10颗星,5颗星以上的研究可以被纳入Meta分析。
统计学处理
采用Cochrane协作网提供的RevMan 5.3软件进行Meta分析[18]。计数资料采用比值比 (odds ratio,OR)为疗效分析统计量;计量资料采用均数差(mean difference,MD)或标准化均数差。各效应量均以95%可信区间 (confidence interval,CI)表示。各纳入研究结果间的异质性采用χ2检验。采用随机效应模型 (random-effects model)对各研究进行Meta分析。
结果

表1 纳入Meta分析研究的基本特征
纳入研究的基本情况及质量评估
初检139项研究,应用Endnote软件去重研究53项,通过阅读题目和摘要排除研究69项,剩余17项,进一步阅读全文和/或研究详细信息后排除13项研究,包括干预措施与研究目的不符合研究2项、与纳入标准不符合研究8项、没有提供足够信息及联系后无回复研究3项,最终纳入4项临床试验研究[19-22]。4项研究对照组均采用anti-VEGF药物治疗方法,2项研究为随机对照试验,Jadad评分均为高质量 (4分)。1项研究为前瞻性预期研究,1项研究为回顾性研究,改良版Newcastle-Ottawa Scale评分均为6颗星,可以被纳入本Meta分析。纳入研究的基本情况见表1,研究中用药及处理见表2。
Meta分析结果
治疗前后最佳矫正视力差值:随访1、3、4和6个月时分别提取数据进行分析,均采用随机效应模型。随访1个月时,研究间不存在统计学异质性(P=0.99,I2=0)。结果显示,DEX组与anti-VEGF组间治疗前后最佳矫正视力差值差异无统计学意义(MD=0.04 ETDRS字母,95%CI: -2.07~2.15 ETDRS字母,P=0.97)。随访3个月时,研究间不存在统计学异质性 (P=0.27,I2=23%)。结果显示,anti-VEGF组较DEX组能较明显地提高治疗前后最佳矫正视力差值 (MD=-6.98 ETDRS字母,95%CI:-10.39~-3.58 ETDRS字母,P<0.0001)。随访4个月时,3项研究比较了治疗前后最佳矫正视力差值,研究间存在统计学异质性 (P=0.002,I2=84%)。结果显示,anti-VEGF组较DEX组能较明显地提高治疗前后最佳矫正视力差值 (MD=-12.18 ETDRS字母,95%CI: -20.34~-4.03 ETDRS字母,P= 0.003)。随访6个月时,3项研究比较了治疗前后最佳矫正视力差值,研究间存在统计学异质性 (P= 0.005,I2=81%)。结果显示,anti-VEGF组较DEX组能较明显地提高治疗前后最佳矫正视力差值 (MD=-11.84 ETDRS字母,95%CI: -19.66~-4.02 ETDRS字母,P=0.003)(图1)。
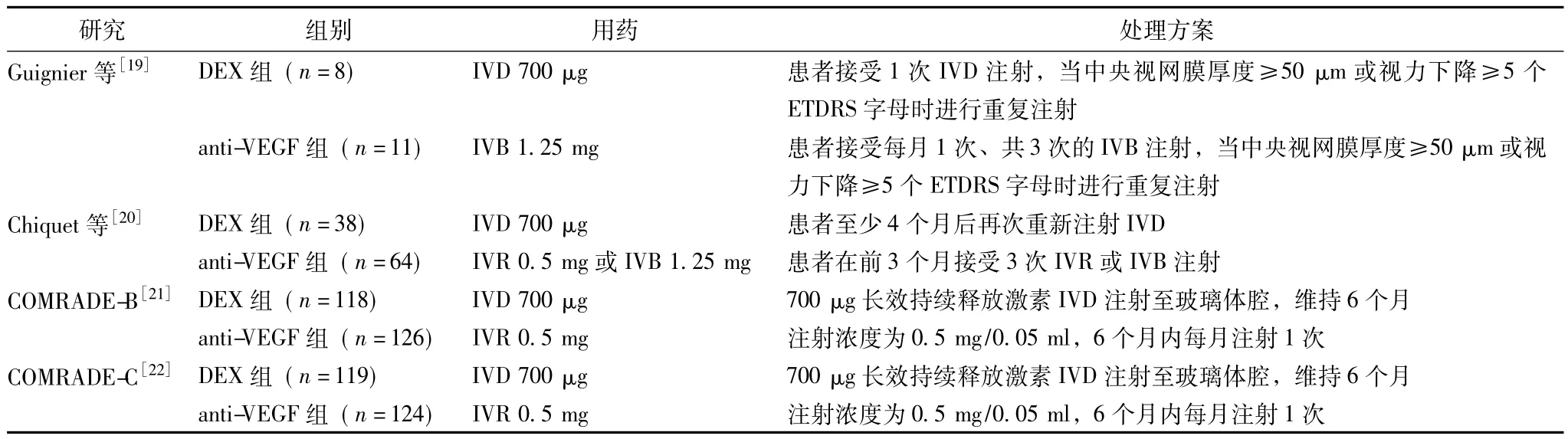
表2 纳入Meta分析研究中各组用药及处理方案

图1 DEX组与anti-VEGF组最佳矫正视力比较的Meta分析结果DEX、anti-VEGF:同表1
视力提高≥15个ETDRS字母的人数比例:随访6个月时,3项研究比较了视力提高≥15个字母的人数比例,研究间存在统计学异质性 (P=0.05,I2= 66%)。结果显示,anti-VEGF组的视力提高≥15个字母的人数比例较DEX组明显增加 (OR=0.22,95% CI:0.10~0.48,P=0.0002)(图2)。
视力下降≥15个ETDRS字母的人数比例:随访6个月时,2项研究比较了视力下降≥15个字母的人数比例,研究间不存在统计学异质性 (P=0.54,I2= 0)。结果显示,DEX组的视力下降≥15个字母的人数比例较anti-VEGF组明显增加 (OR=30.39,95% CI:5.84~158.21,P<0.0001)(图3)。
中央视网膜厚度变化值:随访1个月时,2项研究比较了CRT变化值,研究间存在统计学异质性 (P= 0.08,I2=68%)。结果显示,DEX组与anti-VEGF组间CRT差异无统计学意义 (MD=7.52 μm,95%CI:-147.34~162.38 μm,P=0.92)。随访3个月时,2项研究比较了CRT变化值,研究间不存在统计学异质性(P=0.44,I2=0)。结果显示,DEX组与anti-VEGF组间CRT差异无统计学意义 (MD=30.78 μm,95%CI:-33.19~94.76 μm,P=0.35)。随访6个月时,3项研究比较了CRT变化值,研究间存在统计学异质性 (P= 0.04,I2=68%)。结果显示,anti-VEGF组较DEX组能较明显地减低CRT变化值 (MD=135.86 μm,95%CI: 57.07~214.64 μm,P=0.0007)(图4)。
眼内压升高的人数比例:随访6个月时,2项研究比较了治疗后眼内压升高的人数比例,研究间存在统计学异质性 (P=0.12,I2=59%)。结果显示,DEX组治疗后眼内压升高的人数比例较anti-VEGF组明显增加 (OR=3.54,95%CI:1.64~7.66,P= 0.001)(图5)。
讨论
中央静脉阻塞和分支静脉阻塞并发ME在基本标准治疗方法上有所不同。激光光凝治疗是分支静脉阻塞并发ME的标准治疗方法,而中央静脉阻塞并发ME的激光光凝治疗虽然可以降低ME,但并不能提升视力[23-25]。最近,anti-VEGF和DEX在RVO并发ME的临床治疗上极具前景。DEX(如Ozurdex)为一种可以缓释、生物可降解的植入物,可以通过长期缓慢释放激素来抑制炎症,从而达到治疗ME的目的。同为糖皮质激素的DEX与玻璃体腔注射曲安萘德相比具有药物作用效果持久 (3~4个月)、药物释放具可预期性及药物含量水平稳定等优点[26]。2009年6月18日,美国食品与药品管理局批准 Ozurdex(700 g,Allergan)用于治疗视网膜分支静脉阻塞和视网膜中央静脉阻塞引起的ME。本研究广泛搜集了比较DEX和anti-VEGF在RVO并发ME方面治疗的文献,通过较大样本的对比,以期获得可靠、相对准确的数据,为临床应用提供帮助。
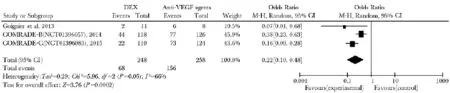
图2 DEX组与anti-VEGF组视力提高≥15个ETDRS字母人数比例的Meta分析结果DEX、anti-VEGF:同表1;ETDRS:同表2

图3 DEX组与anti-VEGF组视力下降≥15个ETDRS字母人数比例的Meta分析结果DEX、anti-VEGF:同表1;ETDRS:同表2
研究表明,anti-VEGF短期疗效较好,因此需反复注射,但远期疗效如何尚不清楚[27-29]。DEX(如Ozurdex)是一种新的可自行降解的糖皮质激素缓释系统,其有效成分是地塞米松,其通过一个22G的推注针头自睫状体平坦部将地塞米松缓释颗粒 (6.50 mm× 0.45 mm大小)推入玻璃体内,切口不需缝合,缓释颗粒不需取出,可缓慢释放地塞米松,作用有效期可达6个月[30]。因为anti-VEGF治疗存在需要重复注药的缺点,反复球内注射相对增加了发生眼内炎、视网膜脱离等严重并发症的风险。而与其相比,玻璃体腔注射DEX可以减少注射次数,延长药物疗效,显示了较好的应用前景。Chiquet等[20]报道眼内压 >21 mm Hg (1 mm Hg=0.133 kPa)在 DEX组 (21%)比 anti-VEGF组 (3.1%)发生率显著升高,差异有统计学意义 (P=0.008)。之后的随访期间,两组均没有眼内炎发生。DEX组3例 (7.9%)患者和anti-VEGF组7例 (10.9%)患者在随访期间行白内障摘除手术,差异无统计学意义 (P>0.05)。Guignier等[19]报道DEX组的眼内压升高率为9%,anti-VEGF组没有眼内压升高病例。两组均没有眼内炎发生。COMRADE-B及COMRADE-C研究[21-22]的眼部不良反应见表3。

图4 DEX组与anti-VEGF组中央视网膜厚度变化值的Meta分析结果DEX、anti-VEGF:同表1

图5 DEX组与anti-VEGF组眼内压升高的人数比例的Meta分析结果DEX、anti-VEGF:同表1
本研究Meta分析结果显示,除随访1个月时anti-VEGF组与DEX组治疗前后最佳矫正视力差值组间差异无统计学意义外,随访 3、4和 6个月时,anti-VEGF组的治疗前后最佳矫正视力差值均优于DEX组;随访6个月时,anti-VEGF组视力提高≥15个ETDRS字母的人数比例高于DEX组,anti-VEGF组视力下降≥15个ETDRS字母的人数比例低于DEX组。说明anti-VEGF组RVO并发ME的治疗后视力较DEX组明显提高,即在视功能-最佳矫正视力改善方面anti-VEGF药物较DEX更好。随访6个月时,anti-VEGF组在降低CRT变化值方面明显优于DEX组。说明anti-VEGF组较DEX组可以明显减少ME,即在解剖指标恢复方面anti-VEGF药物较 DEX更好。随访6个月时,anti-VEGF组眼内压升高的人数比例明显低于DEX组。2015年Bakri等[31]通过对31例RVO引起ME的患者行多次眼内注射DEX后进行临床观察,虽然有45%的患者眼内压升高 (≥22 mm Hg),但是这种升高为短期效应且可控,所有患者仅需常规观察或应用局部降眼压药即可控制,没有患者需要行青光眼手术治疗。这说明,即使多次眼内注射DEX,其眼内压升高仍然是可控的。
单一治疗方式通常优缺点并存,针对RVO并发ME,联合治疗也许是将来临床中越来越多被采用的方式。糖皮质激素具有广谱的抗炎活性,而anti-VEGF类药物则更具特异性,对视网膜及虹膜新生血管可产生有效抑制,两者联合可能起到互补或协同作用;另一方面,糖皮质激素药效时间长,但术后发生白内障、青光眼等并发症的概率也高,anti-VEGF类药物药效时间短,但术后发生眼局部并发症的概率也相对低,两者联合可能减少单一用药剂量、减少注射次数和并发症发生机会。联合疗法的组合模式、剂量设计、治疗顺序、间隔时间等均值得探索。
本研究的不足之处在于,入选Meta分析的研究数量有限,目前DEX与anti-VEGF药物比较治疗RVO并发ME的临床试验 (随机与非随机对照试验)较少,故本研究未绘制漏斗图以对发表偏倚进行检验。考虑到纳入研究的数量,本文的证据强度受限,在临床应用时应结合患者具体情况进行决策。
综上,本Meta分析结果表明,6个月随访期间anti-VEGF治疗较DEX治疗能明显改善最佳矫正视力(治疗前后最佳矫正视力差值、提高≥15个ETDRS字母率的人数比例)以及减少ME(CRT变化值),同时对眼内压的影响较小 (眼内压升高的人数比例)。本研究通过将DEX和anti-VEGF治疗的优劣势进行统计学比较分析,对RVO并发ME的治疗选择及将来的联合治疗具有一定的指导意义,希望今后有更多高质量随机对照试验进一步验证本研究结论。
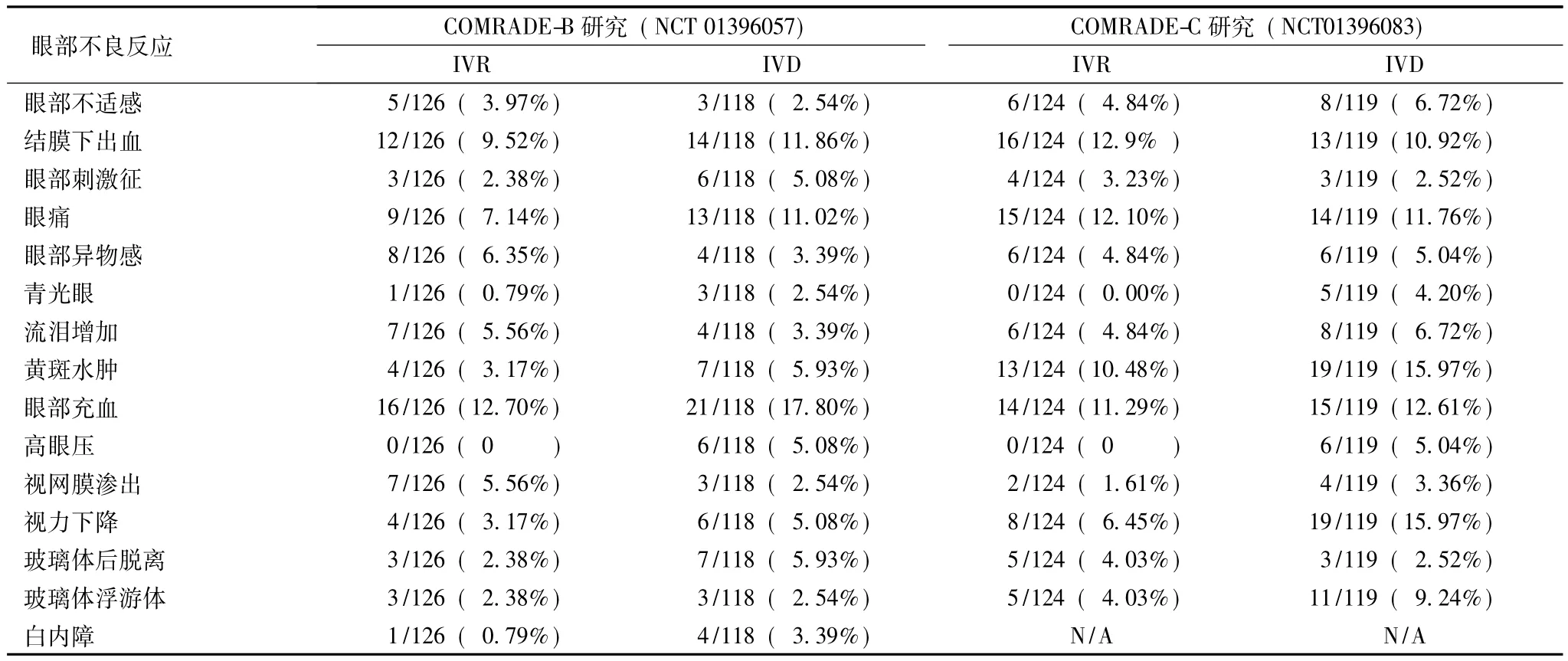
表3 COMRADE-B[21]及COMRADE-C[22]研究中的眼部不良反应
[1]Rogers S,McIntosh RL,Cheung N,et al.The prevalence of retinal vein occlusion:pooled data from population studies from the United States,Europe,Asia,and Australia[J].Ophthalmology,2010,117:313-319.e311.
[2]Cekic O,Cakir M,Yazici AT,et al.A comparison of three different intravitreal treatment modalities of macular edema due to branch retinal vein occlusion[J].Curr Eye Res,2010,35:925-929.
[3]Demir M,Dirim B,Acar Z,et al.Comparison of the effects of intravitreal bevacizumab and triamcinolone acetonide in the treatment of macular edema secondary to central retinal vein occlusion[J].Indian J Ophthalmol,2014,62:279-283.
[4]Ding X,Li J,Hu X,et al.Prospective study of intravitreal triamcinolone acetonide versus bevacizumab for macular edema secondary to central retinal vein occlusion[J].Retina,2011,31:838-845.
[5]Fan C,Wang Y,Ji Q,et al.Comparison of clinical efficacy of intravitreal ranibizumab with and without triamcinolone acetonide in macular edema secondary to central retinal vein occlusion[J].Curr Eye Res,2014,39:938-943.
[6]Figueroa MS,Ruiz Moreno JM.BRAVO and CRUISE:ranibizumab for the treatment of macular edema secondary to retinalvein occlusion[J].Arch Soc Esp Oftalmol,2012,87 Suppl 1:46-53.
[7]Higashiyama T,Sawada O,Kakinoki M,et al.Prospective comparisons of intravitreal injections of triamcinolone acetonide and bevacizumab for macular oedema due to branch retinal vein occlusion[J].Acta Ophthalmol,2013,91:318-324.
[8]Lee K,Jung H,Sohn J.Comparison of injection of intravitreal drugs with standard care in macular edema secondary to branch retinal vein occlusion[J].Korean J Ophthalmol,2014,28:19-25.
[9]Bezatis A,Spital G,Hohn F,et al.Functional and anatomical results after a single intravitreal Ozurdex injection in retinal vein occlusion:a 6-month follow-up—the SOLO study[J].Acta Ophthalmol,2013,91:e340-e347.
[10]Ferrini W,Ambresin A.Intravitreal dexamethasone implant for the treatment of macular edema after retinal vein occlusion in a clinical setting[J].Klin Monbl Augenheilkd,2013,230:423-426.
[11]Haller JA,Bandello F,Belfort R Jr,et al.Randomized,sham-controlled trial of dexamethasone intravitreal implant in patients with macular edema due to retinal vein occlusion[J].Ophthalmology,2010,117:1134-1146.e3.
[12]Haller JA,Bandello F,Belfort R Jr,et al.Dexamethasone intravitreal implant in patients with macular edema related to branch or central retinal vein occlusion twelve-month study results[J].Ophthalmology,2011,118:2453-2460.
[13]Kuppermann BD,Haller JA,Bandello F,et al.Onset and duration of visual acuity improvement after dexamethasone intravitreal implant in eyes with macular edema due to retinal vein occlusion[J].Retina,2014,34:1743-1749.
[14]Schmitz K,Maier M,Clemens CR,et al.Reliability and safety of intravitreal Ozurdex injections.The ZERO study[J].Ophthalmologe,2014,111:44-52.
[15]Yeh WS,Haller JA,Lanzetta P,et al.Effect of the duration of macular edema on clinical outcomes in retinal vein occlusion treated with dexamethasone intravitreal implant[J].Ophthalmology,2012,119:1190-1198.
[16]Higgins JP,Green S.Cochrane Handbook for Systematic Reviews of Interventions Version 5.1.0[updated March,2011][M/OL].The Cochrane Collaboration,2011.http://handbook.cochrane.org.
[17]Wells G,Shea B,O'Connell D,et al.The Newcastle-Ottawa Scale(NOS)for assessing the quality of nonrandomised studies in meta analyses[EB/OL].http://www.ohri.ca/programs/clinical_epidemiology/oxford.asp.
[18]Moher D,Liberati A,Tetzlaff J,et al.Preferred reporting items for systematic reviews and meta-analyses:the PRISMA statement[J].J Clin Epidemiol,2009,62:1006-1012.
[19]Guignier B,Subilia-Guignier A,Fournier I,et al.Prospective pilot study:efficacy of intravitreal dexamethasone and bevacizumab injections in the treatment of macular oedema associated with branch retinal vein occlusion[J].Ophthalmologica,2013,230:43-49.
[20]Chiquet C,Dupuy C,Bron AM,et al.Intravitreal dexamethasone implant versus anti-VEGF injection for treatment-naive patients with retinal vein occlusion and macular edema:a 12-month follow-up study[J].Graefes Arch Clin Exp Ophthalmol,2015,253:2095-2102.
[21]Novartis(Novartis Pharmaceuticals).Efficacy and Safety of Ranibizumab Intravitreal Injections Versus Dexamethasone Intravitreal Implant in Patients With Branch Retinal Vein Occlusion(BRVO)(COMRADE-B).NCT01396057[EB/ OL].(2014-08-04)https://clinicaltrials.gov/ct2/show/ NCT01396057?term=NCT01396057&rank=1.
[22]Novartis(Novartis Pharmaceuticals).Efficacy and Safety of Ranibizumab Intravitreal Injections Versus Dexamethasone Intravitreal Implant in Patients With Central Retinal Vein Occlusion(CRVO)(COMRADE-C).NCT01396083[EB/ OL].(2015-02-25)https://clinicaltrials.gov/ct2/show/ NCT01396083?term=NCT01396083&rank=1.
[23]Argon laser photocoagulation for macular edema in branch vein occlusion.The Branch Vein Occlusion Study Group[J].Am J Ophthalmol,1984,98:271-282.
[24]Central Vein Occlusion Study Group M.Evaluation of grid pattern photocoagulation for macular edema in central vein occlusion.The Central Vein Occlusion Study Group M report[J].Ophthalmology,1995,102:1425-1433.
[25]Hahn P,Fekrat S.Best practices for treatment of retinal vein occlusion[J].Curr Opin Ophthalmol,2012,23:175-181.
[26]Edelman JL.Differentiation introcular glucocorticoids[J].Ophthalmologica,2010,224(Suppl 1):25-30.
[27]Campochiaro PA,Brown DM,Awh CC,et al.Sustained benefits from ranibizumab for macular edema following central retinal vein occlusion:twelve-month outcomes of a phase III study[J].Ophthalmology,2011,118:2041-2049.
[28]Brown DM,Heier JS,Clark WL,et al.Intravitreal aflibercept injection for macular edema secondary to central retinal vein occlusion:1-year results from the phase 3 COPERNICUS study[J].Am J Ophthalmol,2013,155:429-437.
[29]Korobelnik JF,Holz FG,Roider J,et al.Intravitreal aflibercept injection for macular edema resulting from central retinal vein occlusion:one-year results of the phase 3 GALILEO study[J].Ophthalmology,2014,121:202-208.
[30]Fialho SL,Bahar-Cohen F,Silva-Cunha A.Dexamethasone loaded poly(epsiloncaprolactone)intravitreal implnats:a pilot study[J].Eur J Pharm Biopharm,2008,68:637-646.
[31]Bakri SJ,Omar AF,Iezzi R,et al.Evaluation of multiple dexamethasone intravitreal implants in patients with macular edma associated with retinal vein occlusion[J].Retina,2016,36:552-557.
Dexamethasone Intravitreal Implant Compared with Anti-vascular Endothelial Growth Factor Injection for Macular Edema Secondary to Retinal Vein Occlusion:a Meta-analysis
XU Ni1,LIU Cong-wei2,DONG Fang-tian1
1Department of Ophthalmology,Peking Union Medical College Hospital,Chinese Academy of Medical Sciences&Peking Union Medical College,Beijing 100730,China
2Department of Orthopedics,the Second Xiangya Hospital of Central South University,Changsha 410011,China
DONG Fang-tian Tel:010-69156360,E-mail:d_fangtian@sina.com
Objective To compare the efficacy and safety of intravitreal injections of dexamethasone implants(DEX)with anti-vascular endothelial growth factor(VEGF)in the treatment of macular edema(ME)secondary to retinal vein occlusion(RVO).Methods The databases of Cochrane Library,PubMed,EMBASE,Ovid Medline,and ClinicalTrial.gov between January 1948 and June 2015 were searched for studies comparing DEX with anti-VEGF for the treatment of ME caused by RVO with key words“retinal vein occlusion”,“macular edema”,“anti-VEGF”,“pegaptanib”,“Macugen”,“bevacizumab”,“Avastin”,“ranibizumab”,“Lucentis”,“aflibercept”,“Trap-eye”,“Ozurdex”,“dexamethasone invitreal implant”,and“clinical trial”.We evaluated the quality of selected studies using Cochrane or Newcastle-Ottawa scale.Data were extracted and analyzed by Rev-Man 5.3 for Meta-analysis.Results The mean difference in the mean changes of best corrected visual acuity(BCVA)in Early Treatment Diabetic Retinopathy Study(ETDRS)letters comparing DEX with anti-VEGF was 0.04[95%confidence interval(CI): -2.07~2.15;P=0.97]at 1 month,-6.98(95%CI: -10.39~-3.58; P<0.0001)at 3 months,-12.18(95%CI: -20.34~-4.03;P=0.003)at 4 months,and-11.84(95% CI: -19.66~-4.02;P=0.003)at 6 months.A greater reduction of central retinal thickness at 6 months was observed in the anti-VEGF group than in the DEX group(mean difference 135.86 μm;95%CI:57.07~214.64 μm;P=0.0007).The incidence of intraocular pressure increase in the DEX group was significantly higher than that in the anti-VEGF group(OR=3.54,95%CI:1.64~7.66,P=0.001).Conclusions Anti-VEGF showed better effect than DEX in improving BCVA,reducing ME,and less influence on intraocular pressure for ME secondary to RVO.Therefore,anti-VEGF may have higher efficacy and safety than DEX for this condition.
retinal vein occlusion;macular edema;dexamethasone intravitreal implant;anti-vascular endothelial growth factor;Meta-analysis
董方田 电话:010-69156360,E-mail:d_fangtian@sina.com
R774.1
A
1674-9081(2016)03-0168-08
10.3969/j.issn.1674-9081.2016.03.002
2016-01-13)
国家自然科学基金 (30973256)
