一株微杆亚铁氧化菌Microbacterium sp. W5对水中铜离子的吸附行为研究
2016-03-23王弘宇张惠宁
刘 理,王弘宇,张惠宁,杨 开
(武汉大学土木建筑工程学院,武汉 430072)
吸附法是去除废水中有害物质的有效方法,活性炭、天然黏土矿物、合成纳米材料及生物材料已被用作吸附剂去除废水中的重金属离子[1-4]。铜离子作为废水中的常见重金属离子,利用吸附法对其进行去除的问题已得到国内外的广泛关注。林春香[5]等以离子液体 ([Bmim]Cl) 为反应介质,丙烯酸为单体,对纤维素进行均相接枝共聚,并采用油包水反相悬浮技术制得球形纤维素吸附剂,采用静态吸附实验方法研究了该吸附剂对水溶液中 Cu2+的吸附性能。结果表明球形纤维素吸附剂对 Cu2+具有很好的吸附性,首次吸附量达到174.8 mg/g,并具有良好的再生性能,再生3次后吸附剂的吸附容量只下降了8.4%,可以循环使用。王波[6]等通过grafting-from法制备了聚酰胺-胺修饰的氧化石墨烯复合物(GO/PA MAMs) 并研究了GO/PAMAMs对铜离子的吸附行为,结果表明在298K条件下,吸附容量可达167.22 mg/g。Gulay Bayramoglu[7]等采用从土耳其蛇纹石土壤中取得的Ni超富集植物Alyssum discolor对Cu2+和Ni2+进行了吸附。Maibam Dhanaraj Meitei[8]等采用植物Spirodela polyrhiza (L.) Schleiden也对Cu2+进行了吸附研究。然而高效的生物吸附剂仍是环境科学与工程领域的研究热点。本实验利用一株从武汉市东湖深层底泥中筛选出来的硝酸盐还原型厌氧亚铁氧化菌Microbacterium sp. W5在其代谢过程中所产生的生物铁氧化物作为吸附剂。前期工作主要对其生理生化和铁氧化反硝化的特性进行了研究[9]。在此基础之上,本实验研究其在代谢过程中产生的生物铁氧化物对水中重金属Cu2+离子的吸附行为,以期为生物吸附剂的研究提供参考。
1 材料与方法
(1)生物吸附剂的制备。将分离纯化得到的菌株W5接种于灭菌的铁基质自养反硝化培养基中,并于摇床中在150 r/min、30 ℃条件下培养7 d,然后用0.45 μm的滤膜抽滤,将所得的生物铁氧化物放在60 ℃烘箱中烘干后碾磨成粉,制得W5生物吸附剂,pH值为6.8~7.5,铁基质自养反硝化培养基的主要成分见表1[10]。

表1 铁基质自养反硝化培养基的主要成分 g/L
(2)pH对吸附的影响。在Cu2+浓度为100 mg/L,于500 mL溶液中投入1 g吸附剂的条件下,考察pH的变化对吸附的影响,pH的值分别设置为2.0、3.0、4.0、5.0、6.0。
(3)吸附等温线。在30 ℃、pH=5.0的条件下,将吸附剂(1 g/份)分别投加到Cu2+浓度分别为10、20、50、80、100、150、200 mg/L溶液(500 mL)中,在150 r/min条件下震荡,并测定溶液中残留Cu2+浓度,至吸附时间达12 h,Cu2+浓度基本不再变化,可认为吸附已基本达到平衡。用Langmuir和Freundlich方程对数据进行分析,得出吸附参数及回归方程。
(4)吸附动力学。在30 ℃、pH=5.0条件下,取Cu2+浓度为100 mg/L的250 mL溶液,加入0.8 g吸附剂进行吸附,间隔时间分别取5、10、15、20、25、30、60、80、100、120、150、180、210、240、300、360、720 min,对所得数据采用准一级动力学模型和准二级动力学模型进行分析,得出速率常数和回归方程。
(5)傅立叶转换红外光谱分析。将吸附前的吸附剂和充分吸附Cu2+24 h后的吸附剂分别烘干后,进行傅里叶变换红外光谱扫描。通过对比红外光谱图,考察吸附剂在吸附过程中表面官能团的变化情况。
2 结果与讨论
2.1 pH值对吸附的影响
由于Cu2+在碱性溶液中以沉淀形式存在,吸附剂对于Cu2+吸附作用非常小,没有实际吸附意义。因此,着重考察当pH值为2.0~6.0时,pH值对吸附的影响。
从图1中可以看出,pH值对Cu2+的吸附具有显著的影响。当pH值从2.0上升到5.0时,吸附剂对Cu2+的吸附量逐渐增长,在pH=5.0时达到最大。然而,继续增加pH值到6.0,吸附剂对Cu2+的吸附量呈递减趋势。
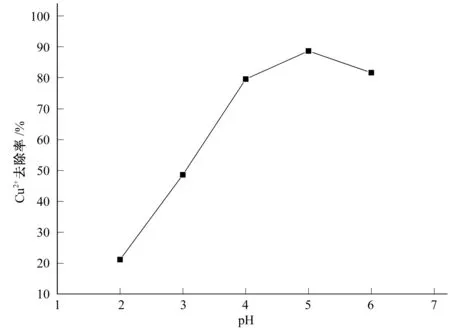
图1 pH值对Cu2+去除率的影响
这是因为在弱碱性(5.0
2.2 吸附等温线
在不同初始离子浓度下吸附剂对铜离子的吸附情况见图2。
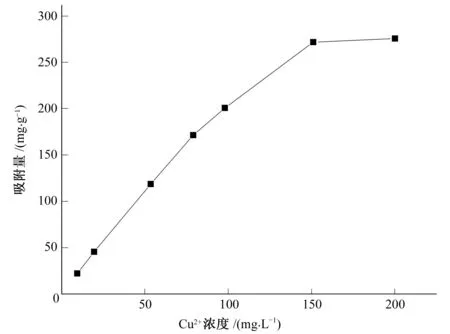
图2 初始Cu2+浓度对吸附的影响
从图2中可以看出,在吸附剂量相同的情况下,初始离子浓度越高,吸附剂的吸附量越高。这是因为溶液中Cu2+的浓度越大,吸附剂上的活性位点周围被越多的铜离子包围,在溶液和吸附剂之间的浓度梯度就越大。所以就会有较多的铜离子被吸附在吸附剂的活性点位,吸附剂吸附Cu2+的量就增加,也越容易达到吸附饱和[12]。
Langmuir方程和Freundlich方程是经典的等温吸附模型,用这两种模型对Cu2+在pH值为5.0条件下的吸附等温线进行拟合。
Langmuir模型可用以下公式表示[13]:
(1)
式中:Ce为溶液中Cu2+的平衡浓度,mg/L;qe为吸附平衡容量,mg/g;qmax为吸附剂的最大吸附容量,mg/g;KL为Langmuir吸附常数,L/mg。
Freundlich模型可用以下公式表示:
(2)
式中:KF为Freundlich吸附常数;1/n为与吸附强度有关的经验参数,和吸附剂的材料特性有关。
对等温吸附分别进行Langmuir和Freundlich模拟,其结果如图3和图4所示。吸附等温方程参数及相关系数见表2。
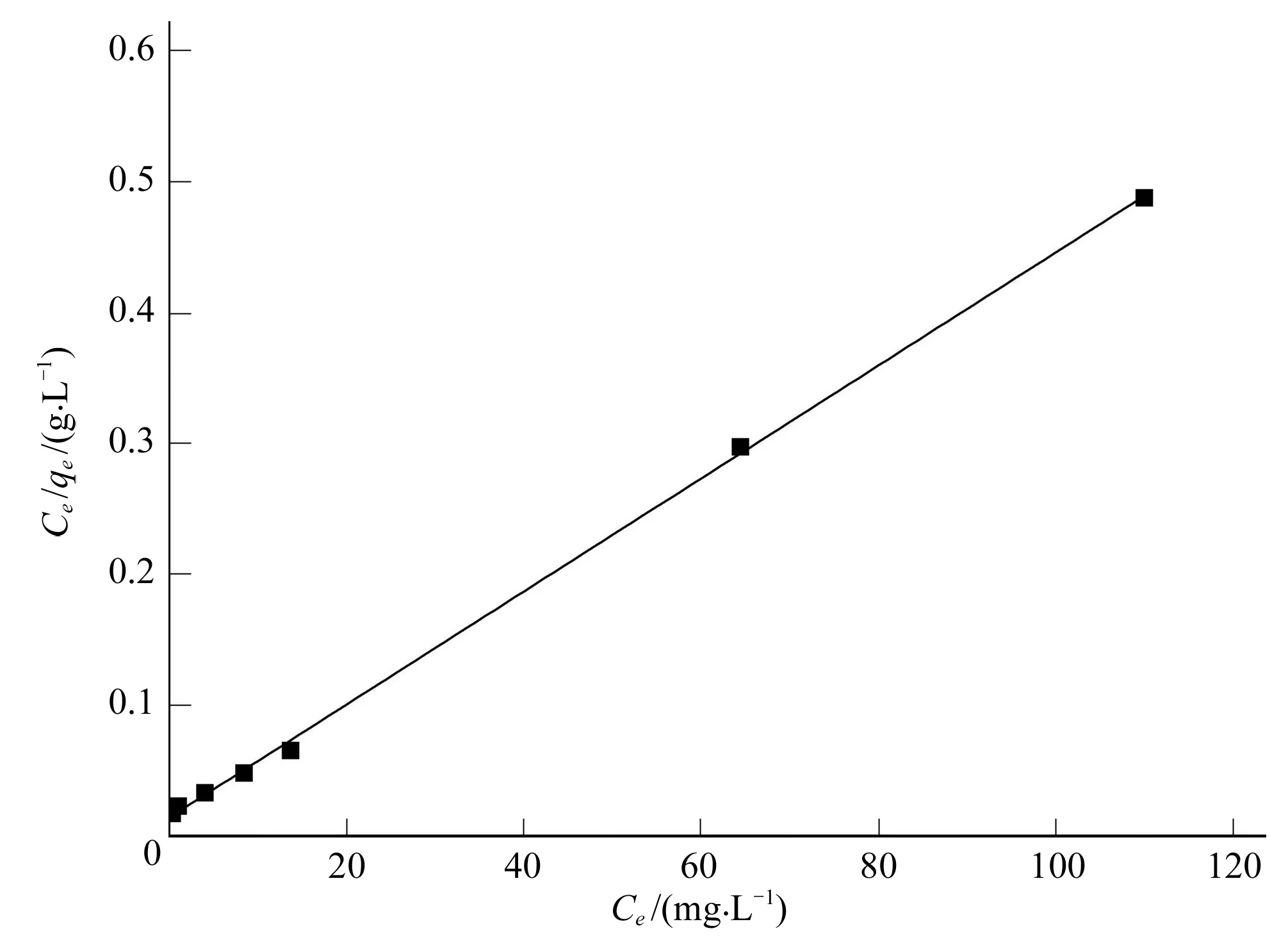
图3 Langmuir等温线
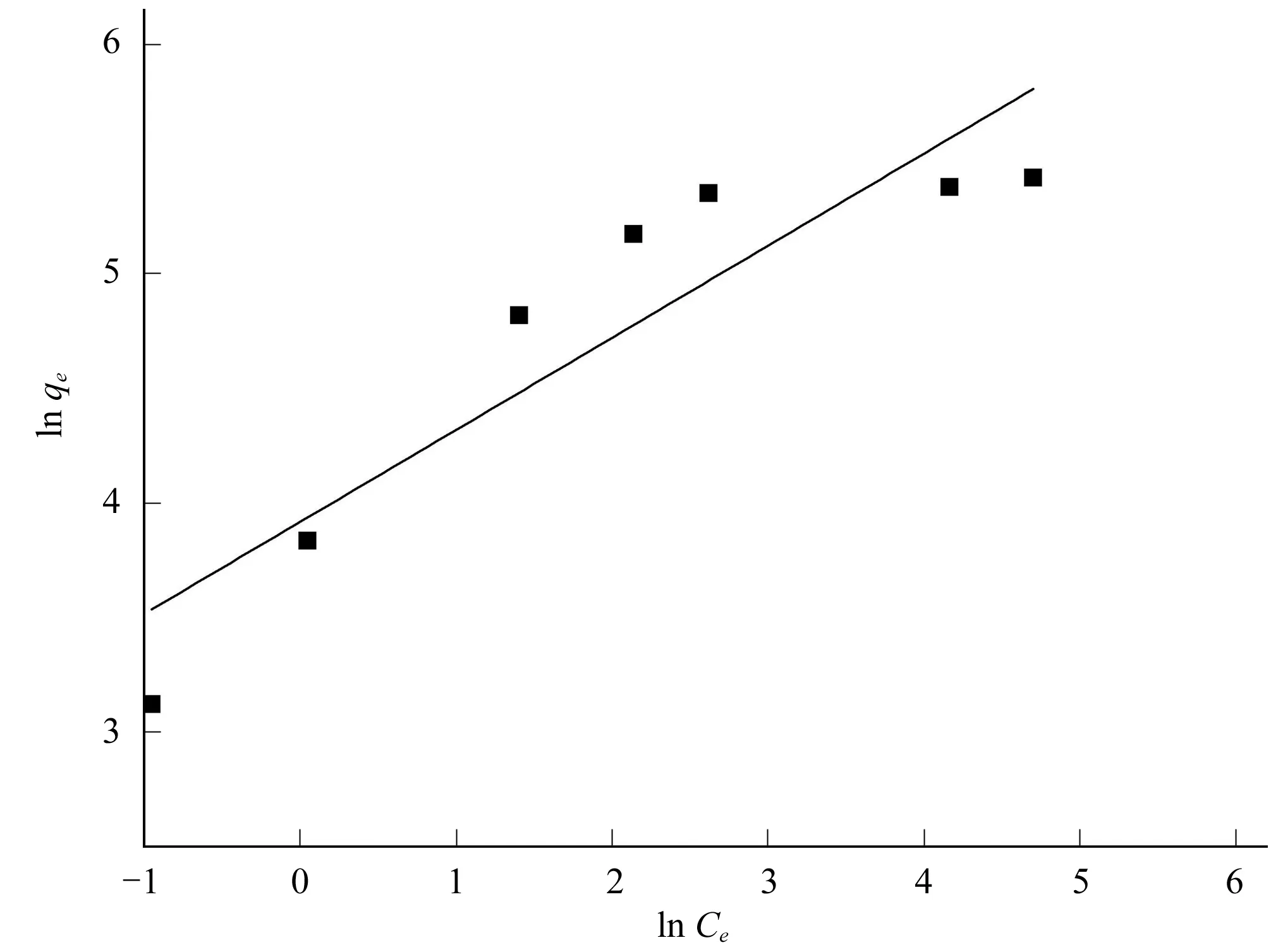
图4 Freundlich 等温线

吸附剂Langmuir模型qmax/(mg·g-1)KL/(L·mg-1)R2Freundlich模型KF/(mg·g-1)nR2Microbacteriumsp.W52500.3070.99950.202.490.837
由表2可以看出, Langmuir模型的相关系数R2=0.999,Freundlich 模型的相关系数R2=0.837。可见吸附剂对Cu2+的吸附行为更符合Langmuir模型,说明该吸附剂对于Cu2+的吸附是单层吸附。通过计算,该吸附剂对Cu2+的理论最大吸附量可以达到250 mg/g。
2.3 吸附动力学
为研究吸附剂对Cu2+的吸附机理,分别利用准一级动力学方程、准二级动力学方程对吸附Cu2+实验数据进行拟合,用各模型线性化后所得方程的相关系数R2来检验拟合结果。
准一级吸附动力学方程:
ln (qe-qt)=lnqe-k1t
(3)
式中:qe为平衡时吸附剂的吸附容量,mg/g;qt为t时刻吸附剂的吸附容量,mg/g;k1为准一级吸附速率常数。
准二级吸附动力学方程:
(4)
式中:k2为准二级吸附速率常数。
分别以ln(qe-qt)对t;t/qt对t分别作图5和图6,对所得数据进行线性回归分析,分别计算两个方程的动力学参数以及回归相关系数,列于表3。
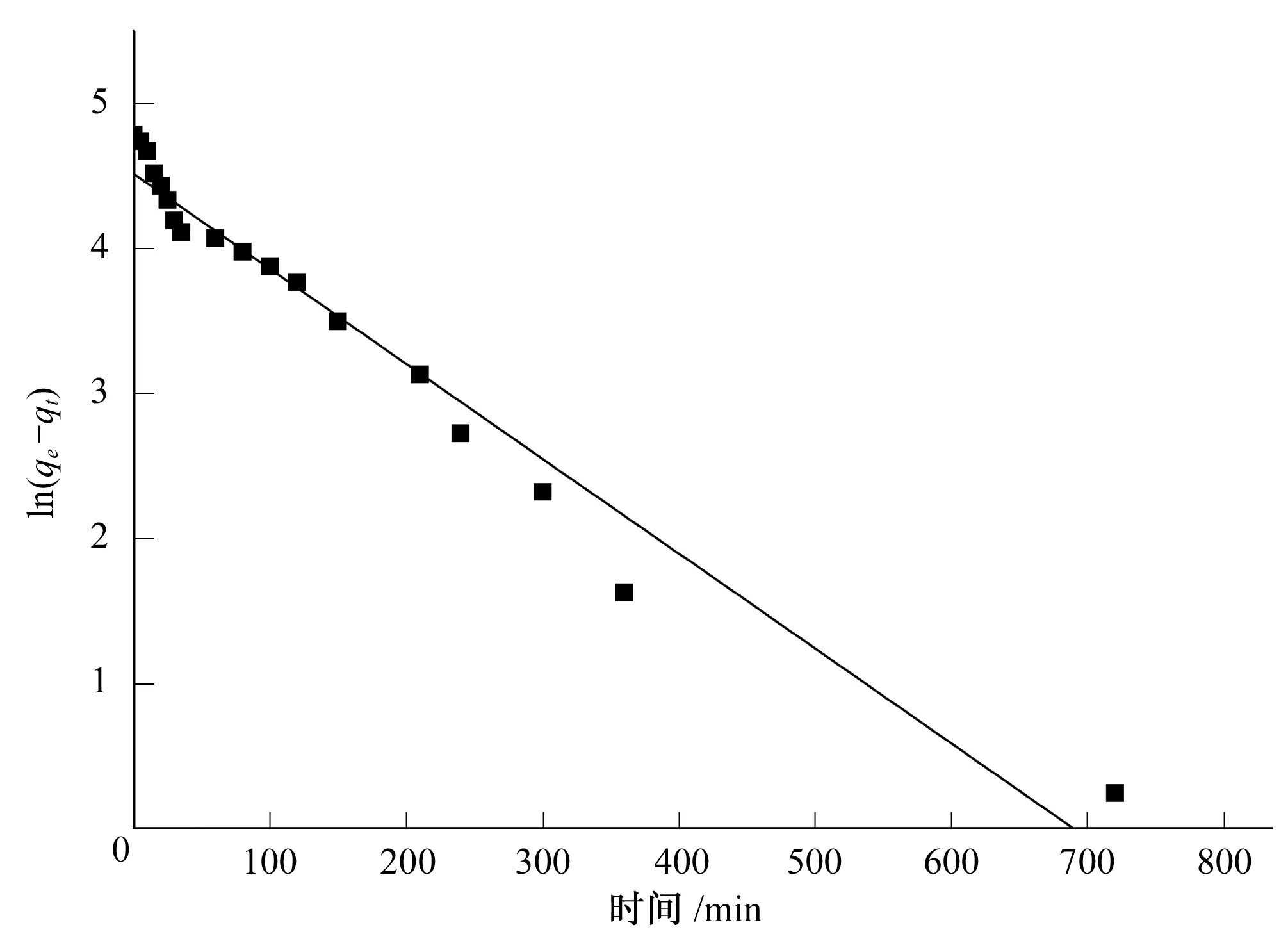
图5 准一级动力学方程
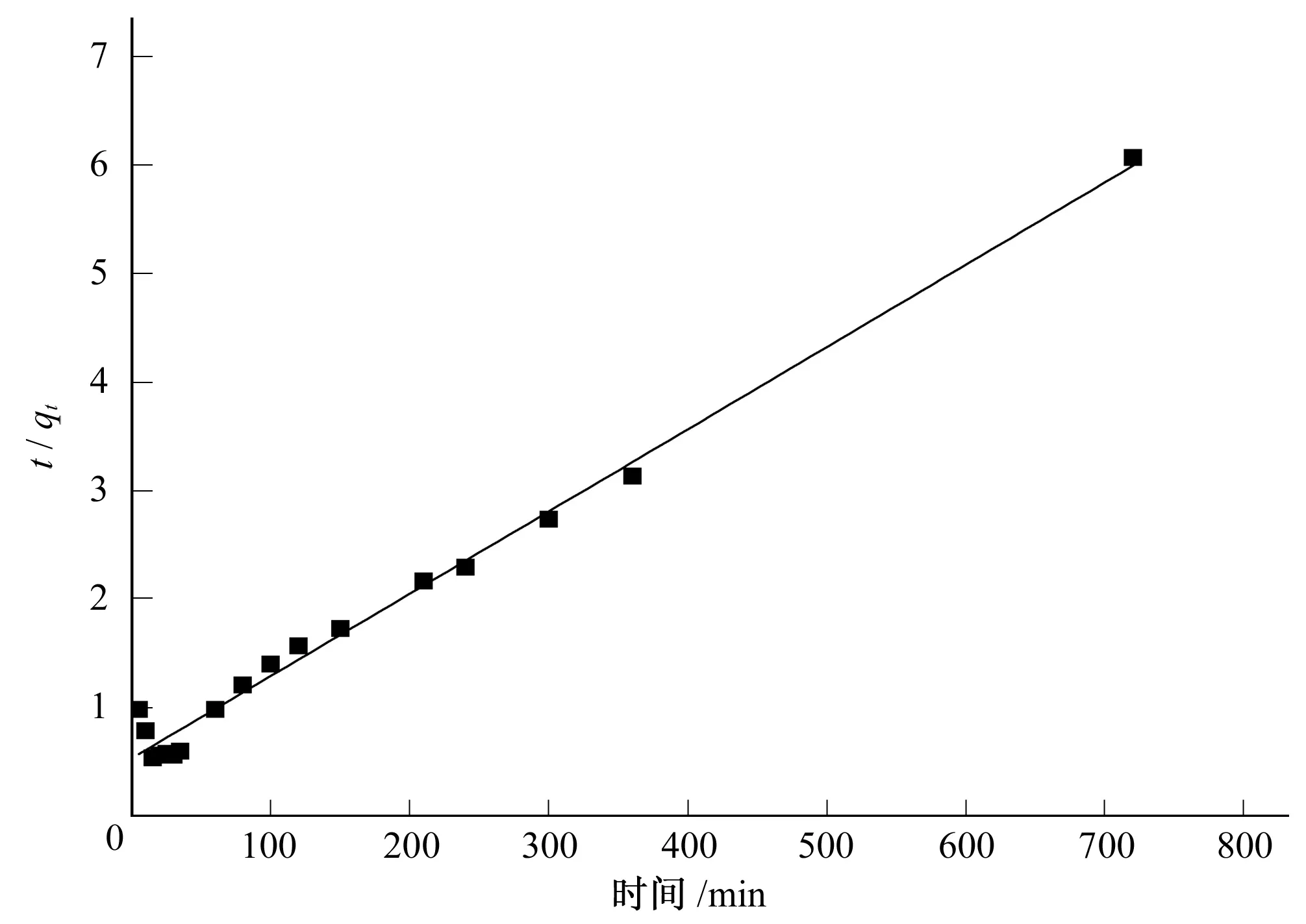
图6 准二级动力学方程
通过表3中的数据可以看出,吸附剂吸附Cu2+的动力学对准二级吸附速率方程有较好的回归效果,用准二级吸附速率方程回归时的相关系数为0.997 1,优于准一级动力学吸附速率方程回归结果0.978 2,说明Cu2+吸附以准二级动力学为最佳模型。用准二级动力学方程计算的平衡吸附量值,计算值与实验值的相差较小,准一级动力学方程的计算值与实验值相差较大,说明吸附剂对Cu2+吸附符合准二级吸附动力学, Cu2+吸附反应过程属于化学吸附反应过程。
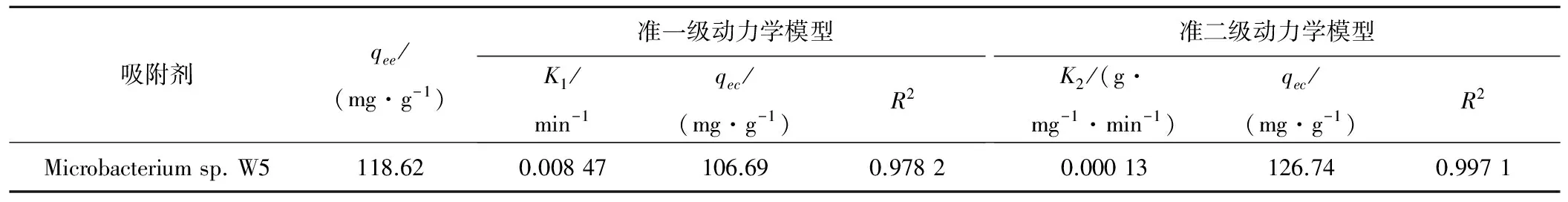
表3 吸附动力学方程参数及相关系数
注:表3中qee表示qe的实验值;qec表示qe的计算值。
2.4 傅里叶变换红外光谱分析
实验采用FTIR红外光谱,通过对吸附剂吸附前后表面官能团变化情况的对比,来确定吸附剂的表面性质以及在Cu2+吸附中起主要作用的官能团。从图7中可以看出,吸附前的吸附剂FTIR光谱表现出大量的频段,显示出其表面的复杂性。3 416 cm-1处的特征峰表明了-OH基团的存在,这显示出在Cu2+的吸附过程中可能有羟基的参与。该频段也有-NH基团重叠[7]。1 042 cm-1处的特征峰是由C-O基团的伸缩振动引起。1 640 cm-1处的特征峰是由羰基(C=O)伸缩振动引起的,可能是仲酰胺。
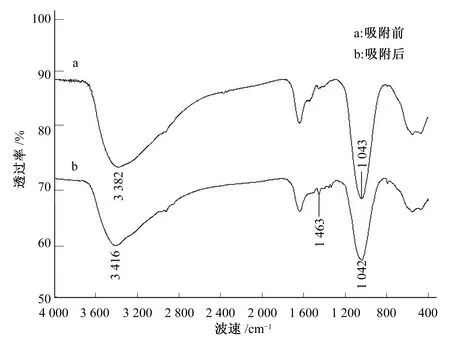
图7 W5吸附Cu2+前后红外光谱图
当吸附剂充分吸附铜离子后,通过光谱可以监测到部分官能团消失或偏移。3 416 cm-1处特征峰偏移至3 382 cm-1,表示Cu2+与羟基的结合,可能会有氨基的参与。1 463 cm-1处的特征峰出现是由于在吸附过程中有羟基的参与。1 042 cm-1至1 043 cm-1处的特征峰偏移是由于C-O的伸缩振动[14]。
3 结 语
(1)硝酸盐还原型厌氧亚铁氧化菌Microbacterium sp. W5在代谢过程中所产生的生物铁氧化物对水中重金属Cu2+离子具有良好的吸附效果。
(2)生物铁氧化物吸附剂对Cu2+的吸附效果与溶液的pH值、溶液初始浓度有关。pH值为5的时候吸附效果最好,pH值偏大或偏小都会降低吸附剂的吸附容量,适当增加溶液初始离子浓度可以提高吸附容量。
(3)吸附剂对Cu2+的吸附符合 Langmuir吸附等温式,属于单分子层吸附,Cu2+的理论最大吸附量可以达到250 mg/g;吸附剂对Cu2+的吸附符合准二级动力学模型,表明以化学吸附为主。
□
[1] Wilson K,Yang H,Seo C W,et al.Select metal adsorption by activated carbon made from peanut shells[J].Biores Technol,2006,97(18):2 266-2 270.
[2] 李芳蓉,何玉凤,王荣民,等.黄原酸化膨润土对Cu2+的吸附性能[J].环境化学,2008,27(6):746-750.
[3] Hao Y M,Chen M,Hu Z B.Effective removal of Cu(Ⅱ) ions from aqueous solution by amino-functionalized magnetic nanoparticles[J].J Hazard Mater,2010, 184( 1/3):392-399.
[4] 陈德翼,郑刘春,党 志,等.Cu2+和Pb2+存在下改性玉米秸秆对Cd2+的吸附[J].环境化学,2008,28( 3):379-382.
[5] 林春香,詹怀宇,刘明华,等.球形纤维素吸附剂对Cu2+的吸附动力学与热力学研究[J].离子交换与吸附,2010,26(3):226-238.
[6] 王 波,贺盛福,张 帆,等.树枝状聚酰胺-胺接枝氧化石墨烯的制备及其对Cu(Ⅱ)的吸附动力学与热力学[J].精细化工,2014,31:998-1 023.
[7] Gulay Bayramoglu,M Yakup Arica,Nezaket Adiguzel.Removal of Ni(II) and Cu(II) ions using native and acid treated Ni-hyperaccumulator plant Alyssum discolor from Turkish serpentine soil [J].Chemosphere,2012,89:302-309.
[8] Maibam Dhanaraj Meitei,Majeti Narasimha Vara Prasad.Adsorption of Cu(II),Mn(II) and Zn(II) by Spirodela polyrhiza (L.)Schleiden: Equilibrium, kinetic and thermodynamic studies [J].Ecological Engineering,2014,71:308-317.
[9] 王弘宇,杨 开,张 倩,等.1株铁基质自养反硝化菌的脱氮特性[J].环境科学, 2014,35(4):1 437-1 442.
[10] Kristina L Straub, Buchholz-Cleven,Berit E E.Enumeration and detection of anaerobic ferrous iron-oxidizing, nitrate-reducing bacteria from diverse european sediments[J].Applied and Environmental Microbiology,1998,64(12):4 846-4 856.
[11] Yongjun Wu,Lijun Zhang,Congli Gao,et al.Adsorption of copper ions and methylene blue in a single and binary system on wheat straw [J].J. Chem. Eng.,2009,54:3 229-3 234.
[12] 李玉飞,高聪丽,豆婵婵,等.麦壳对水溶液中铜离子的动态吸附研究[J].离子交换与吸附,2011,27:103-109.
[13] Yu Liu,YA-Juan-Liu. Biosorption isotherms, kinetics and thermodynamics[J].Separation Purification Technology,2008,61:229-242.
[14] 翁诗甫.傅里叶变换红外光谱分析[M].北京:化学工业出版社,2010.
