心电图左室肥厚患者QRS时限延长的临床意义
2016-03-23匡德俊综述许祥林审校
匡德俊 综述 许祥林 审校
心电图左室肥厚患者QRS时限延长的临床意义
匡德俊综述许祥林审校
【摘要】QRS时限反映整个心室除极的总时间,左心室的结构、形态及功能等异常均可在QRS波群上体现。左心室肥厚患者的解剖重构和电重构可导致左室壁增厚或过度拉伸、左心室内径增大等改变,并可产生不同程度的左心室心肌缺血、左室舒张末期内径增大及左心室射血分数减低等,在心电图上表现为不同程度的QRS时限延长。此外,QRS时限还受左心室肥厚病因病程、电解质紊乱、心率、药物、性别及个体差异等的影响。笔者回顾文献,就QRS时限与心电图左室肥厚的相关性作一综述,旨在为临床决策提供指导。
【关键词】QRS时限;左心室肥厚;心肌重构
【中国图书分类号】R81
作者单位: 563000,贵州省遵义医学院附属医院心电图科
高血压、心脏瓣膜病、先天性心脏病所致左心室肥厚(left ventricle hypertrophy,LVH),以及扩张性心肌病等在心电图上都表现为左室肥厚(劳损)的图形。上述疾病患者的左心室通常存在解剖重构和(或)电重构,甚至伴有不同程度的功能障碍,如不积极治疗易致心力衰竭。QRS波群为整个心室除极的综合波,左心室的结构、形态及功能等异常均可在QRS波群上有所体现(图1)。在心衰患者长期治疗中,长QRS时限是心衰的重要或可靠预测因子,也是其心室收缩功能不全的重要预测因子,可作为病情严重程度及预后不良的评估指标。同时长QRS时限也可用于跟踪评价高血压患者的心衰风险,QRS时限延长是增加慢性心衰患者病死率、心室重构及恶性心律失常的危险因素,与左室重构和更高的病死率密切相关。QRS波群改变可以是肥厚性重塑的早期征兆,笔者参考近年相关文献,旨在阐明QRS时限与心电图左室肥厚的相关性,为临床决策提供指导。
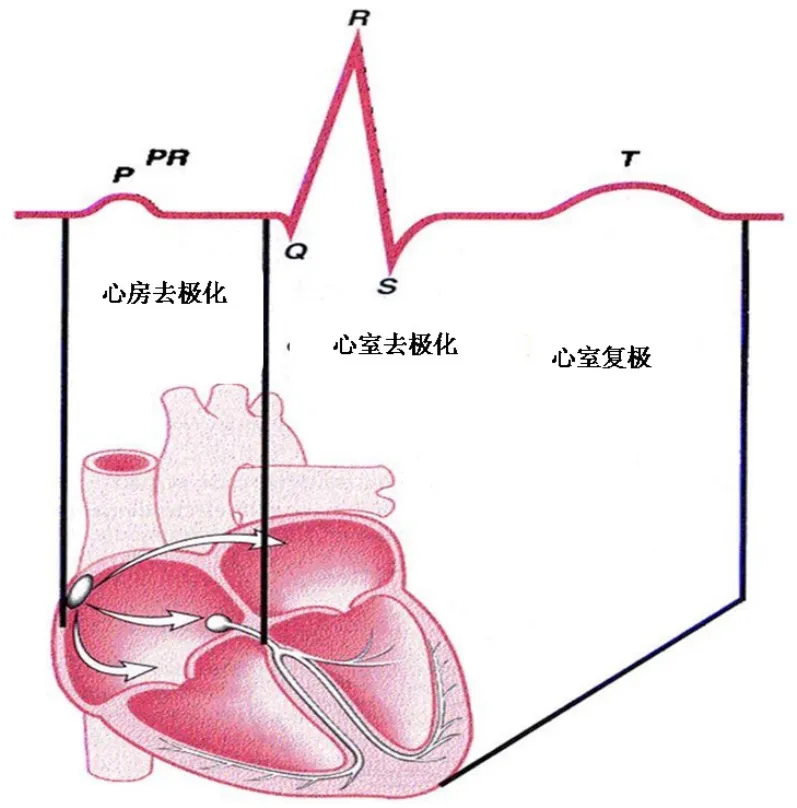
图1 心电图QRS波形图
1 心电图左室肥厚的病因和发病机制
心电图左室肥厚在临床上表现为左心室壁增厚和(或)左心室腔扩大。LVH分为:(1)病理性肥厚,主要包括扩张性心肌病(dilated cardiomyopathy,DCM)、肥厚型心肌病(hypertrophic cardiomyopathy, HCM)、压力负荷过重型和容量负荷过重型LVH等,其中以压力负荷过重型最为常见。心肌肥厚的本质是心肌肥大刺激诱导核内基因异常表达。压力负荷过重型LVH早期先发生左室壁肥厚,心腔不肥厚,反而有变小的趋势,为向心性肥厚。发展到心功能不良时,左心室腔肥厚。容量负荷过重型LVH,左心室回流血量增多,左心室舒张期负荷增重,导致左心室肥厚。(2)病理性LVH通常都存在解剖重构和(或)电重构,并伴有不同程度的功能障碍。解剖重构主要包括心肌细胞肥大、间质纤维增生及血管重构等。肥大的心肌细胞合成蛋白质能力增加,肌小节并联或串联增加,从而引起心室壁增厚、心腔扩大左室重量增加;间质纤维增生指间质成纤维细胞肥大增生及其合成的胶原含量增加。冠状动脉主要表现为外膜纤维化,中层增厚,内膜玻璃样变,内皮细胞增生,冠状动脉舒张功能受限,储备功能下降。就压力负荷过重型和容量负荷过重型LVH而言,病变早期代偿性肥厚致心肌相对灌注不足,心肌重塑导致心肌灌注不足进行性加重,这反过来可能进一步损害其解剖结构和功能,随着病情发展,当肥厚不能代偿增加的心脏应力时左心室腔扩大,易致心脏衰竭发生[1]。左室体积及质量受循环激素和饮食的影响,如胰岛素[2]、甲状腺激素[3]、高果糖饮食[4]等都与LVH发生发展相关。此外,收缩压、年龄、性别、种族、体重指数、血管紧张素-醛固酮刺激及交感神经系统在LVH的发病机制中也起着重要作用。总之,心电图左室肥厚是由于促肥大和抗肥大两种信号之间的平衡被打破而引起的,疾病、环境因素、饮食、遗传因素及神经体液因子与LVH的发生发展密切相关,种族、年龄和性别也可能对其有一定影响。
2 心电图左室肥厚患者QRS时限延长的机制
QRS时限代表整个心室除极的总时间,受心脏性和非心脏性因素影响。前者指心脏结构及功能改变,常见原因及机制与心室内不正常传导有关,如心肌缺血、心肌肥厚、心功能不全和心脏重构患者心肌功能受损致传导能力下降,在心电图上表现为QRS波群增宽,但形态无异常;而非心脏性因素通过影响体表心电图的记录和测量来影响QRS时限,比如外周水肿会缩短QRS时限。肥厚心肌病患者通常存在电重构,导致心室肌除极起始向量发生改变,常出现特异性Q波;电解质紊乱,如高血钾症影响的心室内阻滞在心室肌内各部位都是均匀的,因此可以和左、右束支阻滞或预激综合征等具有特征的QRS波增宽加以区分。
2.1心肌缺血与QRS时限QRS时限延长与心肌组织传导速度较低有关[5],心肌长期缺血缺氧、心肌扩张纤维化等均可减慢心肌组织传导速度,心电图上表现为QRS时限延长。QRS时限延长是心肌缺血的敏感性指标[6],Cantor等[6]研究表明,QRS波时限延长与冠状动脉病变数目、心肌缺血范围及严重程度有关,冠脉近端和主要动脉中段闭塞致QRS时限延长更显著。在病理性肥厚患者中,即使冠状动脉造影正常,往往也提示有心肌缺血的症状和体征[7],这种情况的缺血由冠状动脉微血管功能障碍(coronary microvascular dysfunction,CMD)导致。HCM也以CMD为特征,CMD与局部左室肥厚的程度无关。HCM常为遗传性,与无肌节基因突变的HCM患者相比,严重的微血管功能损害和心肌纤维化更易发生在基因阳性患者中[8]。有研究表明对心肌血流和纤维化的评估可能显著改善HCM患者的风险分级,并对治疗有积极影响[7,9,10]。此外,几乎所有的心肌病都有一定程度的CMD,并可在疾病早期检测,且与疾病的进展和长期预后相关[11]。总之,心肌肥厚、心腔扩大纤维化、冠脉重构及分布稀疏、神经体液改变或运动等都可能会导致或加重心肌缺血,从而导致QRS时限延长。
2.2左心室结构参数与QRS时限QRS时限延长与心肌组织传导速度较低有关[5]。容量负荷过重型LVH、压力负荷过重型LVH患者病程后期或扩张型心肌病患者,左心室心腔扩大使心肌受到一定程度机械牵拉,冲动传导距离也相应延长,解剖重构致心肌损伤和间质纤维化等改变,进而冲动传导速度减慢,使得QRS时限延长。由于不同类型心肌病纤维化或瘢痕导致心肌的纤维取向不同,进而通过影响电兴奋性来不同程度地影响电冲动的传导速度,从而导致QRS时限有较大差异[12]。DCM患者的QRS时限与左心室舒张末期内径(1eft ventricular end diastolic diameter,LVEDD)及左室收缩末内径呈正相关,随着左心室内径的增大而相应延长[13]。在心肌病患者中,相对于左室壁厚度与QRS时限,左室腔扩张与QRS时限的联系更紧密,支持了QRS时限与左室结构参数的一致性[14],表明左室质量、长度、直径、壁厚度和乳头肌位置与QRS时限相关,其中左室长度、直径和质量的增加与QRS时限呈正相关。心电图QRS波群时限≥120 ms组患者的LVEDD值明显高于心电图QRS波群时限<120 ms组患者。影响QRS时限的其他解剖学因素还包括纤维定向、左心室几何形状、浦肯野纤维网络复杂性和左心室壁形状。此外,性别对心室结构参数也有一定影响,男人通常比女人有更大的心室和更长的QRS时限[15]。
2.3左心功能与QRS时限左心室射血分数(1eft ventricular ejection fraction,LVEF)是心衰患者分类的重要指标,各种病因的心电图左室肥厚都可随着病情的发展演变成心衰。心衰患者心脏负荷过重时,会引起心肌细胞病理性肥大和基质过度纤维化的心肌重构反应, 导致心脏机械活动的不同步, 心脏电传导延迟,心电图表现为QRS时限延长[16]。发展为心衰的患者,QRS时限主要与左室收缩功能有关,与LVEF值呈正相关[17]。 QRS时限延长是左室功能不全的专属指标,QRS时限<84 ms可以排除左心室收缩功能不全,QRS时限延长(>120 ms)与更严重的左心室收缩功能障碍相关[18]。
2.4左室肥厚病因及病程与QRS时限肌间质和实质成分的失调、增生导致心肌结构异常,这是LVH的病理基础。高血压性LVH时,除有心肌细胞的肥大外,还常伴有心肌间质细胞增生及胶原纤维异常堆积 ,以及胶原不成比例地过度积聚,这会引起心肌纤维化、心肌肥厚、僵硬度增加及心功能异常等。当左室肥厚向心衰演变时,过重的心脏负荷会引起心脏增大、心肌纤维化及心肌重构等改变,进而导致心室浦肯野纤维和心室肌电传导能力下降。虽然细胞增大可使细胞间连接的传导速度加快,但有限的细胞增大导致的传导速度增快不能弥补心肌肥厚及心衰导致的QRS时限延长;离心性左室肥大也表现出显著的左心室腔扩大,心肌肥厚患者病情进展恶化最终也可导致左心室腔明显扩大及心力衰竭,以上症状均在心电图上表现为QRS时限延长。在一些早期LVH患者,虽然心肌细胞体积增大使传导路程延长,进而增加了QRS时限,但是由于细胞增大使细胞间连接的传导速度加快,可以弥补前者导致的QRS时限延长。当左室肥厚进展为心衰时,QRS时限则与左室内径密切相关。心电图诊断左室肥厚的敏感性和特异性相对较低,其敏感性因诊断标准和左室肥厚的病因不同而异。不同病因的心电图左室肥厚与QRS时限的相关性也不同。所有心肌病,包括DCM和HCM,都有传输方式改变、常染色体显性遗传等共同的要素,具有遗传学异常的LVH患者心律失常和猝死的危险性增加,并有向心衰及其并发症发展的倾向等[19]。不同病因导致的HCM和DCM也存在不同类型和程度的心肌重构和电重构,从而导致QRS时限的差异。
2.5其他QRS波群变化是解剖重构和电重构整合的表现[20]。QRS时限的长短是由参与心脏除极的离子电流确定的。任何改变心肌细胞和心肌细胞间电传导性的因素,除了前面提到的心肌细胞增大、左室腔扩大及纤维化外,高血钾及可利用钠通道变少都可导致QRS波群增宽。HCM或DCM常受遗传因素影响,基因变异可以导致心肌钠通道的改变,心室除极缓慢致QRS时限延长。高血钾症时细胞外K+浓度增高,细胞内外K+浓度梯度减少而致静息期膜电位减少,因而0相上升速度减慢,幅度减低,出现QRS增宽,心室内阻滞。随着细胞外K+浓度的升高,动作电位0相振幅逐渐降低,上升速度越来越慢,心室肌的传导障碍逐渐明显,QRS逐渐增宽。虽然Na+内流是形成心肌细胞动作电位除极期的主要跨膜离子流,但多数有关实验证明在心肌肥厚时Na+流无明显改变。此外,不同药物对QRS时限有不同影响,左西孟旦使QRS时限缩短,而多巴酚丁胺对其无明显作用[21]。药物通过阻断Na+电流来减缓心脏动作电位传导和延长QRS波时限,如静息状态,奎尼丁和氟卡尼诱导QRS时限延长,而美西律却无此效果[22]。Sällström等[23]研究表明氟卡尼可使狗的QRS时限延长,且较高心率使药物诱导的QRS时限延长更明显。此外,心电图电压衰减会导致相应QRS时限缩短,如水肿患者[24],这可能完全或部分抵消了其他因素导致的QRS时限的延长。
3 心电图左室肥厚患者QRS时限延长的临床意义
正常成年人左室壁厚8~11 mm,是右心室壁厚度的3倍。负荷过重型LVH,心室除极时间延长,QRS波群增宽。单纯LVH,QRS时限仅轻度延长,可由60 ms延长到80 ms。重度LVH时,QRS时限可明显延长至100 ms,一般不超过110 ms。左心室肥厚以后,牵拉左束支传导系统,造成左束支及其分支传导延迟或阻滞。这常发生于左心室显著肥厚的患者,QRS时限超出110 ms者,提示LVH合并有束支阻滞或不定型室内阻滞。心肌的电特性改变在心室肥大发展的早期阶段已经存在[25],因此,左心室质量和大小正常的患者,电特性的改变可影响QRS波群,QRS波群改变可以是肥厚性重塑的早期征兆。
心电图左室肥厚患者早期可能存在无任何心电图异常的情况,但随着病情的进展,不同程度的心肌缺血、左室内径增大和纤维化、左心功能降低、电解质紊乱都会通过不同程度的QRS时限延长来体现。各种病因的心电图左室肥厚都有向心衰发展的趋势,而左心室射血分数是公认的判断心衰患者预后及猝死率的指标,而QRS时限与LVEF值呈负相关,QRS波群时限能较好地反映患者的LVEF。QRS时限延长与功能障碍及心衰的发展相关一致;QRS 波时限延长是心衰患者心室收缩功能不全的重要预测因子;在长期治疗中,长QRS时限是新的心衰重要或牢固的预测因子;QRS时限可以用来跟踪评价高血压患者心衰的风险。在发展为心衰的慢性患者中,QRS时限延长是病死率增加、心室重构及心率变异的危险因素,QRS时限>150 ms比QRS时限≤150 ms的患者有更大的心脏自主神经功能干扰,更明显的左室重构和更高的病死率[26]。在一项对双心室起搏心脏衰竭患者的研究中发现,QRS时限与急性血流动力学改变呈线性相关,双心室起搏改善了QRS时限狭窄的患者无血流动力学,提高了在心脏衰竭患者中的潜在临床效益[27]。
4 小 结
临床上各种原因导致的左心室壁肥厚和(或)左室腔扩大都在心电图上表现为左室肥厚(劳损)。病因不同、不同类型或程度不同的LVH或左室腔扩大可能存在心肌缺血、左室内径增大、左心功能降低、间质纤维化及电解质紊乱等其中的一项或多项异常,导致冲动在心肌内的传导速度减慢或传导路程增加,从而引起QRS时限不同程度地改变;此外,QRS时限还受到个体差异的影响。QRS时限延长可以是肥厚性重塑的早期征兆,可以表现左心功能障碍或演变为心衰及严重的程度。但对病因不同、类型不同或不同程度的心电图左室肥厚意义不一样。为使QRS时限这一指标能更好地服务于临床,在分析病情时一定要全面详细,正确地解释其延长的意义。
【参考文献】
[ 1 ]Cuspidi C, Sala C, Negri F, et al. Prevalence of leftventricular hypertrophy in hypertension: an updated review of echocardiographic studies [J]. J Hum Hypertens, 2012, 26(6): 343-349.
[ 2 ]Nkum B C, Micah F B, Ankrah T C, et al. Left ventricular hypertrophy and insulin resistance in adults from an urban community in The Gambia: cross-sectional study [J]. PLoS One, 2014, 9(4): 1-7.
[ 3 ]Caroline L, Gabriela D, Camila M, et al. Non-genomic ERK1/2 activation and integrin αvβ3 contribute to cardiac hypertrophy induced by thyroid hormone [J]. FASEB J, 2015, 29(1): 1043-1044.
[ 4 ]Bouchard-Thomassin A A, Lachance D, Drolet M C, et al. A high-fructose diet worsens eccentric left ventricular hypertrophy in experimental volume overload [J]. Am J Physiol Heart Circ Physiol, 2011, 300(1): H125-H134.
[ 5 ]Stewart R A, Young A A, Anderson C, et al. Relationship between QRS duration and left ventricular mass and volume in patients at high cardiovascular risk [J]. Heart, 2011, 97(21): 1766-1770.
[ 6 ]Cantor A, Yosefy C, Potekhin M, et al. The value of changes in QRS width and in ST-T segment during exercise test in hypertrophic cardiomyopathy for identification of associated coronary artery disease [J]. Int J Cardiol, 2006, 112(1): 99-104.
[ 7 ]Spoladore R, Fisicaro A, Faccini A, et al. Coronary microvascular dysfunction in primary cardiomyopathies [J]. Heart, 2014, 100(10): 806-813.
[ 8 ]Olivotto I, Girolami F M, Sciagrà R, et al. Microvascular function is selectively impaired in hypertrophic cardiomyopathy patients with sarcomere myofilament genemutations [J]. J Am Coll Cardiol, 2011, 58(8): 839-848.
[ 9 ]Maron M S, Olivotto I, Maron B J, et al. The case for myocardial ischemia in hypertrophic cardiomyopathy [J]. J Am Coll Cardiol, 2009, 54(90): 866-875.
[10]Aquaro G D, Todiere G, Barison A, et al. Correspondence: progression of myocardial fibrosis in hypertrophic cardiomyopathy [J]. Heart, 2015, 101(19): 1602.
[11]Caliskan M, Caliskan Z, Gullu H, et al. Increased morning blood pressure surge and coronary microvascular dysfunction in patient with early stage hypertension [J]. J Am Soc Hypertens, 2014, 8(9): 652-659.
[12]Henriquez C S. A brief history of tissue models for cardiac electrophysiology [J]. IEEE Trans Biomed Eng, 2014, 61 (5): 1457-1465.
[13]栗全玲. 扩张型心肌病的心电图改变及QRS时限与左室大小相关性分析[J]. 中西医结合心脑血管病杂志, 2013, 11(5): 629-630.
[14]Chan D D, Wu K C, Loring Z, et al. Comparison of the relation between left ventricular anatomy and QRS duration in patients with cardiomyopathy with versus without left bundle branch block [J]. Am J Cardiol, 2014, 113(10): 1717-1722.
[15]Shenkman H J, Pampati V, Khandelwal A K, et al. Congestive heart failure and QRS duration [J]. Chest, 2002, 122(2): 528-534.
[16]Recke S H. Left ventricular function-concluction impairment rigrdlected by the ECC in chronic aortic regurgitation [J]. Wien Klin Wochenschr, 2011, 123(15-16): 502-507.
[17]Deepak K G, Amil M S, Pentti M R, et al. Abstract 17411: the relationships between QRS duration and morphology, cardiac structure and function, and incident heart failure in the atherosclerosis risk in communities study [J]. Circulation, 2013, 128(22): A17411.
[18]Sandhu R, Bahler R C. Prevalence of QRS prolongation in a community hospital cohort of patients with heart failure and its relation to left ventricular systolic dysfunction [J]. Am J Cardiol, 2004, 93(2): 244-246.
[19]Andrew R H, Arash Y, Houman A. Inherited cardiomyopathies [J]. Med, 2014, 42(10): 584-590.
[20]Bacharova L, Szathmary V, Kovalcik M, et al. Effect of changes in left ventricular anatomy and conduction velocity on the QRS voltage and morphology in left ventricular hypertrophy: a model study [J]. J Electrocardiol, 2010, 43 (3): 200-208.
[21]Yontar O C, Yilmaz M B, Yalta K, et al. Acute effects of levosimendan and dobutamine on QRS duration in patients with heart failure [J]. Arq Bras Cardiol, 2010, 95(6): 738-742.
[22]Cros C, Skinner M, Moors J, et al. Detecting drug-induced prolongation of the QRS complex: new insights for cardiac safety assessment [J]. Toxicol Appl Pharmacol, 2012, 265 (2): 200-208.
[23]Sällström J, Al-Saffar A, Pehrson R. Pharmacokineticpharmacodynamic modeling of QRS-prolongation by flecainide: heart rate-dependent effects during sinus rhythm in conscious telemetered dogs [J]. J Pharmacol Toxicol Methods, 2014, 69(1): 24-29.
[24]Madias J E, Macfarlane P W. Artificial attenuation of ECG voltage produces shortening of the corresponding QRS duration: clinical implications for patients with edema [J]. Pacing Clin Electrophysiol, 2005, 28(10): 1060-1065.
[25]Luis R, Ljuba B. Electrical remodeling in left ventricular hypertrophy-is there a unifying hypothesis for the variety of electrocardiographic criteria for the diagnosis of left ventricular hypertrophy? [J]. J Electrocardiol, 2012, 45 (5): 494-497.
[26]Kearney M T, Zaman A, Eckberg D L, et al. Cardiac size, autonomic function, and 5-year follow-up of chronic heart failure patients with severe prolongation of ventricular activation [J]. J Card Fail, 2003, 9(2): 93-99.
[27]Ploux S, Whinnett Z, Lumens J, et al. Acute hemodynamic response to biventricular pacing in heart failure patients with narrow, moderately, and severely prolonged QRS duration [J]. Heart Rhythm, 2012, 9(8): 1247-1250.
(2015-12-04 收稿2016-01-18修回)
(责任编辑潘奕婷)
• 临床医学经验交流| CLINICALEXPERIENCE •
Clinical significance of QRS prolongation in patients with left ventricular hypertrophy on ECG
KUANG Dejun and XU Xianglin. Department of Electrocardiogram, Hospital Affiliated to Zunyi Medical College, Zunyi 563000, China
【Abstract】The QRS duration on electrocardiogram (ECG) reflects time of ventricular depolarization, and abnormality of structure, morphology and function of left ventricle which can all be showed on the QRS wave group. The anatomic remodeling and electrical remodeling in patients with left ventricular hypertrophy could lead to changes, such as left ventricular wall thickening, overstretch or increase the diameter of left ventricular, etc, and this may result in left ventricular myocardial ischemia, the increase of left ventricular enddiastolic diameter or the decrease of left ventricular ejection fraction in different degree. These changes could be shown by the difference in QRS prolongation on ECG. In addition, the QRS duration was also influenced by pathogenesis, electrolyte disorders, heart rate, drugs, gender and individual differences, etc. The author reviewed literature, summerized relationship between QRS prolongation and the factors above, and its clinical significance, in order to provide guidance on clinical decision-making.
【Keywords】QRS duration; left ventricle hypertrophy; myocardial remodeling
Corresponding author:XU Xianglin, E-mail: xuxianglinxxl@126.com
通讯作者:许祥林,E-mail: xuxianglinxxl@126.com
作者简介:匡德俊,硕士研究生在读,E-mail:1194908688@qq.com
DOI:10.13919/j.issn.2095-6274.2016.02.014
