中药益艾康与HAART药物依非韦伦片相互作用研究*
2016-03-20孟祥乐秦会珍李伟霞胡宇才唐进法李学林徐智儒刘中秋郭会军徐立然
孟祥乐,秦会珍,马 静,李伟霞,胡宇才,鲁 静,唐进法,李学林,徐智儒,肖 峰,刘中秋,郭会军,徐立然**
(1. 河南中医学院第一附属医院 郑州 450000;2. 河南大学药学院 开封 475004;3. 广州中医药大学国际转化医学研究所 广州 510006;4. 上海医药工业研究院药理室 上海 200437)
中药益艾康与HAART药物依非韦伦片相互作用研究*
孟祥乐1,2,3,秦会珍2,马 静1,李伟霞1,胡宇才1,鲁 静1,唐进法1,李学林1,徐智儒4,肖 峰4,刘中秋3,郭会军1,徐立然1**
(1. 河南中医学院第一附属医院 郑州 450000;2. 河南大学药学院 开封 475004;3. 广州中医药大学国际转化医学研究所 广州 510006;4. 上海医药工业研究院药理室 上海 200437)
目的:探讨益艾康胶囊与HAART药物依非韦伦的相互作用。 方法:实验大鼠分别灌胃给予依非韦伦和依非韦伦+益艾康胶囊,并通过LC/MS/MS测定两种给药方式后血浆中依非韦伦浓度,随后使用Phoenix WinNonlin 6.1软件计算药动学参数。结果:符合方法学考察要求:血药浓度在5-500 ng·mL-1范围内线性关系良好,日内、日间精密度RSD均小于10.0%、提取回收率97.0%-104.0%、稳定性较好、受基质影响较小。由两组药代动力学主要参数得知AUC(0-t)、AUC(0-∞)、MRT(0-t)和MRT(0-∞)均显著降低(P<0.05),其它参数无统计学意义(P>0.05)。结论:中药益艾康可能对依非韦伦在大鼠体内药代动力学行为有一定的影响,两者在临床上是否存在相互作用需要进一步研究。
益艾康 HAART药物 依非韦伦 药代动力学
艾滋病(Acquired Immunodeficiency Syndrome,AIDS)是人类免疫缺陷病毒(Human Immunedeficency Virus,HIV)引起的严重危害人类健康的传染性疾病,又被称为“获得性免疫缺陷综合征”。在高效逆转录病毒疗法(Highly Active Antiretroviral Therapy,HAART,又称“鸡尾酒疗法”)发明之后,经过积极的药物治疗,HIV感染已经成为一种可控的慢性疾病[1]。HAART治疗虽然取得了突破性进展,但也存在缺陷:①对HIV/AIDS免疫功能重建有局限性:仅有部分病人可以做到免疫功能重建[2];②不能根除病毒,要求患者长期服用[3],严重的不良反应会降低患者治疗的依从性。大量研究表明,中医药在调节机体免疫功能、减轻临床症状[4]、预防及治疗艾滋病方面有较大潜力,是寻找安全、有效、廉价治疗艾滋病药物的有效途径[5]。河南省中医药研究院研制的“益艾康胶囊”由人参、黄芪、黄芩等药物组成[6],具有健脾补胃、益气养血等功效,能增加机体免疫功能,可提高艾滋病病人CD4+T淋巴细胞数量,有利于艾滋病患者的免疫重建[7]。临床已有病人同时服用HAART药物及益艾康胶囊取得了显著疗效[8]。但是两者之间是否存在相互作用未见研究报道,特别是益艾康胶囊对HAART药物代谢的影响,需要进一步的研究。依非韦伦是一种选择性非核苷类逆转录酶抑制剂,是用于治疗HIV感染的一线药物。本研究旨在探讨益艾康与依非韦伦合用后,益艾康对依非韦伦在大鼠体内的药动学参数是否有影响,可为后续的临床研究提供参考。
1 材料与方法
1.1 材料
1.1.1 仪器
Ultimate 3000液相色谱仪,包括Ultimate 3000型三元输液泵、Ultimate3000型柱温箱、Ultimate 3000型自动进样器和Ultimate3000型真空脱气机(美国戴安公司);串联4000 Q-Trap型质谱仪(美国AB公司);CP225D型电子天平(德国Sartorius公司);5415R型冷冻离心机(德国Eppendorf公司);XW-80A型旋涡混合器(上海医大仪器厂)。
1.1.2 药品与试剂
依非韦伦(Efavirenz,EFV)(美国Sigma公司,批号:112m4701v);盐酸苯海拉明(Diphenhydramine Hydrochloride) (美国Sigma公司,批号:A0286925);益艾康胶囊(YAK)购自河南省中医药研究院,批号:20140321;依非韦伦片(德国Merck公司,批号:T3622);甲醇(色谱纯,德国Merck公司);甲酸铵(色谱纯,美国Sigma公司)。
1.1.3 动物
雄性SD大鼠,体重约200 g,由上海西普尔-必凯实验动物有限公司提供,合格证号:SCXK(沪)2013-0016,动物使用许可证号:SYXK(沪)2014-0018。
1.2 方法
1.2.1 色谱条件和质谱条件
色谱柱:Kromasil®十八烷基硅烷键合硅胶(150 mm × 2.1 mm,3 μm);流动相:A. 10 mmol·L-1甲酸铵水溶液,B. 甲醇;梯度洗脱见表1;进样体积:5 μL;流速:0.3 mL·min-1;柱温:25℃。
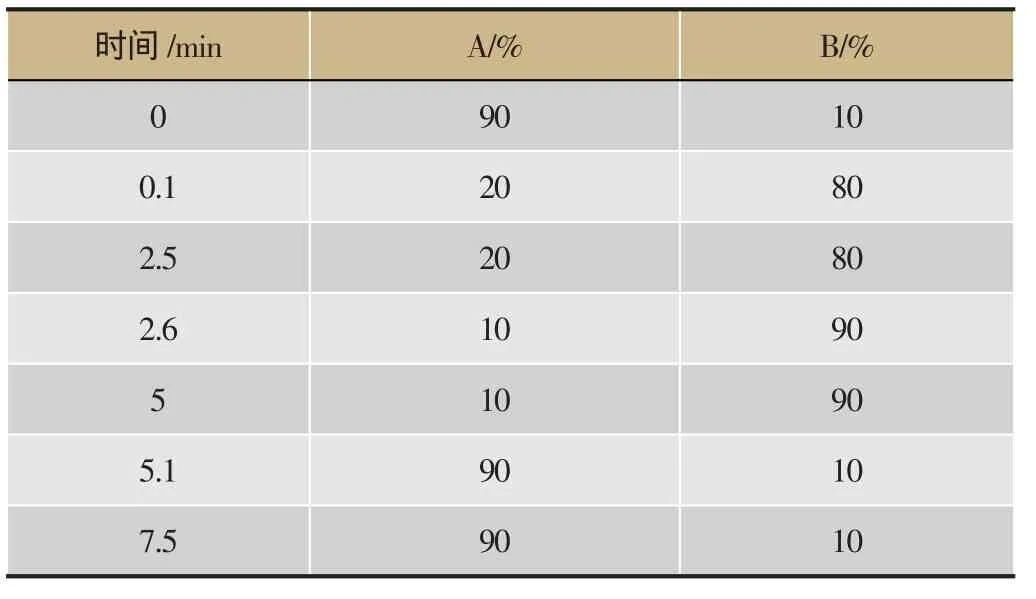
表1 梯度洗脱程序

表2 质谱监测离子对及相关参数
采用API4000 Q-TRAP三重四级杆质谱,TurboIonSprayTM以正离子模式检测依非韦伦及内标苯海拉明。离子源:ESI源;检测方式:正离子检测;扫描方式:多反应监测(MRM)方式,选择监测的离子反应分别为m/z 316.6→ 244.0(依非韦伦);m/ z 256.1 → 167.1(苯海拉明);毛细管电压为3 kV,锥孔电压30 V;离子源温度:150 ℃,去溶剂气温度:550℃;数据处理采用美国AB公司Analyst Version 1.5.1软件,质谱监测离子对及相关参数见表2。
1.2.2 对照品溶液和质量控制样品的制备
(1)制备系列标准溶液
分别取样品和内标适量,精密称定,用适量甲醇溶解,再用50%甲醇水溶液稀释至刻度,配成1.0 mg·mL-1的储备液,于4℃冷冻保存。分别取储备液适量混合,并用50%甲醇水溶液稀释,分别配制成含EFV的浓度为0、0.1、0.2、1、2、4、10 μg·mL-1的系列标准溶液。
(2)内标储备液
取苯海拉明适量,精密称定,加甲醇溶解,再用50%甲醇水溶液稀释至刻度,配制成1.0 mg·mL-1的标准溶液作为内标溶液,于4℃保存,临用前用浓度50%甲醇水溶液稀释至为0.1 μg·mL-1。
(3)系列血浆质控样品的制备
分别吸取上述标准溶液2.5 μL于50 μL空白血浆中,每份样品中加入内标溶液5 μL,配制质量浓度为0、5、10、50、100、200、500 ng·mL-1系列血浆样品,同法配制8、40、400 ng·mL-1的血浆样品作为质控样品。
1.3 药液的准备
取依非韦伦片剂去掉包衣,研钵中研碎,研磨使之成粉末状,称取适量加0.5% CMC-Na溶液配置浓度为6 mg·mL-1的混悬液,灌胃容积为5 mL·kg-1。
取益艾康胶囊内粉末适量,精密称定,加0.5%CMC-Na溶液配置浓度为50 mg·mL-1的混悬液,给药方法:灌胃给药,灌胃容积:5 mL·kg-1。
1.4 血浆样品的采集和处理
SD雄性大鼠6只,禁食12 h后按照30 mg·kg-1剂量灌胃给予EFV 0.5% CMC-Na混悬液,并于给药后0.083、0.25、0.5、1、2、3、4、5、6、8、12及24 h眼眶静脉丛取血,分离血浆,并于-40℃保存。从第2天开始,每天7∶30灌胃给药EFV 0.5% CMC-Na混悬液,并灌胃给予益艾康0.5% CMC-Na混悬液,剂量为每次250 mg·kg-1,每天3次(早8∶30,中12∶30,晚20∶30),连续给药至第6天,并于第7天禁食不禁水饲养12 h后再次灌胃给予EFV 0.5% CMC-Na混悬液,给药后0.083、0.25、0.5、1、2、3、4、5、6、8、12及24 h眼眶静脉丛取血,分离血浆,并于-40℃保存。
取50 μL血浆,加入2.5 μL Meth-H2O、5 μL内标溶液(100 ng·mL-1苯海拉明),用150 μL甲醇沉淀蛋白,13 000 rpm×5 min离心。取上层有机相,0.22 μm微孔滤膜过滤,5 μL进样分析。
1.5 数据处理
采用Phoenix WinNonlin 6.1软件对血药浓度(c)与时间(t)数据进行c-t曲线拟合,进行药动学参数计算,采用GraphPad Priam5进行药时曲线图绘制。
2 结果
2.1 分析方法验证
2.1.1 专属性
空白血浆、空白血浆加EFV对照品和内标苯海拉明标准溶液及大鼠灌胃给药EFV血浆色谱图见图1。由图1可知,该分析方法不受内源性物质干扰,本方法具有较好的专属性。
2.1.2 线性范围及检测限
考察依非韦伦在大鼠血浆中的线性范围,分别吸取上述1.2.2中系列血浆质控样品,按1.2项下方法进行测定,以依非韦伦血浆浓度为横坐标,依非韦伦与内标苯海拉明峰面积的比值为纵坐标,进行线性回归分析,大鼠血浆中依非韦伦在5-500 ng·mL-1浓度范围内标准曲线方程为:Y=1.21×10-4X +7.36×10-5,相关系数为r=0.999 4(线性方程及线性范围如表3)。结果表明,血浆中EFV在5-500 ng·mL-1浓度范围线性关系良好,血浆EFV最低检测限为2 ng·mL-1(S/ N≥3)。
2.1.3 血浆药物回收率及精密度考察
按上述质控样品制备方法制备低、中、高浓度(8、40、400 ng·mL-1)血浆质控样品,每个浓度5批样品,在不同日期连续制备并测定3个分析批,并按血浆样品处理项下方法进行处理后进样分析,由标准曲线反算实测浓度,计算日内、日间精密度并且与实测浓度相比计算回收率,不同浓度质控样品回收率及精密度结果见表4。由表4可知,该方法日内及日间RSD均低于10.0%,方法回收率为97.0%-104.0%,结果表明该试验条件下EFV在血浆中回收率符合要求,说明该方法的精密度良好。
2.1.4 基质效应
用来自1份不同个体的空白血浆同法萃取后的上清配制不同浓度溶液各1份,浓度分别为8、40、400 ng·mL-1,进样分析,记录峰面积A1;按同样的方法配制相同浓度低、中、高三种对照品溶液进样分析,记录峰面积A2,以相同浓度平均峰面积比值(A1/ A2)×100%计算不同浓度下基质效应,EFV低、中、高三个浓度下基质效应见表4。结果表明,该化合物受血浆中基质影响较小,低、中、高浓度受基质影响较为一致。
2.1.5 稳定性考察
按上述方法制成含药物从低到高不同浓度的样品,每个浓度平行制备3份,在室温放置8 h,另2批置-20℃冷冻保存,其中一批反复冻融3次,另一批冷冻保存1周。在上述条件下由低到高不同浓度的血浆样品浓度RSD均低于10.0%,说明该种药物在上述条件下稳定性较好,符合生物样品含量测定要求。
2.2 药时曲线及药动学参数
大鼠单独灌胃给药EFV及合用益艾康0.5%CMC-Na混悬液血药浓度-时间曲线采用Graph Pad Priam 5进行绘制,如图2;采用Phoenix WinNonlin 6.1软件对血药浓度(c)与时间(t)数据进行c-t曲线拟合,并进行药动学参数计算。药动学参数如表5。
与EFV单独给药比较,EFV+YAK联合给药大鼠血浆中依非韦伦的主要动力学参数AUC(0-t)、AUC(0-∞)、MRT(0-t)和MRT(0-∞)均显著降低(P<0.05),其它参数无统计学意义(P>0.05)。

表3 线性方程及线性范围(n=3)

表4 回收率、精密度及基质效应试验结果

图1 血浆样品典型提取离子流色谱图
3 讨论
本研究建立了益艾康胶囊对依非韦伦在大鼠体内药代动力学影响的HPLC-MS测定方法,血浆中内源性物质不干扰样品的测定,依非韦伦血药浓度在5-500 ng·mL-1范围内线性关系良好;低、中、高三个浓度的日内和日间精密度RSD%均小于10.0%;在此条件下依非韦伦稳定性较好;提取回收率范围为97.0%-104.0%;依非韦伦受低、中、高三个浓度下基质的影响较小。EFV单独使用时血浆药动学参数为:Cmax=249.167±114.2 μg·L-1、MRT(0-t)=5.8±0.8 h和MRT(0-∞)=6.5±1.5 h,EFV+YAK联用时血浆药动学参数为∶ Cmax=214.5±100.5 μg·L-1、 MRT(0-t)=4.4±0.5h和MRT(0-∞)=4.9±0.5 h。比较得知,AUC(0-t)、AUC(0-∞)、MRT(0-t)和MRT(0-∞)均显著降低(P<0.05),其它参数无统计学意义(P>0.05)。此次考察结果符合生物样品分析要求。结果表明,益艾康胶囊可能影响依非韦伦在大鼠体内药代动力学特性,二者在临床上是否存在相互作用需要进一步研究。
中西医结合是解决人类面临重大疑难疾病的有效途径[9]。在中国古代中医典籍上对艾滋病虽未有记载,但分析其特点可知,其病因为病毒的侵袭[10,11],导致人体免疫功能损伤在先,多数正气已衰,抗邪无力,六淫外邪更易侵入[12],其根本治疗为扶正固本、调理虚赢、清疫败毒[6,13-15]。中西医结合治疗法是目前临床上防治艾滋病的重要手段,在常规抗病毒治疗的基础上联合中医辨证用药治疗艾滋病的疗效优于常规抗病毒治疗[16],在一定程度上可增加患者治疗的依从性[15],同时可以起到协同增效的作用。因此,开展中国特有的中西医结合治疗HIV/ADIS患者联合用药研究具有重要的现实意义。
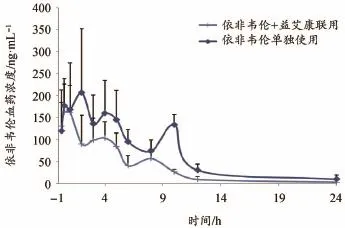
图2 依非韦伦与依非韦伦+益艾康药时曲线

表5 大鼠灌胃给药后依非韦伦药代参数比较
1 金艳涛,许前磊,蒋自强,等. 中医药综合治疗对河南省农村地区HIV/AIDS患者生存质量的影响. 中医杂志, 2016, 57(7): 579-583.
2 金燕. 艾灵颗粒对HAART增效作用的临床研究. 北京:中国中医科学院硕士学位论文, 2007: 61-67.
3 赵红心. 中西医结合治疗艾滋病的机遇与挑战. 中国艾滋病性病, 2008,14(4): 425-427.
4 李强. 关于目前艾滋病临床研究的几点思考. 世界科学技术-中医药现代化, 2013,15(5): 901-904.
5 徐瑶,周则卫. 中医药治疗艾滋病. 中国艾滋病性病, 2007, 13(1): 93-95.
6 杜磊. 益艾康胶囊联合抗病毒药物治疗HIV/AIDS患者47例临床观察. 时珍国医国药, 2010, 21(11): 2954-2955.
7 陆鹏,莫让辉,梁柱石. 黄芪对免疫无应答艾滋病患者CD4+T淋巴细胞数的影响. 中华实验和临床感染病杂志, 2014,8(2): 605-610.
8 魏顺远,康冰,柳凯. 益艾康胶囊治疗艾滋病8年临床观察. 河南预防医学杂志, 2014, 25(1): 108-110.
9 周立华,侯江红,刘爱民,等. 中西药物缓解艾滋病HAART疗法所致骨髓抑制的临床研究. 中华中医学会防治艾滋病分会第六届学术免回论文汇编, 2008: 224-237.
10 刘震,李勇. 艾滋病的中医病因病机及治疗. 中国中药杂志, 2013, 38(15):2501-2503.
11 许前磊,徐立然,郭会军,等. 艾滋病发病与防治中医理论的初步构建. 中医杂志, 2015, 56(11): 909-911.
12 王丹妮,蒋自强,刘成丽,等. 李发枝教授艾滋病发热医案数据挖掘分析. 世界科学技术-中医药现代化, 2013, 15(9): 2052-2056.
13 蒋莲秀,赵海潞,吴丹. 艾滋病中医整体观. 辽宁中医药大学学报, 2014,16(1):149-152.
14 陈军,夏前明. 艾滋病的中医研究近况. 四川中医, 2013, 31(3): 140-142.
15 李亮平,徐立然,扶伟,等. 中医药综合干预对艾滋病病毒感染者/艾滋病患者免疫功能和机会性感染的长期影响. 中医学报, 2016, 212(31): 1-3.
16 刘恭智,欧阳厚淦. 中医药对艾滋病抗病毒治疗辅助疗效观察. 陕西中药, 2013, 29(2): 24,29.
The Investigation of Interactions Between Yi Ai Kang Capsule in Chinese Medicine and Efavirenz, an Antiviral Drug
Meng Xiangle1,2,3, Qin Huizhen2, Ma Jing1, Li Weixia1, Hu Yucai1, Lu Jing1, Tang Jinfa1, Li Xuelin1, Xu Zhiru4, Xiao Feng4, Liu Zhongqiu3, Guo Huijun1, Xu Liran1
(1. The First Affiliated Hospital, Henan University of Traditional Chinese Medicine, Zhengzhou 450000, China;
2. Pharmaceutical College, Henan University, Kaifeng 475004, China
3. International Institute For Translational Chinese Medicine, Guangzhou University of Chinese Medicine, Guangzhou 510006, China;
4. Shanghai Institute of Pharmaceutical Industry, Shanghai 200437, China)
This study aimed at exploring the interactions between Yi Ai Kang (YAK) capsule and efavirenz, a well-known highly active anti-retroviral therapy (HAART) drug. LC/MS/MS was adopted to detect the concentration of efavirenz in the plasma after intragastric administration of efavirenz and the mixed medication of efavirenz and YAK. Then the pharmacokinetic parameters were calculated by the Phoenix WinNonlin 6.1 software. It was found that the measurement met the need of methodological study. The plasma-drug concentration presented a good linear relation within the ranges of 5-500 ng·mL-1, and intra- and inter-day precision were less than 10.0%, while the extraction and the recovery rate varied from 97.0% to 104.0%, featuring a favorable stability and less impact by the substrate. From two main pharmacokinetic parameters, we knew that AUC(0-t), AUC(0-∞), MRT(0-t) and MRT(0-∞)significantly increased (P<0.05), while other parameters presented no statistical significance (P>0.05) in this study. In conclusion, it was demonstrated that YAK capsule influenced the pharmacokinetics properties of efavirenz in rats. However, the interaction between the two prescriptions in clinic still remain to be verified in further studies.
Yi Ai Kang capsule, highly active anti-retroviral therapy, efavirenz, pharmacokinetics
10.11842/wst.2016.10.023
R285.5
A
(责任编辑:马雅静,责任译审:朱黎婷)
2016-06-12
修回日期:2016-06-12
* 国家自然科学基金委-河南省人民政府人才培养联合基金(U1304824):基于DDI的抗艾滋病中药筛选平台的建立及中药YAK抗艾作用机制研究,负责人:孟祥乐; 中国博士后科学基金会特别资助项目(2015T80772): YAK对CD4+T细胞功能的调节及HARRT后IRIS中的作用研究,负责人:孟祥乐;中国博士后科学基金会面上资助项目(2015M582190):基于CMM对TCM治疗AIDS评价研究,负责人:孟祥乐;河南省博士后基金会资助项目(2014-75):中药复方YAK减轻HARRT毒副反应的代谢性机制研究,负责人:孟祥乐;河南省人力资源和社会保障厅济源市科技攻关项目(15013034) :冬凌草抗菌谱及谱效关联研究,负责人:孟祥乐;河南省科技厅“三区”人才计划(2014-566,2015-423):农作物新品种选育,负责人:孟祥乐。
** 通讯作者:徐立然,主任医师,博士生导师,主要研究方向:临床肺病和艾滋病研究。
更正: 现将2016年第18卷第8期1241页作者“朱 玲,朱 彦,杨 峰”更正为“朱 玲1,朱 彦1,杨 峰2”,单位“中国中医科学院中医药信息研究所北京 100700”更正为“1.中国中医科学院中医药信息研究所 北京 100700;2.中国中医科学院针灸研究所 北京 100700”;1250页“Zhu Ling, Zhu Yan, Yang Feng”更正为“Zhu Ling1, Zhu Yan1, Yang Feng2”,“Institute of Information on Traditional Chinese Medicine, China Academy of Chinese Medical Sciences, Beijing 100700, China”更正为“1. Institute of Information on Traditional Chinese Medicine, China Academy of Chinese Medical Sciences, Beijing 100700, China; 2.Institute of Acupuncture and Moxibustion China Academy of Chinese Medical Sciences, Beijing 100700, China”,特此说明。
