水-乙醇体系对双极膜中间界面层的影响
2016-03-19刘小菏李秋花葛亮徐铜文
刘小菏,李秋花,葛亮,徐铜文
(中国科学技术大学化学与材料科学学院,安徽 合肥 230026)
水-乙醇体系对双极膜中间界面层的影响
刘小菏,李秋花,葛亮,徐铜文
(中国科学技术大学化学与材料科学学院,安徽 合肥 230026)
摘要:选取Neosepta BP-1,Fumasep FBM,CJ-BPM三种商业标准双极膜作为研究对象,以水-乙醇为研究体系,通过改变不同乙醇含量,测定双极膜的交流阻抗谱,并且对双极膜的耐溶剂性能进行评价,结果表明BP-1具有良好的耐溶剂性,FBM,CJ-BPM耐溶剂性相对较弱;水解离现象发生在LiCl水-乙醇混合溶液中,随着乙醇含量的增加,双极膜的阻值增加,而水解离程度降低。这种现象可以解释为醇解离能力要远远小于水解离能力,因此乙醇的存在使得中间界面层区域的水浓度降低,进而降低了水解离程度;通过简化算法计算出了不同乙醇含量下,BP-1,FBM的中间界面层厚度,更直观地看出乙醇对双极膜水解离性能的影响。
关键词:水-乙醇体系;膜;离子交换;电化学;交流阻抗谱
2015-06-29收到初稿,2015-08-27收到修改稿。
联系人:徐铜文。第一作者:刘小菏(1989—),女,硕士。
Received date: 2015-06-29.
引 言
双极膜是一种新型的离子交换复合膜,由阴离子交换层、阳离子交换层以及介于这两膜层之间的中间界面层复合而成。双极膜的中间界面层,也就是双极膜两膜层间的过渡区域,它可以是两膜层界面处阴、阳离子交换层的一部分,然而,更多情况下为了改善双极膜的性能,在两膜层间加入一介质层,该介质层具有催化水解离、吸水贮水和粘接两膜层的作用[1-3]。基于双极膜的电渗析具有低能耗、过程简单、环境友好、便于与其他技术集成等突出优点,在污染控制、资源回收以及化工生产过程(特别是有机酸的生产)中具有广阔的和潜在的应用,已成为电渗析工业中新的增长点[4-10]。
目前关于双极膜水解离性能的表征主要通过测定I-V曲线,但I-V曲线只能反映一部分信息;作为辅助手段,交流阻抗谱能够给出在膜结构和功能特性方面的额外信息[11-12]。文献已报道了一些双极膜阻抗谱的研究,Simons等[13]提出了一个非常简单的模型,整个双极膜的阻抗由膜本体的阻抗和双极界面处的阻抗组成,但该模型只考虑了盐离子,不能应用到EFE(electric field enhanced)水解离的情况。Chilcott等[14]提出了一个更为精细的理论模型,在一个相对宽的频率范围内,得到了双极膜中间耗尽层、边界层和外部区域总的导纳方程,但是,同样他们只考虑了盐离子。其他研究采用了电极/溶液界面为特性的模型,关注于水离子对阻抗谱的贡献。水离子在膜相中同步的扩散与反应导致了Gerischer阻抗[15-16],该模型使得理论和实验结果之间趋于一致。除了水体系以外,Chou等[17]研究了复合的双极膜在醇-水溶液中的电流-电压曲线,得出复合双极膜的最大电阻随着加入醇的摩尔分数的增加而增大。
目前,由水和有机溶剂(如醇)构成的非完全水体系的双极膜电渗析为电渗析的应用提供了更为广阔的空间,也解决了一些传统工业难以解决的技术难题[18-19],而相关混合体系双极膜的水解离性能的研究却很少,因此本文选取Neosepta BP-1,FBM,CJ-BPM三种商业双极膜作为研究对象,以水-乙醇为研究体系,测定双极膜的交流阻抗谱,对双极膜的耐溶剂性能进行评价,并且计算出了双极膜在水-乙醇介质中水解离区域的厚度,为双极膜电渗析在水-乙醇体系中的应用提供可靠的表征和筛选手段。
1 实验材料和方法
1.1 材料
实验中所用的双极膜分别是Neosepta BP-1 (Tokuyama Soda Inc., Japan),Fumasep FBM(FuMATech GmbH, Germany),CJ-BPM(合肥科佳高分子材料科技有限公司),它们的性质列于表1中。实验所用的试剂均为分析纯,实验用水为去离子水。

表1 双极膜性能参数Table 1 Properties of bipolar membranes①
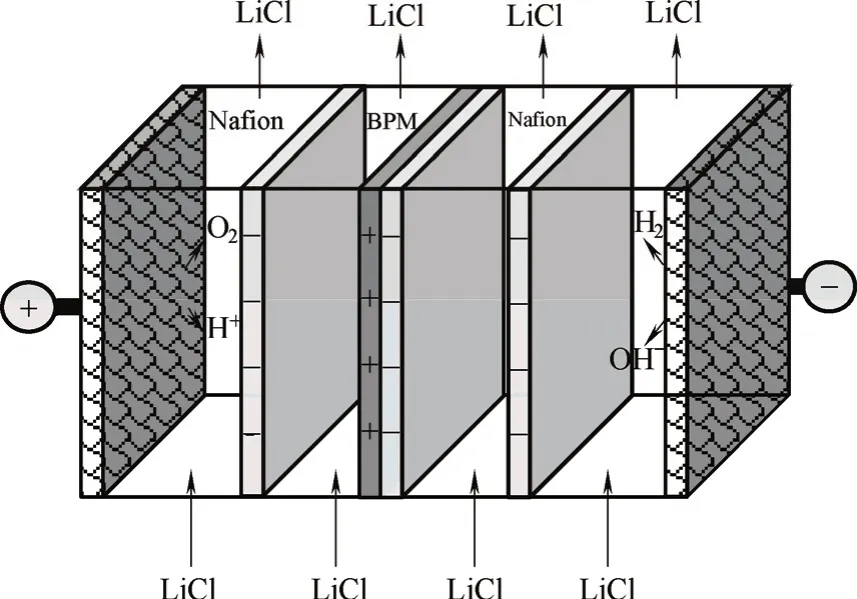
图1 双极膜阻抗谱测试装置:双极膜(BPM)Fig.1 Experimental set-up for bipolar membrane impedance measurements: bipolar membrane (BPM)
1.2 测试方法
实验中所用的电化学交流阻抗谱测试装置如图1所示,电解液和电极液均采用0.5 mol·L-1LiCl,双极膜的有效面积为7 cm2,在测试之前,双极膜浸泡在相应的电解液中2 h,使得电解液与双极膜之间达到平衡状态。在反向偏压条件下,双极膜的电化学阻抗谱通过Autolab PGSTAT 30(Eco Chemie, Netherland)测量系统在恒流模式下获得,为避免电流电极阻抗和膜阻抗的叠合,采用开尔文四端子法的测量技术,装置两侧的钛涂钌电极作为电流电极,双极膜两侧的电压信号则是由一对Ag/AgCl电极测量。电解液通过蠕动泵(BT-100S, 保定雷佛流体科技有限公司)恒速从池下方流入池内并流向膜表面(最小化扩散边界层效应)然后从池上方流出。靠近电极处各放置一张Nafion膜是为了在保证整个系统导电性的同时,阻止两侧电极运行过程中电极反应产物扩散到Ag/AgCl电极处,进而提高整个装置的测量精度。测试中为了降低噪声,任一实验点的数据是10次实验数据的平均值。
1.3 原理
假定双极膜的交流阻抗特性决定于双极膜中间界面层,并且交流阻抗可以通过Nernst-Planck方程和Poisson方程的微小扰动来导出,可以得到双极膜界面处导纳(阻抗的倒数)的表达式

式中,A是膜面积,ˆI是施加于直流电流I上的交流信号的振幅,ˆUD是双极膜结合处的扰动电势降。为了简化,假设双极膜的阴阳膜层是对称的,即dL=dR=d, DiK=Ds(i=1,2;K=N,P),DiK=Dw(i=3,4;K=N,P),ciK=cs(i=l,2;K=L,R),ciK=cw(i=3,4;K=L,R),XN=XP=X,双极膜界面的导纳可以简化为
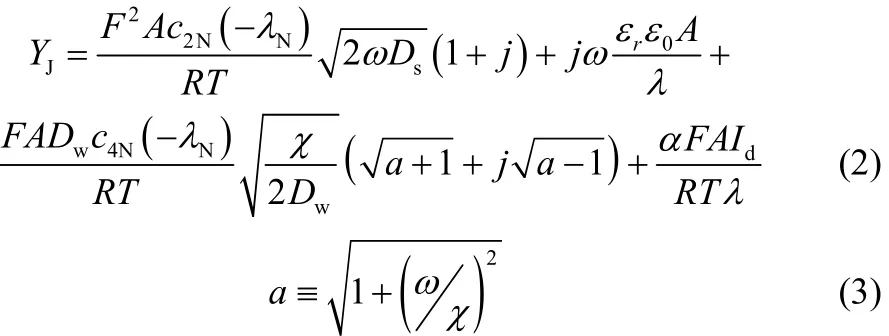
其中,j为虚数,ω是交流阻抗谱的角频率(ω=2πv)。式(2)中的导纳有4项:第1项考虑了膜相中的盐扩散,被称为Warburg导纳;第2项给出了双极膜界面处的几何电容;第3项是关于膜相中H+和OH-同步扩散与反应(也就是Gerischer导纳);最后一项是EFE(第二Wien效应)水解离生成的离子对双极膜阻抗的传导的贡献。
从阻抗谱直接获取界面参数的一个简单方法是利用谱图中峰值的坐标,因为该位置直接与界面的电容有关。计算公式如下

式中,G是当量电导,C是当量电容,ε0是真空介电常数,εr是相对介电常数(对于聚合物膜常取20),Aef是有效接触面积(对于通过流涎法制备的双极膜,典型值是10倍于膜几何面积)[20]。这样根据峰值就可以通过式(4)和式(5)计算出电容,然后由式(6)计算出双极膜中间界面层的厚度l。而中间界面层厚度l可以直观地反映出双极膜水解离区域的大小,厚度的增加会导致膜电阻增加且削弱中间电场强度,导致水解离电压降增加,不利于水解离进行。因此通过该简化公式,可以更直观地看出乙醇含量的增加对双极膜中间界面层的影响。
2 实验结果与讨论
2.1 电流密度对阻抗谱的影响
由于大多数关于频谱分析的实验数据都是以阻抗(Z)的形式报道的,所以,本实验结果以阻抗(Z)给出。图2是Neosepta BP-1双极膜在乙醇含量为20%的情况下,不同电流密度对阻抗谱的影响。从曲线上可以看出在所考虑的频率范围内,曲线在v=vmax获得最大值,最大值随着电流密度的增加而减小。从图中可知,相对于CJ-BPM, BP-1表现出极低的电阻,这主要跟双极膜的极高的离子选择性有关[21]。高的离子选择性主要由以下两个方面引起:第一,膜具有高的同离子排斥,盐扩散被有效的阻碍,因此盐扩散对总阻抗的贡献要远远小于其他膜。第二,对于Neosepta BP-1双极膜EFE水解离起了重要作用。

图2 不同电流密度下Neosepta BP-1双极膜的-Im(Z)对v的对数曲线(乙醇体积分数:20%)Fig.2 Logarithmic plots of -Im(Z) versus v for Neosepta BP-1 membrane at various current densities (volume fraction of ethanol: 20%)
图3是在乙醇含量为20%的情况下,不同电流密度对FBM双极膜阻抗谱的影响。相比于Neosepta BP-1双极膜,FBM双极膜的-Im(Z)最大值出现在低频,这是由于FBM双极膜是直接由阴阳离子交换膜复合而成,没有中间界面介质层,导致双极膜界面电容增加,进而导致了vmax值减小。
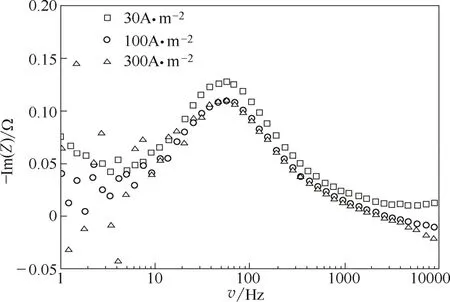
图3 不同电流密度下Fumasep FBM双极膜的-Im(Z)对v的对数曲线(乙醇体积分数:20%)Fig.3 Logarithmic plots of -Im(Z) versus v for Fumasep FBM membrane at various current densities (volume fraction of ethanol: 20%)
图4是在乙醇含量为20%的情况下,不同电流密度对CJ-BPM双极膜阻抗谱的影响。在所考虑的频率范围内,阻抗具有趋于零的低频和高频极限。相对于双极膜BP-1和FBM,阻值相对较高。但随着电流密度的增大,可以有效地降低阻值。另外一个值得注意的地方就是,电流密度为40 A·m-2时,所得的阻抗谱的形状对应于线性扩散现象(Warburg阻抗),盐扩散十分明显,这说明在低的电流密度下,乙醇的增加使得双极膜的极限电流密度增加,双极膜在40 A·m-2时尚未发生水解离。随后随着电流密度增加,当中间界面层的盐离子耗尽时,双极膜到达极限电流密度,发生EFE水解离。
水溶液中,关于电流密度对阻抗谱的影响,文献中已有相关报道[21],随着电流密度的增加阻抗值降低,同时,电流的增加使vmax移向更高值,这与本实验的结果趋势相一致,说明乙醇含量为20%时只是增加了整个体系的阻值,使得双极膜水解离的极限电流密度增加。

图4 不同电流密度下CJ-BPM双极膜的-Im(Z)对v的对数曲线(乙醇体积分数:20%)Fig.4 Logarithmic plots of -Im(Z) versus v for CJ-BPM membrane at various current densities (volume fraction of ethanol: 20%)
2.2 乙醇含量对阻抗谱的影响
图5表明,在电流密度为40 A·m-2时,不同乙醇含量对Neosepta BP-1双极膜阻抗谱的影响。随着乙醇含量的增加,-Im(Z)max增加,而-Im(Z)max出现的频率向低频方向移动。这是因为随着乙醇含量增大,导致溶液整体阻值增加,所以-Im(Z)max增加,而-Im(Z)max出现的频率向低频移动则是因为随着乙醇含量的增加,水的含量减少,导致双极膜中间界面层水解离层形成滞后,所以-Im(Z)最大值出现的频率向低频方向移动。另外值得注意的是,Neosepta BP-1具有良好的耐溶剂性,能够在乙醇溶液内保持完整,并使乙醇发生解离。但是乙醇解离具有非常高的阻值, 说明乙醇解离的电压要远远高于水解离的电压,而目前所用的双极膜的中间层还不能长时间承受过高的电压,所以目前还不能用于大规模的醇解离反应。
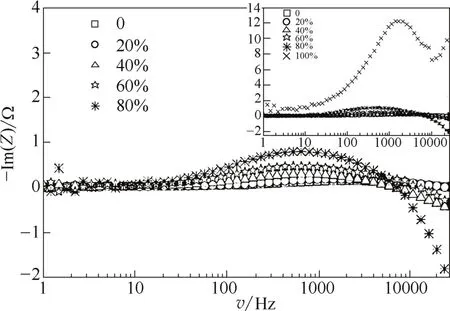
图5 不同乙醇含量下Neosepta BP-1双极膜的-Im(Z)对v的对数曲线(I=40 A·m-2)Fig.5 Logarithmic plots of -Im (Z) versus v for Neosepta BP-1 membrane at different ethanol content (I=40 A·m-2)
图6显示在电流密度为100 A·m-2时,不同乙醇含量对FBM双极膜阻抗谱的影响。随着乙醇含量的增加,-Im(Z)max增加,-Im(Z)max也是向低频方向移动。与Neosepta BP-1双极膜不同的是,FBM双极膜的数据点比较分散,这可能是因为FBM双极膜在低频下发生水解离,而低频下交流阻抗谱测试时间较长且整个测试过程通过蠕动泵循环进行的,导致出现一定的波动。另外乙醇含量增加到60%时,阻值出现了较大的增长,这可能是因为FBM耐溶剂性能不是太好,在60%下已经出现一定程度的溶胀,导致阻值增加较明显。待乙醇含量增加到80%,FBM双极膜表面完全溶胀,无法进行测试。

图6 不同乙醇含量下Fumasep FBM双极膜的-Im(Z)对v的对数曲线(I=100 A·m-2)Fig.6 Logarithmic plots of -Im(Z) versus v for Fumasep FBM membrane at different ethanol content (I=100 A·m-2)
图7所示,在电流密度为110 A·m-2时,不同乙醇含量对CJ-BPM双极膜阻抗谱的影响。随着乙醇含量的增加,趋势同图6,乙醇含量增加导致-Im(Z)max增加,并且-Im(Z)max向低频移动。当乙醇含量增加到40%时,CJ-BPM双极膜完全溶胀,测试无法进行。
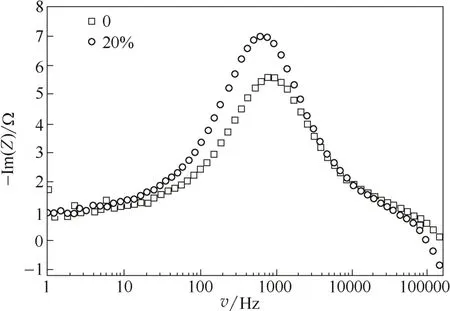
图7 不同乙醇含量下CJ-BPM 双极膜的-Im(Z)对v的对数曲线(I=110 A·m-2)Fig.7 Logarithmic plots of -Im(Z) versus v for CJ-BPM membrane at different ethanol content (I=110 A·m-2)
2.3 乙醇含量对双极膜中间界面层厚度的影响
为了更直观地了解乙醇含量的增加对双极膜中间界面层水解离性能的影响,通过简化式(4)、式(5)和式(6)计算出了中间界面层的厚度。随着乙醇含量的增加,所检测的双极膜BP-1,FBM,CJ-BPM均表现出阻值增加,频率降低,而根据简化公式,中间层厚度正比于两者的乘积,因此中间层厚度与乙醇含量的增加并不呈现一定的线性关系。另外由于CJ-BPM耐溶剂性较差,只得到了乙醇含量为20%的阻抗谱数据,数据较少不能得出乙醇对其中间界面层厚度的影响,因此就不再列出。
从表2中可以看出乙醇含量在0~80%时,实验结果表明随着乙醇含量的增加,中间层厚度呈现增加的趋势,厚度的增加会导致膜电阻增加且削弱中间电场强度,使得水解离电压增加。这说明随着乙醇含量的增加水解离被不同程度的削弱,这种现象可以解释为醇解离能力要远远小于水解离能力,因此乙醇的存在使得中间界面区域的水浓度减少,进而降低了水解离程度。当乙醇含量为100%时,与水-乙醇混合溶液相比,双极膜中间层厚度呈现数量级的增长,这主要还是跟醇解离能力较低有关,这也从侧面说明了在有水存在的情况下不会出现醇的解离。

表2 Neosepta BP-1的中间界面层厚度Table 2 Values of l for Neosepta BP-1
从表3中可以看出随着乙醇含量的增加,FBM中间界面层厚度也是呈现增加的趋势。乙醇含量在0~40%时,中间界面层增加并不明显,水解离只是被一定程度的削弱。而60%时FBM膜溶胀严重,从而引起双极膜界面区域的变化,导致膜阻值增加明显,界面区域厚度增加幅度较大。

表3 Fumasep FBM的中间界面层厚度Table 3 Values of l for Fumasep FBM
3 结 论
(1)BP-1具有良好的耐溶剂性,FBM,CJ-BPM耐溶剂性相对较弱。
(2)所测试双极膜的阻值随着乙醇含量的增加而增加,水解离程度被不同程度地削弱。这种现象可以解释为醇解离能力要远远小于水解离能力,因此乙醇的存在使得中间界面层的水浓度减少,进而降低了水解离程度。
(3)乙醇含量为100%时,BP-1的交流阻抗谱曲线在1762.1 Hz出现峰值,说明在实验条件下BP-1可以实现乙醇的解离。
(4)通过简化公式计算出了不同乙醇含量下BP-1,FBM的中间界面层厚度,随着乙醇含量的增加,中间层厚度增加,厚度的增加会导致膜电阻增加且削弱中间电场强度,导致水解离电压降增加,不利于水解离进行。
References
[1] SIMONS R. A novel method for preparing bipolar membranes [J]. Electrochim Acta, 1986, 31 (9): 1175-1176.
[2] MICHAEL B M, MICHAEL S F. Graphene oxide as a water dissociation catalyst in the bipolar membrane interfacial layer [J]. ACS Appl. Mater. Interfaces, 2014, 6 (16): 13790-13797.
[3] UMEMURA K, NAGANUMA T, MIYAKE H. Bipolar membrane: US 5401408 [P]. 1995-03-28.
[4] HUANG C H, XU T W. Electrodialysis with bipolar membranes (EDBM) for sustainable development [J]. Environ. Sci. Technol., 2006, 40: 5233-5243.
[5] LIU G L, LUO H P, WANG H H, et al. Malic acid production using a biological electrodialysis with bipolar membrane [J]. J. Membrane Sci., 2014, 471: 179-184.
[6] XU T W, YANG W H. Citric acid production by electrodialysis with bipolar membranes [J]. Chem. Eng. Process., 2002, 41: 519-524.
[7] 林晗, 汪群慧, 王丽娟, 等. 双极膜电渗析法分离发酵液中乳酸及离子迁移规律 [J]. 化工学报, 2014, 65 (12): 4823-4830. LIN H, WANG Q H, WANG L J, et al. Lactic acid recovery from fermentation by bipolar membrane electrodialysis and ionic migration [J]. CIESC Journal, 2014, 65 (12): 4823-4830.
[8] TENG L, SHEE F, ARUL J, et al. Performing a three-step process for conversion of chitosan to its oligomers using a unique bipolar membrane electrodialysis system [J]. J. Agric. Food Chem., 2008, 56: 10019-10026.
[9] LIU X H, LI Q H, JIANG C X, et al. Bipolar membrane electrodialysis in aqua-ethanol medium: production of salicylic acid [J]. J. Membrane Sci., 2015, 4: 76-82.
[10] KRYSTYNA P, MARTA J W B. Recovery of fumaric acid from fermentation broth using bipolar electrodialysis [J]. J. Membrane Sci., 2014, 469: 428-435.
[11] HOLDIK H, ALCARAZ A, RAMÍREZ P, et al. Electric field enhanced water dissociation at the bipolar membrane junction from AC impedance spectra measurements [J]. J. Electroanal. Chem., 1998, 442: 13-18.
[12] KEMPERMAN A J B. Handbook on Bipolar Membrane Technology [M]. Enschede: Twente University Press, 2000.
[13] SIMONS R, SAJKEWYCZ N. AC electrical properties in bipolar membranes: experiments and a model [J]. J. Membrane Biol., 1977, 34: 263.
[14] CHILCOTT T C, COSTER H G L, GEORGE E P. AC impedance of the bipolar membrane at low and high frequencies [J]. J. Membrane Sci., 1995, 100: 77-86.
[15] HURWITZ H D, DIBIANI R, MOUSSAOUI R E, et al. Water dissociation in bipolar membranes studied by impedance spectroscopy [C]//BATH U K. Proceedings of Euromembrane, 1995, 1: 89.
[16] GERISCHER H. Wechselstrompolarisation von Elektroden mit einem potential bestimmenden Schritt beim Gleichgewichts potential [J]. I. Z. Phys. Chem., 1951, 198: 256.
[17] CHOU T J, TANIOKA A. Current-voltage curves of composite bipolar membrane in alcohol-water solutions [J]. J. Phys. Chem. B, 1998, 102: 7866-7870.
[18] SANDRA E K, ELANOR K, GEOFF W S, et al. Electrodialysis in aqueous-organic mixtures [J]. Separation & Purification Reviews, 2015, 44: 269-282.
[19] ZHANG F, HUANG C H, XU T W. Production of sebacic acid using two-phase bipolar membrane electrodialysis [J]. Industrial & Engineering Chemistry Research, 2009, 48: 7482-7488.
[20] ANTONIO A, PATRICIO R, JOSÉ A M, et al. Conductive and capacitive properties of the bipolar membrane junction studied by AC impedance spectroscopy [J]. J. Phys. Chem. B, 2001, 105: 11669-11677.
[21] ANTONIO A, HANS H, THOMAS R, et al. AC impedance spectra of bipolar membranes: an experimental study [J]. J. Membrane Sci., 1998, 150: 43-56.
Foundation item: supported by the National Natural Science Foundation of China (21206155).
Influence of aqua-ethanol medium on properties of intermediate layer of a bipolar membrane
LIU Xiaohe, LI Qiuhua, GE Liang, XU Tongwen
(School of Chemistry and Materials Science, University of Science and Technology of China, Hefei 230026, Anhui, China)
Abstract:A bipolar membrane (BPM) was composed of a cation and an anion ion-exchange layer joined together in series. The water dissociation in BPM was then considered as an electric field-enhanced (EFE) phenomenon and its magnitude depended critically on the structure and composition of the bipolar intermediate layer. By changing the different content of ethanol, three commercial bipolar membranes Neosepta BP-1, Fumasep FBM and CJ-BPM were tested by AC impedance spectra and their bipolar membrane solvent resistance were evaluated simultaneously. It was confirmed that BP-1 had good solvent resistance and FBM and CJ-BPM solvent resistances were relatively weak. The experimental results showed that the water dissociation phenomenon occurred in the LiCl water-ethanol mixed solutions, and the local effective value of the BPM resistance increased with an increase in the content of ethanol, while the water dissociation became less obvious. This phenomenon could be explained due to the fact that the dissociative ability of alcohol was weaker than that of water. Thus, the existence of ethanol decreased the concentration of water in the intermediate layer of a bipolar membrane and caused the decrease in the water dissociation effect. By simplifying the algorithm to calculate the intermediate layer thickness of the BP-1 and FBM membranes, it was more intuitive to know the influence of ethanol content on the water dissociation.
Key words:water-ethanol system; membrane; ion exchange; electrochemistry; AC impedance spectra
Corresponding author:Prof. XU Tongwen, twxu@ustc.edu.cn
基金项目:国家自然科学基金项目(21206155)。
中图分类号:TQ 028.8
文献标志码:A
文章编号:0438—1157(2016)01—0309—06
DOI:10.11949/j.issn.0438-1157.20151004
