蒙药孟根乌苏(水银)-18味丸对大鼠肾脏毒性初步研究
2016-03-16佟海英范盎然于雪张月乌吉斯古冷李婧呼日乐巴根北京中医药大学民族医药学研究所北京0009北京中医药大学基础医学院北京0009内蒙古自治区国际蒙医医院内蒙古呼和浩特0000内蒙古医科大学蒙医药学院内蒙古呼和浩特000
佟海英,范盎然,于雪,张月,乌吉斯古冷,李婧,呼日乐巴根.北京中医药大学民族医药学研究所,北京 0009;.北京中医药大学基础医学院,北京 0009;.内蒙古自治区国际蒙医医院,内蒙古 呼和浩特 0000;.内蒙古医科大学蒙医药学院,内蒙古 呼和浩特 000
蒙药孟根乌苏(水银)-18味丸对大鼠肾脏毒性初步研究
佟海英1,范盎然2,于雪2,张月1,乌吉斯古冷3,李婧4,呼日乐巴根4
1.北京中医药大学民族医药学研究所,北京 100029;2.北京中医药大学基础医学院,北京 100029;
3.内蒙古自治区国际蒙医医院,内蒙古 呼和浩特 010020;4.内蒙古医科大学蒙医药学院,内蒙古 呼和浩特 010110
摘要:目的观察孟根乌苏(水银)-18味丸对大鼠肾脏功能的影响,探讨其肾毒性。方法将Wistar雄性大鼠根据体质量随机分为8组:正常对照组,孟根乌苏-18味丸低、中、高剂量组,孟根乌苏炮制品组,硫化汞组,氯化汞组,氯化亚汞组,每组10只。各组大鼠给予相应药物灌胃,连续15 d。分别检测大鼠血清尿素(UREA)、肌酐(CREA)水平,观察肾组织形态学变化,并用电感耦合等离子体发射光谱仪和电感耦合等离子体质谱法检测肾汞蓄积量,原位末端标记法检测肾细胞凋亡,免疫组化检测肾Ⅲ型胶原蛋白表达,实时荧光定量PCR检测肾脏金属硫蛋白(MT)-1、MT-2基因表达。结果氯化汞、氯化亚汞大鼠肾脏指数比正常对照组和孟根乌苏炮制品组显著升高(P<0.01);各组大鼠血清CREA和UREA含量无显著差异。肾脏病理观查结果表明,孟根乌苏-18味丸低剂量组(临床常用剂量)大鼠肾脏出现一定的病理损伤,表现为肾小球轻度肥大、肾小管上皮中度肿胀变性,孟根乌苏-18味丸中、高剂量组肾脏也出现一定损伤,硫化汞组、氯化汞组、氯化亚汞组大鼠肾病理变化更显著。与正常对照组和孟根乌苏炮制品组比较,氯化汞组和氯化亚汞组大鼠肾汞蓄积量显著升高(P<0.01),氯化汞组、氯化亚汞组大鼠肾细胞凋亡率显著升高(P<0.01),硫化汞组、氯化汞组、氯化亚汞组大鼠肾脏Ⅲ型胶原蛋白表达显著升高(P<0.05,P<0.01)。与正常对照组比较,氯化亚汞组大鼠肾组织中MT-1 mRNA表达显著升高(P<0.05),氯化汞组、氯化亚汞组大鼠肾组织中MT-2 mRNA表达显著升高(P<0.05,P<0.01);与孟根乌苏炮制品组比较,氯化亚汞组大鼠肾组织中MT-1 mRNA表达显著升高(P<0.05)。结论临床常用剂量孟根乌苏-18味丸在15 d用药过程中未对大鼠肾脏功能造成明显的损伤。
关键词:孟根乌苏-18味丸;汞化合物;肾毒性;大鼠
孟根乌苏(水银)-18味丸(以下简称“孟根乌苏-18味丸”)为蒙医传统经典复方,具收敛、生肌、燥“协日乌素”之功,载入1984年版《内蒙古蒙成药标准》,方中孟根乌苏(水银)炮制品占11.24%[1]。孟根乌苏炮制品由水银与硫磺等量加热炮制而成,主含硫化汞[2-3],因此,含汞化合物孟根乌苏-18味丸的安全性问题备受关注。本课题组前期已对孟根乌苏炮制品、孟根乌苏-18味丸与氯化汞、氯化亚汞单次给药、连续7 d给药后肾毒性进行了对比研究,结果均显示,常用剂量孟根乌苏炮制品、孟根乌苏-18味丸未对大鼠肾脏造成明显损伤,并且毒性远远低于氯化汞和氯化亚汞[4]。为进一步探究孟根乌苏-18味丸的肾毒性,本研究采用连续灌胃给药15 d,观察孟根乌苏-18味丸对大鼠肾功能、肾组织形态学、肾汞蓄积量、肾细胞凋亡、Ⅲ型胶原蛋白表达及金属硫蛋白(MT)-1、MT-2基因表达的影响。
1 实验材料
1.1动物
清洁级Wistar雄性大鼠80只,6~8周龄,体质量180~200 g,斯贝福(北京)实验动物科学技术有限公司,合格证号SCXK(京)2011-0004。以清洁级大小鼠维持饲料饲养,北京科澳协力饲料有限公司。动物饲养于北京中医药大学SPF级动物房,整个实验过程中动物自由摄食和饮水,室温20~22 ℃,相对湿度为60%~70%,光照周期为12 h,7:00-19:00光照,19:00-7:00黑暗,适应环境7 d后进行实验。
1.2药物
孟根乌苏炮制品,内蒙古自治区国际蒙医医院提供(2012年5月炮制)。孟根乌苏-18味丸组成:水银(制)100 g,文冠木膏75 g,硫黄(制)75 g,苘麻子75 g,木香50 g,肉豆蔻15 g,甘松15 g,白云香75 g,诃子100 g,草乌(制)100 g,草果仁15 g,石菖蒲35 g,决明子75 g,苏格木勒20 g,红花15 g,石膏20 g,丁香15 g,黑云香15 g,内蒙古自治区国际蒙医医院,批号20120916。氯化汞,姜堰市环球试剂厂,批号20130110;氯化亚汞,aladdin公司,批号E1317041;硫化汞,aladdin公司,批号47973。
1.3主要仪器与试剂
Microlab300半自动生化分析仪,荷兰威图科学公司;微波消解仪Ethos,意大利Milestone公司;电感耦合等离子体发射光谱仪(ICP-OES),美国Thermo Fisher公司;电感耦合等离子体质谱仪(ICP-MS),美国Thermo Fisher公司;CFX96型荧光定量PCR仪,美国BIO-RAD公司;反转录试剂盒,美国Thermo Fisher公司;肌酐(CREA)测定试剂盒(批号132721),尿素(UREA)测定试剂盒(批号131031),均由中生北控生物科技股份有限公司提供;Ⅲ型胶原抗体,批号GR30215-3,美国Abcam公司;Tunel试剂盒,货号11684817910,瑞士Roche公司;Hg单元素标准溶液,国家钢铁材料测试中心钢铁研究总院。
2 实验方法
2.1分组与给药
实验大鼠按体质量随机分成8组,每组10只,即正常对照组、孟根乌苏-18味丸低剂量组(0.29 g/kg,临床使用剂量的8倍,Hg 0.015 g/kg)、孟根乌苏-18味丸中剂量组(1.47 g/kg,临床使用剂量40倍,Hg 0.074 g/kg)、孟根乌苏-18味丸高剂量组(2.9 g/kg,临床使用剂量80倍,Hg 0.145 g/kg)、孟根乌苏炮制品组(0.033 g/kg,Hg 0.015 g/kg)、硫化汞组(17.39 mg/kg,Hg 0.015 g/kg)、氯化汞组(4.06 mg/kg,Hg 0.003 g/kg)、氯化亚汞组(7.06 mg/kg,Hg 0.003 g/kg),各组大鼠适应1周后,各组均按10 mL/kg体质量给药,每日1次,连续15 d。
2.2肾脏指数和肾功能检测
大鼠处死前禁食(不禁水)8 h,次日处死前称重,10%水合氯醛腹腔注射麻醉,取出肾脏后,立即用滤纸擦干表面残血,称重,以相应体质量计算肾脏指数,肾脏指数=肾脏质量(mg)÷体质量(g)。腹主动脉采血8~10 mL,室温下放置1 h后,4 ℃、3000 r/min离心10 min,分离血清,按照试剂盒说明测定血清UREA和CREA含量。
2.3肾组织形态学观察
取大鼠同侧肾脏,中性福尔马林固定,石蜡包埋,切片,HE染色,光学显微镜下观察其组织病理变化。
2.4肾汞蓄积量测定
取适量肾组织,精密称定,置洁净的微波消解罐中,加入浓硝酸2 mL,盖上盖子,预消解过夜后,装入微波消解仪中,按照设定消解程序进行样品消解,同时做对照样品。待消解完毕并冷却过夜后,取出内管,将澄清的消解液转移定容于25 mL容量瓶中,摇匀待测。
ICP-OES工作曲线:使用1000 μg/mL的Hg单元素标准溶液(国家钢铁材料测试中心钢铁研究总院)逐级稀释配制成0、1、5、10 μg/mL(5%硝酸介质)的系列标准溶液,用ICP-OES检测。仪器参数:等离子体功率1150 W,雾化气流速0.6 L/min,辅助气流量0.5 L/min,蠕动泵转数50 r/min。
ICP-MS工作曲线:使用1000 mg/L Hg单元素标准溶液(国家钢铁材料测试中心)逐级稀释配制成0、0.5、1、2 ng/mL(2%硝酸介质)的系列标准溶液,用ICP-MS检测。仪器参数:功率1548 W,冷却气流速:13.88 L/min,辅助气流速:0.795 L/min,载气流速:0.952 L/min[5-7]。
2.5原位末端标记法测肾脏凋亡细胞数
按试剂盒说明书对肾组织染色,DAB显色,苏木素轻度复染。光镜观察细胞核呈棕黄色为阳性细胞,镜下随机选取10个视野(×400),观察阳性细胞数及总细胞数,计算细胞凋亡率(阳性细胞数÷总细胞数×100%)。
2.6免疫组化检测肾组织Ⅲ型胶原蛋白表达
肾脏中性福尔马林固定,石蜡包埋、切片,切片厚5 μL。切片常规脱蜡,3%H2O2室温10 min以灭活内源性过氧化物酶。0.01 mol/L枸橼酸盐缓冲液(pH 6.0)高压抗原修复,滴加一抗后4 ℃过夜,滴加生物素化二抗,DAB显色,苏木素复染,脱水,透明,封片。采用美国Media Cybernetics公司Image Pro Plus 6.0医学图像分析系统进行图像分析,镜下随机选取5个视野,测定累积积分光密度(IOD)值[8]。
2.7实时荧光定量PCR检测肾组织金属硫蛋白-1、金属硫蛋白-2基因表达
取大鼠肾组织加入1 mL Trizol液研磨,剧烈振荡以裂解细胞,裂解液转入EP管中,室温下放置5 min;然后加入0.2 mL氯仿,剧烈摇荡离心管15 s。室温下(15~30 ℃)放置2~3 min后,12 000×g(2~8 ℃)离心15 min;取上层水相于一新的离心管,加入等量异丙醇,室温下放置10 min,12 000×g(2~8 ℃)离心10 min;弃上清液,加1 mL 75 %乙醇,重悬RNA沉淀,4 ℃、7 500×g离心5 min;弃上清液,让沉淀RNA在室温下自然干燥或真空干燥5~10 min,并加适量DEPC水溶解RNA沉淀,取其1 µL用DEPC水稀释100倍。测定RNA浓度,并鉴定其纯度(琼脂糖凝胶电泳法)。应用PCR仪进行反转录,反应条件:42 ℃、60 min,70 ℃、8 min,4 ℃保存。反应结束后,应用CFX96型荧光定量PCR仪进行扩增,扩增条件:95 ℃、10 min,95 ℃、15 s,60 ℃、60 s,40个循环。引物由生工生物工程(上海)股份有限公司设计并合成,MT-1正义链:5'-AATGTGCCCAGG GCTGTGT-3',反义链:5'-GCTGGGTTGGTCCGATA CTATT-3';MT-2正义链:5'-TGTGCCTCCGATGGA TCCT-3',反义链:5'-GCAGCCCTGGGAGCACTT-3';以18 s为内标,正义链:5'-CGAACGTCTGCCCTA TCAACTT-3',反义链:5'-CCGGAATCGAACCCTGA TT-3'。目的基因mRNA的相对表达量根据2-ΔΔCt的公式及方法进行换算[9-10]。
3 统计学方法
4 结果
4.1孟根乌苏-18味丸对大鼠肾脏指数、肾功能的影响
大鼠连续给药15 d后,氯化汞组、氯化亚汞组大鼠肾脏指数比正常对照组和孟根乌苏炮制品组显著升高(P<0.01);各组大鼠血清CREA和UREA含量变化不明显,差异无统计学意义(P>0.05)。结果见表1。
表1 各组大鼠肾脏指指数及肾功能相关指标比较(±s))

表1 各组大鼠肾脏指指数及肾功能相关指标比较(±s))
注:与正常对照组比较,*P<0.05,**P<0.01;与孟根乌苏炮制品组比较,△P<<0.05,△△P<0.01(下同)
组别 只数 肾脏指数/(mgg/g)正常对照组100.007 8±0.000 5孟孟孟孟硫氯氯根乌苏-18味丸低根乌苏-18味丸中根乌苏-18味丸高根乌苏炮制品组化汞组化汞组化亚汞组剂量组剂量组剂量组10 10 10 10 10 10 10 0.008 5±0.001 0 0.008 7±0.000 9 0.008 9±0.001 2 0.008 4±0.000 9 0.008 3±0.000 7 0.011 0±0.001 2 0.011 7±0.002 4 0 9 2 **△△**△△CREA/(μmol/L)UREA/(m mol/L)91.40±11.8811.35±2.31 94.00±14 98.18±10 90.44±10 92.22±17 86.00± 7 88.73± 5 90.42±12 .76 .54 .68 .30 .60 .12 .63 11.32±2 11.70± 12.01± 12.02± 9.43± 12.72± 10.91±2 .32 1.97 1.66 1.49 1.57 1.97 .80
4..2孟根乌苏苏-18味丸对大大鼠肾组织形形态学的影响响
正常对照组组肾小球如常常,无肿大,球囊壁未见见增厚;肾小管无变变性,无坏死死,无管型;间质如常;孟根乌乌苏-18味丸丸低剂量组肾肾小球轻度肥肥大,球囊壁壁未见增增厚,肾小管管上皮中度肿肿胀变性;孟孟根乌苏-18味丸中剂量组也可可见低剂量组组病理变化,但未见凋亡亡及坏死死;孟根乌苏苏-18味丸高高剂量组除低低剂量组病理理变化外外,还可见间间质内见炎症症细胞浸润;孟根乌苏炮炮制品组组肾小球轻度度肥大,球囊囊壁未见增厚厚,肾小管上上皮轻度度肿胀变性,,间质血管扩扩张;硫化汞汞组肾小球可可见萎缩缩,周围肾小小球代偿性肥肥大,肾小管管变性明显,大面积积浑浊肿胀及及少量嗜酸性性变,局部见见凋亡,肾小小球囊壁壁略增厚,间间质增宽,少少量纤维组织织增生;氯化汞组大大量肾小球萎萎缩,周围可可见代偿性肥肥大的肾小球,肾小球基底膜及及系膜区增厚厚,肾小管变变性明显,浑浊肿胀胀及嗜酸性变变,凋亡细胞胞多见,另可可见小灶坏死,肾小球囊壁明显显增厚,间质质增宽,纤维维组织增生,局部玻玻璃样变;氯氯化亚汞组肾肾小球以代偿偿性肥大为主,肾小球系膜区增增生,可见少少量肾小球萎萎缩,肾小管变性,浑浊肿胀及及少量嗜酸性性变,可见凋凋亡细胞和点状坏死死,肾小球囊囊壁增厚,间间质增宽,少少量纤维组织增生。结果见图1。
4..3孟根乌苏苏-18味丸对大鼠肾汞蓄积量的影响
与正常对照照组和孟根乌苏炮制品组比较,氯化汞组和和氯化亚汞组组大鼠肾汞蓄积量显著升高(P<0.01)。结果果见表2。
4..4孟根乌苏苏-18味丸对大鼠肾组织细胞凋亡及Ⅲ型胶胶原蛋白表达达的影响
肾细胞凋亡亡Tunel染色色为细胞核着色,淡黄至棕黄色,数量多者表示凋亡比较高,Ⅲ型胶原蛋白表达于肾小球系膜间质,亦可见于肾小管上皮细胞,淡黄至棕黄色。与正常对照组和孟根乌苏炮制品组比较,氯化汞组和氯化亚汞组大鼠肾细胞凋亡率显著升高(P<0.01);硫化汞组、氯化汞组、氯化亚汞组大鼠肾脏Ⅲ型胶原蛋白表达显著升高(P<0.05,P<0.01)。结果见表3、图2、图3。

注:A.正常对照组;B.孟根乌苏-18味丸低剂量组;C.孟根乌苏-18味丸中剂量组;D.孟根乌苏-18味丸高剂量组;E.孟根乌苏炮制品组;F.硫化汞组;G.氯化汞组;H.氯化亚汞组(下同)
表2 各组大鼠肾汞蓄积量比较(±s)

表2 各组大鼠肾汞蓄积量比较(±s)
组别 只数 肾汞蓄积量//(ng/g)正常对照组1052.91±16.36孟根乌苏孟根乌苏孟根乌苏孟根乌苏硫化汞组氯化汞组氯化亚汞-18味丸低剂量-18味丸中剂量-18味丸高剂量炮制品组组组 10组 10组 10 10 10 10 10 1301.72± 1676.04± 1766.62± 1049.81± 1420.25± 103 802.86±16 109 942.86±14 393.93 156.92 87.19 140.07 95.92 737.26**△△585.08**△△
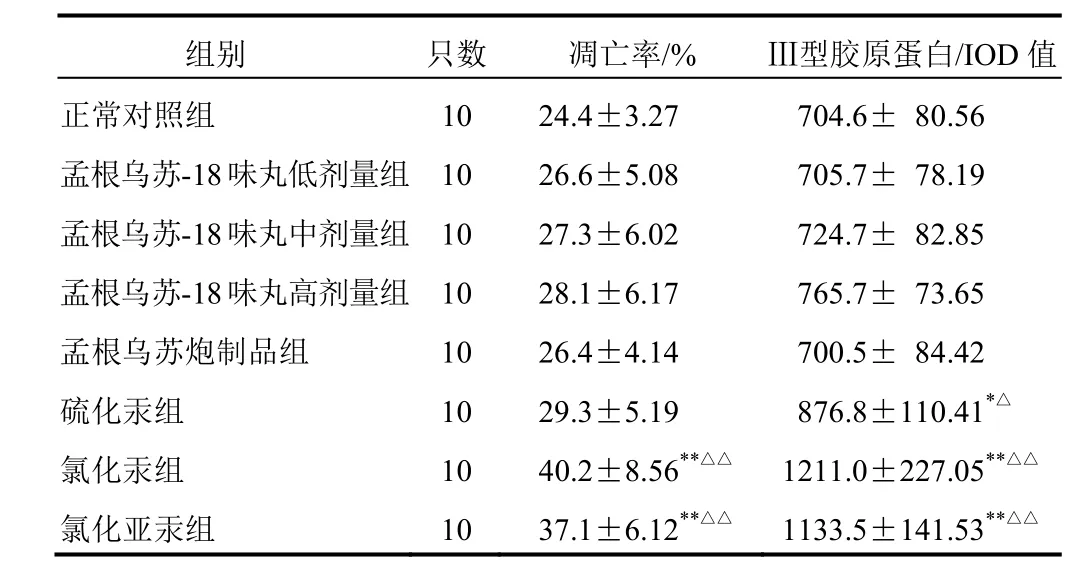
表3 各组大鼠肾组织细胞凋亡率及Ⅲ型胶原蛋白表达比较(——xx ±s)
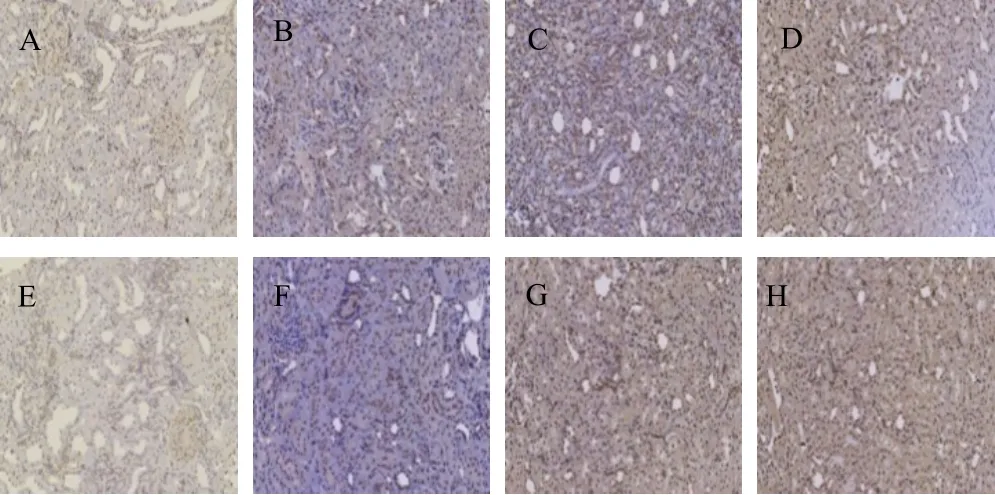
图2 Tu nel法检测各组大鼠肾组织细胞凋亡结果(×200)
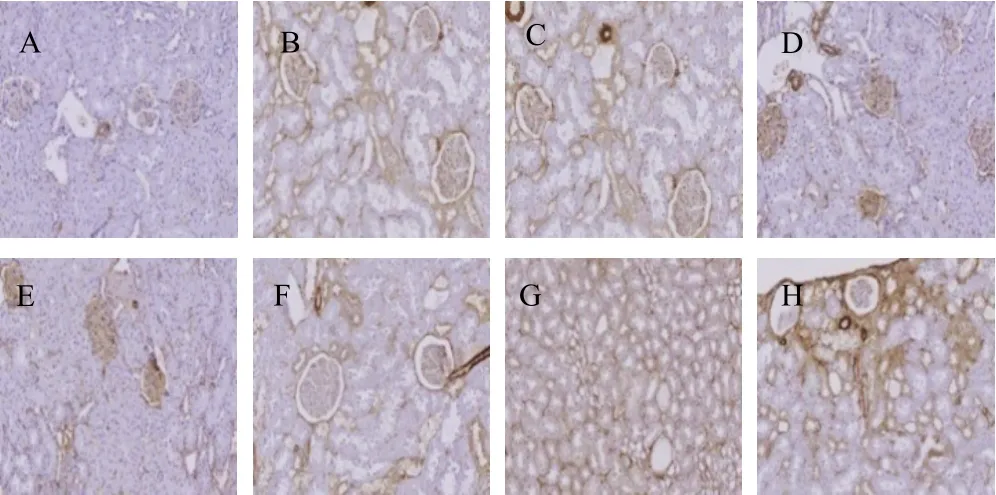
图3 各组大鼠肾组织Ⅲ型胶原蛋白免疫组化染色结果(×200)
4.5孟根乌金-18味丸对大鼠肾组织金属硫蛋白-1、金属硫蛋白-2基因表达的影响
与正常对照组比较,氯化亚汞组大鼠肾组织MT-1 mRNNA 表达显著升高(P<0.005),氯化汞组、氯化亚汞组大鼠肾组织MT-2 mRNA表达显著升高(P<0.05,P<0.01);与孟根乌苏炮制品组比较,氯化亚汞组大鼠肾组织中MT-1 mRNA表达显著升高(P<0.005)。结果见表4。
表4 各组大鼠肾组织MT-1、MT-2 mRNA表达比较(±s,2-ΔΔCt)
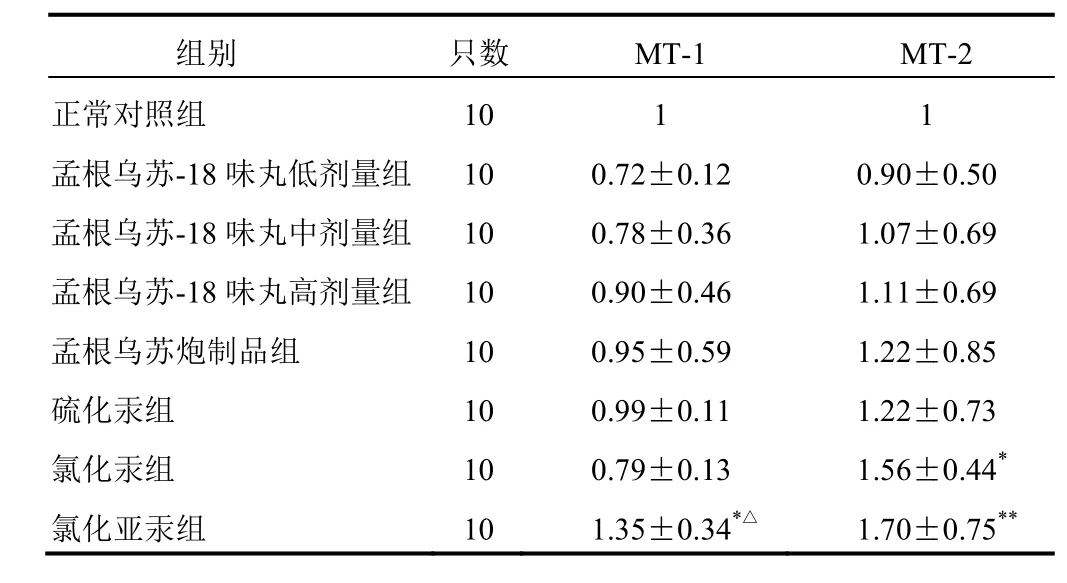
表4 各组大鼠肾组织MT-1、MT-2 mRNA表达比较(±s,2-ΔΔCt)
组别只数 MT-1 MT T-2正常对照组10 11孟根乌苏-18味丸孟根乌苏-18味丸孟根乌苏-18味丸孟根乌苏炮制品硫化汞组氯化汞组氯化亚汞组低剂量组 10中剂量组 10高剂量组 10 组 10 10 10 10 0.72±0.1 0.78±0.3 0.90±0.4 0.95±0.5 0.99±0.1 0 0.79±0.1 0 1.35±0.3 12 0.90± 36 1.07± 6 1.11± 9 1.22± 1 1.22± 3 1.56± 34*△ 1.70± ±0.50 0.69 0.69 0.85 0.73 0.44*0.75**
5 讨论
在前期实验研究中,根根据孟根乌苏-18味丸中汞的的含量,并参考考相关文献研研究[11-12],硫化汞组和氯化亚亚汞组汞摄入量与孟根乌苏苏-18味丸低剂量组相等,氯氯化汞组汞摄入量为20%设计进行研究,结果在7 d给给药实验中,氯氯化亚汞组4只大鼠死亡,可能汞摄入量量过高导致大鼠肾功能衰竭竭。因此,在本研究中,氯化化亚汞组汞摄入量也设计为为孟根乌苏-18味丸低剂量组组汞摄入量200%。
大鼠连续给药15 d后后,孟根乌苏-18味丸、孟孟根乌乌苏炮制品、硫硫化汞、氯化化汞、氯化亚亚汞对其肾功功能无无影响,但氯化化汞组、氯化化亚汞组大鼠鼠肾脏指数显显著增增加,解剖肉眼观察也有肿肿胀现象,表表明氯化汞、氯化化亚汞对大鼠肾脏造成一定定的损伤。肾肾脏病理检查查结果果表明,孟根乌苏-18味丸丸低剂量组大大鼠肾脏出现现一定定的病理损伤,表现为肾小小球轻度肥大大、肾小管上上皮中中度肿胀变性。课题组在7 d给药实验验中也观察到到,大大鼠肾小球轻度肥大,肾小小管上皮轻度度肿胀变性。故随随着给药时间的延长,孟根根乌苏-18味味丸对肾脏的的病理理损伤会有所所增加,尤其其对肾小管的的毒性作用更更显著著。在本实验中,观察到孟孟根乌苏-188味丸中、高高剂量量组肾脏也出现一定损伤,,硫化汞组、、氯化汞组、氯化化亚汞组大鼠肾病理变化更更显著。这也也说明,虽然然孟根根乌苏-18味丸丸中、高剂量量对大鼠肾组组织产生一定定的病病理损伤作用,但其毒性仍仍低于硫化汞汞、氯化汞、氯化化亚汞。肾汞检测结果表明,孟根乌苏苏-18味丸和和孟根根乌苏炮制品品组大鼠肾汞汞含量与正常常对照组无明明显差差异,硫化汞组组大鼠肾汞蓄蓄积量有增高高趋势,氯化化汞组组和氯化亚汞组大鼠汞摄入入量仅为孟根根乌苏-18味味丸低低剂量组的220%,也引起起了肾汞的显显著蓄积。这与肾肾脏是重金属属汞蓄积器官官和靶器官相相符合,并与相关关研究结果相相符合[11-12]。在本实验中中,孟根乌苏炮制制品组与原复复方药物组含含汞相当,但但孟根乌苏炮制品品组较原复方方药物组引起起的肾汞蓄积积少,这一结果也也重复了我们们在7 d实验中中观察到的结结果,说明孟根乌乌苏-18味丸复方可促进进孟根乌苏炮炮制品中汞的生物物利用度。蒙蒙药配方有君君臣佐使的关关系,也说明汞在在一定剂量范范围内有特定定的药理作用用,亟待进一步研研究。
有研究表明,汞可使线粒体内自由基含量增加,刺刺激线粒体膜上蛋白酶活力改变,提高线粒体膜的通透透性,影响AATTP合成,导致细胞色素C释放,进而诱诱导细胞凋亡[13]。在本实验中,肾汞蓄积量较多的氯化化汞组、氯化化亚汞组大鼠肾细胞凋亡显著高于其他组。Ⅲ型胶原的合成、分泌增多及降解减少是许多肾脏疾病发展、细胞外基质积聚和肾间质纤维化的主要原因。在本实验中,发现硫化汞组、氯化汞组、氯化亚汞组大鼠肾脏Ⅲ型胶原蛋白的表达显著增强,说明Ⅲ型胶原蛋白的过度表达促进了肾间质纤维化的发生,进而影响了肾脏功能。
MT是一种富含巯基的金属结合蛋白,汞与巯基有很强的亲和力,与肾组织中含巯基蛋白结合是汞所致肾损伤的主要病理基础。汞可诱导MT的表达,MT的表达可以部分拮抗汞的肾毒性作用。前期研究发现,大鼠给予氯化汞、氯化亚汞1、7 d后,MT mRNA升高是可作为金属暴露和毒性的生物标志,而孟根乌苏炮制品对MT的诱导远低于常见的汞化合物[4]。在本实验中,氯化汞组大鼠肾组织中MT-2 mRNA表达显著增高,氯化亚汞组大鼠肾组织中MT-1和MT-2 mRNA表达显著增高,其他各组与正常对照组比较差异无统计学意义。由于孟根乌苏-18味丸和孟根乌苏炮制品组大鼠肾汞蓄积量少,对机体的影响较小,因此对MT-1和MT-2的mRNA表达无影响,而氯化汞组、氯化亚汞组大鼠肾汞蓄积量远远高于其他组,故显著诱导MT-1和MT-2 mRNA的表达,这从一个侧面反映出氯化汞、氯化亚汞的毒性远远高于孟根乌苏-18味丸、孟根乌苏炮制品。硫化汞组大鼠肾组织汞蓄积量虽然与正常对照组无明显差异,但有增高趋势,并引起了肾脏Ⅲ型胶原蛋白的过度表达,但未引起MT-1和MT-2 mRNA表达的异常,可能与给药剂量、给药时间等有关。
此次研究提示,大鼠连续给药15 d,孟根乌苏-18味丸低剂量组大鼠未发现肾功能改变,以及肾细胞凋亡、胶原蛋白表达和MT-1、MT-2 mRNA表达的异常,但对肾组织产生一定的病理损伤,表明在临床规定用药剂量内不会产生明显毒副作用。但孟根乌苏-18味丸中、高剂量组随着给药时间的延长,肾汞蓄积量会显著增多,并对肾组织产生一定的病理损伤。提示剂量过大可能对肾脏产生一定的影响,其具体毒性机制有待深入研究。
参考文献:
[1] 内蒙古自治区卫生厅.内蒙古蒙成药标准[M].赤峰:内蒙古科学技术出版社,1984:359-360.
[2] 国家中医药管理局《中华本草》编委会.中华本草:蒙药卷[M].上海:上海科学技术出版社,2004:3.
[3] 佟海英,呼日乐巴根,包迎春,等.蒙药孟根乌苏(水银)炮制法探微[J].世界科学技术-中医药现代化,2013,15(4):689-696.
[4] 佟海英,范盎然,白亮凤,等.蒙药孟根乌苏(水银)炮制品、孟根乌苏(水银)-18味丸与硫化汞、氯化汞、氯化亚汞急性毒性的比较研究[J].世界科学技术-中医药现代化,2015,17(3):698-706.
[5] 李伟东,张志杰,陈逸君,等.电感耦合等离子体光谱法/质谱法测定自然铜不同炮制品中砷、铅、铜、镉、汞的含量[J].中国实验方剂学杂志,2012,18(24):181-186.
[6] 汤家铭,米金霞,吴文斌,等.朱砂灌胃给药后汞在孕大鼠脏器内的分布和排泄途径研究[J].上海中医药大学学报,2011,25(6):71-75.
[7] 盛振华,惠恩健,方文忠.微波消解-ICP-OES法测定浙八味中的21种无机元素[J].中华中医药学刊,2013,31(7):1706-1708.
[8] 戴小华,王波,杨帆,等.养肝益水颗粒对自发性高血压大鼠肾脏Ⅰ、Ⅲ、Ⅳ型胶原蛋白和FN的影响[J].中国中西医结合杂志,2014,34(8):1003-1007.
[9] 康峰,吴琨,何海洋,等.朱砂、朱砂安神丸与甲基汞、氯化汞的毒性对比研究[J].中国中药杂志,2010,35(4):499-503.
[10] 彭芳,杨虹,吴芹,等.万胜化风丹对大鼠亚急性毒性的研究[J].中国中药杂志,2012,37(7):1017-1022.
[11] 何海洋,康峰,颜俊文,等.朱砂、朱砂安神丸与氯化汞、轻粉的急性毒性对比[J].中国实验方剂学杂志,2011,17(2):219-223.
[12] 颜俊文,苗加伟,何海洋,等.万胜化风丹、雄黄和朱砂的急性肝肾毒性作用[J].中国药理学与毒理学杂志,2011,25(4):380-385.
[13] 高健,徐兆发,邓宇,等.汞对大鼠肾皮质线粒体ATP酶和膜电位的影响[J].中国职业医学,2009,36(6):461-463.
(修回日期:2015-07-06;编辑:华强)
Preliminary Investigation of Mongolian Meng-gen-wu-su (Mercury)-18-Composition Pills onRenal Toxicity in Rats
TONG Hai-ying1, FAN Ang-ran2, YU Xue2, ZHANG Yue1, WU Jisiguleng3, LI Jing4, HU Rilebagen4(1. Institute of Ethnic Medicine, Beijing University of Chinese Medicine, Beijing 100029, China; 2. School of Basic Medical Sciences, Beijing University of Chinese Medicine, Beijing 100029, China; 3. Inner Mongolia International Mongolian Medicine Hospital, Hohhot 010020, China; 4. College of Mongolian Medicine and Pharmacy, Inner Mongolia Medical University, Hohhot 010110, China)
Abstract:Objective To study the effects of Mongolian Meng-gen-wu-su (Mercury)-18-Composition Pills on renal toxicity in rats; To discuss its Renal Toxicity. Methods Eighty male Wistar rats were randomly divided into eight groups according to the weight (10 rats in each group): normal control group, low-, medium- and high-dose Meng-gen-wu-su-18-Composition Pills groups, Meng-gen-wu-su-18-Composition processed products group, mercuric sulfide group, mercuric chloride group and mercurous chloride group. After one week adaption, oral gavages were given to each group of rats for fifteen days. Serum UREA and CREA content and renal tissue morphological changes were detected; Mercury accumulation in kidney was determined by inductively coupled plasma optical emission spectroscopy and inductively coupled plasma source mass spectrometer; Apoptosis of renal cells was determined by TUNEL; Renal III type collagen protein expressions were determined by Immunohistochemical method; Kidney MT-1, MT-2 gene expression changes were determined by real-time fluorescence quantitative PCR. Results Afterbook=68,ebook=73fifteen-day oral gavages, the rat renal index of mercuric chloride group and mercurous chloride group increased significantly compared with normal control group and Meng-gen-wu-su-18-Composition processed products group (P<0.01); Rat serum CREA and UREA content in all groups had no significant difference. Renal pathologic examination results showed that glomerulus of low-dose Meng-gen-wu-su-18-Composition Pills group, which was commonly used in clinic, appeared some pathological damages, glomerulus appeared mild hypertrophy, renal tubule epithelia swelled to a low degree. The rat kidney of medium- and high-dose Meng-gen-wu-su-18-Composition Pills groups also appeared some damages and such changes were more significant in mercuric sulfide group, mercuric chloride group and mercurous chloride group. Compared with normal control group and Meng-gen-wu-su-18-Composition processed products group, the mercury kidney volume in mercuric chloride group and mercurous chloride group increased significantly (P<0.01); The renal cell apoptosis rates increased significantly in the groups of mercuric chloride and mercurous chloride (P<0.01); The III type collagen protein expressions increased significantly in the groups of mercuric sulfide, mercuric chloride and mercurous chloride (P<0.05). Compared with normal control group, MT-1 mRNA expressions increased significantly in the group of mercurous chloride (P<0.05); MT-2 mRNA expressions increased significantly in the groups of mercuric chloride and mercurous chloride (P<0.05, P<0.01); Compared with Meng-gen-wu-su-18-Composition processed products group, MT-1 mRNA gene expressions increased significantly in mercurous chloride group (P<0.05). Conclusion Meng-gen-wu-su-18-Composition Pills do not cause significant damage to the rat kidney under the clinical commonly used dose during the 15 days medication.
Key words:Meng-gen-wu-su-18-Composition Pills; mercuric compounds; renal toxicity; rats
收稿日期:(2015-06-18)
基金项目:国家科技支撑计划(2012BAI27B05)
中图分类号:R291.2
文献标识码:A
文章编号:1005-5304(2016)02-0067-06
DOI:10.3969/j.issn.1005-5304.2016.02.019
