十六烷基三甲基溴化铵改性沸石对腐殖酸的吸附性能研究*
2016-03-13张国珍高小波武福平巩师俞
张国珍 高小波 武福平 杨 光 巩师俞
(兰州交通大学环境与市政工程学院,甘肃 兰州 730070)
腐殖酸是动植物残骸腐烂后形成的一类具有复杂结构的大分子有机酸,一般存在于地表水、土壤、河流、有机沉淀物中[1],其分子内含有羧基、羰基等多种活性官能团[2]。腐殖酸主要包括黄腐酸、富里酸和亲水性小分子有机物[3],是环境污染物的重要络合剂或吸附剂,对各种污染物的环境行为、毒性和生物有效性有重要影响。另外,在水厂消毒时,腐殖酸还会产生对人体有较大毒害作用的消毒副产物[4]48。因此,去除水中的腐殖酸对当前水环境治理具有重要的现实意义。
去除水中腐殖酸主要有吸附法、强化絮凝法、光电化学法等[5]。其中,吸附法具有处理高效、费用低廉和操作简单等优点,被认为是去除水中腐殖酸最有效的方法。大孔隙的吸附剂(如活性炭等)在吸附

表1 沸石的主要化学成分
腐殖酸过程中,其孔隙很容易被腐殖酸大分子络合物堵塞[6],进而影响吸附性能。沸石表面孔隙较小,吸附性能受孔隙堵塞影响相对较弱;但由于沸石表面的亲水官能团和负电荷,导致其对腐殖酸的吸附性能不佳[7]。阳离子表面活性剂改性沸石对水中多种污染物有较好的去除效果[8]611-612。因此,选择合适的阳离子表面活性剂对沸石进行改性是必要的。目前,许多学者已经考察了十六烷基三甲基溴化铵(CTAB)改性沸石对水中菲、硝酸盐、铬酸盐、三氯生等的吸附性能[8]611-617,[9-11]。
本研究以CTAB为改性剂,制备了CTAB改性沸石,用于吸附水中的腐殖酸。考察了pH、吸附时间及腐殖酸初始浓度对CTAB改性沸石吸附腐殖酸的影响;分别拟合了吸附等温方程和反应动力学方程;采用扫描电子显微镜(SEM)、X射线光电子能谱仪(XPS)、傅立叶转换红外光谱分析仪(FTIR)对沸石改性前后进行结构表征,以期为水环境治理中腐殖酸的去除提供基础依据。
1 材料及方法
1.1 材料与仪器
沸石为选自甘肃省白银市的天然斜发沸石,呈砖红色,用去离子水反复冲洗后煮沸,于105 ℃烘干后过30目筛备用。沸石的主要化学成分如表1所示。
试剂:CTAB、NaOH、HCl均为分析纯;腐殖酸为化学纯。
仪器:752紫外—可见分光光度计、JSM-5600LV型SEM、VG ESCALAB-210型XPS、IRPrestige-21型FTIR。
1.2 腐殖酸溶液的配制
称取一定质量的腐殖酸,加入去离子水搅拌,用NaOH溶液调节pH为10.0左右,搅拌使其充分溶解,用0.45 μm醋酸纤维酯滤膜过滤后得到腐殖酸溶液。
1.3 腐殖酸浓度的测定
溶液中腐殖酸浓度采用紫外分光光度法测定[12],采用254 nm波长处的吸光度来表征。
1.4 CTAB改性沸石的制备
称取沸石10 g,加入0.02 mol/L的100 mL CTAB溶液中,在恒温振荡器上控制温度为25 ℃、转速为120 r/min,振荡24 h,用去离子水反复冲洗干净,置于90 ℃的恒温干燥箱中烘干,即制得CTAB改性沸石。
1.5 吸附实验
称取1 g CTAB改性沸石,分别投加到100 mL一定腐殖酸初始浓度的溶液中,用HCl溶液调节pH,在温度为25 ℃、转速为200 r/min条件下恒温振荡一段时间后,进行过滤,测定腐殖酸浓度,根据式(1)和式(2)计算吸附容量。
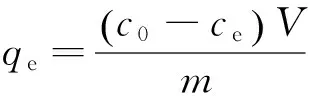
(1)
(2)
式中:qe为平衡吸附容量,mg/g;c0为腐殖酸初始质量浓度,mg/L;ce为腐殖酸平衡质量浓度,mg/L;V为腐殖酸溶液体积,L;m为吸附剂质量,g;qt为腐殖酸t时刻吸附容量,mg/g;ct为腐殖酸t时刻质量浓度,mg/L;t为吸附时间,min。
1.6 热力学和动力学拟合模型
1.6.1 吸附等温方程
Langmuir吸附等温方程和Freundlich吸附等温方程分别见式(3)和式(4)[13]。
(3)
qe=KFce1/n
(4)
式中:qm为最大吸附容量,mg/g;KL为Langmuir吸附常数,L/mg;KF为Freundlich吸附常数,mg1-1/n·L1/n/g;n为经验常数。
1.6.2 反应动力学方程
准一级反应动力学方程和准二级反应动力学方程分别见式(5)和式(6)[14]:
(5)
(6)
式中:k1为准一级反应动力学常数,min-1;k2为准二级反应动力学常数,g/(mg·min)。
1.7 结构表征
采用SEM进行形貌分析,分辨率可达3.5 nm;采用XPS测定元素组成;采用FTIR进行红外光谱分析,波数为400~4 000 cm-1。
2 结果与讨论
2.1 吸附时间的影响
控制腐殖酸初始质量浓度为10 mg/L、pH为7.0,考察吸附时间对CTAB改性沸石吸附腐殖酸的影响,结果如图1所示。由图1可知,CTAB改性沸石对腐殖酸的吸附容量和去除率均随着吸附时间的延长而增加,在吸附时间为180 min时,吸附容量达到0.23 mg/g,去除率达到23.0%。吸附时间大于180 min后,吸附容量和去除率的增长均趋于缓和。为尽可能缩短吸附时间,CTAB改性沸石对腐殖酸的吸附时间选择180 min。
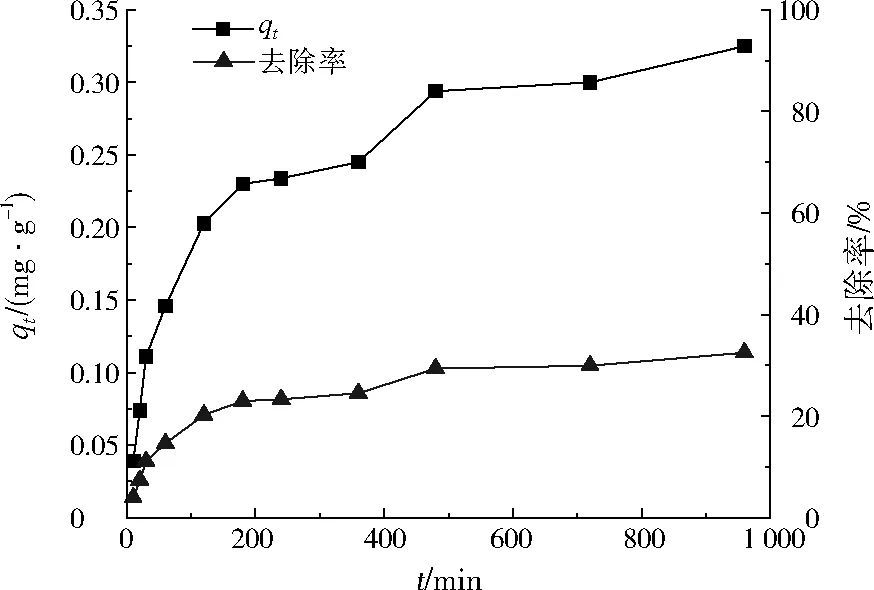
图1 吸附时间对CTAB改性沸石吸附腐殖酸的影响Fig.1 Effect of adsorption time on humic acid adsorption by CTAB modified zeolite
2.2 腐殖酸初始浓度的影响
设置腐殖酸初始质量浓度分别为1、3、5、10、15、20 mg/L,调节pH为7.0,吸附180 min后,考察腐殖酸初始浓度对CTAB改性沸石吸附腐殖酸的影响,结果如图2所示。由图2可知,随着腐殖酸初始质量浓度由1 mg/L增大到20 mg/L,CTAB改性沸石对腐殖酸的吸附容量逐渐增加,从0.04 mg/g增加到0.44 mg/g。这是由于腐殖酸表面带有负电荷,在水中易与CTAB改性沸石带有的正电荷相互作用[15]。而随着腐殖酸初始浓度增加,CTAB改性沸石对腐殖酸的去除率逐渐降低,与ANIRUDHAN等[16]的研究结果一致。综合考虑CTAB改性沸石对腐殖酸的吸附容量和去除率,在腐殖酸的初始质量浓度为10 mg/L时,吸附容量为0.33 mg/g,去除率为32.5%,吸附容量和去除率相对较高,因此选择腐殖酸的初始质量浓度为10 mg/L。

图2 腐殖酸初始质量浓度对CTAB改性沸石吸附腐殖酸的影响Fig.2 Effect of humic acid initial mass concentration on humic acid adsorption by CTAB modified zeolite
2.3 pH的影响
控制腐殖酸初始质量浓度为10 mg/L、吸附时间为180 min,调节pH为3.0、5.0、7.0、9.0、11.0,考察pH对CTAB改性沸石吸附腐殖酸的影响,结果如图3所示。由图3可知,随着溶液pH的增大,CTAB改性沸石对腐殖酸的吸附容量不断减小:pH为3.0时,吸附容量为0.37 mg/g;pH为11.0时,吸附容量为0.09 mg/g。这是由于随着溶液pH的增大,OH-浓度增大,中和了CTAB改性沸石表面的正电荷,使CTAB改性沸石对腐殖酸的吸附容量减小。腐殖酸的去除率随pH的变化与吸附容量的变化一致。由此可见,酸性条件有利于CTAB改性沸石对腐殖酸的吸附。虽然pH为7.0时,CTAB改性沸石对腐殖酸的吸附容量仅为0.16 mg/g,小于pH为3.0时的吸附容量,但考虑到实际水体pH接近中性,故将pH定为7.0。

图3 pH对改性沸石吸附腐殖酸的影响Fig.3 Effect of pH on humic acid adsorption by CTAB modified zeolite
2.4 吸附等温方程的拟合
设置温度为25 ℃、转速为200 r/min、pH为7.0、腐殖酸初始质量浓度分别为1、3、5、10、15、20 mg/L,分别利用Langmuir吸附等温方程和Freundlich吸附等温方程进行非线性拟合(见图4),吸附等温方程相关参数见表2。拟合Langmuir吸附等温方程和Freundlich吸附等温方程时,R2分别为0.998、0.967,说明CTAB改性沸石对腐殖酸的吸附更符合Langmuir吸附等温方程,因此CTAB改性沸石对腐殖酸的吸附机制为单分子层吸附,并且吸附位点是等效的[4]51。

图4 吸附等温方程拟合结果Fig.4 Fitting results of adsorption isotherm equations

Langmiurqm/(mg·g-1)KL/(L·mg-1)R2FreundlichKF/(mg1-1/n·L1/n·g-1)nR20.6380.1470.9980.1021.8310.967
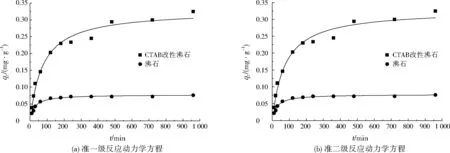
图5 反应动力学方程拟合结果Fig.5 Fitting results of reaction kinetic equations

项目qe/(mg·g-1)准一级反应动力学方程k1/min-1R2准二级反应动力学方程k2/(g·mg-1·min-1)R2沸石0.0825.1180.9840.5130.984CTAB改性沸石0.3374.8590.9780.0410.978
2.5 反应动力学方程的拟合
在温度为25 ℃、转速为200 r/min、腐殖酸初始质量浓度为10 mg/L,pH为7.0条件下,分别利用准一级反应动力学方程和准二级反应动力学方程对沸石和CTAB改性沸石吸附腐殖酸的过程进行非线性拟合(见图5),反应动力学方程相关参数见表3。k1、k2能反映沸石或CTAB改性沸石对腐殖酸的吸附速率,k1、k2越大,说明对腐殖酸的吸附速率越快。由表3可知,利用准一级反应动力学方程和准二级反应动力学方程拟合时,CTAB改性沸石对腐殖酸的吸附速率明显快于沸石。拟合准一级反应动力学方程和准二级反应动力学方程时,沸石的R2均为0.984,CTAB改性沸石的R2均为0.978,说明沸石或CTAB改性沸石吸附腐殖酸的过程均可利用准一级反应动力学方程或准二级反应动力学方程进行拟合。CTAB改性沸石对腐殖酸的平衡吸附容量明显大于沸石,可以看出CTAB改性沸石对腐殖酸的吸附性能优于沸石。

图6 SEM分析结果Fig.6 Results of SEM analysis
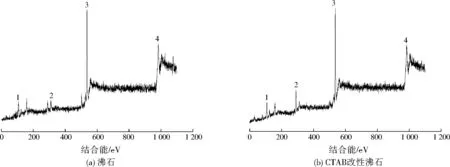
注:1—Si;2—C;3—O;4—Na。图7 XPS分析结果Fig.7 Results of XPS analysis
2.6 结构表征
2.6.1 SEM分析
对沸石和CTAB改性沸石进行SEM分析,结果如图6所示。由图6可知,沸石表面和CTAB改性沸石表面均凹凸不平,但CTAB改性沸石的沟槽、凹坑较少,且表面颜色较浅,说明CTAB改性沸石已负载CTAB,但未引起晶体结构变化。
2.6.2 XPS分析
对沸石和CTAB改性沸石进行XPS分析,结果如图7和表4所示。CTAB改性沸石中C占22.43%,相比沸石中C所占比例明显增加。这主要是由于CTAB中含有大量季铵型阳离子,而沸石经CTAB改性的过程中,季铵型阳离子通过离子交换作用将官能团表面的C附着于沸石表面,这有利于提高CTAB改性沸石对腐殖酸的吸附性能。
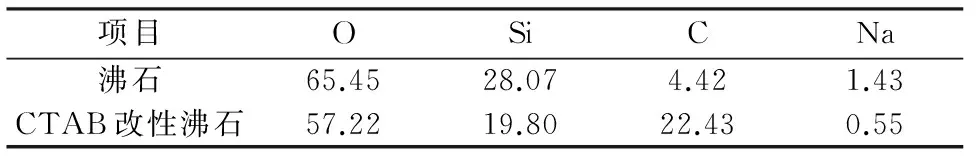
表4 主要元素的质量分数
2.6.3 FTIR分析
对沸石、CTAB改性沸石和吸附实验后的CTAB改性沸石进行FTIR分析,结果如图8所示。由图8可知,CTAB改性沸石相比沸石,在2 850、2 920 cm-1处出现甲基和亚甲基的伸缩振动吸收峰,表明CTAB改性沸石已负载CTAB,与SEM分析结果(见图6)一致。对于吸附实验后的CTAB改性沸石,3 500~3 700 cm-1处有大量的锯齿峰,源于醇和酚的羟基伸缩振动;2 200~2 400 cm-1处出现较宽的吸收峰,源于苯酚、醇与羧酸的羟基伸缩振动;1 500~2 000 cm-1处的锯齿峰源于羧酸、酰胺、酯等的羰基伸缩振动。因此,经过吸附实验,腐殖酸已大量被CTAB改性沸石吸附。

图8 FTIR分析结果Fig.8 Results of FTIR analysis
3 结 论
(1) 在温度为25 ℃、转速为200 r/min的条件下,选择pH为7.0、腐殖酸初始质量浓度为10 mg/L、吸附时间为180 min,CTAB改性沸石对腐殖酸的吸附容量为0.16 mg/g。
(2) 吸附等温方程的拟合结果表明,Langmuir吸附等温方程比Freundlich吸附等温方程的拟合效果更好,说明CTAB改性沸石对腐殖酸的吸附机制为单分子层吸附。准一级反应动力学方程和准二级反应动力学方程均可以描述CTAB改性沸石对腐殖酸的吸附。
(3) 与沸石相比,CTAB改性沸石中C所占比例明显增加,改性效果良好;CTAB改性沸石上出现了亚甲基、甲基的伸缩振动吸收峰,说明CTAB改性沸石已负载CTAB;吸附实验后的CTAB改性沸石出现羟基与羰基伸缩振动吸收峰,说明腐殖酸已被大量吸附。
[1] 曾宪成.腐植酸从哪里来,到哪里去[J].腐植酸,2012(4):1-10.
[2] 王海涛,朱琨,魏翔,等.腐殖酸钠和表面活性剂对黄土中石油污染物解吸增溶作用[J].安全与环境学报,2004,4(4):52-55.
[3] 王津南,李爱民,张龙,等.吸附法去除水体中腐殖酸的研究进展[J].环境污染与防治,2008,30(8):73-74.
[4] 方金鹏,张盼月,曾光明,等.改性斜发沸石吸附水中腐殖酸的研究[J].中国给水排水,2008,24(23).
[5] 王亚军,马军.水体环境中天然有机质腐殖酸研究进展[J].生态环境学报,2012,21(6):1155-1165.
[6] SUMMERS R S,ROBERTS P V.Activated carbon adsorption of humic substances:Ⅱ.size exclusion and electrostation interactions[J].Journal of Colloid & Interface Science,1988,122(2):382-397.
[7] 赵艳玲,闫凤美,张军丽,等.沸石的交联壳聚糖改性及对腐殖酸的吸附研究[J].化学世界,2014,55(7):396-397.
[8] 李佳,林建伟,詹艳慧,等.溴化十六烷基吡啶改性沸石对水中菲的吸附作用[J].环境科学,2014,35(2).
[9] 李小建,王德汉.改性沸石对水体中硝酸盐的吸附机理及其残渣的资源化利用[J].中国环境管理干部学院学报,2011,21(2):13-17.
[10] 张宏华,林建伟.HDTMA改性沸石对铬酸盐的吸附作用研究[J].浙江工业大学学报,2010,38(5):494-498.
[11] 何敏祯,胡勇有,雷超,等.HDTMA改性沸石对三氯生的吸附特性研究[J].环境科学学报,2013,33(1):20-28.
[12] ZHOU Qunhui,CABANISS S E,MAURICE P A.Considerations in the use of high-pressure size exclusion chromatography (HPSEC) for determining molecular weights of aquatic humic substances[J].Water Research,2000,34(14):3505-3514.
[13] 马伟.固水界面化学与吸附技术[M].北京:冶金工业出版社,2011.
[14] 钱吉彬,杨朗,张华,等.镇江斜发沸石对氨氮的吸附动力学及热力学研究[J].环境工程学报,2011,5(2):327-330.
[15] 杨慧芬,张伟娜,胡瑞娟.十六烷基三甲基溴化铵改性沸石对水中Cr(Ⅵ)的吸附去除率[J].硅酸盐学报,2010,38(11):2144-2146.
[16] ANIRUDHAN T S,RAMACHANDRAN M.Surfactant-modified bentonite as adsorbent for the removal of humic acid from wastewaters[J].Applied Clay Science,2007,35(3):276-281.
