Fenton氧化技术修复六氯环己烷污染土壤特性研究*
2016-03-12倪茂飞俞哲彬杨延梅黄启飞田书磊
倪茂飞 俞哲彬 李 娜 杨延梅 杨 帅 李 川 黄启飞 田书磊#
(1.重庆工商大学环境与资源学院,重庆 400067; 2.中国环境科学研究院固体废物污染控制技术研究所,北京 100012; 3.东北大学秦皇岛分校资源与材料学院,河北 秦皇岛 066004;4.重庆交通大学河海学院,重庆 400074)
六氯环己烷(HCHs)作为一种持久性有机污染物(POPs),已被国际癌研究机构确定为2B致癌物质,其毒性反应会对动物的肝肾器官、中枢神经造成严重的影响,于2011年列入了《关于持久性有机污染物的斯德哥尔摩公约》管控名单。而在20世纪70年代,中国HCHs的生产和使用量大,截至1983年停产时,其累积生产量已达到490万t[1],占全世界生产总量的33%[2]。众多学者已对HCHs在土壤中的残留量进行了研究[3-9],结果表明,中国西南地区HCHs残留量较大。农田土壤中的HCHs残留质量浓度为4.35~394.07 ng/g[10]。因此,农用土壤和工业土壤中农药类POPs污染备受关注[11-12]。

表1 原土壤理化性质背景值
目前,常见的土壤修复技术包括物理、化学和生物修复技术,如换土/客土法、固定/稳定化和微生物修复等技术。但这些修复技术一般存在场地要求高、费用高、周期长、效率低、不能根本治理等缺点,在工程实例中已逐渐被新兴的修复技术所取代。近年来,Fenton氧化技术以其能耗低、后处理工程简单和环境友好等特点,在土壤修复研究中得到大量的关注[13-17]。然而,却鲜有关于Fenton氧化剂对同一物质不同异构体特性研究的报道,因此有必要对这方面研究进行补充。
本研究以中国西南地区某废弃HCHs生产企业的污染土壤作为研究对象,分析了Fenton氧化时间、催化剂种类、催化剂投加量和H2O2投加量对HCHs修复效果的影响,并对比了同等条件下,4种HCHs异构体(α-HCH、β-HCH、γ-HCH和δ-HCH)的去除效果。为Fenton氧化修复典型POPs污染土壤提供了基础方法理论,同时也为中国履行《关于持久性有机污染物的斯德哥尔摩公约》提供技术支撑。
1 材料与方法
1.1 试验用污染土壤制备
试验用污染土壤取自中国西南地区某废弃HCHs生产企业,土壤类型为紫色土,其基本理化性质见表1。将土壤在冷冻干燥机中进行冷冻干燥,充分混匀并除去杂质,之后将其研磨搅拌并过80目筛待用。该场地曾是西南地区大型农药生产企业,历史上对HCHs、双氯苯基三氯乙烷(DDTs)进行大规模集中生产,并于20世纪80年代停产,厂区污染物在土壤中残留数年。
土壤理化性质及分析方法如下:(1)土壤颗粒密度根据《森林土壤土粒密度的测定》(LY/T 1224—1999)进行测定;(2)土壤容重根据《土工试验方法标准》(GB/T 50123—1999)中的环刀法进行测定;(3)含水率根据《森林土壤含水量的测定》(LY/T 1213—1999)中烘干法进行测定;(4)土壤总孔隙度根据LY/T 1224—1999和GB/T 50123—1999中的环刀法进行测定;(5)pH根据《土壤pH的测定》(NY/T 1377—2007)进行测定;(6)土壤渗透系数根据《森林土壤渗滤率的测定》(LY/T 1218—1999)进行测定;(7)土壤有机质根据《土壤有机质测定法》(NY/T 85—1988)进行测定。
1.2 试剂与仪器
1.2.1 主要仪器
GC-2010型高效气相色谱仪;MGS-2200型氮吹仪;SC-3610型离心机;KQ5200DE型数控超声波清洗仪;RE52CS-1旋转蒸发器;FD-1A-50型冷冻干燥机;KJDHZ-82型恒温水浴振荡箱;AG-285型电子分析天平。
1.2.2 主要试剂
佛罗里硅土;丙酮、正己烷、二氯甲烷、无水硫酸钠、Fe2O3粉末、Fe2(SO4)3晶体、FeSO4·7H2O晶体、铁粉,均为分析纯;H2O2溶液(质量分数为30%)。
1.3 试验方法
所有样品均设置3组平行,试验结果取其算术平均值。
1.3.1 样品添加
用电子分析天平准确称取200 g已制备好的污染土壤,加入三角瓶中。向其中依次加入催化剂和H2O2溶液,之后将三角瓶置于25 ℃、150 r/min恒温水浴振荡箱中振荡。反应一定时间后,取样测定土壤中HCHs的残留浓度。
1.3.2 试验条件设置
(1) Fenton氧化时间试验
以FeSO4·7H2O晶体为催化剂,当催化剂投加量为5%(质量分数)、H2O2投加量为20 g/mL时进行试验。每隔10 min对污染土壤中的HCHs进行测定,直至去除效果稳定为止。
(2) 催化剂种类试验
当催化剂投加量为5%、H2O2投加量为20 g/mL时进行100 min试验,考察Fe2O3粉末、Fe2(SO4)3晶体、FeSO4·7H2O晶体、铁粉等4种催化剂对污染土壤中HCHs的去除效果。
(3) 催化剂投加量试验
以FeSO4·7H2O晶体为催化剂,当H2O2投加量为20 g/mL时进行100 min试验,考察催化剂投加量(1%、2%、3%、4%和5%)对污染土壤中HCHs的去除效果。
(4) H2O2投加量试验
以FeSO4·7H2O晶体为催化剂,当催化剂投加量为5%时进行100 min试验,考察H2O2投加量(10、15、20 g/mL)对污染土壤中HCHs的去除效果。
1.3.3 数据处理
以HCHs去除率(η,%)表征Fenton氧化技术对污染土壤中HCHs的去除效果,并按式(1)计算。
(1)
式中:c0为原土壤中HCHs质量浓度,ng/g;c为Fenton氧化后HCHs质量浓度,ng/g。
1.4 分析方法
1.4.1 样品预处理
样品提前采用超声提取。称取10 g样品加入50 mL聚四氟乙烯离心管中,再加入30 mL正己烷/丙酮提取液(体积比为1∶1),提前超声30 min(35 ℃),离心,将上层提取液转入250 mL圆底烧瓶,重复提取3次,合并提取液,并采用旋转蒸发器浓缩至1 mL(35 ℃)。
1.4.2 样品提取
样品采用硅酸镁层析柱净化。硅酸镁层析柱:在带有筛孔的层析柱(内径1 cm,长35 cm)自上而下依次装填无水硫酸钠2 cm、活化佛罗里硅土10 cm、无水硫酸钠2 cm,边加填料边用洗耳球敲击层析柱以确保装填密实。使用前用50 mL正己烷预淋洗,避免填料中存在明显的空气。待正己烷刚好淹没硫酸钠层时,关闭柱阀。将浓缩后的样品加入硅酸镁层析柱,过柱后用50 mL正己烷/二氯甲烷(体积比4∶1)洗脱,洗脱液浓缩并经高纯氮气吹干,用正己烷定容至1 mL,上机进行气相色谱分析。
1.4.3 气相色谱测定条件
进样器温度280 ℃。升温程序:初始温110 ℃,保持1 min,以10 ℃/min速度升至180 ℃,保持1 min,再以6 ℃/min速度升至210 ℃,保持1 min,然后以10 ℃/min速度升至300 ℃,保持1 min。载气:高纯氦气(纯度>999.999%),柱流量1.0 mL/min。进样器模式:分流体积比5∶1,进样量1 μL。
2 结果与讨论
2.1 Fenton氧化时间对HCHs去除效果的影响
Fenton氧化时间对HCHs去除效果的影响如图1所示。由图1可知,刚开始的一段Fenton氧化时间内,4种HCHs异构体的去除率都是随着Fenton氧化时间的延长而逐渐增大,当Fenton氧化反应超过40 min后,4种HCHs异构体的去除率则增加得较缓慢甚至趋于稳定,其中β-HCH的去除率最高,最终稳定时间为100 min,其去除率为96.7%;α-HCH次之,Fenton氧化时间在70 min后达到稳定,其去除率为79.9%;γ-HCH和δ-HCH分别在Fenton氧化时间为60、80 min后达到稳定,其去除率分别为54.8%和51.8%。

图1 Fenton氧化时间对HCHs去除效果的影响Fig.1 Effects of the oxidation time on the HCHs removal efficiency
由图1还可知,不同HCHs异构体的反应速率和去除效果存在差异,但HCHs的去除率曲线保持较好的一致性。这说明,各种HCHs异构体具有相同的去除机制。试验中,β-HCH稳定性最强,而γ-HCH的稳定性最弱[18-20],但其去除效果却刚好相反。这证明,Fenton氧化机制中存在与光、热稳定性和异构能力无关的元素。SAWYER等[21]认为,是由于亲核加成所形成的原始反应中间体[LmFe2+O—OH]对环烃类有机物进行配位反应所造成的。KREMER等[22]进一步研究显示,其中间产物为离子对配合物(Ⅰ)和络离子(Ⅱ),方程式如式(2)至式(4)所示,因而其Fe3+/H2O2体系有可能是降解HCHs的另一因素。
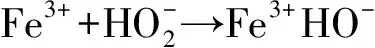
(2)
Fe3+HO-(Ⅰ)+O·→Fe(HO2)2+(Ⅱ)
(3)
Fe(HO2)2+(Ⅱ)+H2O2→Fe3++OH-+H2O+O2
(4)
为保证HCHs异构体均反应完全,本试验的Fenton氧化时间最佳为100 min。
2.2 催化剂种类对HCHs去除效果的影响
催化剂种类对HCHs去除效果的影响如图2所示。由图2可见,FeSO4·7H2O晶体对β-HCH的去除率最高,为96.7%;α-HCH和γ-HCH也均是在FeSO4·7H2O晶体作催化剂条件下获得最高去除率,分别为79.1%和54.8%。这说明,FeSO4·7H2O晶体结构可以更好地和H2O2接触,产生具有强氧化效果的HO·[23]。但是,所有催化剂对δ-HCH的去除率相差不大,在51.8%~53.1%内。这说明,Fenton氧化对δ-HCH的去除已经达到化学平衡,去除率不再随HO·产生量的增加而增大。

图2 催化剂种类对HCHs去除效果的影响Fig.2 Effects of the various catalysts on the HCHs removal efficiency
不同催化剂种类对HCHs的去除效果存在一定差异,其中Fe2+去除效果最佳,而Fe3+和Fe0对不同HCHs异构体的去除率并不一致,证明Fenton试剂中与H2O2的主要还原剂为Fe2+,而Fe3+和Fe0可以延长H2O2寿命,其催化效率依赖于在土壤空隙水中的溶解率和本身的存在形态[24],反应方程如式(5)至式(8)所示。
HO·+HO2→H2O+O2
(5)
HO·+Fe2+→Fe3++OH-
(6)
HO·+H2O2→H2O+HO2·
(7)
HO·+HO·→H2O2
(8)
在足量催化剂和H2O2条件下HCHs的去除率存在平衡点。LIN等[25]认为,H2O2可以与氧化物表面HO·发生副反应形成内圈层化合物,从而抑制HO·的生成,而异构体相互竞争进一步增大了该反应的速率,导致HO·与Fe2+接触量不断减少,促使Fenton反应达到平衡。该试验最佳催化剂为FeSO4·7H2O晶体。
2.3 催化剂投加量对HCHs去除效果的影响
催化剂投加量对HCHs去除效果的影响如图3所示。由图3可见,当催化剂投加量为4%时,HCHs的去除率开始稳定。α-HCH和δ-HCH去除率在催化剂投加量为4%时达到最高,分别为79.1%和51.8%,继续增大催化剂投加量,其去除率变化不大。这说明,对于α-HCH和δ-HCH,在催化剂投加量为4%时HO·的氧化效果开始饱和,过量的HO·不被其利用。β-HCH和γ-HCH去除率在催化剂投加量为5%时达到最高,分别为96.7%和54.8%,相比于催化剂投加量为4%时去除率增幅不大。这说明,催化剂投加量为4%时HCHs的Fenton氧化反应已经达到化学平衡,过量的Fe2+会与HO·反应[26]或使H2O2迅速分解[27],从而影响去除率。当催化剂投加量为1%时,β-HCH的去除率最低,为20.0%,随着催化剂投加量的增大,其去除率迅速增加;而此时α-HCH去除率最高,为38.6%。说明催化剂的利用率存在差异,这与土壤类型、污染物种类及其浓度有关[28]。为考虑各种HCHs异构体充分反应且HCHs总的去除率最大,本试验催化剂投加量最佳为5%。
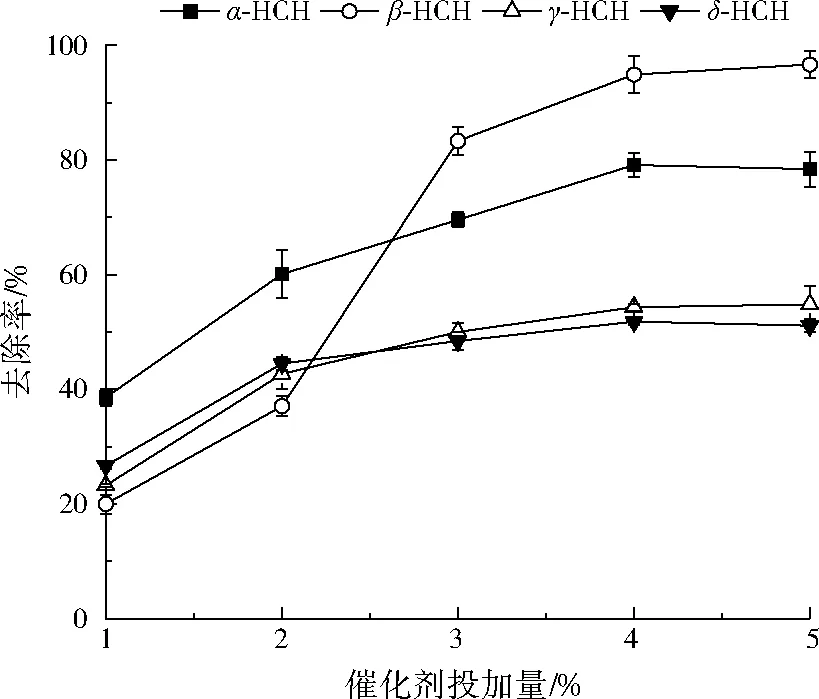
图3 催化剂投加量对HCHs去除效果的影响Fig.3 Effects of the catalyst quantity on the HCHs removal efficiency
2.4 H2O2投加量对HCHs去除效果的影响
H2O2投加量对HCHs去除效果的影响如图4所示。
由图4可知,当H2O2投加量为10 g/mL时,各HCHs异构体已经具有了一定的去除率,其中β-HCH去除率最高,为51.7%。继续增大H2O2投加量至15 g/mL时,β-HCH和δ-HCH的去除率已接近最大值,分别为95.5%和51.0%,但是α-HCH和γ-HCH去除率仍会因H2O2投加量的增大而明显增大,分别为65.4%和47.2%。说明增大H2O2投加量对HCHs去除具有促进作用,但不同HCHs异构体对H2O2的需求量存在差异。当H2O2投加量为20 g/mL时,各HCHs异构体的去除率均到达最高,α-HCH、β-HCH、γ-HCH和δ-HCH去除率分别为79.1%、96.7%、54.8%和51.8%。可见,增大H2O2投加量可促进HCHs异构体的去除。HCHs去除率在H2O2投加量为15~20 g/mL时迅速稳定,说明过量的HO·被H2O2消耗较少,因为它与Fe2+的反应速率较快,这与MATER等[29]的研究结果相似。而投入过量的H2O2时,会发生式(7)的反应,降低其Fenton氧化效率[30]。
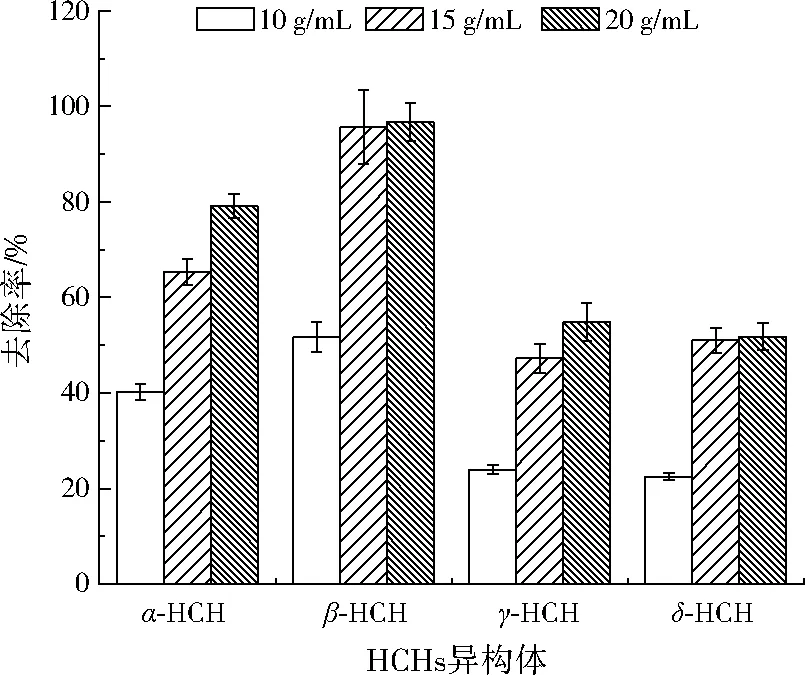
图4 H2O2投加量对HCHs去除效果的影响Fig.4 Effects of the H2O2 quantity on the HCHs removal efficiency
因此,综合考虑成本及效率等因素,本试验最佳H2O2投加量为20 g/mL。
2.5 HCHs的Fenton氧化去除率比较
对比研究HCHs异构体在最优条件下的去除效果,分析评价基于Fenton氧化技术修复HCHs污染土壤的可行性、经济性和环境友好性,结果如表2所示。
如表2所示,在以FeSO4·7H2O晶体为催化剂、
Fenton氧化时间为100 min、催化剂投加量为5%、H2O2投加量为20 g/mL的最优条件下,各HCHs异构体去除率已接近独立试验最大值,其中α-HCH和δ-HCH稍低于单因素考察试验最大值79.9%和51.8%,但保证了HCHs总的去除率最大,且简化了工艺过程,无需分类投加。在最优条件下,4种HCHs异构体的去除效果存在差异,其结果为β-HCH(96.7%)>α-HCH(79.2%)>γ-HCH(54.8%)>δ-HCH(51.3%)。
由此可见,该试验条件温和、药品及设备易于管理且经济实用、Fenton氧化时间短且去除率高,用Fe2+和H2O2进行反应,其产物绿色安全、不易引起二次污染。因此,其具有较高的可行性、经济性和环境友好性,是一种优秀的HCHs污染土壤修复方法。今后需进一步对其工艺条件进行优化,将其投入到大规模的原位土壤修复工作中,为HCHs污染场地修复提供理论依据和技术支持。
3 结 论
(1) HCHs可通过Fenton氧化降解,其去除率与Fenton氧化时间、催化剂种类、催化剂投加量以及H2O2投加量有关。
(2) 延长Fenton氧化时间可以促进HCHs的去除,其去除率在100 min后达到稳定;Fe2+的催化效率优于Fe3+和Fe0,最佳催化剂为FeSO4·7H2O晶体;增大催化剂投加量可促进HCHs的去除,催化剂投加量最佳为5%;较高投加量的H2O2有利于产生更多的HO·,H2O2投加量最佳为20 g/mL。
(3) Fenton氧化对HCHs的去除机制具有一致性,但不同HCHs异构体的去除率存在差异。在以FeSO4·7H2O晶体为催化剂、Fenton氧化时间为100 min、催化剂投加量为5%、H2O2投加量为20 g/mL的最优条件下,β-HCH去除率最高(96.7%),α-HCH去除率次之(79.2%),γ-HCH和δ-HCH去除率分别为54.8%和51.3%。
(4) Fenton氧化技术是一种优秀的HCHs污染土壤修复技术。通过对其试验条件及HCHs异构体的去除效果进行比较,可知其具有较高的可行性、经济性和环境友好性,具有较大的HCHs污染场地原位修复应用前景。

表2 最优条件下HCHs异构体的去除效果
[1] LI Jun,ZHANG Gan,QI Shihuan,et al.Concentrations,enantiomeric compositions,and sources of HCH,DDT and chlordane in soils from the Pearl River Delta,South China[J].Science of the Total Environment,2006,372(1):215-224.
[2] HUA Xiaomei,SHAN Zhengjun.The producticn and application of pestidices and factor analysis of their pollution in environment in China[J].Advances in Environmental Science,1996,2(3):33-45.
[3] 蒋煌峰,王学彤,孙阳昭,等.上海市城区土壤中有机氯农药残留研究[J].环境科学,2010,31(2):409-414.
[4] 赵炳梓,张佳宝,朱安宁,等.黄淮海地区典型农业土壤中六六六(HCH)和滴滴涕(DDT)的残留量研究Ⅰ.表层残留量及其异构体组成[J].土壤学报,2005,42(5):761-768.
[5] 杨国义,万开,张天彬,等.广东省典型区域农业土壤中六六六(HCHs)和滴滴涕(DDTs)的残留及其分布特征[J].环境科学研究,2008,21(1):113-117.
[6] 朱小龙,魏小芳,陈其思,等.典型农药生产场地DDTs和HCHs残留水平及垂直分布特征[J].地球与环境,2014,42(4):489-495.
[7] 潘峰,王利利,赵浩,等.某林丹生产企业搬迁遗留场地土壤中六六六的残留特征[J].环境科学,2013,34(2):705-711.
[8] 燕云仲,薛南冬,周玲莉,等.挖掘扰动对污染场地空气中六六六、滴滴涕分布的影响[J].环境科学研究,2014,24(6):642-648.
[9] 姬艳梅,王小文,梁宝翠,等.土壤中有机氯农药的污染状况与生态毒性研究[J].农业灾害研究,2011(2):41-43.
[10] PEREIRA R C,CAMPS ARBESTAIN M,GARRIDO B R,et al.Behaviour of α-,β-,γ-,and δ-hexachlorocyclohexane in the soil-plant system of a contaminated site[J].Environmental Pollution,2006,144(1):210-217.
[11] LI Guogang,LI Hongli.The present status of persistent organic pollutants (POPs) environmental monitoring in China[J].Environmental Monitoring in China,2004,20(4):53-60.
[12] ZHU Youfeng,LIU Hui,XI Zhiquan,et al.Organochlorine pesticides (DDTs and HCHs) in soils from the out skirts of Beijing,China[J].Chemosphere,2005,60(6):770-778.
[13] 徐金兰,雷绒娟,邓海鑫,等.Fenton改性对土壤有机物氧化及修复石油污染土壤的影响[J].石油学报,2014,30(6):1113-1118.
[14] 曾华冲,杨利芝,徐宏勇,等.Fenton试剂氧化法修复2,4-二氯酚污染土壤的研究[J].生态环境,2008,17(1):221-226.
[15] WEEKS K R,BRUELL C J,MOHANTY N R,et al.Use of Fenton’s reagent for the degradation of TCE in aqueous systems and soil slurries[J].Soil and Sediment Contamination,2000,9(4):331-345.
[16] AMARANTE D.Applying in situ chemical oxidation several oxidizers provide an effective first step in groundwater and soil remediation[J].Pollution Engineering,2000,32(2):40-42.
[17] TSAI T T,KAO C M,YEH T Y,et al.Remediation of fuel oil-contaminated soils by a three-stage three-stage treatment system[J].Environmental Engineering Science,2009,26(3):651-659.
[18] 庄相宁,许端平,谷庆宝.土壤中HCHs热解吸动力学研究[J].安全与环境学报,2014,14(3):251-255.
[19] KUNKEL A M,SEIBERT J J,ELLIOTT L J,et al.Remediation of elemental mercury using in situ thermal desorption (ISTD)[J].Environmental Science and Technology,2006,40(7):2384-2389.
[20] 张新英.典型POPs农药污染土壤热解吸修复技术研究[D].阜新:辽宁工程技术大学,2012.
[21] SAWYER D T,SOBKOWIAK A,MATSUSHITA T. Metal [MLx:M=Fe,Cu,Co,Mn]/hydroperoxide induced activation of dioxygen for the oxygenation of hydrocarbons:oxygenated Fenton chemistry[J].Acc. Chem. Res.,1996,29(9):409-416.
[22] KREMER M L,STEIN G.The catalytic decomposition of hydrogen peroxide by ferric perchlorate[J]. Transactions of the Faraday Society,1959,55(6):959-973.
[23] 刘安安.电动力-Fenton氧化法修复苯酚污染土壤研究[D].长春:吉林大学,2013.
[24] 燕启社,孙红长,周长波,等.类Fenton氧化在污染土壤中的应用[J].生态环境,2008,17(1):216-220.
[25] LIN S S,GUROL M D.Catalytic decomposition of hydrogen peroxide on iron oxide:kinetics,mechanism,and implications[J].Environmental Science and Technology,1998,32(10):1417-1423.
[26] 乔瑞平,漆新华,孙承林,等.Fenton试剂氧化降解微囊藻毒素-LR[J].环境化学,2007,26(5):614-617.
[27] 张会琴,郑怀礼,廖宏头,等.微波促使类Fenton反应催化氧化降解染料吖啶橙[J].工业水处理,2010,30(8):54-57.
[28] BACIOCCHI R,BONI M R,APRILE L.Hydrogen peroxide lifetime as an indicator of the efficiency of 3-chlorophenol Fenton’s and Fenton-like oxidation in soils[J].Journal of Hazardous Materials,2003,96(2/3):305-329.
[29] MATER L,ROSA E V C,BERTO J,et al.A simple methodology to evaluate influence of H2O2and Fe2+concentrations on the mineralization and biodegradability of organic compounds in water and soil contaminated with crude petroleum[J].Journal of Hazardous Materials,2007,149(2):379-386.
[30] 朱濛,涂晨,胡学锋,等.Fenton法和类Fenton法降解土壤中的二苯砷酸[J].环境化学,2015,34(6):1078-1085.
