通脉丸有效组分配伍浓缩液在大鼠体内的毒代动力学研究*
2016-03-06陈天朝刘瑞霞于兰兰
陈天朝,刘瑞霞,于兰兰
(1. 河南中医学院第一附属医院 郑州 450000;2. 河南中医学院药学院 郑州 450008)
通脉丸有效组分配伍浓缩液在大鼠体内的毒代动力学研究*
陈天朝1**,刘瑞霞2,于兰兰2
(1. 河南中医学院第一附属医院 郑州 450000;2. 河南中医学院药学院 郑州 450008)
目的:本研究通过通脉丸方中各味中药有效组分提取液的不同配伍,研究其内部的减毒机制,为其安全性评价提供依据。方法:分别灌胃给予大鼠8组通脉丸有效组分不同配伍浓缩液,采用UPLC检测给药后不同时间点大鼠体内士的宁的血药浓度,应用SPSS软件拟合毒代动力学参数。结果:士的宁在大鼠体内符合非房室模型,第1-8组毒代动力学参数AUC(0-t)分别为10.271 9±3.224 7、8.806 1±1.245 8、13.496 6±4.582 5、11.031 5±2.873 2、9.929 1±1.499 7、5.042 0±2.171 2、15.136 2±6.353 3、5.751 5±1.492 8 μg·h·mL-1。通脉丸原方与其余配伍方在大鼠体内产生的毒性不同,AUC减少率大小顺序为第6组>第8组>第2组>第5组>第1组>第4组>第3组>第7组,“丹参、赤芍、琥珀、蜂蜜”减毒作用最强。结论:UPLC分析方法适用于大鼠血浆士的宁的测定。
配伍减毒 士的宁 毒代动力学 药动学参数
通脉丸是由附子、黄芪、两头尖、制马钱子、当归、赤芍、甘草等中药组成的纯中药制剂,已有30余年的使用历史[1]。具有祛风湿、通经络、消肿痛之功效,用于治疗血栓闭塞性脉管炎、动脉硬化闭塞症、风寒湿痹、四肢惊挛等肢体缺血性疾病,临床疗效显著[2]。
通脉丸方中毒性药材如马钱子是影响通脉丸安全有效的关键,马钱子的主要成分为生物碱,其中士的宁占总生物碱的35%-50%,其次为马钱子碱。马钱子碱是其镇痛的主要成分,士的宁是其主要毒性成分[3]。目前的研究显示,小鼠灌服给药,士的宁的LD50是马钱子碱的1/71.25,对中枢神经系统和免疫系统及肾脏有毒性作用,因士的宁的治疗剂量和中毒剂量比较接近,其吸收速率大于消除速率,长期、大量服用马钱子就会造成体内短时间内含量过高而引起中毒[4]。因此本研究以通脉丸方中士的宁作为指标性成分进行其在大鼠体内的毒代动力学研究,得到相关的药动学参数,探讨其体内动力学过程的差异,从数据角度对通脉丸的安全性、减毒机制以及体内释放过程进行客观分析。
1 材料
1.1 仪器与试剂
H-Class 超高效液相色谱仪(美国Waters公司);ZRS-8C智能溶出试验仪(天津大学无线电厂);TGL-16B离心机(上海安亭科学仪器厂);QL-901混匀仪(海门市其林贝尔仪器制造有限公司);BF-2000氮气吹干仪(北京八方世纪科技有限公司);Sartorius-CP225D电子天平(德国赛多利斯);DT300A电子天平(上海医用激光仪器厂);摩尔智能超纯水器 (重庆摩尔水处理设备有限公司);KQ-100DE型数控超声波清洗器(昆山市超声仪器有限公司);士的宁对照品(中国药品生物制品检定所,批号:110705-200306,纯度大于98%);磷酸二氢钾(天津市永大化学试剂有限公司,批号:20100110);庚烷磺酸钠(山东禹王实业有限公司,批号:2010073001);甲醇、乙腈、磷酸均为色谱纯(北京迪马欧泰科技发展中心)。
1.2 实验药材
通脉丸方中各味中药有效组分提取液,由课题组成员徐丽军提供。处方所用药材由河南中医学院第一附属医院段晓颖主任药师鉴定,结果为:①制附子:毛茛科植物乌头Aconitum carmichaeliiDebx.的子根炮制品;批号:110107,产地:广西;②黄芪:豆科植物蒙古黄芪Astragalusmembranaceus(Fisch.) Bge.var.Mongholicus(Bge.) Hsiao的干燥根;批号:110601,产地:内蒙古;③两头尖:毛茛科植物多被银莲花Anemone raddeana Regel的干燥根茎;批号:120308,产地:东北;④马钱子:马钱科植物马钱Strychnosnux-vomica L.的干燥成 熟 种 子;批号:111101,产地:广西;⑤当归:伞形科植物当归Angelica sinensisOliv.Diels的 根;批 号:110701,产地:甘肃;⑥赤芍:毛茛科植物芍药Paeonialactiflora Pall的干燥根;批号:120310,产地:河北;⑦丹参:唇形科植物丹参Salvia miltiorrhizaBge.的干燥根及根茎;批号:120303,产地:安徽;⑧陈皮:芸香科植物橘Citrus reticulata Blanco的干燥成熟果皮;批号:120303,产地:浙江;⑨洋金花:茄科植物白花曼陀罗Daturametel L.的干燥花;批号:120320,产地:江苏;⑩甘草:豆科植物甘草GlycyrrhizauralensisFisch.的干燥根和根茎;批号:120303,产地:东北;⑪琥珀:古代松科属植物的树脂埋藏地下后年久凝结而成的化石样物质;批号:110812,产地:云南。
1.3 实验动物
清洁级Wistar大鼠,体质量300±30 g,雌雄各半,由山东鲁抗医药股份有限公司提供,许可证编号:SCXK(鲁)20080002。
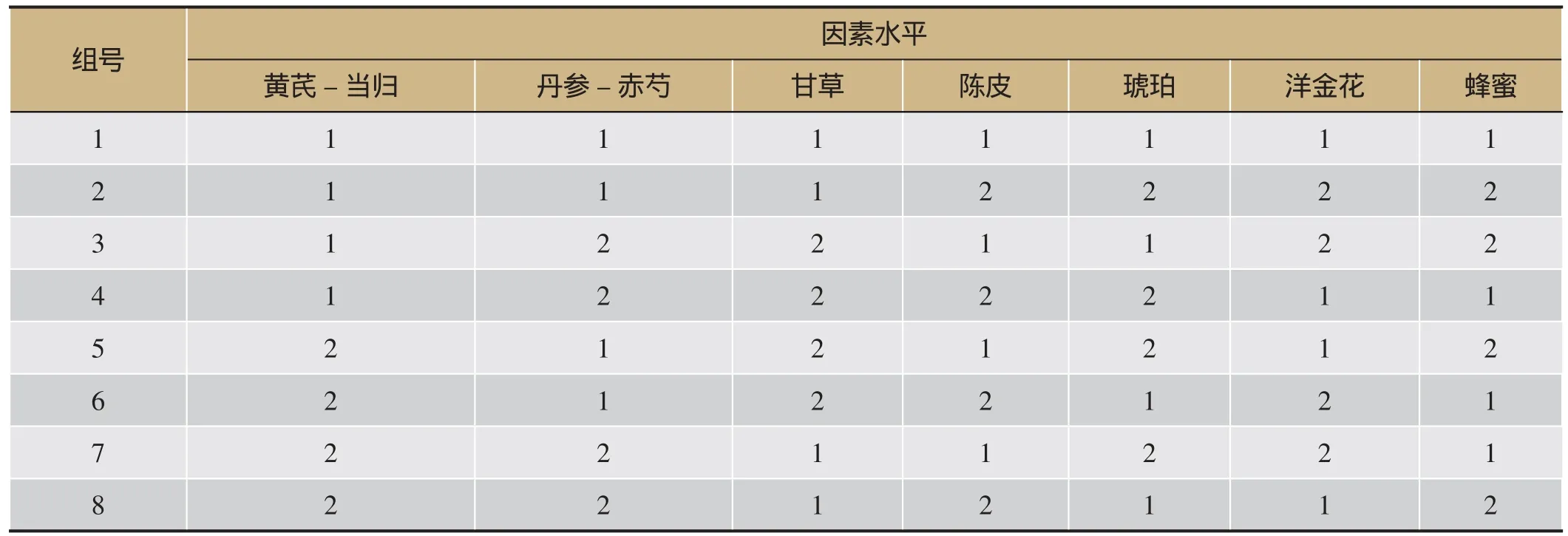
表1 因素水平表
2 实验方法
2.1 通脉丸方中各味中药有效组分配伍方案
通过对通脉丸的制剂处方分析,结合药效及毒性等特点将处方中各味中药为8组,“两头尖、附子、马钱子”为一组,“黄芪、当归”为一组,“丹参、赤芍”为一组,蜂蜜、甘草、陈皮、琥珀和洋金花分别各为一组。按照正交设计表[5-7]L(827)将其中除去“两头尖、附子、马钱子”这一组之外的7组为7个因素,得到8种不同配比,见表1。两个水平为有和没有。将这8种不同配比分别与“两头尖、附子、马钱子”这一组配伍得到八组灌胃用药。
2.2 灌胃用药的制备
通脉丸方中各味中药的有效组分提取液由课题组另一成员徐丽军提供,徐丽军已测定饮片中指标成分的含量和所提取有效组分含量,计算出处方比例所需药液的体积。按照配伍方案设计将相应的有效组分提取液混合,浓缩至4.5 g·mL-1的药液,其中蜂蜜为河南中医学院第一附属医院制剂室炼制的中蜜,琥珀粉碎直接加入药液。
2.3 色谱条件
Waters Acquity UPLC BEH C18色谱柱(1.7 μm,2.1 mm×50 mm);流速0.18 mL·min-1;检测波长260 nm;流动相:酸水-乙腈(77:23),酸水:0.02 mol·L-1磷酸二氢钾与0.01 mol·L-1庚烷磺酸钠等量混合,并用10%磷酸调体系pH为2.5;柱温30 ℃;进样量1 μL。
2.4 对照品溶液的配制
精密称取士的宁对照品适量,加甲醇溶解,得到士的宁对照品储备液。
2.5 方法学考察
进行线性关系、定量限、精密度、稳定性、提取回收率等试验考察。
2.6 大鼠颈外静脉插管手术[8-10]
2.6.1 插管导管的制作
取PE管长度约11 cm,管两侧剪平口。使用之前用记号笔做两处位置标记分别为3.5 cm处和5.5 cm处,在一端插入一枚大头针,将其在生理盐水中浸泡备用。
2.6.2 插管手术
配制10%水合氯醛溶液,按照300 mg·kg-1大鼠的量进行麻醉,用电推剪剔去大鼠左侧颈胸部和颈背部的毛,用碘伏对手术区域及手术器械进行消毒。将已经麻醉的大鼠背位固定在大鼠固定台上。于大鼠颈中线偏左侧,从外上到内下做一个约1 cm左右的纵切口,使用眼科镊剥离其皮下组织使其左颈外静脉显露并游离,结扎静脉远心端,在颈外静脉管壁制造出一个横向切口,沿此切口将插管插入颈外静脉。回抽有血,注入生理盐水后无渗漏则表明插管位置合适,用0.1 mL的0.1%肝素钠溶液封管后用大头针封堵插管,将管固定。将大鼠俯卧于大鼠固定台上,在其颈后部正上方作一个横切口,将固定好的插管从大鼠颈胸部切口引至颈背部切口,缝合切口,用碘伏消毒处理,插管完成。
2.6.3 插管后的护理
手术完成后将大鼠单笼饲养,注意保暖。待大鼠清醒后注意观察大鼠有无异常、切口有无感染等,如果发现有异常应及时处理,术后隔天疏通导管,用0.1%肝素钠溶液封管。
2.7 血浆样品预处理方法
取待测大鼠肝素抗凝全血,4000 r·min-1离心15 min,用取样器精密吸取上层血浆200 μL,置离心管中,加入25%-28%氨水100 μL,置旋涡混合器上混合30 s,然后加入甲基叔丁基醚1.5 mL,再涡旋1 min,离心10 min,收集甲基叔丁基醚液;剩余物重复以上萃取操作一次,合并两次萃取液后40℃氮气流吹干。残渣加入甲醇100 μL溶解,涡旋,15 000 r·min-1离心10 min,取上清液进样测定[3]。
2.8 大鼠血浆样品测定
正常大鼠8组,每组各5只,给药前禁食12 h,不禁水。给药前称体重,给药剂量为0.64 mL药液/100 g大鼠,记下各只大鼠给药的准确时间,于给药后2、4、6、24、28、31、48、52、55 h不同时间点大鼠静脉插管取血0.45 mL,同时注入等体积生理盐水,全血置于含有肝素钠的离心管中备用。按照血浆样品的处理方法将血浆样品处理后,使用UPLC测定不同时间点的血浆药物浓度。
2.9 数据处理
采用已建立的UPLC法测定不同时间点大鼠血浆中士的宁的浓度,以时间为横坐标,血药浓度为纵坐标,建立士的宁的血药浓度-时间曲线以及各个组的平均血药浓度-时间曲线;采用药动学软件Winnonlin 5.2,计算各个组的毒代动力-学参数。本实验所得的计量资料用均数±标准差±s表示,各个组的毒代动力学参数比较采用t检验[11,12],P<0.05为差异有显著性意义,其他配伍组的AUC与通脉丸原方组(第1组)的AUC进行比较,计算AUC减少率[AUC减少率(%)=(通脉丸原方组AUC-其他配伍组AUC)/通脉丸原方组AUC]。
3 结果
3.1 线性范围及最小检测限
取大鼠空白血浆200 μL,分别加入一定浓度的士的宁对照品溶液,制成系列浓度的对照品溶液,按实验方法“2.7项”操作,吸取上述一系列不同浓度血浆质控样品溶液1 μL进样测定峰面积,以士的宁峰面积对含士的宁血浆浓度进行线性回归,得回归方程Y=10 336 665X+148.822 5,R=0.999 9,结果表明士的宁在进样量0.000 043 2-0.010 800 0 μg与峰面积呈良好线性关系,按峰高为基线噪音3倍计算,血浆中士的宁最低检测浓度为0.043 2 μg·mL-1。
3.2 回收率实验
将一定量的士的宁对照品溶液加入到空白血浆样品制成高、中、低 3个浓度的样品,依实验方法“2.7项”下处理。测得血浆高、中、低浓度样品绝对回收率为85.48-87.94,平均相对回收率为99.31%-105.54%,RSD(%)值均小于15%,n=6,符合生物样品含量测定要求。
3.3 精密度实验
取大鼠空白血浆,分别加入高、中、低浓度士的宁对照品溶液,按标准曲线制备方法进行测定。日内差异: 一天内重复 5 次,RSD(%)均小于10%,日内精密度良好。日间差异:每天测定一次,连续测定 5 天,结果RSD(%)均小于10%,日间精密度良好。
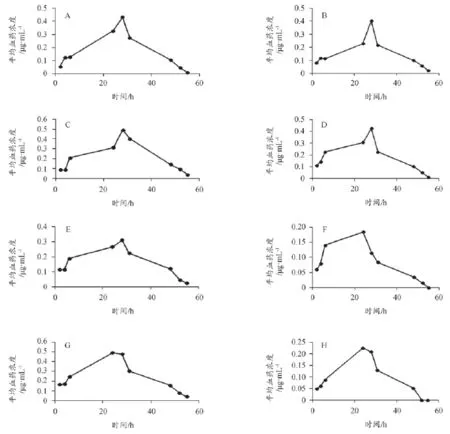
图1 大鼠灌胃第1-8组通脉丸有效组分浓缩液后士的宁的平均血药浓度-时间曲线
3.4 稳定性考察
将生物样品按相应的“2.7项”下进行样品处理,室温25℃放置,分别在0、6、12、24 h进样测定,结果RSD(%)均小于15%。样品在室温下24 h内稳定性良好。-20 ℃冷冻,室温下自然溶解,反复冻融3次,测得士的宁的浓度RSD值均小于15%,显示血浆样品反复冻融3次后稳定性良好。
3.5 毒代动力学研究结果
3.5.1 不同时间点大鼠血浆样品中士的宁含量测定结果
大鼠灌胃通脉丸方有效组分配伍浓缩液后所测得的士的宁平均血药浓度-时间数据曲线见下图1。
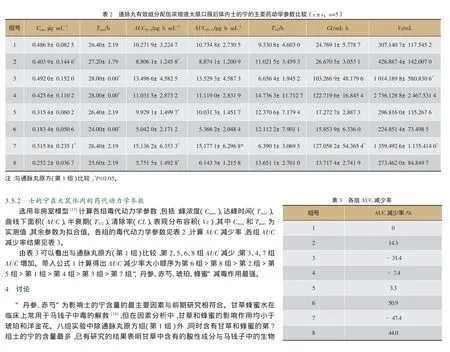
碱成盐,降低生物碱在体内的毒性,分析实验结果与以后研究结果不相符合的原因一方面可能为第7组实验配伍中除了甘草和蜂蜜之外,还有另一个因素陈皮的有效组分,陈皮与甘草、蜂蜜产生了相互作用,影响了甘草、蜂蜜的减毒作用,另一方面可能为处方量的甘草和蜂蜜不足够产生减毒作用,同时经过单独的工艺优选后提取的甘草有效组分与蜂蜜配伍不能达到甘草与蜂蜜配伍后的减毒作用。
中药毒代动力学作为中药安全性评价研究中的重要部分,能够有效解释毒性试验结果和预测人体安全性,是连接毒理试验现象和人用中药可能发生的不良反应评价之间的桥梁[15]。但中药复方化学成分的复杂性和多样性、中药配伍的变异性和机体状态的不可预测性,给中药复方药代动力学研究带来许多问题[16]。因此应注重采用新技术、新方法,对中药复方的代谢过程及毒效机制进行探索,以寻求更好的复方药代动力学研究途径,为中药的临床安全性评价提供更为可靠的依据。
本课题选择的是单次给药,采用灌胃给药的方式进行实验。毒代动力学是在毒性剂量下进行的实验研究,根据通脉丸方浓缩液急性毒性实验得出灌胃给药LD50为107.48 g·kg-1[17],再结合课题前期研究结果确定给药剂量为28.8 g·kg-1,相当于人临床服用剂量(按每天10 g计)的33倍。
1 陈天朝,王俊杰.通脉丸中竹节香附素A及总皂苷含量测定.中国当代医药,2012,19(1): 5-7.
2 陈天朝,李丽,梁启超,等.测定大鼠血浆中士的宁和马钱子碱含量的方法研究.世界科学技术-中医药现代化,2015,17(11): 2341-2348.
3 陈天朝,程伟,宋薇,等. UPLC测定大鼠血浆中士的宁的含量.中国实验方剂学杂志,2014,20(24): 127-129.
4 赵珍东,黄兆胜.马钱子毒副作用研究进展.国医论坛,2003,18(1): 50-51.
5 孙美利,李蕾,王和宇,等.斑鸠菊果实中总黄酮的提取工艺研究.世界科学技术-中医药现代化,2015,17(5): 1108-1112.
6 朱红兵,席凯强. SPSS 17.0中的正交试验设计与数据分析.首都体育学院学报,2013,25(3): 283-288.
7 李北兴,王伟昌,张大侠,等.正交设计和均匀设计在优化噻虫胺悬浮剂物理稳定性上的应用.中国农业科学,2015,48(2): 280-292.
8 王晶晶,焦昆,李兵,等.介绍一种新的大鼠颈外静脉插管方法.实验动物科学,2008,25(2): 52-53.
9 刘盼盼,颜双泉,陈马云,等.小鼠经颈外静脉右心导管法测定心室压力的实验方法研究.中国应用生理学杂志,2014,30(2): 189-192,195.
10 汤海涛,邢雪,张大伟.大鼠颈外静脉置管方法的改进.临床普外科电子杂志,2014,2(1): 29-31.
11 胡良平,高辉.如何正确运用t检验.中西医结合学报,2008,6(2): 209-212.
12 冯变英,张旭,张春枝.关于t检验方差分析及多重比较的研究.太原师范学院学报(自然科学版),2012,11(4): 59-61.
13 李波,孙美,杨正明,等.藏药仁青芒觉配伍佐塔的药代动力学对比研究.中国中药杂志,2015,40(14): 2887-2892.
14 张德放,邱维彬,王坤.马钱子的毒性及中毒解救的研究.辽宁中医杂志,2011,38(4): 713-714.
15 高方圆,袁伯俊,马秀娟,等.中药毒代动力学研究进展.中国新药杂志,2015,24(21): 2448-2452,2458.
16 李雪溦,张红阳,朱继孝.中药复方药物代谢动力学研究进展.中医药通报,2015,14(5): 65-69.
17 陈天朝,宋薇,王丽,等.通脉丸方浓缩液的急性毒性实验.中国现代药物应用,2013,7(8): 132-134.
Toxicokinetics of Tongmai Pills and the Effectiveness of Its Combination Components Concentrate in Rats
Chen Tianchao1,Liu Riuxia2,Yu Lanlan2
(1. The First Affiliated Hospital of Henan University of Traditional Chinese Medicine,Zhengzhou 450000,China; 2. School of Pharmacy,Henan University of Traditional Chinese Medicine,Zhengzhou 450008,China)
This study aimed to investigate the mechanism of internal attenuation and provide references for safety evaluation by extracting effective components from the Chinese herbs of Tongmai pills. Rats were dividedinto eight groups and intragastrically administered with the concentrated decoction of the Tongmai prescription. Serum strychnine levels of all groups were detected by UPLC at various time points after administration. At last,its fitting parameters in toxicokinetic were calculated using SPSS software. It was found that the parameters of serum strychnine in rats fitted with the non-compartmental model with the AUC(0-t)outputs as follows: 10.271 9±3.224 7,8.806 1±1.245 8,13.496 6±4.582 5,11.031 5±2.873 2,9.929 1±1.499 7,5.042 0±2.171 2,15.136 2±6.353 3,5.751 5±1.492 8 μg·h·mL-1. Different toxicities between the concentrated decoction from Tongmai pills (group 1) and other decoctions consisting of the some herbs in Tongmai pills (group 2-group 8) were showed in this study with the AUC outputs ranging from the most to the least as follows: group 6,group 8,group 2,group 5,group 1,group 4,group 3 and group 7. So the decoction with salvia,red peony,amber and honey presented the strongest toxicity attenuated effect. In conclusion,it was demonstrated that UPLC worked well in determining serum strychnine of rats.
Compatibility for toxicity attenuation,strychnine,toxicokinetic,pharmacokinetic parameters
10.11842/wst.2016.05.024
R285
A
(责任编辑:朱黎婷,责任译审:朱黎婷)
2016-03-11
修回日期:2016-04-07
* 河南省教育厅科技攻关项目(2011A360003):基于系统论通脉丸减毒机制的研究,负责人:陈天朝;河南省教育厅重点项目(13A350597):基于药辅统一的中药丸剂释药机制研究,负责人:陈天朝。
** 通讯作者:陈天朝,主任药师,硕士研究生导师,主要研究方向:中药新剂型研究。
