微波、射频及电凝对离体猪股骨干骺端制热效应的对照研究*
2016-03-06闫飞飞谢远龙冯帆胡超蔡林雷军
闫飞飞 谢远龙 冯帆 胡超 蔡林 雷军
微波、射频及电凝对离体猪股骨干骺端制热效应的对照研究*
闫飞飞 谢远龙 冯帆 胡超 蔡林 雷军*
目的探索微波、射频及电凝对离体猪股骨干骺端的制热效应的差异,以指导临床应用。方法取30条新鲜成年猪股骨,随机分成微波组、射频组和电刀组,每组10个样本,分别采用微波、射频和电刀进行加热(60 W·300 s),旁开加热点5、10、15、20mm测温,比较三组的凝固范围、温度的分布及变化趋势。结果三组凝固范围横径分别为(23.3±1.5)、(14.8±1.1)、(10.8±1.3)mm,纵径分别为(28.1±2.2)、(25.3±1.5)、(22.1±1.8)mm,横纵径均为微波>射频>电刀(<0.05)。病理切片证实肉眼所见的凝固范围与病理切片凝固范围基本一致。微波组在旁开中心5、10、15mm处的温度均显著高于射频组和电刀组,而三组在旁开中心20mm处温度无显著差异。三组热场分别在240、210和140秒内达到稳态,距离加热中心越近温度越高,上升速度越快。结论 微波、射频及电凝对股骨干骺端均具有制热灭活作用,微波热场温度最高,凝固范围大,射频次之,而电刀制热效应最小。
微波;射频消融;高频电刀;股骨;干骺端;动物实验
微波消融(Microwave ablation,MWA)的基本原理是通过发射电磁波场(915MHz or 2.45 GHz),引起周围组织中偶极分子的旋转来产生热量,从而使组织发生凝固性坏死[1];射频消融(Radiofrequency ablation,RFA)则是通过射频发射改变电流活动,引起局部离子震荡,产生高温使组织发生凝固性坏死[2];电刀热凝也是利用射频原理,即通过变压变频将高频电流聚集起来,极短时间内的震荡电流引起局部离子震荡摩擦产生大量的热,直接摧毁与有效电极尖端相接触下的组织[3]。三者都是通过高温使肿瘤细胞凝固坏死,但产热原理、产热效率及热场分布等均存在差异,各有优缺点。
肿瘤热疗在临床使用中常面临热毁损肿瘤组织和保护正常组织热损伤的矛盾,既要尽可能杀灭肿瘤组织,又要避免热点周围正常组织热毁损伤。然而目前对于骨组织局部加热后热量传递及周围热场分布的研究颇少。本实验拟继续深化MWA、RFA和电刀对离体猪干骺端松质骨的制热效应研究,并在此基础上对电刀是否可作为肿瘤热疗的辅助方式进行探讨。
1 材料与方法
1.1 实验仪器
1.1.1MWA系统:南京九洲医疗设备研发中心内冷式微波治疗仪。工作频率(2450±50)MHz,输出功率:5~120W 逐步可调,步进 5W;内冷式硬质天线外径为 2.0mm,长度150mm。自带水循环动力泵,室温生理盐水(20℃)作为降温水源。
1.1.2RFA系统:柯惠医疗器械有限公司提供的Cool-tipTMRF Ablation System E,工作频率 375 kHz,输出功率:5~150 W,阻抗测量范围:10~500,电极直径为 1.2mm,长度150mm。室温生理盐水(20℃)作为灌注水源。
1.1.3 美国进口威力高频电刀ForceFX-8C:具有单、双极两种输出模式,频率 300~750kHz、单极切割最大输出功率300W,单极电灼凝血的最大输出功率为120W,工作时电流均从负极板返回主机,本实验选用固定功率为60W的单电极电凝输出模式;
1.1.4 测温系统:武汉泰伦特科技有限公司提供的多点测温仪,采用NTC热敏测温探头(头部尺寸1.3×1.5mm),可同时监测八通道温度变化,测温范围0~200℃。
1.2 实验方法
取30条新鲜成年猪股骨远端干骺端,根据数据随机法分成微波组、射频组和电刀组三组,每组10个样本,均采用临床常用的功率和时间组合即60 W·300 s(本实验根据相关研究报告及临床经验,设定该功率和时间组合)。用3.0mm克氏针打孔,插入电极作为加热中心,旁开中心5、10、15和20mm,用1.5mm克氏针打孔,插入NTC热敏测温探头实时测温,所有孔深均为2cm。300秒后停止加热,继续监测2分钟内各测温孔自然冷却下温度衰减情况;测温结束后,测凝固区横径,再沿各钻孔的连线纵行切开标本,测凝固区纵径,并观察形态学特征。再将标本脱钙切片等后行HE染色处理,镜下重点观察凝固区临界范围。
1.3 统计分析
统计分析采用SPSS19.0软件。凝固范围以最大横径和纵径,以及横径和纵径均数评定。计量资料以(±s)表示,两组间均数比较采用t检验,多组间比较采用方差分析,<0.05为差异有统计学意义。
2 结果
2.1 标本形态学观察
分别采用微波、射频及电刀对标本进行凝固(60 W· 300s),凝固结束后,肉眼观察干骺端横断面(图1a,1b,1c)及沿各钻孔的连线纵行切开截面的凝固范围(图1d,1e,1f):三组的凝固区均可见明显的炭化带,微波组凝固范围最大(图1a,1d),射频组次之(图1b,1e);电刀组范围最小(图1c,1f)。(彩图见插页)

图1a,1d为微波组凝固后标本;图1b,1e为射频组凝固后标本;图1c,1f为电刀组凝固后标本(图中白色箭头所指为凝固炭化区;A为微波,射频及电刀电极插入通道,B,C,D,E为旁开加热中心距离为5、10、15及20mm的测温通道)
2.2 标本病理学观察
分别将三组标本进行HE染色处理后镜下观察,可以发现肉眼所见的凝固范围与病理切片凝固范围基本一致。(彩图见插页)

图2a,2b,2c分别为微波,射频,电刀组病理标本(HE×40,图中白色箭头所示为标本炭化带边缘)
2.3 三组标本凝固范围的比较
凝固结束后测得三组标本的的横径分别为(23.3±1.5)、(14.8±1.1)、(10.8±1.3)mm,微波>射频>电刀(<0.05);纵径分别为(28.1±2.2)、(25.3±1.5)、(22.1±1.8)mm,微波>射频>电刀(<0.05)。(表1)
表1 三组标本凝固范围的比较(±s)

表1 三组标本凝固范围的比较(±s)
注释:a与电刀组比较<0.05,b与射频组比较<0.05
方法 横径(mm) 纵径(mm)微波组射频组电刀组23.3±1.5ab 28.1±2.2ab14.8±1.1a 25.3±1.5a10.8±1.3 22.1±1.8
2.4 三组凝固方式温度-时间效应变化的比较
微波、射频及电刀组热场在240、210、140秒均达到稳态,三组距离加热中心越近温度越高,上升速度越快(图3)。(彩图见插页)三组距加热中心5mm处的平均稳态温度分别为(130.2±1.5)、(104.0±2.3)、(87.3.0±3.2)℃,10mm处分别为(87.3±2.1)、(71.6±1.5)、(61.8±3.8)℃,15mm处平均温度分别为(67.2±2.2)、(57.1±3.1)、(51.2±2.9)℃,均为微波明显高于射频高于电刀(<0.05);20mm处平均稳态温度分别为(23.3±0.3)、(23.2±0.2)、(23.4±0.3)℃,无明显统计学差异(>0.05)(表2)。
表2 三组凝固温度分布比较(±s,n=10)
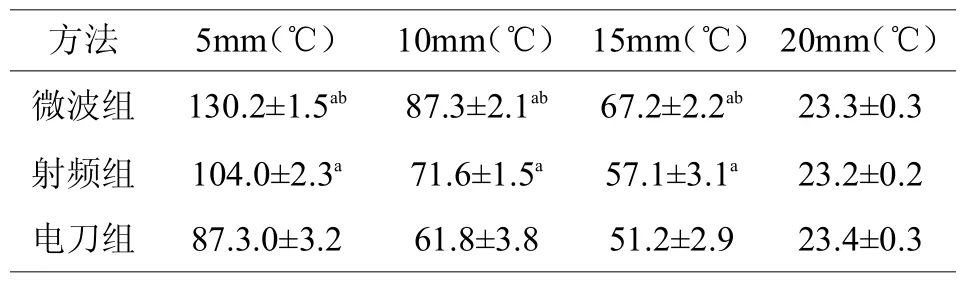
表2 三组凝固温度分布比较(±s,n=10)
注释:a与电刀组比较<0.05,b与射频组比较<0.05
方法微波组射频组电刀组5mm(℃) 10mm(℃) 15mm(℃)20mm(℃)130.2±1.5ab 87.3±2.1ab 67.2±2.2ab 23.3±0.3 104.0±2.3a 71.6±1.5a 57.1±3.1a 23.2±0.2 87.3.0±3.2 61.8±3.8 51.2±2.9 23.4±0.3
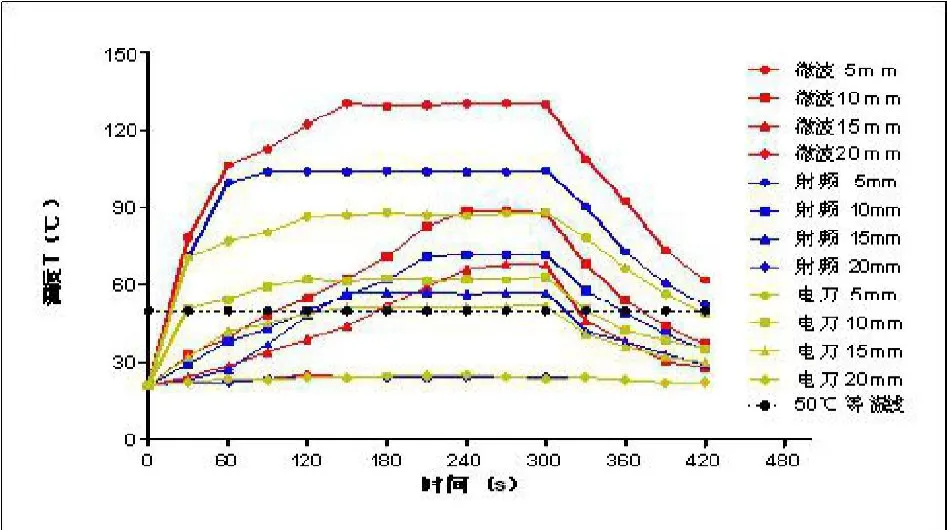
图3 微波、射频及高频电刀对离体猪股骨远端松质骨凝固的温度-时间关系
3 讨论
肿瘤的热疗是继肿瘤手术、放疗、生物治疗、化疗后的又一新型的疗法[4]。损伤细胞和组织的机制主要是通过局部高热导致肿瘤细胞基质蛋白、线粒体酶和核酸组蛋白复合物凝聚等[5]。近来,Zhe Y等[6]实验证明MWA处理后的肿瘤细胞,特别是在原位消融中,可通过免疫反应诱导特异性抗肿瘤效果。目前,热消融已在骨肿瘤的治疗中得到越来越多的应用[7-12],RFA已成为治疗骨样骨瘤的循证方法的选择,MWA或RFA,单独或联合骨水泥可用于转移性骨肿瘤的姑息治疗,在减轻病人疼痛及改善生活质量上效果显著[1];骨肿瘤的热消融既起到了杀灭肿瘤组织的作用,又可以极大程度地保留了自体骨量,为骨的再生和修复提供了良好条件[13]。虽已取得较好的临床疗效,但也存在消融范围不精确,安全性能不高等问题,进而导致邻近组织损伤,术后复发率高,术后再骨折等并发症的出现[14]。高频电刀利用高频电流,虽可使肿瘤产生局部高温,发生凝固性坏死,但可否将其热效应用于肿瘤热疗,目前尚无定论。施鑫等[15]提出在股骨近端巨细胞瘤的手术治疗时用高频电刀反复烧灼残腔骨壁有助于消灭残留的肿瘤细胞。所以,通过本实验研究,继续深化对三者产热效率、制热效应及热场分布的研究,并在此基础上,展开对电刀是否可成为肿瘤热疗的一种辅助方式的探讨,进而来指导临床。
本实验在相同功率及加热时间下,发现微波的凝固范围、热场温度均显著大于射频大于电刀,这主要是三者与组织的作用方式不同所致。通过观察凝固后的标本可以发现,三组加热中心均有形成不同程度的炭化带,微波范围最大,射频和电刀次之。而微波与后两者最大不同在于其对组织有一定的穿透力,穿透组织的偶极子均为热源,可以自体加热[16]。且对于低热传导的松质骨来说,穿透性更佳,其对组织热传导系数的依赖明显小于射频和电刀[17]。而射频和高频电刀通过射频波使周围组织产生交变电流,引起电极周围组织中自由离子发生震荡,摩擦生热并传导扩散,产热部位主要位于电极周围几毫米内,易受组织内自由离子浓度和周围组织电导率的影响,凝固范围的扩大主要靠传导散热[18]。所以笔者分析,影响凝固范围不同的主要原因是高温导致电极周围发生组织脱水炭化,而微波发射的电磁波可以穿越炭化带,使范围可以在热传导的基础上进一步扩大,而射频和电凝易受组织内自由离子浓度和周围组织电导率影响,且当电极周围组织脱水炭化时阻抗上升,限制了热量的产生及传导,不利于消融范围的继续扩大。所以临床上正在尝试向病灶内注射盐水或铁离子复合物等方法来改善组织热传导[18]。而电刀与RFA相比,虽制热原理相同,但因二者电极性能的差别、电刀缺乏冷循环系统等,使得其工作时热量分布不均匀,仅集中于电刀周围,可爆发性导致组织脱水炭化,限制热量的产生及传导,导致其凝固范围及热场温度不如RFA。
本实验证明,MWA、RFA和电刀的热场分别在240、210和140秒内达到稳态,距离加热中心越近温度越高,上升速度越快。三组的温度变化都局限于加热中心15mm以内,20mm处温度未受热效应的明显影响,说明该功率及加热时间下,三者的热效应的有效半径均不超过15mm。既往研究表明,骨细胞热耐受阈值为50℃·30s,4~6分钟即发生不可逆的细胞坏死[19]。目前认为,50℃为肿瘤热耐受的极限,50℃以上的温度区域为有效温度场,而实验中三者距中心15mm以内,在加热及降温的过程中,都可在一定时间内满足有效温度场的要求,但就凝固区范围看,并不与50℃以上的高温区完全吻合,而是在垂直电极方向上略小于50℃高温区,可能由于离加热中心较远的地方,虽也可以达到50℃以上,但温度相对较低,加之维持时间不够,并未能引起骨组织在肉眼观察下形态学改变。
因此,微波、射频及电凝对股骨干骺端均具有制热灭活作用,微波较射频热场温度高,凝固范围大,在较大骨肿瘤的治疗中宜选用微波。射频消融较微波有更好的温控性。相比之下,电刀的制热效应较低,凝固范围受多种因素影响差异较大,且缺乏冷循环及温度监测系统等,使高频电刀在肿瘤热疗的作用上无法与前二者相比,但其同样具备高温灭活肿瘤细胞的功能,如在病灶刮除后的残腔行一定时间的加热凝固以杀死残留肿瘤细胞等,可作为一种辅助治疗手段供选择,但需注意避免对周围正常组织的热损伤。
[1]Ringe KI,Panzica M,von Falck C.Thermoablation of Bone Tumors[J].RoFo,2016,3,16.
[2]Shuichi Y,Toshio K,Yuichi O,et al.Thermal influence of radiofrequency ablation for bone:anexperimental study in normal rabbit bone[J].Skeletal Radiology,2014,43(4):459-465.
[3]朱弋,李晓东,贺建林.高频电刀应用到的三个物理效应分析[J].中国医学装备,2011,08(2):39-40.
[4]闫向勇,刘文超.热疗在肿瘤治疗中的研究进展[J].世界中西医结合杂志,2014,9(2):213-216.
[5]Chu K F,Dupuy D E.Thermal ablation of tumours:biological mechanisms and advances in therapy[J].Nature Reviews Cancer, 2014,14(3):199-208.
[6]Zhe Y,Jie G,Minghua Z,et al.Treatment of osteosarcoma with microwave thermal ablation to induce immunogenic cell death[J]. Oncotarget,2014,5(15):6526-6539.
[7]Basile A,Failla G,Reforgiato A,et al.The use of microwaves ablation in the treatment of epiphyseal osteoid osteomas[J].Cardiovasc Intervent Radiol,2014,37:737-742.
[8]Kostrzewa M,Diezler P,Michaely H,et al.Microwave ablation of osteoid osteomas using dynamic MR imaging for early treatment assessment:preliminary experience[J].J Vasc Intervent Radiol, 2014,25:106-111.
[9]Yamakado K,Matsumine A,Nakamura T,et al.Radiofrequency ablation for the treatment of recurrent bone and soft-tissue sarcomas in non-surgical candidates[J].Int J Clin Oncol,2014,19(5): 955-962.
[10]Pusceddu C,Sotgia B,Fele RM,et al.Combined Microwave Ablation and Cementoplasty in Patients with Painful Bone Metastasesat HighRiskof Fracture[J].Cardiovasc Intervent Radiol,2016, 39(1):74-80.
[11]Pezeshki P S,Davidson S R,Akens M K,et al.Helical coil electrode radiofrequency ablation designed for application in osteolytic vertebral tumors-initial evaluation in a porcine model[J].Review of Philosophy&Psychology,2015,1(3):351-370.
[12]Ahmed M,Solbiati L,Brace CL,et al.Image-guided tumor ablation:standardization of terminology and reporting criteria-a 10-year update[J].Radiology,2014,273:241-260.
[13]姬振伟,范清宇,张明华,等.微波消融原位灭活保肢技术在骨肿瘤治疗中的研究进展[J].中国骨与关节外科,2013(3):287-290.
[14]Foster R C B,Stavas J M.Bone and soft tissue ablation[J].Seminars in Interventional Radiology,2014,31(2):167-179.
[15]任可,施鑫,吴苏稼,等.股骨近端巨细胞瘤的诊断和手术治疗[J].中国矫形外科杂志,2012,20(7):577-580.
[16]姚子龙,张余.微波消融治疗骨肿瘤的研究进展[J].广东医学,2014,35(21):3438-3442.
[17]任刚,韦兴,姚雨,等.微波与射频对离体猪股骨干骺端制热效应的对照研究[J].中国骨与关节杂志,2013(5):293-296.
[18]Hong K,Georgiades C.Radiofrequency Ablation:Mechanism of Actionand Devices[J].J Vasc Interv Radiol,2010,21(8 Suppl): 179-186.
[19]汝鸣,蔡郑东,郑龙坡,等.Paiban骨组织单电极射频消融的范围及热场分布[J].中国组织工程研究与临床康复,2008,12(30): 5865-5868.
Swine femoral metaphysis ablation experiment in vitro:a comparative study of heating effects between microwave,radiofrequency and high frequency electrotome
Yan Feifei,Xie Yuanlong,Feng Fan,et al.
Department of Orthopedics,the Zhongnan Hospital of Wuhan University, Wuhan Hubei,430071,China
ObjectiveTocompare the heatingeffects between microwave,radiofrequencyandhigh frequencyelectrotomein porcine femoral metaphysis.Methods Microwave,radiofrequency and high frequency electrotome were applied for 300 seconds at 60 Watts in 30 porcine femoral metaphysis.Thermal sensors were placed at 5,10,15 and 20mm from the electrodes,thediameter and shape,the distribution andvariationtendency of temperaturein the coagulation zone,werecompared between three groups.Results The transverse diameters of lesions ablated with microwave,radiofrequency and electrotomewere(23.3±1.5),(14.8±1.1)and(10.8±1.3)mmrespectively,Thelongitudinal diameterswere(28.1±2.2), (25.3±1.5)and(22.1±1.8)mm respectively,andboth of two diameterswere thattheformerwassignificantly longer than the later than the last(<0.05).The coagulation zone observed directly by eyes is consistent basically with pathological section.The temperature5,10,15mmfromthe centers of microwaveweresignificantlyhigherthanthe radiofrequencygroup than the electrotome group,but there was no significant difference in three groups at the temperature 20mm from the centers.The three groups could reach the steady-state at 240,210 and 140s independently,the shorter the distance to the heating point,the higher temperature reached and faster the temperature rose.Conclusion Both of Microwave,radiofrequency and electrotome have heating effects to inactivate porcine femoral metaphysis.The temperature of the heating zone and the boundary of microwave are highest and largest in these three groups,followed by radiofrequency,and the heating effect of high frequency electrotome was not as good as the other two groups.
Microwaves;Radiofrequencyablation;Highfrequencyelectrotome;Femur;Epiphyses;Animal experimentation
R318.03
A
10.3969/j.issn.1672-5972.2016.06.01
swgk2016-04-00091
闫飞飞(1991-)男,硕士在读。研究方向:脊柱、骨肿瘤。
*[通讯作者]雷军(1975-)男,博士,副主任医师。研究方向:骨外科。
2016-04-27)
湖北省自然科学基金面上项目(基金号:2014CFB742)
武汉大学中南医院骨四科,湖北武汉430071
