封管法制备有机碳稳定同位素样品存在的问题和改进
2016-03-06曹蕴宁刘卫国
曹蕴宁,刘卫国,
(1. 中国科学院地球环境研究所 黄土与第四纪地质国家重点实验室,西安 710061;2. 西安交通大学 人居环境与建筑工程学院,西安 710049)
封管法制备有机碳稳定同位素样品存在的问题和改进
曹蕴宁1,刘卫国1,2
(1. 中国科学院地球环境研究所 黄土与第四纪地质国家重点实验室,西安 710061;2. 西安交通大学 人居环境与建筑工程学院,西安 710049)
有机碳稳定同位素的高精度测定是利用地质样品有机碳同位素研究气候和植被变化等的基础。通过实验发现低有机碳含量样品同位素测定误差相对较大,其中样品收集过程是主要的影响因素之一。本文针对这个问题,主要从杂质气体干扰入手,在一步冷冻分离CO2和H2O,或分步冷冻分离CO2和H2O的收集方法,以及改变收样管体积三方面进行条件实验研究,讨论了封管法制备有机碳稳定同位素样品气体收集过程对有机碳稳定同位素组成的影响。结果表明:(1)CO2气体的纯化收集是封管法制备有机碳稳定同位素样品的一个重要步骤,收集时杂质气体含量越高,对样品有机碳稳定同位素组成的影响越大;(2)在相同的杂质气体背景条件下,与一步冷冻分离CO2和H2O的方法相比,分步冷冻CO2和H2O的方法能够显著减小杂质气体对有机碳稳定同位素测定的影响;(3)小体积收样管能够显著提高有机碳稳定同位素样品的离子流强度,进而提高低有机碳含量样品的稳定碳同位素测定精度。
有机碳稳定同位素;样品制备;封管法
有机碳稳定同位素在古环境、古植被、古气候和土壤碳循环,以及有机质来源等诸多研究领域已有广泛应用(林本海和刘荣谟,1992;段毅和罗斌杰,1998;沈吉等,1998;刘卫国等,2002;张恩楼等,2002;Liu et al,2003;饶志国等,2005;于贵瑞等,2005;Liu et al,2005;罗光强等,2009;王国安等,2012;张成君等,2012;袁红朝等,2014)。目前有机碳稳定同位素分析方法主要有4种:(1)多次循环分析系统,(2)通用分析系统,(3)封管法,(4)连续流装置。封管法也称密闭安瓶法,在国内,刘荣谟等(1990)首先建立并改进了封管法,该方法可用于分析黄土,纤维素等样品的有机碳稳定同位素。王楚等(1992)介绍了使用设备简单,适合我国中小实验室使用的一种封管法,能够用于分析制备湖泊沉积物及各种物态的石油分馏物的有机碳稳定同位素样品。封管法与其他几种有机碳稳定同位素分析方法相比,操作稍复杂,但样品氧化充分,无记忆效应,分析精度高,因而广泛应用于国内外稳定同位素实验室。
高精度有机碳稳定同位素分析方法近年来受到越来越多研究者的关注和重视。有机碳稳定同位素分析过程主要包括样品前处理,CO2气体的制备以及质谱分析。随着高精度同位素质谱分析仪器的不断完善,仪器本身因素对样品测定结果的影响越来越小。因此,近年来人们对如何提高有机碳稳定同位素测定精度的研究多集中在样品预处理方法和样品制备条件上,如王金权(2005)对比研究了两种不同预处理方法对岩石样品有机碳同位素的影响,曹蕴宁等(2005)研究了不同酸处理条件去除碳酸盐,样品制备是否加铜丝以及氧化条件等对土壤有机碳同位素组成的影响,吴夏等(2008)研究了样品的粒度,不同酸浓度,洗除样品残余酸和烘干温度等前处理条件对岩石样品有机碳同位素组成的影响,迟云平等(2012)研究了不同实验材料,不同仪器及不同温度对沉积物有机碳同位素组成的影响,李阳阳等(2012)对比研究了封管法和在线法对黄土有机碳同位素分析的影响,祝孟博等(2015)研究了不同酸处理方式,不同干燥方式等预处理方法对不同类型样品有机碳同位素组成的影响。但对CO2气体制备,尤其是CO2气体纯化收集过程对样品有机碳稳定同位素组成影响的研究很少。
实验中笔者发现低有机碳含量样品稳定同位素测定误差相对较大,这限制了有机碳稳定同位素地球化学在环境研究中的应用。而CO2气体的纯化收集是封管法制备有机碳稳定同位素样品的一个重要步骤,是影响样品δ13C的可能因素之一。因此,本文研究封管法制备有机碳稳定同位素样品CO2气体收集时杂质气体对有机碳稳定同位素组成的影响;对比研究一步冷冻分离CO2和H2O及分步冷冻分离CO2和H2O的方法对样品有机碳稳定同位素组成的影响;对比研究大体积收样管和小体积收样管收集CO2对样品离子流强度的影响。目的是找出低有机碳含量样品同位素测定误差相对较大的可能原因,探明封管法制备有机碳稳定同位素样品CO2气体收集过程对稳定碳同位素组成的影响及如何消除或减小该影响,从而进一步提高封管法测试样品有机碳稳定同位素组成的精度和准确性。
1 实验方法
1.1 有机碳稳定同位素分析样品制备
样品有机碳稳定同位素分析主要包括以下三个步骤:样品前处理;CO2气体的制备;质谱分析。本文采用封管法进行有机碳稳定同位素样品制备,具体实验步骤如图1所示。
为避免空白影响,实验所用器皿均先用稀酸浸泡,然后用蒸馏水冲洗干净,在500℃加热4小时。
本研究选用的样品有国家标准物质GBW04407(炭黑)以及不同类型天然样品。天然样品包括洛川表土T-1,太白山表土SN-2,洛川黄土Luo-193,Luo-253,西峰黄土XF01(1)1392及青海岩石样品泥岩,泥灰岩和长石砂岩。对于天然样品,及时置于烘箱中以40℃烘干,然后缩分、研磨,过100目筛,将过筛后的样品保存于干净铝箔袋中。取适量样品,加盐酸去除其碳酸盐,将除净碳酸盐的样品冲洗至中性,烘干后研磨,保存在预处理过的玻璃小瓶中。将前处理好的样品装入石英样品管中,同时加入氧化铜,铜丝和铂丝,抽真空至10-3Pa,熔封石英样品管,然后放入马弗炉内850℃恒温至少2.5小时,以保证有机质充分氧化。待样品管炉冷至室温后,取出,置于CO2气体纯化装置上,用液氮和液氮-酒精冷阱除去水分,收集纯净的CO2气体。对于有机碳稳定同位素标准物质的制备,不需进行样品前处理,CO2气体的制备过程与天然样品相同。
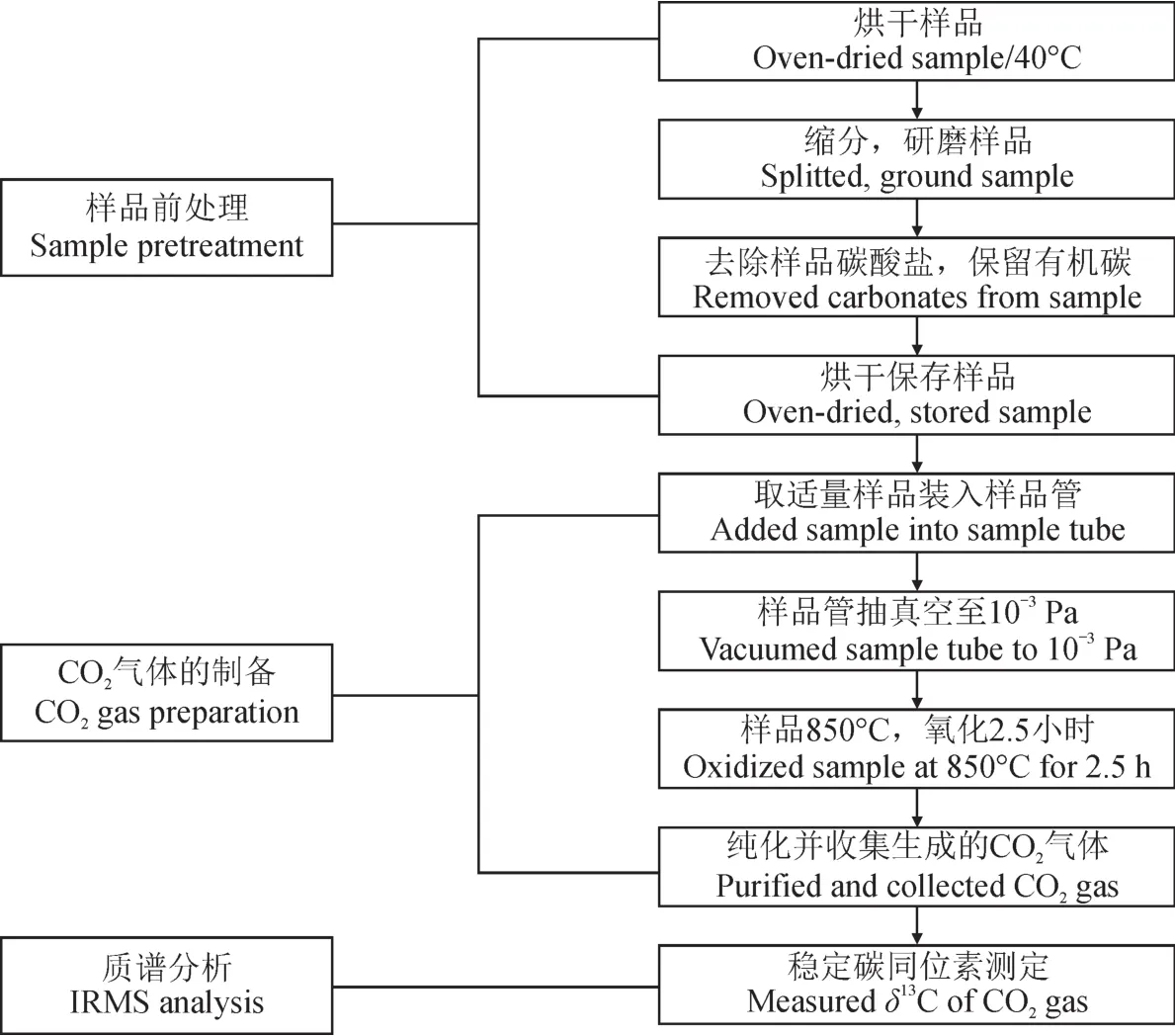
图1 封管法制备有机碳稳定同位素样品流程图Fig.1 Flow chart of organic carbon stable isotope analysis by using sealed tube method
本文的研究内容仅涉及流程图中“纯化并收集生成的CO2气体”这一实验环节。
1.2 质谱分析
将收集到的CO2气体在MAT-251型质谱仪双路进样系统上进行稳定碳同位素分析。
稳定碳同位素组成的表达式为:
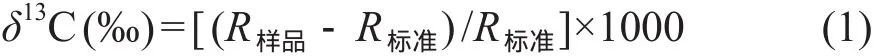
式中,R样品为样品的稳定碳同位素比值(13C /12C),R标准为标准的稳定碳同位素比值(13C/12C)。
稳定碳同位素组成相对V-PDB标准。所有样品的同位素分析均在中国科学院地球环境研究所同位素实验室进行,各类样品的测定精度用实验室工作标准控制,每批样品至少带1个工作标准,标准样品的重复分析误差<0.2‰。
2 结果与讨论
2.1 杂质气体对收集CO2稳定碳同位素组成的影响
有机质碳氧化生成的CO2气体需经纯化收集(去除H2O和杂质气体)才能进行质谱测定。为研究纯化收集过程杂质气体是否会对有机碳稳定同位素结果产生影响,人为给真空管路中放入适量空气,通过平衡扩散调节管路内空气的压力在0.05—15.7 mbar。
选取有机碳稳定同位素国家标准物质GBW04407(炭黑,δ13C = (-22.43 ± 0.07)‰)和洛川表土样品T-1,按1.1中方法对表土样品进行前处理。测定了炭黑和T-1表土样品纯化收集CO2时不同空气与CO2压力比值下的有机碳稳定同位素组成,结果如图2所示。空气与CO2的压力比值分别为0.007,0.48以及2.96时,炭黑的δ13C值分别为-22.61‰,-23.38‰以及-25.14‰。空气与CO2的比值分别为0.004,0.17以及0.5时,T-1表土的δ13C值分别为-24.70‰,-25.01‰以及-25.15‰。炭黑和T-1表土样品的有机碳稳定同位素结果均表现出冷冻收集CO2气体时,杂质气体含量越高,碳同位素组成越偏负的趋势。当杂质气体与CO2的压力比值超过0.2,炭黑和T-1有机碳稳定同位素的偏差均大于0.2‰。
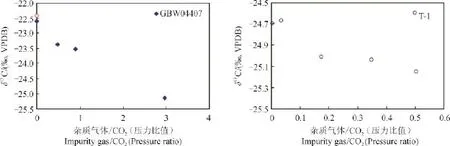
图2 杂质气体对收集CO2气体稳定碳同位素组成的影响Fig.2 Effect of air background on theδ13C of CO2gas collection
文献中报道大气稳定碳同位素组成通常在-8‰左右(Robinson and Scrimgeour,1995;Kuzyakov,2006),比炭黑的稳定碳同位素组成-22.43‰明显偏正,收集反应生成的CO2气体时,若混入空气中的CO2,稳定碳同位素比值理论上应比-22.43‰偏正。但目前大气中CO2的含量一般为380 μmol · mol-1,在本实验中,大气中CO2与样品CO2的量相比不足以对其δ13C值产生显著的影响。在T-1样品的实验中笔者观察到相同样品用量条件下杂质气体含量越高,冷冻收集的CO2气体的离子流强度相对越低。这表明冷冻收集CO2气体时,不是由于杂质气体(空气)本身的碳同位素对样品碳同位素组成产生影响,而是由于管路中杂质气体,其中包括氮气等不能被液氮冷冻住的杂质气体压力高干扰了CO2气体的冷冻收集,使CO2气体没有被完全冷冻。冷冻收集CO2的过程产生了同位素分馏,导致先收集到的CO2气体稳定碳同位素组成偏负,而剩余的未收集完全的CO2气体稳定碳同位素组成偏正。
2.2 两种冷冻收集CO2气体方法对有机碳稳定同位素组成的影响
张鸿斌(1986)指出燃烧生成的CO2和H2O先用液氮冷冻在冷指中,然后换用- 60℃冷冻剂冻住H2O分离出CO2。而多数文章中提到的冷冻方法均是用不同冷冻剂一步分离冷冻H2O和CO2(王楚等,1992;沈吉和王楚,1997)。那么不同冷冻收集CO2气体的方法是否会对其稳定碳同位素组成产生影响?
封管法制备有机碳稳定同位素样品的冷冻收集示意图如图3所示,A为收样管,B为冷阱,C为样品管,装在可弯折的波纹管内。第一种是一步冷冻分离CO2和H2O的收集方法,也是目前收集CO2气体的通常做法:先将整个真空管路抽好真空,然后将冷阱B的温度用液氮-酒精冷冻剂调至-60—-80℃,用于冷冻样品氧化生成的H2O,同时将收样管A浸在液氮中,准备收集CO2气体。抽好波纹管腔内真空后折断其内石英样品管C,样品中的H2O被冷冻在冷阱B内,而CO2气体则经过冷阱B,被液氮冷冻在收样管A内。冷冻5分钟后,抽掉管路中不能被冷冻住的杂质气体,以获得纯净的CO2气体供质谱测定。第二种是分步冷冻分离CO2和H2O的收集方法:抽好整个真空管路的真空,先将冷阱B的温度用液氮冷冻剂调至-196℃,将石英样品管C折断,样品氧化生成的H2O和CO2同时被冷冻在冷阱B内。冷冻5分钟后,抽掉管路中不能被冷冻住的杂质气体,然后将收样管A浸在液氮中,将冷阱B的液氮换成液氮-酒精冷冻剂,这时H2O仍被冷冻在冷阱B内,而CO2气体被释放出来,再被液氮冷冻收集在收样管A内。
本研究选取炭黑标准,测定不同杂质气体比例条件下,分别用两种冷冻收集方法收集的CO2的有机碳稳定同位素组成,结果如图4所示。杂质气体与CO2的比值为 0.008,用两种冷冻方法测得的结果很接近,均在误差范围内;杂质气体与CO2的比值为0.5,用第一种冷冻方法测得的结果比标准值偏负0.9‰,而用第二种方法测得的结果偏负0.17‰;杂质气体与CO2的比值为3时,用第一种方法测得的结果比标准值偏负2.71‰,而用第二种方法测得的结果仅偏负0.47‰。
从图中可以看出,杂质气体与CO2的比值低于0.2时,用两种冷冻方法收集得到的CO2气体稳定碳同位素组成没有显著差异。随着杂质气体的比例增高,两种冷冻方法获得的样品稳定碳同位素组成均呈偏负趋势,但第一种方法的结果比第二种方法的结果偏负的趋势更为显著,表明第二种收集方法能显著减小CO2收集过程中产生的同位素分馏。这可能是由于在相同的杂质气体背景条件下,第二种方法首先将CO2和H2O同时冷冻在冷阱B内,冷阱B的体积和液氮直接接触的表面积均比收样管A大,能够冷冻住更多的CO2气体,减小了因收集不完全产生的同位素分馏。第二种方法的第二步将CO2从冷阱B再冷冻至收样管A内的收集基本是完全的,因为收集5分钟后再次抽管路真空时真空计的读数几乎没有变化。以上结果表明第二种冷冻方法虽然也不能够完全收集CO2气体,但在相同杂质气体背景条件下,与第一种冷冻方法相比,显著减小了杂质气体对收集CO2的影响,提高了有机碳稳定同位素测定的准确度。
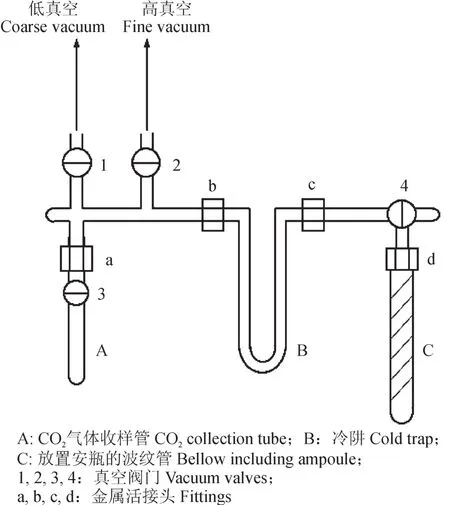
图3 封管法有机碳稳定同位素分析CO2气体纯化收集装置示意图Fig.3 Sketch of CO2gas puri fi cation and collection device by using sealed tube method for stable carbon isotope analysis
两种冷冻收集方法获得的不同天然样品的有机碳稳定同位素组成结果如表1所示。从结果中可以看出,两个装样量最多的样品(2)泥岩和Luo-193,也是有机碳含量相对较低的样品,用两种冷冻收集方法获得的有机碳同位素的差值最大,用第一种冷冻方法比第二种冷冻方法获得的碳同位素组成分别偏负0.52‰和0.56‰。同时在样品收集过程中也注意到(2)泥岩样品在冷冻收集CO2气体后,抽杂气时真空度下降最多,说明样品氧化生成的气体中杂质气体相对较多。
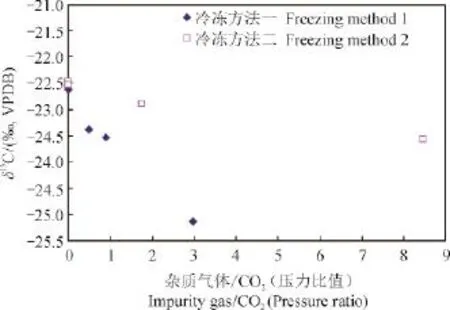
图4 两种冷冻方法收集CO2对GBW04407标准稳定碳同位素组成的影响Fig.4 The effects of two freezing methods on theδ13C of GBW04407 standard
因此,对于有机碳含量低,氧化产物中除CO2和H2O外,杂质气体含量高的天然样品,在纯化收集CO2气体时设法消除或减小收集过程中可能产生的碳同位素分馏,是减小样品有机碳稳定同位素测定误差的一个有效措施。
2.3 改进的小体积收样管
质谱测定要求被分析气体的离子流强度在一定的范围内,强度过高会超出检测限,过低会降低质谱的测定精度。因此样品生成CO2气体的离子流强度应在合适的范围内才能保证有机碳稳定同位素的测定精度和准确度。
传统使用的CO2气体收样管是油脂活塞收样管,活塞部分依靠真空脂密封。收样管内部体积为28 ± 2 mL。对于植物样品或有机质含量相对较高的土壤和沉积物样品,一般样品用量从2 —500 mg,用该收样管收集的CO2气体的离子流强度一般可达到1 V以上,能满足质谱仪准确测定的下限需要。但对于有机碳含量很低的样品,特别是老地层或岩石样品等,样品制备受样品量和石英反应管体积等的限制,样品氧化生成的CO2气体离子流强度非常低,仅零点几伏或更低,质谱测定的偏差会明显增大。
为提高此类样品测定的精确度,本研究从提高样品的离子流强度着手,将大体积油脂收样管改进为小体积无油脂收样管。改进的小体积收样管内部体积为1.4 ± 0.1 mL,仅为传统收样管体积的4%—6%。而且小体积收样管依靠优质橡胶圈密封,不使用真空脂,可避免真空油脂对系统的可能污染。

表1 两种冷冻方法收集CO2对不同天然样品有机碳稳定同位素组成的影响Tab.1 The effects of two freezing methods on theδ13C values of natural samples
为测试小体积收样管对提高样品离子流强度的效果,本研究选用太白山土壤样品,准确称量样品量,比较了传统油脂收样管与小体积无油脂收样管在相同样品用量条件下收集到的土壤样品SN-2产生的CO2气体的离子流强度,结果如图5所示。从图中可以看出,SN-2的样品量分别为5 mg、10 mg、15 mg、20 mg以及40 mg,用小体积收样管收集的CO2气体的m/z44离子流强度分别为0.8 V、1.5 V、2.2 V、2.8 V以及5.2 V,均显著高于用大体积收样管收集的CO2气体的m/z44离子流强度:0.4 V、0.9 V、1.4 V、2.0 V及4.2 V。离子流强度提高的幅度为24%—100%,平均提高58%。从结果中还可以看出,CO2气体的m/z44离子流强度相对越低,用小体积收样管收集的CO2气体的离子流强度提高的幅度相对越大,这将显著提高相同样品量条件下低有机碳含量样品的m/z44离子流强度。
用改进的小体积收样管收集的CO2气体的m/z44离子流强度显著高于大体积收样管收集到的CO2气体的离子流强度。这是由于在质谱仪上使用双路进样系统测试时,进样系统管路的体积是一定的,小体积收样管内CO2气体的压力相对较高,能够使收样管内的CO2气体更多地平衡到质谱仪的进样系统管路中,提高质谱仪管路中CO2气体的压力,从而提高样品m/z44的离子流强度,进而可提高低含量样品的测定精度。

图5 两种体积收样管收集的土壤样品(SN-2)离子流强度的比较Fig.5 Comparison of ion current intensities of soil sample (SN-2) by using collecting tubes with different volumes
3 结论
通过对封管法制备有机碳稳定同位素样品CO2气体收集过程的研究,得到以下结论:
(1)CO2气体纯化收集是封管法制备有机碳稳定同位素样品过程中一个重要的步骤。杂质气体干扰是CO2气体收集过程中一个重要影响因素,杂质气体与CO2气体的压力比值超过0.2,对GBW04407(炭黑)稳定碳同位素组成有显著影响,且杂质气体含量越高,对稳定碳同位素组成的影响越大。
(2)一步冷冻分离CO2和H2O及分步冷冻分离CO2和H2O这两种冷冻方法在杂质气体含量较低时对炭黑的有机碳稳定同位素组成没有显著影响;而当杂质气体与CO2的压力比值大于0.2时,一步冷冻分离CO2和H2O收集的CO2稳定碳同位素组成明显偏负,而分步冷冻CO2和H2O的方法能够显著减小CO2收集过程中产生的同位素分馏。
(3)利用改进的小体积收样管能有效提高样品CO2的离子流强度,尤其是当CO2气体的m/z44离子流强度低于1 V时,小体积收样管能够提高CO2气体的离子流强度60%以上,这将显著提高相同样品量条件下低有机碳含量样品的m/z44离子流强度,进而能够提高样品的质谱测定精度。
曹蕴宁, 刘卫国, 宁有丰, 等. 2005. 土壤有机碳同位素样品制备过程的影响因素讨论[J].地球化学, 34(4): 395 – 404. [Cao Y N, Liu W G, Ning Y F, et al. 2005. Effects of soil sample preparation process onδ13C of organic matter [J].Geochimica, 34(4): 395 – 404.]
迟云平, 张 洒, 吴 松, 等. 2012. 不同实验条件对早新生代沉积物有机碳同位素的影响[J].地球学报, 33(6): 967 – 976. [Chi Y P, Zhang S, Wu S, et al. 2012. The in fl uences of different experimental conditions on organic carbon isotopes of early Cenozoic sediments [J].Acta Geoscientica Sinica, 33(6): 967 – 976.]
段 毅, 罗斌杰. 1998. 深海现代沉积有机质碳同位素组成变化的古气候证据[J].海洋地质与第四纪地质, 18(4): 53 – 58. [Duan Y, Luo B J. 1998. Palaeoclimate evidence for carbon isotopic changes of organic matters in modern deep-sea sediments [J].Marine Geology & Quaternary Geology, 18(4): 53 – 58.]
李阳阳, 王 琴, 崔琳琳, 等. 2012. 不同分析方法对黄土有机碳同位素分析的影响[J].地球环境学报, 3(4): 936 – 941. [Li Y Y, Wang Q, Cui L L, et al. 2012. Differences inδ13C values of bulk organic matter from Chinese loess obtained using two analytic methods [J].Journal of Earth Environment, 3(4): 936 – 941.]
林本海, 刘荣谟. 1992. 最近800 ka黄土高原夏季风变迁的稳定同位素证据[J].科学通报, 37(18): 1691 – 1693. [Lin B H, Liu R M. 1992. Stable isotopic evidence of the summer monsoon evolution during the last 800 ka in Chinese Loess Plateau [J].Chinese Science Bulletin, 37(18): 1691 – 1693.]
刘荣谟, 刘 禹, 孙福庆. 1990. 安瓶法制备有机碳δ13C同位素样品方法[M]//佚名. 环境地球化学与健康. 贵阳: 贵州科技出版社: 123 – 125. [Liu R M, Liu Y, Sun F Q. 1990. Method for preparation organicδ13C samples by sealing tube method [M]// Anon. Environmental Geochemistry and Health. Guiyang: Guizhou Science and Technology Publishing House: 123 – 125.]
刘卫国, 宁有丰, 安芷生, 等. 2002. 黄土高原现代土壤和古土壤有机碳同位素对植被的响应[J].中国科学(D 辑), 32(10): 830 – 836. [Liu W G, Ning Y F, An Z S, et al. 2002. Modern soil and paleosol organic carbon isotope response to vegetation of Chinese Loess Plateau [J].Science in China (Series D), 32(10): 830 – 836.]
罗光强, 耿元波, 袁国富. 2009. 碳同位素在草地生态系统碳循环中的应用与展望[J].地理科学进展, 28(3): 441 – 448. [Luo G Q, Geng Y B, Yuan G F. 2009. Application and prospect of carbon isotope in the study of carbon cycle in grassland ecosystem [J].Progress in Geography, 28(3): 441 – 448.]
饶志国, 陈发虎, 曹 洁, 等. 2005. 黄土高原西部地区末次冰期和全新世有机碳同位素变化与C3/C4植被类型转换研究[J].第四纪研究, 25(1): 107 – 114. [Rao Z G, Chen F H, Cao J, et al. 2005. Variation of soil organic carbon isotope and C3/C4vegetation type transition in the western Loess Plateau during the last glacial and Holocene periods [J].Quaternary Sciences, 25(1): 107 – 114.]
沈 吉, 王 楚. 1997. 静态灼烧氧化法制备有机碳同位素质谱分析样品[J].分析测试技术与仪器, 3(2): 113 – 116. [Shen J, Wang C. 1997. Preparation of organic carbon isotopic sample formass spectrometric analysis by static combustion [J].Analysis and Testing Technology and Instruments, 3(2): 113 – 116.]
沈 吉, 吴瑞金, 安芷生. 1998. 大布苏湖沉积剖面有机碳同位素特征与古环境[J].湖泊科学, 10(3): 8 – 12. [Shen J, Wu R J, An Z S. 1998. Characters of the organicδ13C and paleoenvironment in the section of Dabusu Lake [J].Journal of Lake Sciences, 10(3): 8 – 12.]
王 楚, 沈 吉, 王苏民. 1992. 封管法制备有机碳同位素质谱分析样[J].湖泊科学, 4(4): 81 – 85. [Wang C, ShenJ, Wang S M. 1992. A method of sealing tube to prepare samples for mass spectrometric analysis of organic carbon isotopes [J].Journal of Lake Sciences, 4(4): 81 – 85.]
王国安, 张雷雷, 柳晓娟. 2012. 利用土壤有机质的碳同位素变化探讨环境因子和生物学因子对土壤有机碳周转的影响[J].地球环境学报, 3(4): 960 – 968. [Wang G A, Zhang L L, Liu X J. 2012. Assess the effects of environmental and biotic factors on the turnover of soil organic carbon through vertical variations in carbon isotope of soil organic matter [J].Journal of Earth Environment, 3(4): 960 – 968.]
王金权. 2005. 样品预处理对有机碳同位素分析结果的影响[J].古生物学报, 44(3): 472 – 477. [Wang J Q. 2005. Sample-pretreatment effects on analytical results of organic C-isotopes [J].Acta Palaeontologica Sinica, 44(3): 472 – 477.]
吴 夏, 黄俊华, 白 晓, 等. 2008. 沉积岩总有机质碳同位素分析的前处理影响[J].地球学报, 29(6): 677 – 683. [Wu X, Huang J H, Bai X, et al. 2008. Sample-pretreatment effects on analytical results of total organic carbon isotopes in sedimentary rocks [J].Acta Geoscientica Sinica, 29(6): 677 – 683.]
于贵瑞, 王绍强, 陈泮勤, 等. 2005. 碳同位素技术在土壤碳循环研究中的应用[J].地球科学进展, 20(5): 568 – 577. [Yu G R, Wang S Q, Chen P Q, et al. 2005. Isotope tracer approaches in soil organic carbon cycle research [J].Advances in Earth Science, 20(5): 568 – 577.]
袁红朝, 李春勇, 简 燕, 等. 2014. 稳定同位素分析技术在农田生态系统土壤碳循环中的应用[J].同位素, 27(3): 170 – 178. [Yuan H C, Li C Y, Jian Y, et al. 2014. Stable isotope technique in the soil carbon cycling research of agricultural ecosystems [J].Journal of Isotopes, 27(3): 170 – 178.]
张成君, 张宛漪, 樊 荣, 等. 2012. 湖泊环境早期成岩作用对沉积物中有机质C / N和碳同位素组成的影响[J].地球环境学报, 3(4): 1005 – 1012. [Zhang C J, Zhang W Y, Fan R, et al. 2012. Early diagenesis impacting C/N and organic isotopic compositions in the lacustrince sediments [J].Journal of Earth Environment, 3(4): 1005 – 1012.]
张恩楼, 沈 吉, 夏威岚, 等. 2002. 青海湖沉积物有机碳及其同位素的气候环境信息[J].海洋地质与第四纪地质, 22(2): 105 – 108. [Zhang E L, Shen J, Xia W L, et al. 2002. Environmental records from organic carbon and its isotope of Qinghai Lake sediment [J].Marine Geology & Quaternary Geology, 22(2): 105 – 108.]
张鸿斌. 1986. 有机碳、氢同位素质谱分析样静态制备技术[J].地球化学, 2: 108 – 112. [Zhang H B. 1986. A technique for static preparation of samples for mass spectrometric analysis of organic carbon and hydrocarbon isotopes [J].Geochimica, 2: 108 – 112.]
祝孟博, 宋建中, 彭平安. 2015. 预处理过程对不同类型样品中有机碳含量和稳定碳同位素测定的影响[J].地球与环境, 43(4): 476 – 482. [Zhu M B, Song J Z, Peng P A. 2015. Influences of pretreatment procedures on determination of total organic carbon and stable carbon isotope in different samples [J].Earth and Environment, 43(4): 476 – 482.]
Kuzyakov Y. 2006. Sources of CO2ef fl ux from soil and review of partitioning methods [J].Soil Biology & Biochemistry, 38: 425 – 448.
Liu W G, An Z S, Zhou W J, et al. 2003. Carbon isotope and C/N ratios of suspended matter in rivers: An indicator of seasonal change in C4/ C3vegetation [J].Applied Geochemistry, 18(8): 1241 – 1249.
Liu W G, Yang H, Cao Y N, et al. 2005. Did an extensive forest ever develop on the Chinese Loess Plateau during the past 130 ka?: A test using soil carbon isotopic signatures [J].Applied Geochemistry, 20 (3): 519 – 527.
Robinson D, Scrimgeour C M. 1995. The contribution of plant C to soil CO2measured usingδ13C [J].Soil Biology & Biochemistry, 27(12): 1653 – 1656.
Problems and improvements of preparing organic carbon stable isotope samples by sealing tube method
CAO Yunning1, LIU Weiguo1,2
(1. State Key Laboratory of Loess and Quaternary Geology, Institute of Earth Environment, Chinese Academy of Sciences , Xi'an 710061, China; 2. School of Human Settlement and Civil Engineering, Xi'an Jiaotong University, Xi'an 710049, China)
Background, aim, and scopeHigh precision measurement of organic carbon stable isotope (δ13C) is the basis for its application in the reconstruction of past changes in climate and vegetation types. It has been observed that the measurement error ofδ13C for samples with low organic carbon content was relatively large, partly due to the problem in the CO2collecting process. To solve this problem, the effect of CO2gas collecting process on theδ13C of organic carbon was investigated from three aspects: impurity gas on the process of CO2freezing, freezing CO2and H2O by one step and freezing CO2and H2O step by step, and the effect of collection tubes with different volumes.Materials and methodsThe national standard material (GBW04407) and different types of natural samples were analyzed using sealed tube method to study the effect of CO2gas collecting process on theδ13C oforganic carbon. The natural samples were treated with 2 mol·L-1HCl for 24 h at room temperature to remove carbonates and acid soluble organic material. The treated samples were washed with distilled water and dried at 40℃, and then were combusted for at least 2.5 h at 850℃ in an evacuated and sealed quartz tube in the presence of Cu oxide, Cu wire and Pt wire. The CO2was then puri fi ed and isolated by cryogenic distillation for C isotope analysis. To investigate the effect of CO2gas collecting process on theδ13C of organic carbon, the air pressure in the vacuum line was arti fi cially adjusted within the range of 0.05 mbar to 15.7 mbar; two CO2freezing methods were used, freezing CO2and H2O by one step and freezing CO2and H2O step by step; and two kinds of collection tubes with different volumes were used.ResultsThe results showed that: (1) in the CO2gas collection process, theδ13C values of standard material (GBW04407) were -22.61‰, -23.38‰ and -25.14‰ when the pressure ratio of air to CO2gas were 0.007, 0.48 and 2.96. Theδ13C values of soil sample (T-1) were -24.70‰, -25.01‰ and -25.15‰ when the pressure ratio of air to CO2gas were 0.004, 0.17 and 0.5. The results both showed a trend that the higher concentration of impurity gas, the lowerδ13C value of sample. When the impurity gas and CO2pressure ratio is larger than 0.2, the deviations ofδ13C values of GBW04407 and T-1 were greater than 0.2‰. (2) When the ratio of impurity gas to CO2ranges from 0 to 0.008, theδ13C values of GBW04407 obtained by the two freezing methods were very close, both within the error range; when the ratio of impurity gas to CO2was 0.5, theδ13C value of GBW04407 obtained by the fi rst freezing method (freezing CO2and H2O by one step) was 0.9‰ negative than the standard value, while the result by the second method (freezing CO2and H2O step by step) was 0.17‰ negative than the standard value; when the ratio of impurity gas to CO2was 3, theδ13C value of GBW04407 obtained by the fi rst freezing method was 2.71‰ negative than the standard value, while the result by the second method was only 0.47‰negative than the standard value. (3) A surface soil sample SN-2 were weighed 5 mg, 10 mg, 15 mg, 20 mg and 40 mg, the ion current intensity ofm/z44 produced by these samples were 0.8 V, 1.5 V, 2.2 V, 2.8 V, and 5.2 V, respectively by using a small volume of sample collection tube. Those were signi fi cantly higher than values obtained by using a large volume of sample collection tube, which are 0.4 V, 0.9 V, 1.4 V, 2.0 V, and 4.2 V, respectively.DiscussionIn experiments, we noted that the higher the content of impurity gases in the vacuum line, the lower the ion current intensity and theδ13C values of CO2gas. This suggests that the negative trend ofδ13C values of CO2with increasing content of impurity gases in vacuum line is not due to theδ13C values of impurity gas (air) itself, but because the CO2gas is not completely frozen. The method of freezing CO2and H2O step by step can decrease the fractionation of carbon isotope than freezing CO2and H2O by one step. Probably because with larger surface area of trap B, more CO2can be frozen there by liquid nitrogen. Therefore, this method decreases the fractionation of carbon isotope due to incomplete CO2freezing. The ion current intensity ofm/z44 of samples increased 100%—24%, 58% averagely by using small volume collection. This is because the CO2gas pressure is relatively high in small volume collection tube, so more CO2gas can balance into the mass spectrometer to enhance the ion current intensity ofm/z44 of sample, furthermore, enhancing ion current intensity ofm/z44 can improve the accuracy of isotope measurement.Conclusions(1) The puri fi cation and collection of CO2gas is an important step in the preparation of testing samples organic carbon stable isotope. The higher the concentrations of impurity gas in the sample, the greater the impact on theδ13C of sample; (2) with same impurity gas background, freezing CO2and H2O step by step can signi fi cantly reduce the in fl uence of impurity gas onδ13C of samples; (3) using collection tubes with small volume could significantly enhance the ion current intensity of CO2, and therefore can improve the accuracy ofδ13C measurements for samples with low organic carbon contents.Recommendations and perspectivesThe results provide a signi fi cant improvement for reducing errors ofδ13C measurements with low organic carbon contents. It is recommended that appropriate freezing method and sample collection tube can improve the accuracyand precision ofδ13C measurement.
organic carbon stable isotope; sample preparation; sealing tube method
LIU Weiguo, E-mail: liuwg@loess.llqg.ac.cn
10.7515/JEE201602010
2015-11-17;录用日期:2015-12-07
Received Date:2015-11-17;Accepted Date:2015-12-07
国家自然科学基金项目(41303010)
Foundation Item:National Natural Science Foundation of China (41303010)
刘卫国,E-mail: liuwg@loess.llqg.ac.cn
