临床微生物自动化的现状与展望
2016-02-26肖学会,陈学兵
·综述·
临床微生物自动化的现状与展望
肖学会 综述,陈学兵 审校
(湖北省荆门市第一人民医院检验科,湖北荆门 448000)
关键词:微生物技术;自动化;现状
传统的微生物诊断主要包括病原菌的培养、鉴定、药敏试验,耗时较长无法满足临床对快速诊断的需求[1]。虽然部分医院的细菌鉴定和药敏已经实现了自动化,但标本的接种、划线、分离、培养依旧靠手工操作。除少数发达国家外,极少有实验室达到了临床微生物的整体自动化。
随着科学技术的进步,临床微生物的自动化的时代已经来临。尤其是基质辅助激光解析离子飞行质谱的出现及液体转运培养基的使用[2-3],为临床微生物的自动化提供了巨大的可能性。
1阻碍临床微生物的自动化的几个因素
1.1临床微生物标本复杂临床生化、免疫和临床血液学以血标本为主,以真空采血管采集和传输,标本处理易于标准化和处理。临床微生物标本则不然,首先标本类型繁杂,既有液体类型的血液、体液标本,也有非液体类型的组织、大便等标本。其次是采集标本的容器大小、形态、容积各异。此外,标本的采集和运送方式亦是多种多样,如呼吸道的咽拭子在咽部采集,以运送培养基运送。血培养标本则需采集外周静脉血,注入特制的血培养瓶后运送。标本的处理复杂,有的标本需离心浓缩,有的标本需酶消化处理,有的标本需半定量接种,有的标本需定量接种。依据目标分离菌的不同特性,标本还需选择合适的培养基,放置在不同的温度、不同的气体环境中培养。依据不同微生物生长速度不同,在长短不一的生长时间内对目标菌进行观察。
1.2机器无法取代人的判断微生物检验操作过程中,每一步皆离不开人的经验性判断。如接种时平板类型的选择、划线分区方式,尤其是平板上生长菌落中可疑菌落与正常菌落的筛选[4],生化反应阴阳性的判读,血培养阳性污染菌的区分等,现行的仪器尚无法完全取代人脑的功能。
1.3自动化的成本高自动化设备占用空间大,硬件投入成本高,中小医院与经济不发达地区难以实现。由于临床微生物检验标本量不及临床生化和临床免疫学检验的标本量大,自动化设备虽能减轻工作量,但不能增加检验科的收入,加上临床微生物检验的试剂耗材支出比远高于临床生化检验,这也是导致临床微生物自动化普及不广的原因之一。
2推动临床微生物自动化的几个因素
2.1临床微生物标本量的增加由于人口老龄化,多重耐药菌的出现及感染控制的需要[5],临床微生物标本检测量以每年10%~15%的速度递增。越来越多的微生物实验室选择了每周7 d、每天24 h的工作模式来应对增长迅猛的工作量。选用临床微生物自动化设备可减轻工作量,缩短TAT[6]。一般情况下,微生物实验室工作人员会在每天早晨上班时间处理生长的平板和各种生化试管、药敏试验,若平板在中午或周末时间长出可见菌落,须等到隔日上午方能得到审阅并处理,这会导致不必要的时间延迟。若引入自动化设备,可快速报告检验结果。
2.2溯源性方面的诉求临床微生物标本类型复杂,大多实验室并未使用条码系统,而是以常规的编号处理标本。如果在接收标本、接种标本、培养标本、鉴定标本的任一环节出错,会导致最终结果出错。临床微生物自动化对标本从开始就采用条码系统标记,作为唯一识别代号,与人工编号相比,不易出错,且溯源性好。
2.3技术的进步临床微生物实验室引入了转送培养基转送标本,这类培养基的特点是不仅有采样拭子,还有一个液相的基质,液相基质使得标本中细菌得到匀质化,这为自动涂片和自动接种提供了可能。MALDI-TOFMS改变了传统微生物鉴定的模式:当平板上出现了可见菌落,无需革兰染色,直接将菌落涂布到检测板上,加入微量基质,干燥后放入飞行质谱仪内检测,结果可在10 min至1 h内检测出来。MALDI-TOF MS还可直接检测阳性血培养液[7]、尿液中的细菌和真菌[8]。数字图像技术与人工智能的发展 临床微生物自动化的一个设计难点在于机器无法取代人脑作出自己的判断。随着数字图像技术的发展[9],数字平板系统可实时监测到平板上的菌落生长情况,在电子屏幕上放大,直接观察菌落的大小、形态、溶血情况,数字平板系统还可检测到肉眼不可见的菌落。阴性标本可直接处理报告,阳性标本可依靠内置的逻辑规则,模拟人脑作出判断。如柯玛嘉念珠菌显色培养基上长出绿色的菌落,仪器会判读为白色念珠菌,结合平板上的标本条码号,将此ID号患者标本报告检出白色念珠菌。数字图像技术的应用,临床微生物技师可与临床医师实时共享标本信息,便于远程会诊和教学[10]。标本信息可保存很长时间,即使标本丢弃,标本的原始信息依然保留,便于溯源。
3当前临床微生物自动化进展
主要以分析前的自动标本接种以及分析中的自动平板孵育、自动平板影像系统为主。分析后以数据管理软件为主。
3.1分析前的自动化自动化的平板接种仪是一种用于划线接种培养基的革命性突破,以机器取代人工繁琐重复的劳动。自动化的平板接种仪可提高接种的准确性和重复性,且可分离更多数量的菌落,在混合菌感染时分离效果突出[11]。同时无需人工干预,提高了生物安全性。对于液基标本,皆选择全自动接种划线方式,而对于像组织类非液态标本,法国生物梅里埃的PREVI-Isola须先将这类标本在试管内用液体均质化,然后再按液基标本接种的方式。而BD公司的inoqulATM对固态标本,采用专利的磁性滚珠技术[12],在人工点样后,利用客户自己选择的划线模式,在各种不同的平板上接种,且获得的菌落数量是手工划线法的3~5倍。手工划线长度最长约125 cm,磁珠法划线长度最长约4 m。已上市的主要有4种产品有PREVI Isola、Innova、WASP和InoqulA[12]。
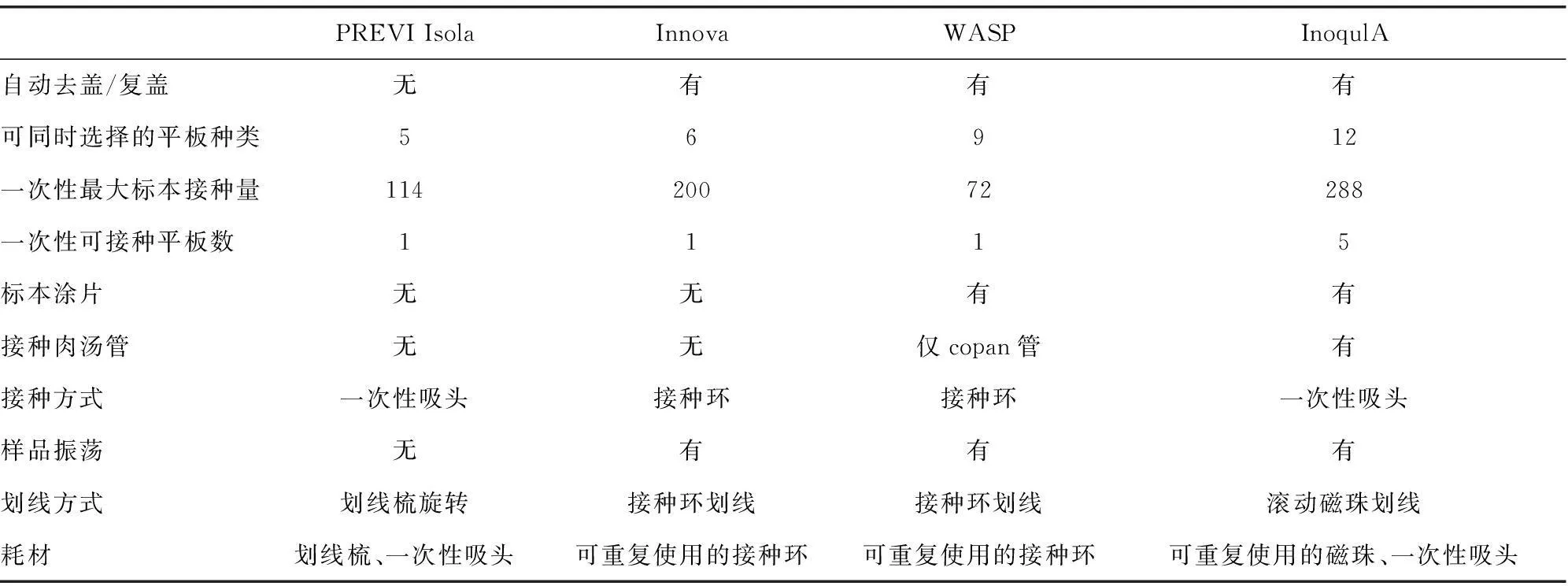
四种自动化的平板接种仪参数比较
3.2分析中的自动化分析中的自动化有自动平板孵育系统、智能数字平板读取系统。BD公司的inoqulATM自动平板孵育系统可依照平板上的条码,自动分类存储培养皿,每个孵育箱最多可保存1 150个培养皿。依据培养条件的不同存储培养皿,自动化的平板接种后可自动送入到自动平板孵育系统。精确控制的温湿度,保证微生物的最佳生长条件。培养后平板的处理是常规微生物工作中的一个繁琐耗时的环节,且通常在固定的时间处理。智能数字平板读取系统配备有高清拍照系统,提供优质的数字平皿影像。培养过程中,可根据用户设定的时间自动拍照定时传递培养结果。这大大改变了微生物检验的工作模式,数字平皿影像可在电脑屏幕或IPad上同时显示同一位患者的所有培养结果,并与患者的历史结果比对,工作站可放在独立的房间,也可在远程办公。由于用户可设定间隔时间自动拍照,可减少阳性标本的处理延迟时间,提高检验效率[9]。MALDI-TOF MS技术的出现加速了临床微生物自动化进程。Mutters等[13]将InoqulA kirestra全自动化的数字图像技术结合MALDI-TOF MS技术,对219例血培养进行快速鉴定,并与传统的鉴定方法比较。血培养报警阳性后,立即转种至血平板上,一旦自动化系统侦测到平板上长出菌落,将菌落放入飞行质谱仪内快速鉴定。结果发现此方法较传统法早30.6 h报告鉴定结果,鉴定成功率为98.4%,快速鉴定使12%的患者调整了适宜的抗菌药物治疗方案。BD公司正在研发一种装置,可从平板上直接将单个菌落接种在Bruker MALDI-TOF MS的测试板上,快速鉴定细菌和真菌。
3.3分析后的自动化分析后的数据管理,可更好地对鉴定和药敏结果上报临床。BD公司推出的数据管理软件BDEpicenterTM,在细菌鉴定和药敏结果出来后,可以不依赖微生物实验室发放报告,软件系统直接整合患者的检验结果,临床医生在工作站可马上获取结果。对于危急值结果,甚至可将结果直接推送到临床医生的手机上,可自动去除重复的数据进行流行病学分析。生物梅里埃的Myla对于危急值结果也可通过短信、网络报警灯的方式进行发布与远程警报,对多重耐药菌(MDRO)和血培养污染菌进行分析跟踪。
4微生物整体自动化解决方案
目前已推出或正在研发的微生物整体自动化产品主要有:BD的Kiestra TLA,生物梅里埃的FMLA,Copan的WASPLab。KiestraTLA于2006年首次装机,截至目前全球约40家用户。它主要包括自动平板分类(SortA),平板自动贴条码(BarcodeA),平板自动划线接种(InoqulA),带数字影像功能的智能孵育系统(ReadA)。该公司正在开发MalditofA模块能从平板挑取菌落,在Bruker质谱仪上快速鉴定。有研究者评估了使用Kiestra TLA前后TAT及检验效率的变化,显示了该系统的较传统手工检验的优势[14]。FMLA尚处于研发阶段,主要由Previ Isola自动接种仪、带数字影像功能的智能孵育系统,孵育系统间以轨道相连。Myla是控制整个系统的中间体软件。FMLA正在研发与VitekMS质谱仪相连,取单个菌落或菌悬液作快速鉴定和药物敏感试验。
WASPLab于2012年首次装机使用,主要由WASP自动平板接种仪、智能孵育系统、数字平皿系统组成。此系统的特色是系统给每个接种后的平板分配一个独立的位置,检验人员给出指令后可取出特定患者的平板人工审阅,判读后重新载入机器,也可仪器自动判读,仪器可自动进行药物敏感试验,当前也在考虑研发与Vitek MS 质谱仪或Bruker质谱仪整合进行快速鉴定。
5小结与展望
当前临床微生物自动化处于局部性和相对性的自动化阶段,整体的依赖轨道连接的自动化还处于研发之中[15]。制约临床微生物自动化的关键技术在于快速药物敏感试验,流式细胞术[16],MALDI-TOF MS可能会是快速药物敏感试验的两个突破点[17-18]。无疑,整体的临床微生物自动化可大大节省结果报告时间,更高效能、更高质量地为临床提供服务。但目前临床微生物整体自动化的现有用户不多,对它的功能评价有待更深入的研究。
参考文献
[1]Fazzeli H,Arabestani MR,Esfahani BN,et al.Development of PCR-based method for detection of Enterobacteriaceae in septicemia [J].J Res Med Sci,2012,17(7):671-675.
[2]Seng P,Rolain JM,Fournier PE,et al.MALDI-TOF-mass spectrometry applications in clinical microbiology[J].Future Microbiol,2010,5(11):1733-1754.
[3]Robinson GL,Harris AD,Morgan DJ,et al.Survival of methicillin-resistant Staphylococcus aureus and vancomycin resistant Enterococcus spp.for an extended period of transport[J].J Clin Microbiol,2012,50(24):2466-2468.
[4]Bourbeau PP,Ledeboer NA.Automation in clinical microbiology.[J].J Clin Microbiol,2013,51(16):1658-1665.
[5]Peterson LR,Hamilton JD,Baron EJ,et al.Role of clinical microbiology laboratories in the management and control of infectious diseases and the delivery of health care[J].Clin Infect Dis,2001,32(4):605-611.
[6]Bourbeau PP,Swartz BL.First evaluation of the WASP,a new automated microbiology plating instrument [J].Clin Microbiol,2009,47(10):1101-1106.
[7]Konnerth S,Rademacher G,Suerbaum S,et al.Identification of pathogens from blood culture bottles in spiked and clinical samples using matrix-assisted laser desorption ionization time-of-flight mass-spectrometry analysis[J].BMC Res Notes,2014,27(4):405.
[8]Burillo A,Rodríguez-Sánchez B,Ramiro A,et al.Gram-stain plus MALDI-TOF MS (Matrix-Assisted Laser Desorption Ionization-Time of Flight Mass Spectrometry) for a rapid diagnosis of urinary tract infection[J].PLoS One,2014,9(1):e86915.
[9]Franco G.Zeroing in on digital imaging in microbiology[J].MLO Med Lab Obs,2014,46(1):20-21.
[10]Ledeboer NA,Dallas SD.Point-counterpoint:the automated clinical microbiology laboratory:fact or fantasy[J].J Clin Microbiol.,2014,52(30):3140-3146.
[11]Froment P,Marchandin H,Vande Perre P,et al.Automated versus manual sample inoculations in routine clinical microbiology:a performance evaluation of the fully automated InoqulA instrument[J].J Clin Microbiol,2014,52(7):796-802.
[12]Novak SM,Marlowe EM.Automation in the clinical microbiology laboratory[J].Clin Lab Med,2013,33(3):567-588.
[13]Mutters NT,Hodiamont CJ,de Jong MD,et al.Performance of Kiestra total laboratory automation combined with MS in clinical microbiology practice[J].Ann Lab Med,2014,34(2):111-117.
[14]Mischnik A,Mieth M,Busch CJ,et al.First evaluation of automated specimen inoculation for wound swab samples by use of the Previ Isola system compared to manual inoculation in a routine laboratory:finding a cost-effective and accurate approach [J].J Clin Microbiol,2012,50(26):2732-2736.
[15]王云峰.自动化临床微生物实验室建设与感染性疾病临床实验室诊断的现状与展望[J].中华检验医学杂志,2013,36(7):592-594.
[16]Rudensky B,Broide E,Berko N,et al.Direct fluconazole susceptibility testing of positive Candida blood cultures by flow cytometry[J].Mycoses,2008,51(3):200-204.
[17]Vogne C,Prod′Hom G,Jaton K,et al.A simple,robust and rapid approach to detect carbapenemases in Gram negative isolates by MALDI-TOF mass spectrometry:validation with triple quadripole tandem mass spectrometry,microarray and PCR[J].Clin Microbiol Infect,2014,20(12):1106-1112.
[18]Ovia?o M,Fernández B,Fernández A,et al.Rapid detection of enterobacteriaceae producing extended spectrum beta-Lactamases directly from positive blood cultures by matrix-assisted laser-desorption-ionization time-of-flight mass spectrometry (MALDI-TOF-MS)[J].Clin Microbiol Infect,2014,20(11):1146-1157.
更正
本刊2015年第36卷第23期3437页《早产窒息新生儿同型半胱氨酸联合心肌酶测定的临床价值》作者单位由“延吉市第二人民医院检验科”更正为“延边第二人民医院检验科”,作者简介由“李春姬,男,副主任检验医师,主要从事临床生物化学与检验研究”更正为“李春姬,女,主管技师,主要从事临床生物化学与检验研究”。
《国际检验医学杂志》编辑部
2016年1月10日
(收稿日期:2015-09-28)
DOI:10.3969/j.issn.1673-4130.2016.01.035
文献标识码:A
文章编号:1673-4130(2016)01-0080-03
作者简介:肖学会,女,副主任技师,主要从事临床微生物检验研究。
