维药铁线蕨总黄酮抗炎平喘作用研究
2016-02-18阿迪拉木阿依甫江麦合苏木艾克木古孜力努尔依马木阿不都热依木玉苏甫
阿迪拉木·阿依甫江, 麦合苏木·艾克木, 古孜力努尔·依马木, 阿不都热依木·玉苏甫
(1新疆医科大学维吾尔医学院, 乌鲁木齐 830011;2新疆维吾尔自治区中医民族医药管理局, 乌鲁木齐 830001)
维药铁线蕨总黄酮抗炎平喘作用研究
阿迪拉木·阿依甫江1, 麦合苏木·艾克木1, 古孜力努尔·依马木1, 阿不都热依木·玉苏甫2
(1新疆医科大学维吾尔医学院, 乌鲁木齐830011;2新疆维吾尔自治区中医民族医药管理局, 乌鲁木齐830001)
摘要:目的研究维药铁线蕨总黄酮(Total Flavones from Adiantum capillus-veneris L.,TFAV)的抗炎平喘作用。方法将实验动物昆明种小鼠随机分为TFAV低、中、高剂量组(0.1、0.2、0.4 g/kg体质量)和生理盐水组、阳性对照组(急支糖浆),采用小鼠耳廓二甲苯致炎法、小鼠氨水引咳法、小鼠气管酚红排泌法观察TFAV的抗炎、止咳、化痰作用。将实验动物豚鼠随机分为TFAV低、中、高剂量组(0.061、0.122、0.244 g/kg体质量)和生理盐水组、阳性对照组(氨茶碱,0.025 g/kg体质量),采用整体动物药物引喘法观察TFAV的平喘作用。以昆明种小鼠为实验动物,按最大给药量法(药物最大浓度为0.5 g/mL,最大剂量为0.04 mL/g)灌胃给药,连续观察15 d,评价铁线蕨总黄酮单次口服给药的安全性。并根据单次口服给药的安全性结果,将60只昆明种小鼠随机分为实验Ⅰ、Ⅱ组和空白对照组,灌胃给药,连续观察7 d,测定出最大给药量。结果与空白对照组比较,TFAV能显著抑制小鼠耳廓肿胀(P<0.05);TFAV能延长小鼠咳嗽潜伏期(P<0.05),并减少咳嗽次数(P<0.05);TFAV可促进小鼠气管酚红分泌量(P<0.05);可延长豚鼠哮喘潜伏期(P<0.05)。急性毒性实验中未出现中毒反应及死亡。小鼠口服TFAV最大给药量为40 g/kg体质量,相当于60 kg体质量成人临床生药日用量的160倍。结论TFAV具有良好的抗炎、镇咳、祛痰及平喘作用;TFAV口服急性毒性小,安全性高。
关键词:铁线蕨总黄酮; 抗炎; 止咳; 祛痰; 平喘; 急性毒性
铁线蕨(Adiantum capillus-veneris L.)为铁线蕨科铁线蕨的全草,其分布广泛,在中国主要分布于长江以南各省区,北达陕西、甘肃和河北等地。在新疆主要产于北部(阿勒泰地区)山区[1]。铁线蕨是维吾尔医常用药材,是维吾尔医复方制剂异常黑胆质成熟剂的组成药之一,其具有消炎解毒、止咳化痰、平喘利肺、消肿止痛等功效,临床上常用于哮喘、胸肺黏稠性顽疾、肺炎、头痛胸痛、气喘气短、久咳痰多、发烧等症[2]。有研究报道,铁线蕨提取物具有抗炎、止咳、祛痰、平喘等作用[3]。但对其活性成分及治疗哮喘等呼吸系统疾病的作用机理等方面的研究尚未见报道。本研究通过相关的药理实验探讨TFAV的抗炎、止咳、祛痰、平喘及急性毒性作用,阐明铁线蕨治疗哮喘等呼吸系统疾病的物质基础,评价其安全性,旨在为铁线蕨资源的开发和利用提供科学依据。
1材料与方法
1.1仪器与试剂电热恒温水浴锅(北京市光明医疗仪器有限公司,DZKW-S-4),电子天平(上海舜宇恒平科学仪器有限公司,XS1003S),UV-240型分光光度计(上海棱光技术有限公司,GD5410023),数控超声波清洗器(昆山市超声仪器有限公司,KQ3200DE)。二甲苯(天津市福晨化学试剂厂,批号:20131124),急支糖浆(太极集团重庆涪陵制药厂有限公司,批号:141011248),浓氨水(天津市福晨化学试剂厂,批号:20140327),氯化乙酰胆碱(国药集团化学试剂有限公司,批号:131126),磷酸组胺(上海源叶生物科技有限公司,批号:20131009),氨茶碱(山西云鹏制药有限公司,批号:B141101),苯酚红、碳酸氢钠(分析纯)。
1.2实验动物昆明种小鼠(体质量为18~22 g)、豚鼠(体质量为160~200 g)均为清洁级,由新疆医科大学实验动物中心提供[生产许可证:SYXK(新)2011-0001]。
1.3实验药材铁线蕨全草药由新疆维吾尔医院门诊药房提供,经新疆维吾尔医院制剂中心质检部主任药师艾尼外尔·塔力甫鉴定为铁线蕨科铁线蕨(Adiantum capillus-veneris L.)的全草(批号:20141002)。总黄酮粉末由本课题组前期对铁线蕨全草采用50%乙醇回流提取,经大孔树脂和聚酰胺纯化而得,总黄酮质量分数>50%。
1.4实验方法
1.4.1小鼠耳廓二甲苯致炎实验[4]昆明种小鼠50只,随机分成5组:空白对照组(0.9%氯化钠溶液)、阳性对照组(急支糖浆,5.0 g/kg体质量)及 铁线蕨总黄酮(TFAV)低、中、高剂量组(0.1、0.2、0.4 g/kg体质量),每组10只,雌雄各半。连续灌胃给药7 d,灌胃体积均为0.02 mL/g。末次给药后30 min,于小鼠右耳两侧均匀涂布二甲苯0.03 mL致炎,左耳不涂作为对照。致炎1 h后颈椎脱臼处死小鼠,以直径为8.00 mm的打孔器取双耳对称耳片,精密称取,以左、右耳片重量差为肿胀程度,计算肿胀抑制率:
抑制率=(平均肿胀度空白对照组-平均肿胀度给药组)/平均肿胀度空白对照组×100%
1.4.2小鼠氨水引咳实验[5]昆明种小鼠50只,雄雌各半,随机分为5组:空白对照组(0.9%氯化钠溶液)、阳性对照组(急支糖浆,5.0 g/kg体质量)及TFAV低、中、高剂量组(剂量同“1.4.1”项下),每组10只。连续灌胃给药7 d。于末次给药后1 h,将小鼠放入体积为2.5 L的密闭的玻璃钟罩内,用氨水(浓度为25%)喷雾,每次5 s,以小鼠出现咳嗽的时间(从喷雾开始到小鼠出现咳嗽的时间)、咳嗽次数(5 min内的咳嗽次数)为观察指标。
1.4.3小鼠气管酚红排泌实验[6]昆明种小鼠50只,随机分为5组:空白对照组(0.9%氯化钠溶液)、阳性对照组(急支糖浆,5.0 g/kg体质量)及TFAV低、中、高剂量组高(剂量同“1.4.1”项下),雄雌各半,每组10只。连续灌胃给药7 d,于末次给药后30 min,腹腔注射5 g/L酚红生理盐水溶液0.01 mL/g,30 min后处死动物,仰位固定,解剖分离出气管,分别放入预先盛有2.0 mL 5% NaHCO3溶液的试管中,超声波清洗15 min,使气管段中的苯酚红完全释放,离心,取上清液,用分光光度计于560 nm处比色,测定OD值,折算成酚红含量。
1.4.4整体动物药物引喘法[7]取健康豚鼠60只,雄雌兼用,体质量150~200 g,先将豚鼠分别置于2.5 L的玻璃钟罩内,以恒压喷入2%氯化乙酰胆碱和0.1%组胺等溶剂混合液15 s引喘,喷雾停止后立即观察豚鼠出现喘息性抽搐的潜伏期(即从喷雾开始到哮喘发作,直至抽搐跌倒的时间),选择潜伏期小于120 s的豚鼠用于正式实验,并以此作为给药前潜伏期。挑选合格动物,随机分为5组:空白对照组(0.9%氯化钠溶液)、阳性对照组(氨茶碱,125 mg/kg体质量)及TFAV低、中、高剂量组(0.061、0.122、0.244 g/kg体质量)。连续灌胃给药7 d,于末次给药后1 h分别置于2.5 L的玻璃钟罩内,用上述的引喘方法引喘,记录豚鼠的引喘潜伏期,超过360 s以360 s计算。
1.5急性毒性实验
1.5.1预实验[8]取昆明种小鼠20只,雌雄各半,随机分为实验组与对照组,每组10只。适应性饲养3 d。给药前禁食不禁水14 h,称重。实验组按最大给药浓度(0.5 g/mL)和最大剂量(0.04 mL/g)一次灌胃TFAV。对照组灌胃等量的生理盐水。给药后再禁食2 h并立即观察动物反应,包括饮食、活动、体毛、排泄、精神状态等情况。连续定时观察15 d,详细记录期间小鼠死亡数和一般情况。观察给药前后第0、1、3、5、7、9、11、13天及处死之前小鼠体质量变化情况。第14天将全部动物处死、解剖,检查主要脏器有无异常病变情况。
1.5.2最大给药量的测定[9]昆明种小鼠60只,随机分成3组:实验Ⅰ、Ⅱ组与空白对照组,每组20只,雌雄各半。给药前禁食不禁水14 h,称重。实验组以最大给药浓度(0.5 g/mL)和最大给药剂量(0.04 mL/g)灌胃,其中实验I组每日1次,实验Ⅱ组每日2次灌胃,间隔为8 h,灌胃1 d。空白对照组灌胃等量的生理盐水。连续定时观察7 d。详细观察并记录小鼠的饮食、活动、体毛、排泄、精神状态以及给药前后0、3、5 d和处死之前小鼠体质量变化情况。第7天将小鼠全部处死、解剖,检查主要脏器有无异常病变情况,计算最大给药量。
1.6统计学方法采用SPSS 17.0软件对数据进行统计学处理,实验数据以均数±标准差(-x±s)表示。两组间比较采用t检验,多组比较采用单因素方差分析,以P<0.05为差异具有统计学意义。
2结果
2.1小鼠耳廓二甲苯致炎实验结果与空白对照组比较,阳性对照组及TFAV高剂量组小鼠耳廓肿胀度差异有统计学意义(P<0.05);TFAV低、中、高剂量组的肿胀抑制率随剂量的增加而升高,见表1。

表1 TFAV对二甲苯致小鼠耳肿胀的影响(-x±s, n=10)
注:与空白对照组比较,*P<0.05。
2.2小鼠氨水引咳实验结果与空白对照组比较,阳性对照组及TFAV中、高剂量组小鼠咳嗽反应的潜伏期及咳嗽次数差异有统计学意义(P<0.05~0.01),见表2。
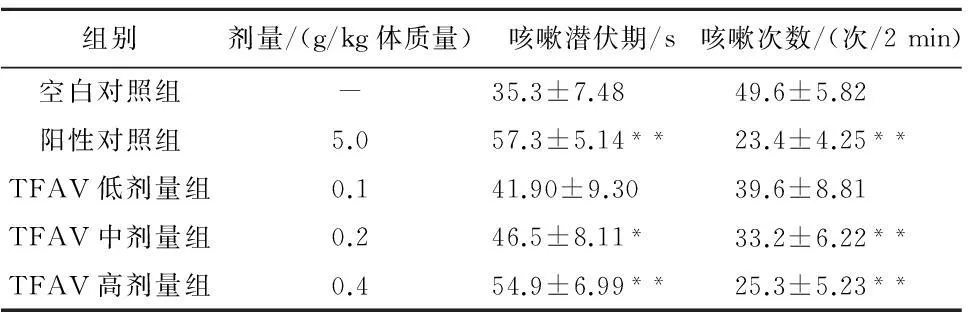
表2 铁线蕨总黄酮对小鼠咳嗽反应的影响(-x±s, n=10)
注:与空白对照组比较,*P<0.05,**P<0.01。
2.3小鼠气管酚红排泌实验结果酚红的标准曲线为Y=193.66X-0.001 52,r=0.999 4。与空白对照组比较,阳性对照组和TFAV中、高剂量组小鼠气管酚红排泄量差异有统计学意义(P<0.05),见表3。
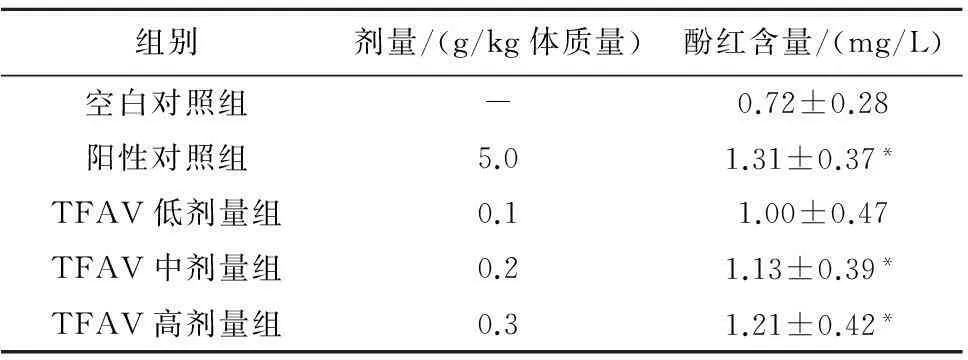
表3 铁线蕨总黄酮对气管酚红排泄量的影响(-x±s, n=10)
注:与空白对照组比较*P<0.05。
2.4整体动物药物引喘法结果与空白对照组比较,阳性对照组及TFAV中、高剂量组豚鼠的引喘潜伏期差异有统计学意义(P<0.05),与给药前比较,阳性对照组及TFAV低、中、高剂量组豚鼠的引喘潜伏期差异有统计学意义(P<0.05),见表4。
表4豚鼠喷雾致喘实验(-x±s, n=10)

组别剂量/(g/kg体质量)引喘潜伏期/s给药前给药后空白对照组-73.4±10.973.2±10.6阳性对照组0.12577.7±17.5102.0±20.4*#TFAV低剂量组0.178.2±18.980.3±23.7#TFAV中剂量组0.270.6±15.187.1±14.4*#TFAV高剂量组0.474.0±12.195.6±13.5*#
注:与空白对照组比较,*P<0.05;与给药前比较,#P<0.05。
2.5急性毒性预实验通过预实验发现,最大给药量法灌胃给药观察14 d,实验组小鼠外观、饮食状况、呼吸及四肢活动正常,未见异常分泌物,无一只死亡。各组小鼠平均体质量显著增长(P<0.01)。与对照组相比,实验组小鼠毛发更为光亮。解剖小鼠,与对照组相比,实验组小鼠主要脏器未出现肉眼可见的明显病变,见表5。
2.6急性毒性实验最大给药量的测定预实验过程中未见小鼠出现明显的中毒症状,测不出LD50,因此进行最大给药量的测定。实验Ⅱ组第2次灌胃后小鼠出现不动、卧等体征,但无抽搐、惊厥等异常现象,灌胃后1~3 h后逐步恢复正常。给药后第2天实验Ⅱ组小鼠明显兴奋、不静。与对照组比较,实验I、Ⅱ组小鼠在饮食、外观、精神状态方面无明显差异。7 d后解剖,发现主要脏器未出现肉眼可见的明显病变。各组小鼠体质量明显增加(P<0.05),但各组体质量差异无统计学意义(P>0.05)。小鼠口服TFAV 最大给药量为每天40 g/kg体质量,见表6、7。

表5 TFAV对小鼠体质量的影响(-x±s, n=10)

表6 TFAV耐受量实验小鼠体质量变化(-x±s, n=20)

表7 TFAV急性毒性实验小鼠反应情况
3讨论
铁线蕨是维吾尔医常用药材,全草入药,主要含黄酮类、挥发油、三萜类、糖类、甾体类等化学成分,具有消炎解毒、止咳化痰、平喘利肺、消肿止痛等功效。铁线蕨对哮喘等呼吸系统疾病的治疗效果显著。呼吸系统疾病的临床表现有气道高反应、黏液高分泌以及可逆性的气流受限,气道的慢性非特异性炎症是其基本的病理变化[10]。本研究显示,在急性炎症模型中,TFAV高剂量能显著地抑制小鼠耳廓肿胀(P<0.05),抑制率随着剂量的增加而升高,说明TFAV对炎症反应所致的呼吸系统疾病有一定治疗作用。本实验应用化学刺激法,用浓氨水雾化吸入,刺激小鼠副交感神经系统引发咳嗽,结果表明TFAV中、高剂量对氨水引发的咳嗽具有显著的拮抗作用(P<0.05),能延长浓氨水诱导的小鼠咳嗽潜伏期,减咳嗽次数,表明其具有明显的止咳作用。痰液是引起咳嗽的重要因素之一,呼吸道上所积累的痰状物质会刺激黏膜引起咳嗽。因此通过稀释痰液,改善呼吸道分泌物的增加,可以挥发祛痰作用[5]。本实验采用小鼠气管酚红分泌法观察TFAV的祛痰作用,结果表明TFAV中、高剂量明显增加小鼠气管的酚红排泌量(P<0.05),提示TFAV增加气管分泌液,使呼吸道分泌物利于咳出,从而达到化痰作用。在组胺-乙酰胆碱致豚鼠哮喘实验中,TFAV中、高剂量均能明显延长豚鼠哮喘的潜伏期(P<0.05),提示TFAV通过拮抗组胺、氯化乙酰胆碱对气管平滑肌的痉挛作用,抑制气道反应性,从而发挥平喘作用。
药物安全性评价是判断新药安全性的关键。急性毒性实验可以为药物对机体的毒效应提供初步资料[11]。本研究通过急性毒性实验发现,15 d内各组小鼠饮食和活动状况良好,未出现中毒反应及死亡。单次灌胃的最大剂量达到20 g/kg体质量,超过了安全剂量(10 g/kg体质量)[7],由此证明TFAV急性毒性实验是安全的。实验组小鼠毛发更为光亮,TFAV可能有促毛发生长的作用。通过最大给药量实验发现给药后第2天实验Ⅱ组小鼠明显兴奋、
不静,由此可见TFAV可能有兴奋作用。小鼠最大给药量为40 g/kg体质量,相当于60 kg体质量成人临床生药日用量的160倍。
综上所述,本研究结果提示,TFAV具有良好的抗炎、止咳、化痰、平喘作用,说明黄酮类成分是铁线蕨治疗哮喘等呼吸系统疾病的活性部位之一,本研究结果为铁线蕨的临床应用提供了一定依据,但其作用机理有待进一步研究。虽然TFAV急性毒性实验结果显示其安全性较高,但其观察时间较短,还需要进一步进行长期毒性实验,以保证临床用药的安全性。
参考文献:
[1]新疆维吾尔自治区卫生厅.维吾尔药材标准[S].乌鲁木齐:新疆科技卫生出版社,1993:297.
[2]中华人民共和国卫生部药典委员会.中华人民共和国卫生部药品标准[S].乌鲁木齐:新疆科技卫生出版社,1999:78.
[3]Ibraheim ZZ, Ahmed AS, Gouda YG. Phytochemical and biological studies of Adiantum capillus-veneris L. [J]. Saudi Pharmaceutical J, 2011, 19(2):65-74.
[4]麦合苏木·艾克木,努尔江·肉孜,于洋.维药神香草乙酸乙酯部位的抗炎、止咳、化痰、祛痰及平喘作用研究[J]. 中国民族医药杂志,2014,20(4):39-42.
[5]陈晓芳,张倩,吴文倩,等.枇杷花醇提物止咳化痰作用实验研究[J].中成药,2013,35(1):167-169.
[6]王丹,向阳,常军民.天山花楸平喘胶囊镇咳、祛痰、平喘、抗炎及免疫作用研究[J].中国实验方剂学杂志,2013,19(23):262-265.
[7]张宏涛,张淑锋,陈雪莲,等.瘤果黑种草子总黄酮抗炎及平喘作用[J]. 中国实验方剂学杂志,2014,20(1):166-169.
[8]杨鸿,吴彦,刘钊,等.抗氧化中药有效组分复方的急性毒性及致突变性研究[J].中国实验方剂学杂志,2014,20(12):185-189.
[9]姜华,张丽,黄聪琳,等. 藏药镰形棘豆总黄酮苷元急性毒性实验研究[J].西部中医药,2013,26(8):50-52.
[10]史锁芳,杨兴蟋,李萍.平喘颗粒药效学及抗炎机理研究[J].中国中医急症,2014,23(6):1056-1059.
[11]周立国.药物毒理学[M].北京:中国医药出版社,2003:146-162.
(本文编辑施洋)
·基础医学研究·
·民族肿瘤学·
Anti-inflammatory and anti-asthmatic effects of total flavones from
Adiantum capillus-veneris L. on animal models
Ayupjan Adila1, Ekim Mahsum1, Iman Guzalnur1, Yusup Abduriyim2
(1InistituteofTraditionalUyghurMedicine,XinjiangMedicalUniversity,Urumqi830011,China;
2AdministrationBureauofTraditionalChineseMedicineandEthnicGroupMedicineof
XinjiangUyghurAutonomousRegion,Urumqi830001,China)
Abstract:ObjectiveTo evaluate the anti-inflammatory and anti-asthmatic effects of total flavones from Adiantum capillus-veneris L. (TFAV). MethodsThe Kunming mice were randomly devided into TFAV low-dose group (0.1g/kg), mid-dose group (0.2g/kg),high-dose group (0.4 g/kg), control group and Jizhi syrup group and mice models, ie, ear edema induced by xylene, cough induced by ammonia, tracheal phenol red excretion were set up to observe the anti-inflammatory, antitussive and expectorant effects of TFAV. guinea pigs were randomly devided into TFAV low-dose group(0.061 g/kg), mid-dose group(0.122 g/kg), high-dose group(0.24g/kg), control group and aminophylline group(0.025g/kg) and asthma model was induced by chemicals to observe the antiasthma effects of TFAV. Kunming mice received intragastic (ig) administration by maximum dosage method (Maximum drug concentration for 0.5 g/mL,Maximum dose for 0.04 mL/g). The reaction of mice was observed in the 15 days. Base on the results, sixty mice were randomly divided into the control groupⅠ,Ⅱ, and control group and observed 7 days. ResultsCompared with the control group,TFAV could decrease ear swelling and the frequency of cough (P<0.05), prolong the latent period (P<0.05), promote tracheal phenol red excretion (P<0.05) and prolonged make the guinea pig asthma latency. No acute toxicity was observed in the control group. The maximum dosage of TFAV by ig in mice was 40 g/kg body mass, which was about 160 times of adult chemical daily dose (15 g). ConclusionTFAV has the significant anti-inflammatory, antitussive, expectorant and antiasthma effects; TFAV is safe to a certain extent.
Keywords:total flavones of Adiantum capillus-veneris L.; anti-inflammatory; antitussive; expectorant; antiasthma; toxic effects
通信作者:谢惠芳,女,副教授,博士,研究方向:环境与健康,E-mail:xhfworld@sina.com。 马遇庆,女,博士,教授,主任医师,硕士生导师,研究方向:食管癌基础研究,E-mail: mayuqing-patho@hotmail.com。
作者简介:董娟娟(1988-),女,硕士,研究方向:环境与健康研究。 李梦妍(1982-),女,在读硕士,住院医师,研究方向:食管癌基础研究。
基金项目:国家自然科学基金 (81460480),新疆维吾尔自治区高校科研计划项目(XJEDU2012I26) 国家自然科学基金(81260308),新疆重大疾病医学重点实验室开放课题项目(SKLIB-XJMDR-2014-12)
[收稿日期:2015-7-29]
doi:10.3969/j.issn.1009-5551.2016.01.004
中图分类号:R969
文献标识码:A
文章编号:1009-5551(2016)01-0017-05
