溶剂热法制备石墨烯/Sb2S3纳米复合材料及其光催化性能
2016-02-07朱启安王建霞胡耐根魏明扬杜寒宇蒋叔立
朱启安, 王建霞, 胡耐根, 魏明扬, 杜寒宇, 蒋叔立
(1. 湘潭大学 化学学院,环境友好化学与应用省部共建教育部重点实验室,湖南 湘潭 411105;2.新余学院 新能源科学与工程学院,江西 新余 338004)
溶剂热法制备石墨烯/Sb2S3纳米复合材料及其光催化性能
朱启安1*, 王建霞1, 胡耐根2, 魏明扬1, 杜寒宇1, 蒋叔立1
(1. 湘潭大学 化学学院,环境友好化学与应用省部共建教育部重点实验室,湖南 湘潭 411105;2.新余学院 新能源科学与工程学院,江西 新余 338004)
以天然鳞片石墨为原料,通过改进的Hummers法制备了氧化石墨(GO),然后以GO、三氯化锑(SbCl3)和硫代乙酰胺(CH3CSNH2, TAA)为反应物,1,2-丙二醇为溶剂,通过溶剂热法制备了石墨烯/Sb2S3(RGO/Sb2S3)纳米复合材料.用XRD、FT-IR、SEM、UV-Vis DRS、PL光谱等手段对复合材料的物相、官能团、形貌和光学性能进行了表征;并通过降解罗丹明B(RhB)对其光催化活性进行了考察.结果表明:所制备的复合材料中Sb2S3为正交晶相;Sb2S3与复合材料对可见光均有较强吸收,其能带间隙分别为1.55 eV和1.43 eV;PVP和GO的浓度对材料的形貌、复合效果和光催化活性有重要的影响,当GO浓度为0.5 mg/mL时,所制备复合材料(RGO/Sb2S3-0.5)的复合效果最好,有很多粒径为85~100 nm的硫化锑纳米颗粒附着在石墨烯片层表面及片层之间,其在PL谱中的发射峰最低,光生电子-空穴对的分离效果最好,光催化效率最高,在300 W氙灯照射下,9 h后其降解率达90%以上,是纯Sb2S3的1.3倍.另外,以对苯二甲酸(TA)为荧光探针,证明了光催化过程中羟基自由基(·OH)的存在;通过加入·OH消耗剂维生素C(Vc),进一步证明了在光催化过程中·OH起了非常重要的作用.
硫化锑;石墨烯;复合材料;光催化
当前,人类面临着十分严重的环境污染问题,这已成为制约人类社会发展的瓶颈.半导体多相光催化技术由于能直接利用太阳光和空气中的氧气来彻底降解环境中的有毒有害污染物而受到人们的普遍关注.而Sb2S3是一种Ⅴ-Ⅵ族的重要直接带隙半导体材料,其在可见光区具有很大的光吸收系数(α=105cm-1)和相对狭窄的能带间隙(大约1.7 eV),使其在利用太阳光光催化[1-5]降解环境污染物方面拥有巨大的应用前景.但是,用Sb2S3作光催化剂与许多其他的光催化剂一样,存在着光生电子-空穴对容易复合、光催化效率低的缺陷.石墨烯(graphene)是一种具有sp2杂化的单原子层碳材料,其中存在的大π键使得π电子能够自由移动,这种特殊的结构使得石墨烯具有许多优异性能,如突出的导热性能和力学性能、完美的量子隧道效应以及半整数量子霍尔效应,特别是极高的电子迁移率[200 000 cm2/(V·s)]和强导电能力[6-7],若将其与Sb2S3等半导体材料复合既可以利用Sb2S3对可见光吸收能力强的特点,又可利用石墨烯电子迁移率高、导电能力强的特点,促进光生电子-空穴对的分离,从而提高Sb2S3在可见光下的光催化效率.另外,石墨烯拥有巨大的比表面积(2 630 m2/g),在光催化过程中能吸附反应物而使反应物在其表面富集,提高了反应物的浓度,从而提高了光催化反应的速率[8-9].近年来,已有一些关于石墨烯基光催化材料研究的文献报道,但有关纳米Sb2S3与石墨烯复合制备成石墨烯/Sb2S3纳米复合材料(RGO/Sb2S3) (RGO表示石墨烯或还原氧化石墨烯)研究的文献报道还很少.由于溶剂热法制备的复合材料具有复合效果好、团聚程度低、结晶度高、尺寸可调等优点,因此,本文以天然鳞片石墨为原料,通过改进的Hummers法[10-11]制备了氧化石墨(GO),然后以硫代乙酰胺(TAA)为还原剂和硫源,1,2-丙二醇为溶剂,采用溶剂热法首次制备了RGO/Sb2S3纳米复合材料,并用XRD、FT-IR、SEM、UV-Vis DRS、PL光谱等手段对该复合材料进行了表征,考察了其可见光光催化活性.
1 实验部分
1.1 仪器和试剂
日本理学D/max-2500/PC型X射线衍射仪(XRD),靶电压40 kV,靶电流250 mA,CuKα辐射,λ=0.154 18 nm,扫描区间5°~70°;日本电子JSM-6610LV型扫描电子显微镜(SEM);美国赛默飞世尔Nicolet-6700型傅里叶红外光谱仪(FTIR);日本岛津UV-2500型紫外-可见分光光度计(UV-Vis);美国安捷伦FTI QM-40型荧光光谱仪(FS);巩义予华KH-50型水热反应釜.
天然石墨粉 (青岛金日来石墨有限公司),硫代乙酰胺(TAA, 天津市光复精细化工研究所),三氯化锑(天津光复精细化工研究所),高锰酸钾(长沙市湘科精细化工厂),五氧化二磷(汕头市西陇化工厂),过硫酸钾 (天津风船化学试剂有限公司),浓硫酸(恒阳市凯信化工试剂有限公司),1,2-丙二醇(汕头市西陇化工股份有限公司),聚乙烯吡咯烷酮(PVP, 天津市大茂试剂厂).试剂均为分析纯.
1.2 材料的制备
1.2.1 氧化石墨(GO)的制备 GO制备采用改进的Hummers氧化方法[12-13],具体过程如下:(1) 预氧化.将2 g天然石墨粉加入3 mL 80 ℃的浓H2SO4、1 g K2S2O8和1 g P2O5的混合物中,然后,将得到的蓝黑色混合物在电热套上80 ℃加热反应6 h,自然冷却到室温,再用适量去离子水小心地将其稀释.此过程放出大量的热.减压过滤,用去离子水洗涤直到滤液呈中性,得预氧化石墨,将其在空气中干燥过夜.(2) 氧化.将得到的预氧化石墨用Hummers法氧化,即将预氧化的石墨加入0 ℃用冰水浴冷却的46 mL浓H2SO4中,在搅拌下慢慢加入6 g KMnO4,此过程温度控制在20 ℃以下.然后,将混合物在35 ℃下搅拌2 h,用90 mL去离子水稀释(用冰水浴控制温度在50 ℃以下),15 min后,加入280 mL去离子水和5 mL 30%的H2O2使反应停止,此时混合物变成亮黄色且伴有大量气泡冒出.将混合物减压过滤,得棕黄色滤饼.将滤饼用500 mL 1∶10的HCl溶液分5次离心洗涤以去掉金属离子,再用去离子水洗涤、离心,直到用BaCl2溶液在洗涤液中检测不出SO42-为止,得到的产品在60 ℃干燥.
1.2.2 RGO/Sb2S3复合材料的制备 取20 mg研细的GO,将其加入40 mL的1,2-丙二醇中,超声分散2 h,得到0.5 mg/mL的GO分散体系.称取0.23 g的三氯化锑加入上述GO分散体系中,稍加热,磁力搅拌使其溶解后,再搅拌 1 h,使Sb3+或SbO+充分吸附在GO片上.然后在上述分散体系中分别加入0.4 g 聚乙烯吡咯烷酮(PVP)、0.225 g硫代乙酰胺(TAA),搅拌均匀,再将混合液转移至50 mL的聚四氟乙烯反应釜中,在恒温干燥箱中100 ℃下反应12 h.反应完成后,自然冷却至室温,离心分离,用去离子水和无水乙醇交替洗涤各3次,得到的产品在50 ℃干燥12 h,得产品,标记为RGO/Sb2S3-0.5.另外,保持其他条件不变,在GO浓度分别为0、0.02、0.1、0.2、2 mg/mL下制得产品,产品分别标记为Sb2S3、RGO/Sb2S3-0.02、RGO/Sb2S3-0.1、RGO/Sb2S3-0.2、RGO/Sb2S3-2;同法制备不加PVP的产品RGO/Sb2S3-0.5.
1.3 光催化性能研究
1.3.1 光催化性能的测试方法 以制得的复合材料RGO/Sb2S3为光催化剂、罗丹明B(RhB)为目标降解物对其可见光光催化性能进行考察.将60 mg催化剂加入盛有100 mL 10 mg/L的罗丹明B溶液中,在黑暗中超声分散10 min,再在暗处磁力搅拌30 min,使罗丹明B在催化剂表面达到吸附平衡,测定其吸光度作为初始吸光度A0.然后以300 W氙灯为光源进行可见光降解实验(氙灯的顶端距反应液面15 cm),同时不断磁力搅拌,每隔1 h取样5 mL,离心分离,除去催化剂粉末后,取上层清液在RhB的最大波长处(554 nm)测定其吸光度Ax,并由此计算出罗丹明B的降解率X=(C0-C)/C0=(A0-Ax)/A0×100%.
1.3.2 光催化剂稳定性测试方法 选取光催化性能最好的样品作光催化剂,将光催化降解罗丹明B(RhB)实验后的溶液离心分离,得到的催化剂粉末先用蒸馏水洗涤3次,再用无水乙醇超声洗涤1次,干燥,在相同实验条件下测定所得到的光催化剂光催化活性的变化.由于催化剂的少量损失,可按比例减少罗丹明B溶液的用量,循环测定几次.
1.3.3 研究光催化过程中产生的羟基自由基(·OH)的实验方法 用无荧光活性的对苯二甲酸(TA)作探针分子,其与光催化过程中产生的羟基自由基(·OH)反应生成具有荧光活性的2-羟基对苯二甲酸(2-HTA)[14],根据2-HTA产生的荧光发射峰的强度可间接证明光催化过程中产生的·OH的多少.具体实验方法为:取8.3 mg TA加入溶有8 mg NaOH的100 mL去离子水中,充分搅拌使TA溶解,再加入20 mg光催化剂,充分搅拌,得混合液.然后,与光催化实验过程一样,将混合液在300 W氙灯照射下,每隔30 min取 5 mL样品,离心分离去掉催化剂粉末后,测试其清液的荧光光谱(激发波长为315 nm).为进一步研究光催化过程中产生的·OH,在光催化反应体系中加入·OH消耗剂维生素C(Vc),其他步骤同光催化性能测试方法.
2 结果与讨论
2.1 样品的SEM分析

2.1.1 GO和RGO的SEM分析 图1为通过改进的Hummers法制备的GO和以硫代乙酰胺为还原剂将GO还原为RGO的SEM图.从图1(a)可以看出,GO呈片状,表面较粗糙,可能是其表面的含氧基团所造成的[15].图1(b)是其还原后生成的RGO的SEM图,由图可以看到经还原后的石墨片层较薄,表面光滑且有明显的褶皱,这是石墨烯特有的褶皱片层结构,且石墨烯为无序堆积.
2.1.2 GO浓度对形貌的影响 图2是不同GO浓度通过溶剂热法在100 ℃下反应12 h所制备的复合材料的SEM图.由图2可以看出,当GO浓度为0 mg/mL时,样品Sb2S3中不仅有粒径为0.2~0.8 μm的微米颗粒,而且还有长2.5~7 μm、直径0.14~1 μm的微米棒;当GO浓度为0.02 mg/mL时,石墨烯片很少,而硫化锑颗粒很多,颗粒粒径在0.15~0.42 μm之间,且颗粒有严重的团聚、结块现象;当GO浓度增加到0.1 mg/mL时,石墨烯片较0.02 mg/mL时增多,Sb2S3颗粒的粒径为0.11~0.89 μm,也有团聚现象,且有一些Sb2S3颗粒不在石墨烯片上,复合效果较差;而当GO浓度为0.5 mg/mL时,有很多粒径为85~100 nm的硫化锑纳米粒子附着在石墨烯片层上,片层很薄,呈透明的薄纱状,在片层与片层之间也附着大量的硫化锑纳米粒子,纳米粒子的分布较均匀,没有团聚,且不在石墨烯片层上的颗粒很少,复合效果好;当GO浓度增加到1 mg/mL和2 mg/mL时,RGO片层增多,附着在RGO片层上的Sb2S3纳米颗粒相对减少,其粒径有所增大.此外,从图2(d)~(f)还可观察到越是平整光滑的区域,附着的硫化锑纳米颗粒越少,因而可推测在褶皱和片层的边沿处残留的含氧官能团比较多,对纳米硫化锑的束缚作用相对较强,而在平整光滑区域的硫化锑颗粒容易滑动,并在边缘和褶皱处发生融合.

2.1.3 PVP对样品形貌的影响 PVP(聚乙烯吡咯烷酮)是一种具有良好水溶性的分散剂,通常可以用来处理石墨烯和纳米粒子以防止它们的堆积和团聚,并控制纳米粒子的生长[16].图3是在120 ℃下反应12 h不加PVP所制备RGO/Sb2S3-0.5的SEM图,图2(d)是相同条件下加入PVP制备的RGO/Sb2S3-0.5的SEM图.将图3与图2(d)对比可知,不加PVP制备的RGO/Sb2S3-0.5石墨烯片层较厚且表面粗糙不平,附着在石墨烯片上的Sb2S3颗粒较少,大部分Sb2S3不在石墨烯片层上,复合效果较差,且硫化锑的粒径(100~230 nm)也比加入PVP制备的样品大,团聚更严重,说明PVP在形成RGO/Sb2S3复合材料中起了非常重要的作用.
2.2 样品的XRD分析
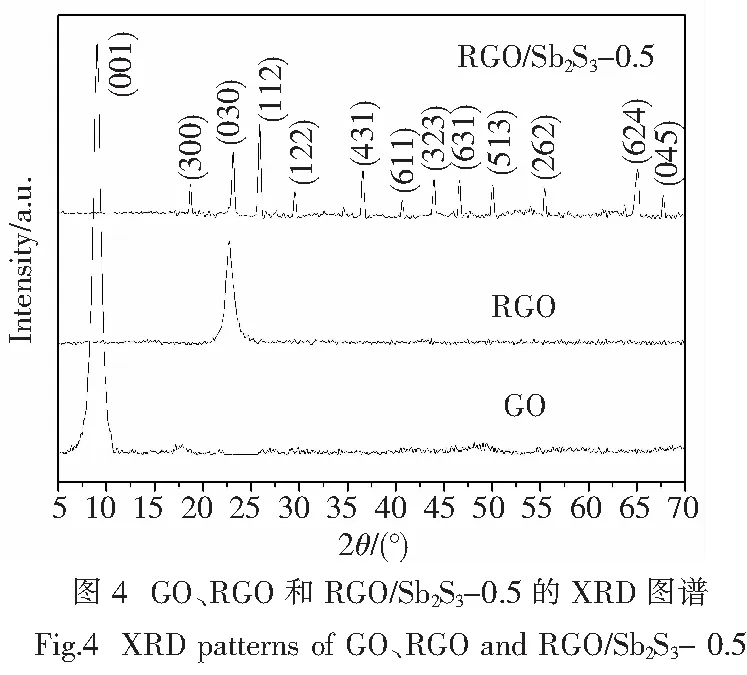
图4是GO、RGO及样品RGO/Sb2S3-0.5的XRD谱图.由标准卡片JCPDS No.75-1621可知天然石墨的最强衍射峰为2θ=26.23°,对应于(002)晶面,其晶面间距d002=0.339 5 nm.从图4可以看出,天然石墨经氧化后生成的GO在(002)处的衍射峰完全消失了,在2θ=9.10°处出现了强度大且尖锐的衍射峰,对应于(001)晶面[12],这表明天然石墨已被氧化成了GO.当GO被硫代乙酰胺还原为RGO后,这个强而尖的衍射峰消失了,而在2θ=22.72°处出现弱而宽的衍射峰,表明GO已被硫代乙酰胺还原了.由布拉格公式2dsinθ=nλ计算可知GO(001)晶面的晶面间距为d001=0.971 7 nm,RGO的晶面间距为d=0.391 4 nm.由此可见,GO的片层间距(0.971 7 nm)比原料石墨的片层间距(0.339 5 nm)大得多.这是因为经氧化后石墨烯片层上生成的大量含氧基团增大了石墨烯的夹层空间,从而使GO的晶面间距变大.从以上的计算还可以看出,RGO的片层间距(0.391 4 nm)比GO (0.971 7 nm)小,但比原料天然石墨的(0.339 5 nm)要大,这说明GO片层间的大多数含氧官能团被还原了,但仍有少量的含氧官能团未被还原,使层间距比原料天然石墨要大.此外,样品RGO/Sb2S3-0.5的XRD谱图与正交晶相Sb2S3的标准谱图(JCPDS No.51-1418)的衍射峰相吻合,衍射峰峰形尖锐,衍射强度较高,说明样品为结晶良好的Sb2S3;但谱图中没有出现GO或RGO的衍射峰,这是因为生成的Sb2S3纳米颗粒插入石墨烯片层之间,使经GO还原生成的RGO片的有序堆砌被破坏.
2.3 样品的FTIR分析
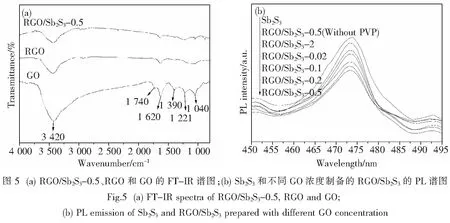
图5(a)是样品RGO/Sb2S3-0.5、RGO和GO的红外光谱图.图中GO在3 420 cm-1处的吸收峰是—OH的伸缩振动峰,且峰较宽而强,1 740 cm-1处是—COOH上CO的伸缩振动峰,1 620 cm-1处是—OH的弯曲振动峰,1 390 cm-1处是C—OH的伸缩振动峰,1 221 cm-1处是Ar—OH上C—O的伸缩振动峰,而1 050 cm-1处是烷氧基C—O的伸缩振动峰.与GO的峰相比,可以看出RGO和RGO/Sb2S3-0.5在1 740、1 221 cm-1处的吸收峰消失,在3 420、1 620、1 390、1 040 cm-1处的吸收峰明显减弱,说明GO表面和边缘的含氧官能团—COOH、—OH和—O—被硫代乙酰胺部分或全部还原了[11,13,17].
2.4 样品的PL分析
光致发光(PL)光谱是一种检测半导体固相材料光学性质的方法,PL发射光谱是由自由载流子的再复合而产生的,它揭示了电荷载流子的分离效果,即PL信号越强,电子-空穴对再复合越严重[18].图5(b)是在激发波长为370 nm的条件下测得的不同GO浓度制备的RGO/Sb2S3的PL光谱.从图中可以看出,除不加PVP制备的RGO/Sb2S3-0.5和RGO/Sb2S3-2样品外,随GO浓度的增加,PL发射峰逐渐降低,说明随着GO浓度的增加,Sb2S3与RGO复合效果越来越好,更有利于光生电子在石墨烯片层结构中的迁移,从而有效阻止了光生电子-空穴对的复合,其中样品RGO/Sb2S3-0.5的发射峰最低,光生载流子的分离效果最好.而不加PVP制备的RGO/Sb2S3-0.5和RGO/Sb2S3-2的PL发射峰较强、光生载流子分离效果较差,可能是其RGO与Sb2S3的复合效果较差造成的.
2.5 样品的UV-Vis DRS分析
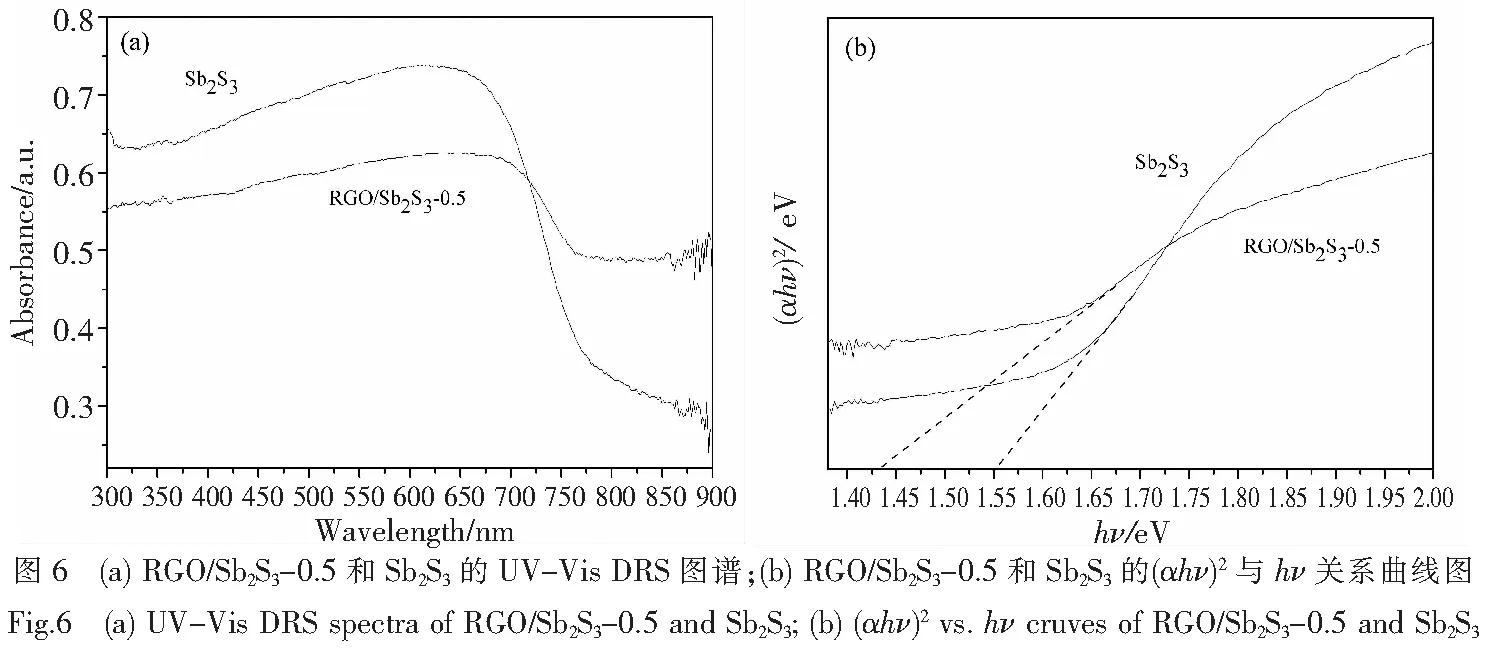
紫外-可见漫反射光谱(UV-Vis DRS)是研究固体半导体材料的重要表征手段,通过UV-Vis DRS可以了解半导体材料的光吸收特性和能带间隙的大小.图6(a)是复合材料RGO/Sb2S3-0.5和Sb2S3的紫外-可见漫反射光谱.从图6(a)可以看出,Sb2S3在400~700 nm处有较宽的强吸收峰,而RGO/Sb2S3-0.5在400~750 nm处也有较宽的强吸收峰,虽由于石墨烯的遮挡,RGO/Sb2S3-0.5对可见光的吸收能力稍有减弱,但其吸收边向长波方向移动,更有利于其对可见光的吸收.据文献报道[19],对于Sb2S3等直接带隙半导体材料,在吸收边附近其光吸收系数α与入射光光子能量hν之间存在如下关系:αhν=(hν-Eg)1/ 2(式 中α为光吸收系数,hν为入射光光子能量,Eg为带隙宽度),因此,在吸收边附近(αhν)2与hν呈线性关系.对所制备样品的紫外-可见漫反射光谱进行处理,作出 (αhν)2与 hν的关系曲线,将曲线的线性部分外推至与横坐标相交,交点的值即为能带间隙值Eg[图6(b)].从图6(b)可知,Sb2S3的能带间隙Eg约为1.55 eV,而与石墨烯复合得到的RGO/Sb2S3-0.5的能带间隙Eg约为1.43 eV,由此可见,其能带间隙变小,吸收峰进一步红移,其对可见光有更好的响应.原因有待进一步研究.
2.6 复合材料的光催化性能
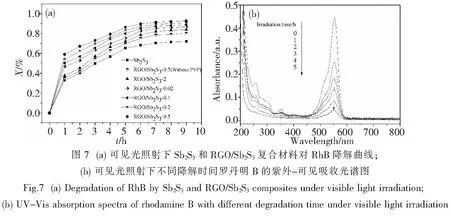

2.6.1 不同GO浓度样品的光催化活性 以制得的复合材料RGO/Sb2S3和Sb2S3为光催化剂,RhB为目标降解物对其可见光光催化性能进行考察.图7(a)为可见光照射下,Sb2S3和不同GO浓度制备的复合材料RGO/Sb2S3光催化降解RhB的效果图.从图7(a)可以看出,当GO的浓度从0.02、0.1、0.2 mg/mL增加到0.5 mg/mL时,样品的降解率逐渐增大,其中以RGO/Sb2S3-0.5的光催化活性最高,经9 h的降解,RhB的降解率达93%,是Sb2S3的约1.3倍.这是因为随着GO浓度的增加,将有更多的硫化锑附着在石墨烯片层上,石墨烯与硫化锑复合得越好[图2(b)~(d)],相互之间接触越充分,使激发产生的光生电子能更好地从Sb2S3转移到石墨烯片层结构中,从而降低了光生电子与空穴的复合概率.从PL谱[图5(b)]也可以看出,依上述次序样品的PL谱发射峰依次降低,光生电子-空穴对更容易分离,量子效率越来越高,因此RhB的光催化降解率也依次提高.但当GO的浓度增加到2 mg/mL时,所制样品的降解率比0.5 mg/mL时的明显降低,这是因为随着氧化石墨烯用量的增加,Sb2S3的量相对减少,不但复合效果变差,而且其对可见光的吸收能力也会相应减弱,从而导致其光催化活性的降低.另外,Sb2S3明显比石墨烯复合的光催化剂RGO/Sb2S3的光催化活性低,经9 h的降解,RhB的降解率仅为72%,说明石墨烯的复合大大提高了其光催化活性.从图7(a)还可以看出,加入PVP制备的RGO/Sb2S3-0.5对RhB的降解率明显高于不加PVP制备的RGO/Sb2S3-0.5,这是由于PVP的加入使得Sb2S3与石墨烯复合得更好,Sb2S3粒径更小[图2(d)与图3],从而使其光催化活性更高.图7(b)是用RGO/Sb2S3-0.5作光催化剂,光催化降解RhB溶液不同时间后其紫外-可见吸收光谱的变化曲线.由图可知,随着光照时间的延长,在554 nm左右的特征吸收峰及其他吸收峰逐渐降低,说明RhB被降解了,且随着光照时间的延长,RhB在554 nm左右的特征吸收峰发生蓝移.据文献报道,这是因为罗丹明B在光催化降解过程中,发生了脱乙基反应[20].
2.6.2 复合材料的光催化稳定性 为考察复合光催化剂RGO/Sb2S3在光催化降解罗丹明B过程中的稳定性,以RGO/Sb2S3-0.5为光催化剂进行了5次循环光催化降解罗丹明B的实验,结果如图8所示.从图8可以看出,RGO/Sb2S3-0.5经5次循环光催化降解实验后,其光催化活性只稍有下降,说明催化剂具有较高的光催化稳定性.
2.6.3 降解过程中产生的羟基自由基(·OH)的分析 在光催化过程中加入对苯二甲酸(TA)作探针分子,以315 nm为激发波长对光照后产生的2-HTA溶液做荧光光谱(FS谱),反应生成的2-HTA在425 nm出现强的发射峰,根据发射峰的强度可检测光催化产生·OH的多少.图9(a)是以RGO/Sb2S3-0.5为光催化剂在不同光照时间下TA溶液的FS谱图.从图9(a)可以看出,随着光照时间的延长,荧光发射强度越来越大,说明催化剂在可见光照射下随光照时间的延长产生的·OH越来越多.为进一步证明光催化降解是因为产生了·OH,在光催化过程中加入·OH消耗剂Vc,结果如图9(b)所示.由图9(b)可见,在加入0.2 g Vc消耗掉部分·OH后,光催化效率降低了10%以上,因此,RhB的降解是由于光催化过程中产生的·OH的作用[17].

3 结 论
首先,通过改进的Hummers法制备了氧化石墨(GO),然后以SbCl3、硫代乙酰胺和GO为原料,1,2-丙二醇为溶剂,用溶剂热法制备了RGO/Sb2S3复合材料.考察了GO浓度、PVP对复合材料中Sb2S3的形貌及复合效果的影响.用XRD、FT-IR、SEM、UV-Vis DRS、PL谱等手段对RGO/Sb2S3的物相、官能团、形貌和光学性能等进行了表征,并以罗丹明 B 为目标降解物,对复合材料的可见光光催化性能进行了考察.结果表明,生成的Sb2S3属正交晶系,Sb2S3与RGO/Sb2S3-0.5对可见光均有较强吸收,加入的PVP和GO浓度对材料的复合效果有较大的影响.当GO浓度为0.5 mg/mL时,材料的复合效果最好,有很多粒径为85~100 nm的硫化锑纳米颗粒附着在石墨烯片层上,其在PL谱中的发射峰最低,光生电子-空穴对的分离效果最好,光催化效率最高(9 h后RhB的降解率达93%),比相同条件下制备的Sb2S3对RhB的降解率(73%)提高了近20%.在光催化过程中,以TA为荧光探针对产生的·OH进行了探究,并且通过加入Vc进一步证明了在光催化过程中·OH起了非常重要的作用.复合材料在光催化过程中具有较高的稳定性.
[1] IM S H, LIM C S, CHANG J A, et al. Toward interaction of sensitizer and functional moieties in hole-transporting materials for efficient semiconductor-sensitized solar cells[J]. Nano Lett, 2011, 11(11): 4789-4793.
[2] LI K Q, HUANG F Q, LIN X P. Pristine narrow-bandgap Sb2S3as a high-efficiency visible-light responsive photocatalyst[J]. Scripta Mater, 2008, 58(10): 834-837.
[3] LIU G, SUN C, YAN X, et al. Iodine doped anatase TiO2photocatalyst with ultra-long visible light response: correlation between geometric/electronic structures and mechanisms[J]. J Mater Chem, 2009, 19(18): 2822-2829.
[4] SHUAI X, SHEN W. A facile chemical conversion synthesis of Sb2S3nanotubes and the visible light-driven photocatalytic activities[J]. Nano Res Lett, 2012, 7(1): 1-8.
[5] LI N, LIU G, ZHEN C, et al. Battery performance and photocatalytic activity of mesoporous anatase TiO2nanospheres/graphene composites by template-free self-assembly[J]. Adv Funct Mater, 2011, 21(9): 1717-1722.
[6] WU U J, BAI S, SHEN X, et al. Preparation and characterization of graphene/CdS nanocomposites[J]. Appl Surf Sci, 2010, 257(3): 747-751.
[7] LI K, XIONG J, CHEN T, et al. Preparation of graphene/TiO2composites by nonionic surfactant strategy and their simulated sunlight and visible light photocatalytic activity towards representative aqueous POPs degradation[J]. J Hazard Mater, 2013, 250: 19-28.
[8] ZHANG X, SUN Y, CUI X, et al. A green and facile synthesis of TiO2/graphene nanocomposites and their photocatalytic activity for hydrogen evolution[J]. Int J Hydrogen Energy, 2012, 37(1): 811-815.
[9] HUMMERS W, OFFEMAN R. Preparation of graphitic oxide[J]. J Am Chem Soc, 1958, 80(6):1339.
[10] KOVTYUKHOVA N I, OLLIVIER P J, MARTIN B R, et al. Layer-by-layer assembly of ultrathin composite films from micron-sized graphite oxide sheets and polycations[J]. Chem Mater, 1999, 11(3): 771-778.
[11] TAO W, CHANG J, WU D, et al. Solvothermal synthesis of graphene-Sb2S3composite and the degradation activity under visible light[J]. Mater Res Bull, 2013, 48(2): 538-543.
[12] CHENG B, SAMULSKI E T. One-step, ambient-temperature synthesis of antimony sulfide (Sb2S3) micron-size polycrystals with a spherical morphology[J]. Mater Res Bull, 2003, 38(2): 297-301.
[13] 于美, 刘鹏瑞, 孙玉静, 等. 石墨烯-银纳米粒子复合材料的制备及表征[J]. 无机材料学报,2012,27(1): 89-94.
[14] SHEN J F, LI T, LONG Y, et al. One-step solid state preparation of reduced graphene oxide[J]. Carbon, 2012, 50(6): 2134-2140.
[15] RONG X S, QIU F X, ZHANG C, et al. Preparation, characterization and photocatalytic application of TiO2-graphene photocatalyst undervisible light irradiation[J]. Ceram Int, 2015, 41(2): 2502-2511.
[16] 王志栋, 徐自力, 杨英歌, 等. 利用水溶性聚合物 PVP 作稳定剂合成 CdS, CdSe 半导体纳米晶体[J]. 材料导报, 2006, 20(F11): 53-57.
[17] SOOKHAKIAN M, AMIN Y M, BASIRUN W J, et al. Hierarchically ordered macro-mesoporous ZnS microsphere with reduced graphene oxide supporter for a highly efficient photodegradation of methylene blue[J]. Appl Surf Sci, 2013, 283(20): 668-677.
[18] 刘保顺, 何鑫, 赵修建, 等. 纳米TiO2的表面能态及光生电子-空穴对复合过程的研究[J]. 光谱学与光谱分析, 2006, 26(2): 208-212.
[19] HAN Q F, CHEN J. YANG X J, et al. Preparation of uniform Bi2S3nanorods using xanthate complexes of bismuth(Ⅲ)[J]. J Phys Chem C, 2007, 111(38):14072-14077.
[20] FU H, ZHANG S, XU T, et al. Photocatalytic degradation of RhB by fluorinated Bi2WO6and distributions of the intermediate products[J]. Environ Science Technol, 2008, 42(6):2085-2091.
责任编辑:罗 联
Solvothermal Synthesis and Photocatalytic Performance of Graphene/Sb2S3Nanocomposites
ZHUQi-an1*,WANGJian-xia1,HUNai-geng2,WEIMin-yang1,DUHan-yu1,JIANGShu-li1
(1.KeyLaboratoryofEnvironmentallyFriendlyChemistryandApplicationsofMinistryofEducation,CollegeofChemistry,XiangtanUniversity,Xiangtan411105; 2.CollegeofNewEnergyScienceandEngineering,XinyuUniversity,Xinyu338004China)
Graphite oxide (GO) was prepared with natural flake graphite powder as raw material by a modified Hummers method, and then graphene/Sb2S3(RGO/Sb2S3) nanocomposites were successfully synthesized via solvothermal method, using GO, antimony sulfide (SbCl3) and thioacetamide (CH3CSNH2, TAA)as the reactants, 1,2-propanediol as solvent. The crystal phase, functional groups, morphologies, and optical performance of the composites were characterized by XRD, FT-IR, SEM, UV-Vis DRS and PL spectra. The photocatalytic activity was investigated through the degradation of rhodamine B (RhB). The results show that, the Sb2S3of the as-prepared composites are of orthorhombic-phase. Both Sb2S3and composites have strong absorption to visible light, and the band gap of them is 1.55 eV and 1.43 eV, respectively. PVP and the concentration of GO have great influence on the morphologies, composite effects and photocatalytic performance of the materials. When the concentration of GO is 0.5 mg/mL, the as-prepared composite (RGO/Sb2S3-0.5), on the surface and between the graphene flake layers of which many antimony sulfide nanoparticles with the particle diameter of 85~100 nm are loaded, has the best composite effect, the lowest emission peak in the PL spectra, best separation effect of photo-generated electron-hole pairs and the highest photocatalytic efficiency. The degradation rate reaches more than 90% after 9 h under 300 W xenon-lamp irradiation, which is 1.3 times higher than Sb2S3. In addition, the existence of hydroxyl radicals (·OH) in the process of photocatalysis is proved using terephthalic acid (TA) as fluorescent probe.It is proved that ·OH plays a very important role in the photocatalytic degradation process by adding ·OH scavenger vitamin C(Vc).
antimony sulfide; graphene; composite; photocatalysis
2016-04-08
国家自然科学基金项目(21276215)
朱启安(1963—), 男,湖南 湘潭人,教授.E-mail:zqa7887551@163.com
O627.8; O613.62
A
1000-5900(2016)04-0034-09
