布氏菌病活疫苗活菌计数项目能力验证结果分析
2016-02-07王楠李旭妮于晓辉徐磊张媛刘博李建毛开荣蒋玉文
王楠,李旭妮,于晓辉,徐磊,张媛,刘博,李建,毛开荣,蒋玉文
(中国兽医药品监察所,北京 100081)
布氏菌病活疫苗活菌计数项目能力验证结果分析
王楠,李旭妮,于晓辉,徐磊,张媛,刘博,李建,毛开荣,蒋玉文*
(中国兽医药品监察所,北京 100081)
为了解全国布氏菌病活疫苗生产企业活菌计数能力,2015年对该项目进行了能力验证分析,每名参比企业发放布氏菌活疫苗(S2株)样品3份,要求在规定时间内对其进行活菌计数并提交结果报告。结果显示,参比的17家企业中,15家结果“满意”,2家企业结果“不满意”,表明全国大部分布氏菌病活疫苗生产企业具备可信任的布氏菌病活疫苗活菌计数检测能力。
布氏菌病活疫苗;活菌计数;能力验证;结果分析
布氏菌病是一种严重威胁人类健康的动物源性人畜共患病,进入21世纪以来,布病疫情在我国快速反弹,防控形势十分严峻。动物布氏菌病防治以预防为主,因此布氏菌病疫苗质量的优劣直接影响布氏菌病的防控效果。截至2012年,我国具有布氏菌病活疫苗生产文号的企业有14家,年产量超过2.5亿头份[1]。为了解全国布氏菌病活疫苗生产企业活菌计数能力,中国兽医药品监察所组织实施了布氏菌病疫苗生产企业活菌计数项目能力验证。
1 材料与方法
1.1 测试样品
1.1.1 样品制备 委托生产企业制备布氏菌病活疫苗(S2株)240瓶,制备方法同《中华人民共和国兽用生物制品规程》[2]。样品密封、粘贴标签,于-18 ℃以下保存。
1.1.2 样品均匀性检验 按照CNAS-GL03:2006《能力验证样品均匀性和稳定性评价指南》[3]要求进行。样品均匀性检验按5%比例从样品中随机抽取12瓶,每个样品分别在同一试验条件下进行检验,重复两次。
1.1.3 样品稳定性检验 考虑到本测试样品可能受温度影响较大,所以,稳定性检验包括静置状态和邮寄状态。
1.1.3.1 静置状态检验 样品在-18 ℃以下保存的稳定性检测:检测周期为21 d,每隔7 d检测一次,连续检测3次,每次随机检测3瓶样品。
1.1.3.2 邮寄状态检验 选择距离最远的3个实验室分别邮寄1份样品,3瓶/份,实验室收到样品后反馈样品状态并原样寄回,收到返回的邮寄样品后立即开封检测。
1.1.4 样品发放 按照随机抽取样品的原则,采用隔热泡沫塑料盒内置样品3瓶和2个生物冰袋,最外层包装为纸箱,由EMS快递至各实验室,同时将样品状态确认表、作业指导书和结果报告等文件随样品同时邮寄。
1.2 参加单位 报名参加单位包括具有布氏菌病活疫苗生产文号的兽用生物制品生产企业共计17家,各参加实验室拥有唯一性代码,结果统计中用唯一性代码代替实验室名称,结果评价结束后发放能力验证合格实验室证书。
1.3 试验方法 本次实验室间比对采用《中国兽药典》活菌计数的方法[4]。

Z比分值计算公式:Z=(X-XM)/NormIQR,式中:Z为稳健比分值;X为检验数据;XM为中位值;NormIQR为标准化四分位距,NormIQR =0.7413×四分位间距(IQR)。
1.5 结果评价依据 本次能力验证采用综合评价方式,既重结果,也重过程。统计结果仅作为评价依据之一,评判依据还包括检测思路是否清晰、报告填写是否规范、原始记录是否符合要求、检测结果是否准确等。
2 结果与分析
2.1 样品的均匀性检验 采用单因子方差分析法进行样品均匀性检验,结果表明:计算得到F值=0.75,该值小于临界值F0.05(11,12)=2.72,表明在0.05的显著性水平下,该样品是均匀的。
2.2 样品的稳定性检验 采用t检验法统计分析样品稳定性检验。静置状态检验结果表明:计算得到的t值=1.22,该值小于临界值t0.05(5)=2.57,表明在0.05的显著性水平下,该样品在静置状态下,21 d内是稳定的。邮寄状态检验结果表明:计算得到的t值=0.48,该值小于临界值t0.05(5)=2.57,表明在0.05的显著性水平下,该样品在邮寄状态下是稳定的。
2.3 检验结果及统计分析
2.3.1 检验结果 各参比企业均能在规定的时间内按照《作业指导书》的检验要求,将能力验证结果报告和原始检验记录及时反馈,汇总17家参比企业的检验结果见表1。
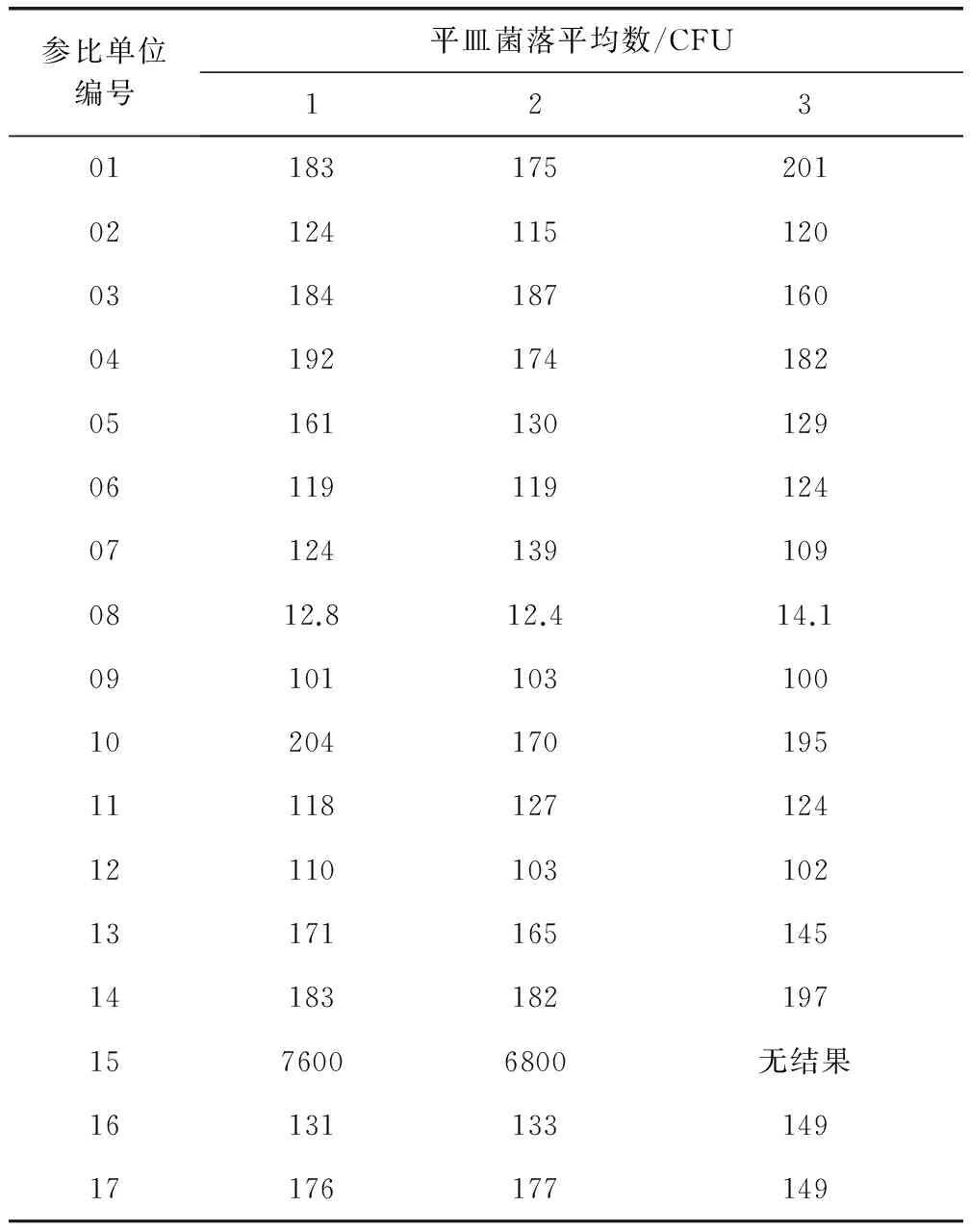
表1 参比单位检验结果汇总表
2.3.2 检验结果的参数及统计结果 结果统计处理参照CNAS-GL02:2014《能力验证结果的统计处理和能力评价指南》[6],检测结果中编号为08和15的参比单位平皿菌落平均数出现极端值(平皿菌落平均数大于200CFU或小于40 CFU),为了避免极端值对其他检验结果的统计分析产生影响,实际统计中将其剔除,其余15家参比单位给予的3瓶样品的检测结果均参与统计分析。根据Z比分数计算公式,统计参数值结果见表2,Z比分数统计结果见表3,各参比单位的Z比分数序列图见图1。结果表明,15家企业的ΙZΙ值均≤2,统计结果为“满意”。
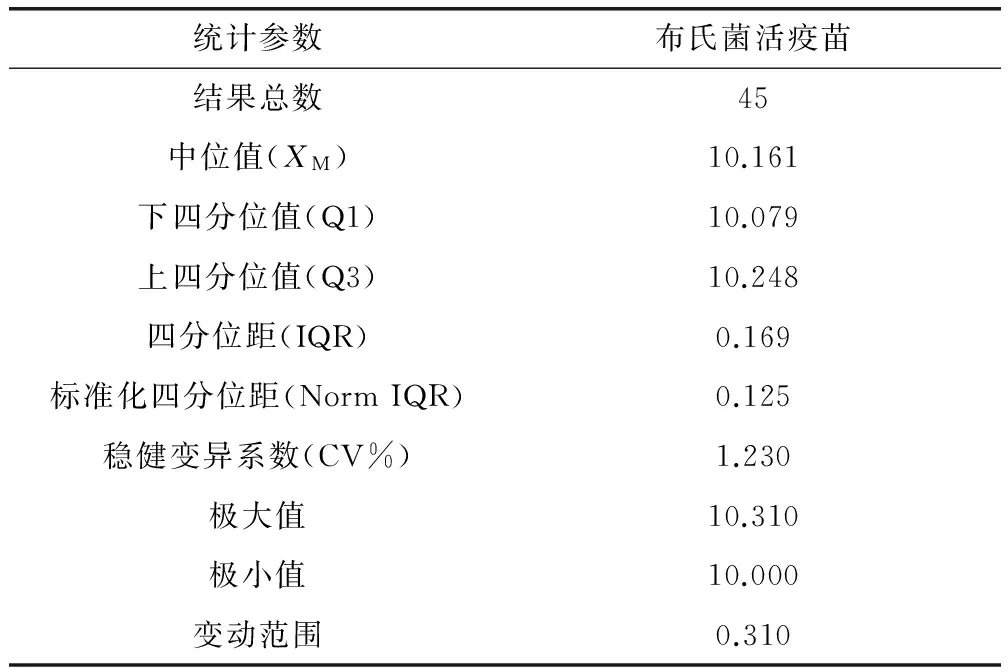
表2 参比单位检验结果稳健统计参数
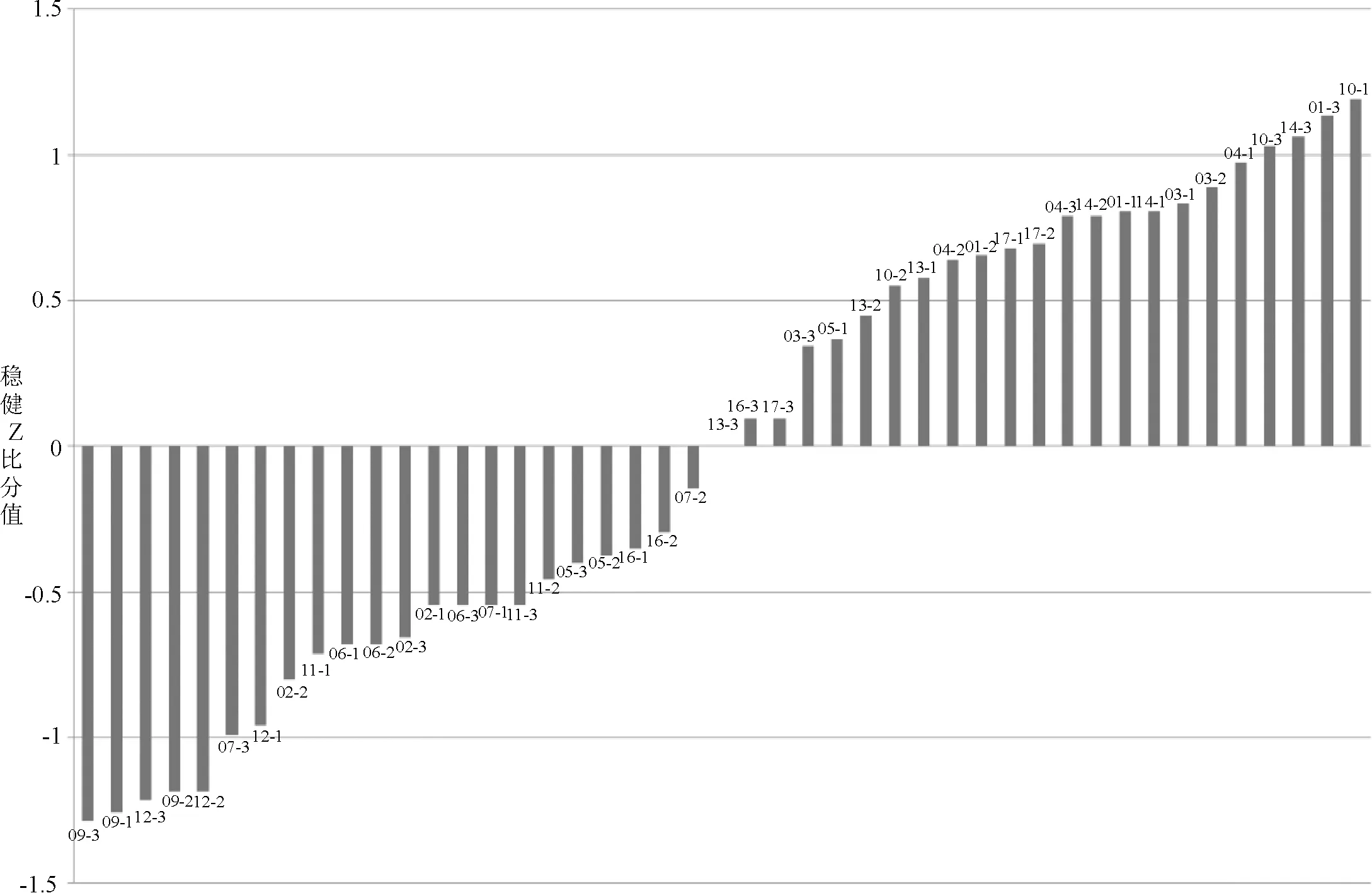
图1 活菌计数结果Z比分数序列图
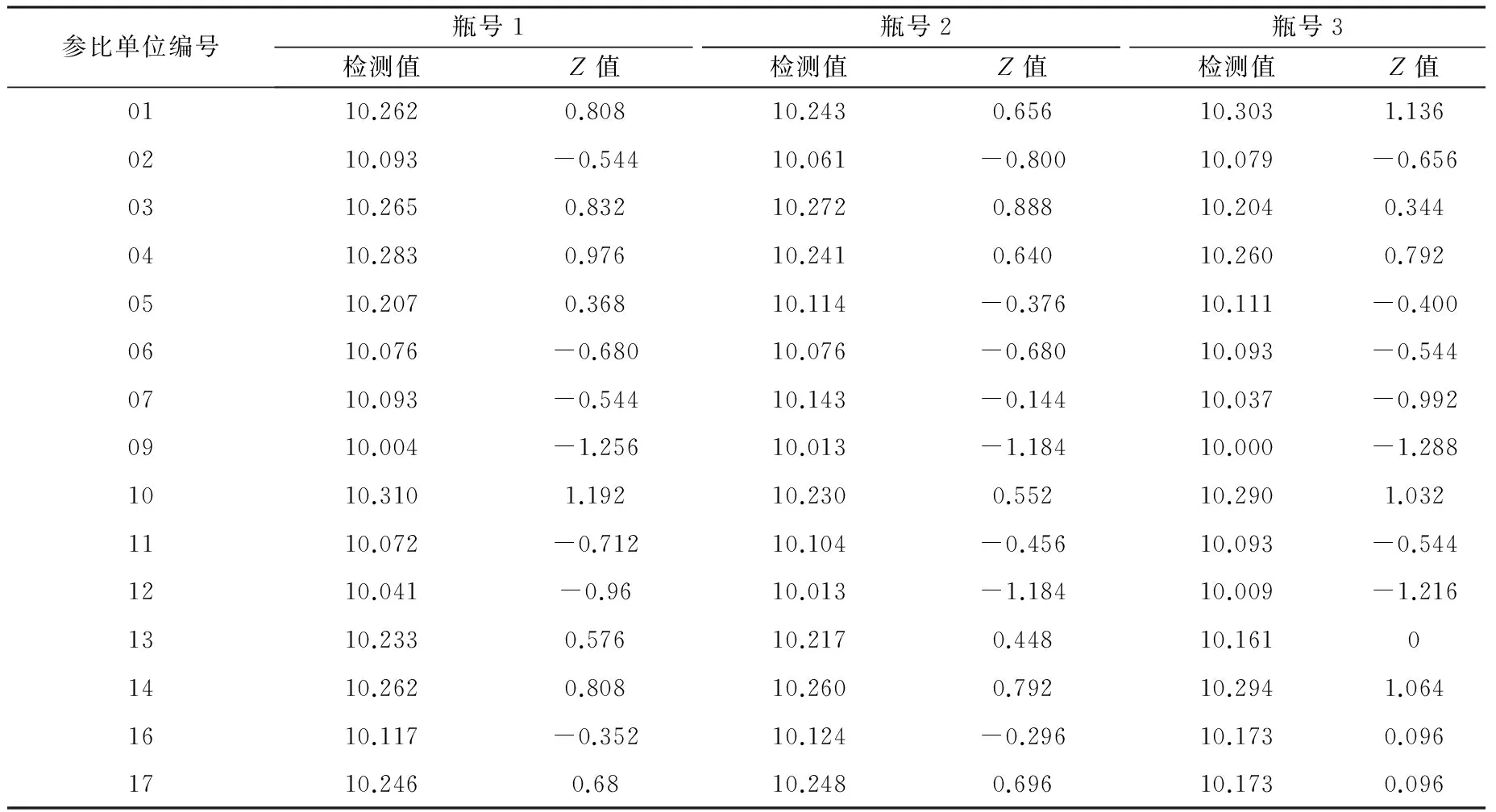
参比单位编号瓶号1瓶号2瓶号3检测值Z值检测值Z值检测值Z值0110.2620.80810.2430.65610.3031.1360210.093-0.54410.061-0.80010.079-0.6560310.2650.83210.2720.88810.2040.3440410.2830.97610.2410.64010.2600.7920510.2070.36810.114-0.37610.111-0.4000610.076-0.68010.076-0.68010.093-0.5440710.093-0.54410.143-0.14410.037-0.9920910.004-1.25610.013-1.18410.000-1.2881010.3101.19210.2300.55210.2901.0321110.072-0.71210.104-0.45610.093-0.5441210.041-0.9610.013-1.18410.009-1.2161310.2330.57610.2170.44810.16101410.2620.80810.2600.79210.2941.0641610.117-0.35210.124-0.29610.1730.0961710.2460.6810.2480.69610.1730.096
表中的“检测值”为检验结果对数值
2.3.2 综合评价结果 对原始检验记录,检验报告和统计结果的进行综合分析后认为:15/17家参比企业能够按照《中国兽药典》和《作业指导书》的规定完成检验,结果满意。但是,仍发现存在的一些问题(表4),经过综合评价后,15家企业在本次能力验证中获“满意”结果,2家企业获“不满意”结果。
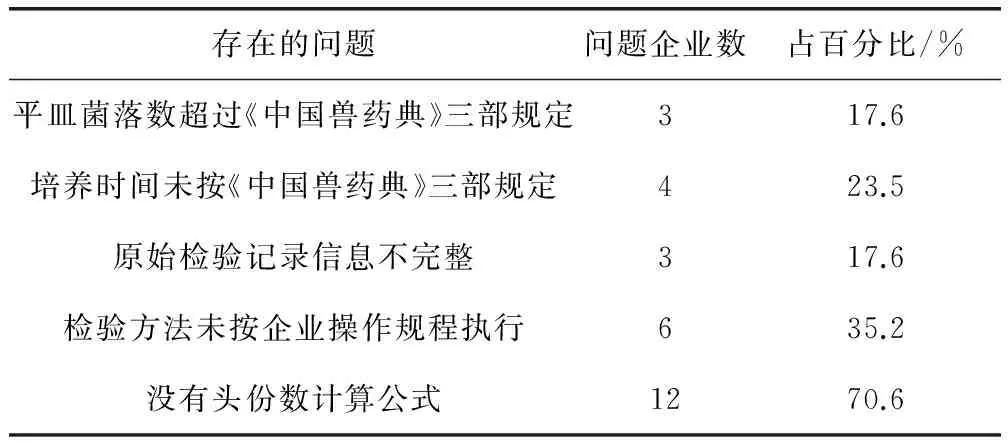
表4 综合评价存在的问题汇总表
3 讨论
本次能力验证的样品为活微生物,考虑到其特殊性质,样品稳定性检验中增加邮寄状态的稳定性检验。样品邮寄正值夏季气温较高,三个地点的邮寄天数为3~5 d,邮寄过程中样品的活菌数虽有一定下降,但是经过统计学分析,不同邮寄地点和邮寄天数的样品检测结果差异并不显著,说明采用隔热泡沫塑料盒内置样品和生物冰袋,外层包装为纸箱,由EMS快递至各实验室的方法可行。
本次能力验证的结果评价采用综合评价的方式,目的是在对结果数据进行科学统计分析的基础上,全面考察企业布氏菌病活疫苗活菌计数项目的检测能力。通过综合评价的方式,我们发现布病活疫苗在活菌计数的质量控制过程中存在一些问题,例如①不能有效控制菌落计数的稀释度。3/17(17.6%)家企业存在布病活疫苗活菌计数的平皿菌落数超过《中国兽药典》规定(>200 CFU/个)导致单个平皿菌落数过多,无法计数。②未严格执行企业内部操作规程中规定的培养时间进行检验。由于布氏菌菌落特性是生长缓慢,培养时间应至少72 h以上否则无法用肉眼清晰辨认菌落,4/17(23.5%)家企业培养时间仅为48 h左右。③相关检验记录不完整,检验信息无法溯源。如原始检验记录中缺失培养基种类,名称和批次、稀释液种类和批次、稀释过程等相关信息。又如,检验中发现6/17(35.2%)家企业检验报告中试验步骤十分简单,反映出检验人员在检验过程中未按照企业操作规程执行,或是企业制定操作规程不够详细。④原始检验报告中没有明确注释头份数的计算过程和公式,头份数的计算结果对于指导临床用药至关重要,如果头份数计算偏大,疫苗无法达到免疫效果;反之,头份数计算偏小,疫苗安全性存在隐患。本次能力验证中发现,12/17(70.6%)家企业未能在原始检验报告中清晰注释头份数的计算过程和公式,如果头份数结果错误,将无法确定是否由计算过程导致。由于不同企业和不同批次的半成品加入稀释液的数量不同和稀释的方法也不同,应将各种变量(平板菌落数的平均数、溶解液量、稀释倍数和平皿滴加菌液量)代入头份数计算公式,从而得出的布病活疫苗头份数更为科学准确。由此可见,仅仅将活菌计数统计结果作为细菌活疫苗活菌计数能力验证的评价依据尚不够全面,需采用综合评价的方式,客观、具体的反映出企业检验能力和质量控制中存在的问题。如何制定更科学、合理的综合评价方式,是我们今后组织能力验证活动中需要进一步思考的问题。
[1] 王楠,程君生,丁家波,等.布氏菌病活疫苗的生产现状与质量分析[J].中国兽药杂志,2013,47(4): 49-50.
[2] 农业部兽用生物制品规程委员会.中华人民共和国兽用生物制品规程[M].化学工业出版社,2000: 157-158.
[3] 中国合格评定国家认可委员会.CNAS—GL03:2006能力验证样品均匀性和稳定性评价指南[S]. 2006.
[4] 中国兽药典委员会.中华人民共和国兽药典[M].中国农业出版社,2010:附录19-20.[5] 张媛,张磊,李建,等.稳健统计方法及t检验法在活菌技术能力比对中的应用[J]. 中国兽药杂志,2013,47(4): 19-20.
[6] 中国合格评定国家认可委员会.CNAS GL 02:2006能力验证结果的统计处理和能力评价指南[S]. 2006.
(编辑:李文平)
Analysis of the Proficiency Testing of Live Bacteria Counting of Brucellosis Vaccine
WANG Nan, LI Xu-ni, YU Xiao-hui, XU Lei, ZHANG Yuan, LIU Bo,LI Jian, MAO Kai-rong, JIANG Yu-wen*
(ChinaInstituteofVeterinaryDrugControl,Beijing100081,China)
In order to ensure the product quality of brucellosis vaccine, proficiency testing of brucellosis vaccine live bacteria counting has been organized by China Institution of Veterinary Drug Control,further investigate and compare the companies' testing capabilities. The samples of brucellosis vaccine have been sent to the companies, and then they should submit the test result paper within the given time. 17 national veterinary biologics companies have participated in the proficiency testing. Results of 15 companies were determined as satisfactory while results of the other 2 companies were determined as unsatisfactory after comprehensive evaluation. In conclusion, the result shows that most national manufacturers own trusted brucellosis vaccine testing capabilities.
brucellosis vaccine; live bacteria counting; proficiency test; result analysis
北京市科技新星计划(Z141107001814013)
王楠,副研究员,从事人畜共患类兽用生物制品检验和研究工作。
蒋玉文。E-mail:jiangyuwen@ivdc.org.cn
2016-01-14
A
1002-1280 (2016) 05-0015-04
S855.12
