模拟训练(十)
2016-01-05王程杰
王程杰
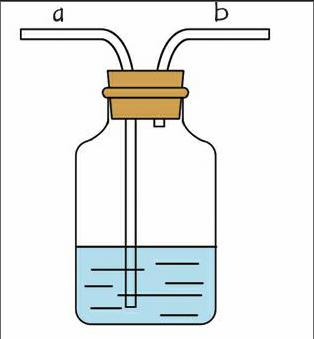

1. 医院给病人输氧气时要用到类似下图所示的装置。关于该装置,下列说法中错误的是( )。
A. 图中b导管是连接氧气钢瓶的导气管
B. 图中b导管是连接病人吸氧气的塑料管
C. 该装置主要用来观测是否有氧气输出及其输出的速度
D. 该装置可用来洗去有害的CO气体
2. 下列叙述中正确的是( )。
A. 霉变大米必须清洗后方可食用
B. 糖、脂肪、蛋白质都是由碳、氢、氧三种元素组成的
C. 奶类中含有钙元素,蔬菜中不含钙元素
D. 人体缺少碘元素会引起甲状腺肿大
3. 甲、乙两同学想了解碳酸钾溶液的酸碱性,他们做了以下研究。
【设计与实验】用pH试纸来检测碳酸钾溶液的酸碱性
(1)根据两位同学的实验可得出碳酸钾溶液酸碱性的结论:______________。
(2)根据两位同学的实验操作,你认为____同学操作不规范,为什么?
(3)如果实验室没有pH试纸和酸碱指示剂,又要一次测定碳酸钾溶液的酸碱性,那么可选用_______试液来进行实验。
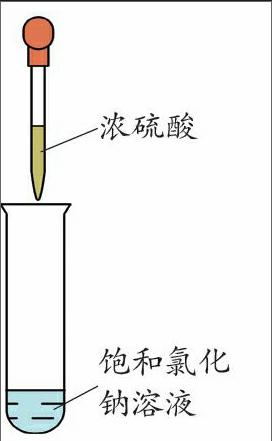
4. 如右上图所示,向盛有1.5mL饱和氯化钠溶液(温度为10℃)的试管中用滴管逐滴加约10滴浓硫酸(约0.5mL),边滴加边振荡,待冷却到10℃时,试管内有不少晶体析出。产生的晶体是什么呢?甲同学答:浓硫酸具有吸水性,小试管内本是饱和氯化钠溶液,吸去部分水后就析出了NaCl晶体。但乙同学答:0.5mL浓硫酸滴入1.5mL氯化钠溶液中后,也就变成了稀硫酸,哪里还谈得上吸水性呢?10℃时,NaCl溶解度为35.8g/100g,而Na2SO4溶解度仅为9g/100g,所以试管内析出的是硫酸钠晶体。老师又补充说:水中如果析出硫酸钠晶体,该晶体的化学式是Na2SO4·10H2O。还已知,10℃时饱和氯化钠溶液的密度是1.33g/mL,98%浓硫酸密度是1.84g/mL。请根据上述信息回答:
(1)上述实验中析出的晶体是什么?说出理由。
(2)请设计简单的鉴别方法来证明(1)中的观点(设计实验方法,写出操作步骤)。
(适合初中学生)
5. 家具店里有些华丽的家具常标有“聚酯家具”字样,以下说法中正确的是( )。
A. 用聚酯塑料和木屑经混合、热压制成的板材做出的家具叫聚酯家具
B. 采用聚酯漆在家具木材表面涂上漆膜后的家具叫聚酯家具
C. 用聚酯塑料板材制成的家具叫聚酯家具
D. 聚酯家具保光保色性能好,表面硬度高,耐热耐酸碱,绝缘性高
6. 在373K时,把0.05mol N2O4气体通入一注射器内,体积达到500mL,立即出现棕色。反应进行到2s时,NO2的浓度为0.02mol/L。在60s时,体系已达平衡,此时注射器内压强为开始时的1.6倍。下列说法中正确的是( )。
A. 前2s,以N2O4的浓度变化表示的平均反应速度为0.01mol/L·s
B. 在2s时体系内的压强为开始时的1.1倍
C. 在平衡时体系内含0.025mol N2O4
D. 平衡时,如果压缩注射器体积,则可提高N2O4的转化率
7. 生产硫磺的方法之一是对硫铁矿加强热使其分解,分解生成的硫蒸气进入一特定容器冷凝而成为固态硫磺。请回答:
(1)硫铁矿加强热时的反应方程式为________,反应需在_____条件下进行,原因是_____________。
(2)厂家为防止SO2污染环境,把厂里烟囱拔高,但生产厂家附近的树木仍屡屡死亡,其原因是_______________。
8. 农业上有种杀菌剂叫“石硫合剂”,石硫合剂是由生石灰、硫磺加水再经加热熬制而成的。石硫合剂含多硫化钙(CaSn)。多硫化钙在空气中与二氧化碳等酸性物质接触易析出多硫化氢(H2Sn),该过程的化学反应方程式是___________;多硫化氢是一种极不稳定的黄色液体。
试用化学方程式和简要文字来说明多硫化钙具有杀菌作用的原因:___________。熬制石硫合剂时,必须用陶罐、瓷锅,不能使用铜锅或铝锅,这是因为___________。
9. 工业上常用漂白粉跟酸反应放出的氯气质量对漂白粉质量的百分比(x %)来表示漂白粉的优劣。
(1)漂白粉与酸的反应方程式为【提示:反应物为Ca(ClO)2、CaCl2、H2SO4】_______________。
(2)现为了测定一瓶漂白粉的 x %,进行了如下实验:称取漂白粉样品2g,加水研磨后,转入250mL容量瓶内,用水稀释至刻度,摇匀后取出25mL,加入过量的KI溶液和过量的稀硫酸,静置。待漂白粉放出的氯气与KI完全反应后,用0.1mol/L的Na2S2O3标准溶液滴定反应中生成的碘,该化学反应方程式为(提示:反应物为Na2S2O3、I2,产物之一为Na2S4O6)_______________。
(3)滴定时用去Na2S2O3溶液20mL,试由上述数据计算该漂白粉的 x %。
(适合高中学生)
2015年 第 11 期答案
1. AD 2. AC 3. CD 4. B
5.(1)⑤⑥
(2)难溶于水,不溶于稀H2SO4
(3)①②和④,复分解反应,因为这三种物质分属酸、碱、盐,它们都符合发生复分解反应的条件
6. BC 7. AD
8.(1)2Hg + 2HClO = Hg2OCl2 + H2O,氯氧化汞
注:Hg2OCl2也可写成HgO·HgCl2或HgCl2·HgO
(2)7N2H4 = 8NH3 + 3N2 + 2H2
(3)乙烷中的碳原子没有孤对电子,肼中的氮原子有1对孤对电子,过氧化氢中的氧有2对孤对电子,使A-A键的键能减小
9. (1)4Na2SO3 = 3Na2SO4 + Na2S
(2)SO42-离子的检出:SO42- + Ba2+ = BaSO4↓,不溶于盐酸
S2-离子的检出:方法1是加沉淀剂,如S2- + Pb2+ = PbS↓(黑);方法2是加盐酸,S2- + 2H+ = H2S↑(可闻到硫化氢的特殊气味)
