食品中12种防腐剂多通量测定方法的研究
2015-12-31陈幸莺
陈幸莺
(湘潭市食品药品检验所,湖南湘潭 411100)
食品防腐剂能抑制食品中微生物的繁殖,防止腐败变质,延长保存期。但是食品中防腐剂的使用存在超范围、超量使用问题,更有少数不法之徒为牟取暴利,使用工业用防腐物质作为食品防腐剂,严重侵犯了消费者的健康权益。
食品中食品添加剂丙酸、富马酸二甲酯、山梨酸、苯甲酸、脱氢乙酸、对羟基苯甲酸酯类的检测方法,已有相应的单独测定食品中某一种或多种防腐剂的标准方法。中国国家标准测定食品中丙酸钙(钠)[1]、山梨酸、苯甲酸[2]、脱氢乙酸[3]及对羟基苯甲酸酯类[4]的检测方法中,丙酸是用水蒸气蒸馏,山梨酸、苯甲酸、脱氢乙酸用乙醚提取,浓缩后以丙酮定容,对羟基本甲酸酯类是以乙醚提取,浓缩后以乙醇定容。湖南省地方标准[5]是采用气相色谱方法测定食品中富马酸二甲酯的,高杨[6]、曹淑瑞等[7-9]在采用气质法、液相法测定多种对羟基苯甲酸酯的研究中,对于此12种防腐剂的提取,分别使用了乙醚、丙酮、乙醇、乙腈、乙酸乙酯等有机溶剂及不同的提取方式。可见,尚无一次性同时检测以上12种防腐剂的方法。本研究旨在通过简化、优化多种防腐剂的提取方法,探索气相色谱法一次性同时测定食品中丙酸、富马酸二甲酯、山梨酸、苯甲酸、脱氢乙酸、对羟基苯甲酸甲酯、对羟基苯甲酸乙酯、对羟基苯甲酸丙酯、对羟基苯甲酸丁酯、对羟基苯甲酸异丙酯、对羟基苯甲酸异丁酯、对羟基苯甲酸庚酯12种防腐剂含量的准确、可靠、快速、简便的分析方法。
1 材料与方法
1.1 试剂和材料
乙酸乙酯:色谱纯,国药集团化学试剂有限公司;
无水硫酸镁:分析纯,天津市科密欧化学试剂有限公司,于马弗炉700℃灼烧5 h,置于干燥器中备用;
盐酸溶液:1+1(V/V);
乙酸锌溶液:200 g/L;
亚铁氰化钾溶液:106 g/L;
12种防腐剂标准品:纯度大于或等于98.5%,国家标准物质中心。
1.2 仪器与设备
气相色谱仪:GC2010型,配氢火焰离子化检测器(FID),日本岛津公司;
超声波清洗器:KQ-500B型,西安精大检测设备有限公司;
涡旋混合器:SK-1型,金坛市天竟实验仪器厂;
离心机:H1850R型,湘仪离心机仪器有限公司。
1.3 试验方法
1.3.1 气相色谱测定条件的优化
(1)色谱柱的选择:DB-1石英毛细管柱,30 m×0.25 mm ×0.25 μm;DB-5 石英毛细管柱,30 m ×0.25 mm ×0.25 μm;DB-FFAP 石英毛细管柱,30 m × 0.25 mm × 0.25 μm。
(2)柱温的选择:恒温:165℃[3];程序升温:100℃(0.5 min)→15℃/min→240℃(28 min);80℃(0.5 min)→15℃/min→240℃(28 min)。
(3)其他色谱条件:进样口温度:250℃;检测器温度:250 ℃;载气:氮气,纯度≥99.999%,柱流量:1.0 mL/min;空气流量:400 mL/min;氢气流量:47 mL/min;尾吹气流量:30 mL/min;进样量:1 μL;进样方式:分流进样,分流比:5︰1。
1.3.2 标准溶液的配制 分别准确称取各防腐剂标准品适量,用乙酸乙酯溶解,配成浓度为10 mg/mL的标准储备液置于棕色容量瓶中,用刻度吸管准确量取各标准储备溶液,用乙酸乙酯配成混合标准储备溶液,浓度为1.0 mg/mL。将混合标准储备溶液用乙酸乙酯稀释成 1.28,6.40,16.00,40.00,80.00,100.00,200.00,500 μg/mL 的浓度作为混合标准工作溶液。
1.3.3 不同提取溶剂的试验 取匀质后的待测样品(10.00±0.01)g于100 mL比色管中,加20 mL水(含蛋白质的物质,加5 mL乙酸锌溶液,5 mL亚铁氰化钾溶液),加1 mL盐酸溶液(1+1),分别加入10 mL乙醚、丙酮、乙腈、乙酸乙酯作为提取溶剂对不同食品样品中的12种防腐剂进行提取。提取液涡旋2 min,超声20 min。转入50 mL离心管,以5 000 r/min离心10 min,取上清液至10 mL比色管中,加0.5 g无水硫酸镁,涡旋2 min,过0.45 μm 有机相滤膜。
1.3.4 不同提取方式的试验 分别采用超声波2,5,10,15,20 min,涡旋萃取 2,5,10,15,20 min,涡旋 2 min+ 超声波 20 min提取3种提取方式,分别测定添加在酱油样品中的12种防腐剂含量,以考察不同提取方式的提取效率。
1.4 精确度、线性、检出限及回收率
(1)分别对面包、饮料、酱、酱油、食用槟榔、果汁等食品样品中的12种防腐剂待测组分进行6平行测定,计算检测结果的实验室内变异系数。
(2)在1.0~1 000.0 μg/mL 的范围内,对12种防腐剂标准物质,选取多个浓度进行测定,计算每一种防腐剂标准曲线的线性相关系数。
(3)以仪器测量时的3倍信噪比,测得方法最低检出限。
(4)对于食品防腐剂含量为0.1~0.4 g/kg的酱油、饮料、糕点、酱、食用槟榔等样品,违禁物质——富马酸二甲酯(本试验添加)含量为1~3 mg/kg的食用槟榔、酱油等样品,分别添加为0.5~4.0 mg的标准物质,来测定有效待测组分的回收率。
1.5 方法的验证
以文献[1]中方法分别对不同食品样品中的丙酸组分进行测定;以文献[5]中方法分别对不同食品样品中的富马酸二甲酯组分进行测定;以文献[10]、[11]中方法相组合,分别对面包、辣椒酱、酱油、果汁等食品样品中山梨酸、苯甲酸、脱氢乙酸等3种组分进行测定;以文献[4]中方法分别对不同食品样品中对羟基苯甲酸酯类等组分进行测定,验证本试验方法的准确性。
2 结果与分析
2.1 色谱条件的选择
以非极性柱 DB-1、中等极性柱 DB-5、极性柱DB-FFAP来检测分离此12种防腐剂。试验显示,DB-1和DB-5柱检测时,丙酸标准品与溶剂峰出峰时间接近,样品检测时不能有效分离,而DB-FFAP柱同时检测12种防腐剂组分时,能取得满意的分离效果。DB-1和DB-5柱可用于除丙酸外的其他11种防腐剂的分离检验,但被测组分的出峰顺序与DBFFAP柱有所不同。
当色谱柱温度为恒温分析时不能有效分离丙酸和富马酸二甲酯、对羟基苯甲酸异丙酯和对羟基苯甲酸甲酯组分,且出峰拖尾严重,影响检测结果的准确性。当程序升温的初始温度高于100℃时,丙酸和富马酸二甲酯组分不能有效分离的问题同样存在。当选择柱温条件为:80℃(0.5 min)→15℃/min→240℃(28 min)时,对标准物质和样品进行测定,12种防腐剂的分离度好、峰面积大(标准品的色谱图及部分检测样品的色谱图见图1~3)。

图1 12种防腐剂标准品(各单品种0.08 μg)气相色谱图Figure 1 Twelve kinds of preservatives standard material(0.08 μg each single variety)by gas chromatogram
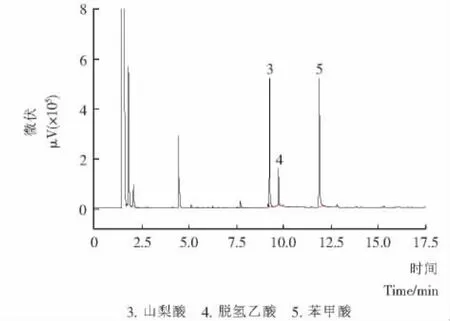
图2 辣椒酱样品防腐剂检测气相色谱图Figure 2 Chili sauce sample preservatives test by gas chromatogram
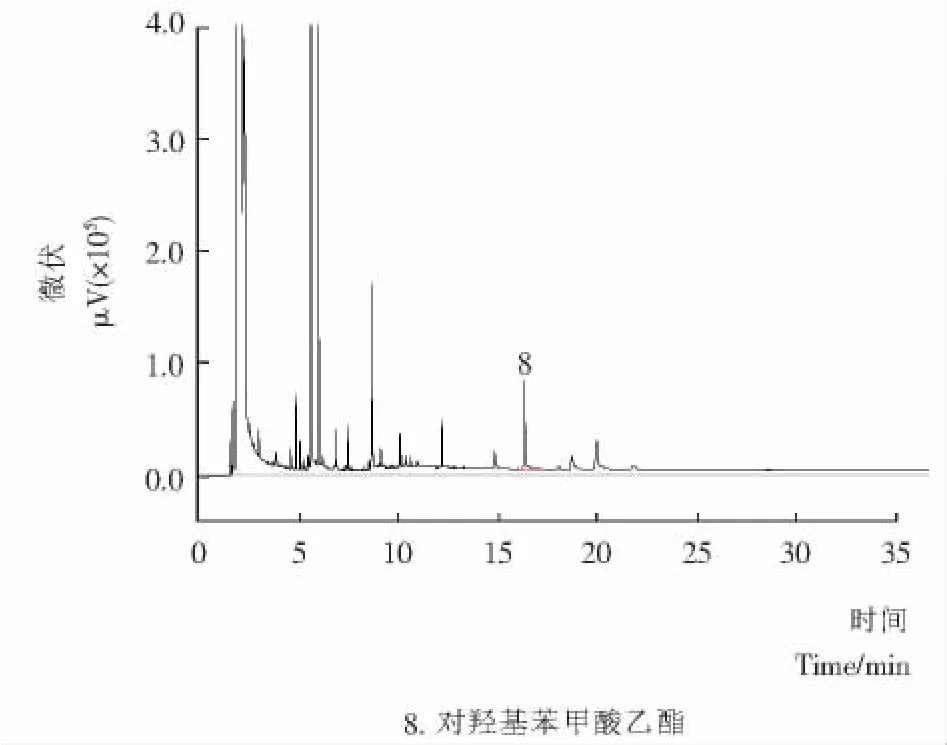
图3 食用槟榔样品防腐剂检测气相色谱图Figure 3 Edible betel nut samples preservatives test by gas chromatogram
2.2 提取溶剂对食品中12种防腐剂提取效率的影响
因乙醇的亲水性,本试验将其排除在外。本试验采用乙醚、丙酮、乙腈、乙酸乙酯等试剂进行提取。结果(表1)表明,采用乙醚、乙腈、乙酸乙酯浸提12种防腐剂的效果都不错。3种溶剂相比较而言,乙醚沸点低、稳定性较差,乙腈毒性较大,费用较高,乙酸乙酯毒性较低、稳定性较好,费用较低,综合考虑,本试验选择了乙酸乙酯作为浸提溶剂。
2.3 提取方式对食品中12种防腐剂提取效率的影响
在检测山梨酸、苯甲酸、脱氢乙酸、对羟基苯甲酸酯类的标准方法[1-4]中,均是以多次浸提、合并提取液后浓缩的方式进行有效待测组分的提取。在检测富马酸二甲酯的标准方法[5]中,是以固相萃取的方式进行有效待测组分的提取。本试验进行的超声波提取、涡旋萃取单因素试验结果表明,在提取初期(0~2 min)时,涡旋提取比超声波提取效果要好。随着提取时间的增加,两种提取方式的有效待测组分提取率都随之升高,但超声波提取的效果更明显。当提取时间达到20 min之后,两种提取方式对防腐剂提取效率到达最大值,检测结果无显著性差异。采用涡旋2 min+超声20 min的组合提取方式进行相同样品的提取测定(见表2),结果显示,以超声波涡旋混合提取方式来进行提取的效果最优。
2.4 方法的精确度、线性、检出限及回收率
2.4.1 精密度 本试验按每种防腐剂各取一种食品样品进行6次平行测定(见表3),结果表明:12种防腐剂平行测定的实验室内变异系数符合《实验室质量控制规范食品理化检测》(GB/T 27404—2008)附录F要求的含量为1~10 mg/kg样品的变异系数≤7.5%;含量为100~1 000 mg/kg样品的变异系数≤3.8%的要求,表明本试验方法重现性良好。
2.4.2 方法的线性范围 选取 1.28,6.40,16.00,40.00,80.00,100.00,200.00,500.00,1 000.00 μg/mL浓度的12种防腐剂混合标准溶液进行气相色谱测定,12种防腐剂的线性相关系数R均在0.999 9以上(见表4),符合《实验室质量控制规范食品理化检测》(GB/T 27404—2008)附录F要求的相关系数不应低于0.99的要求,线性关系良好。
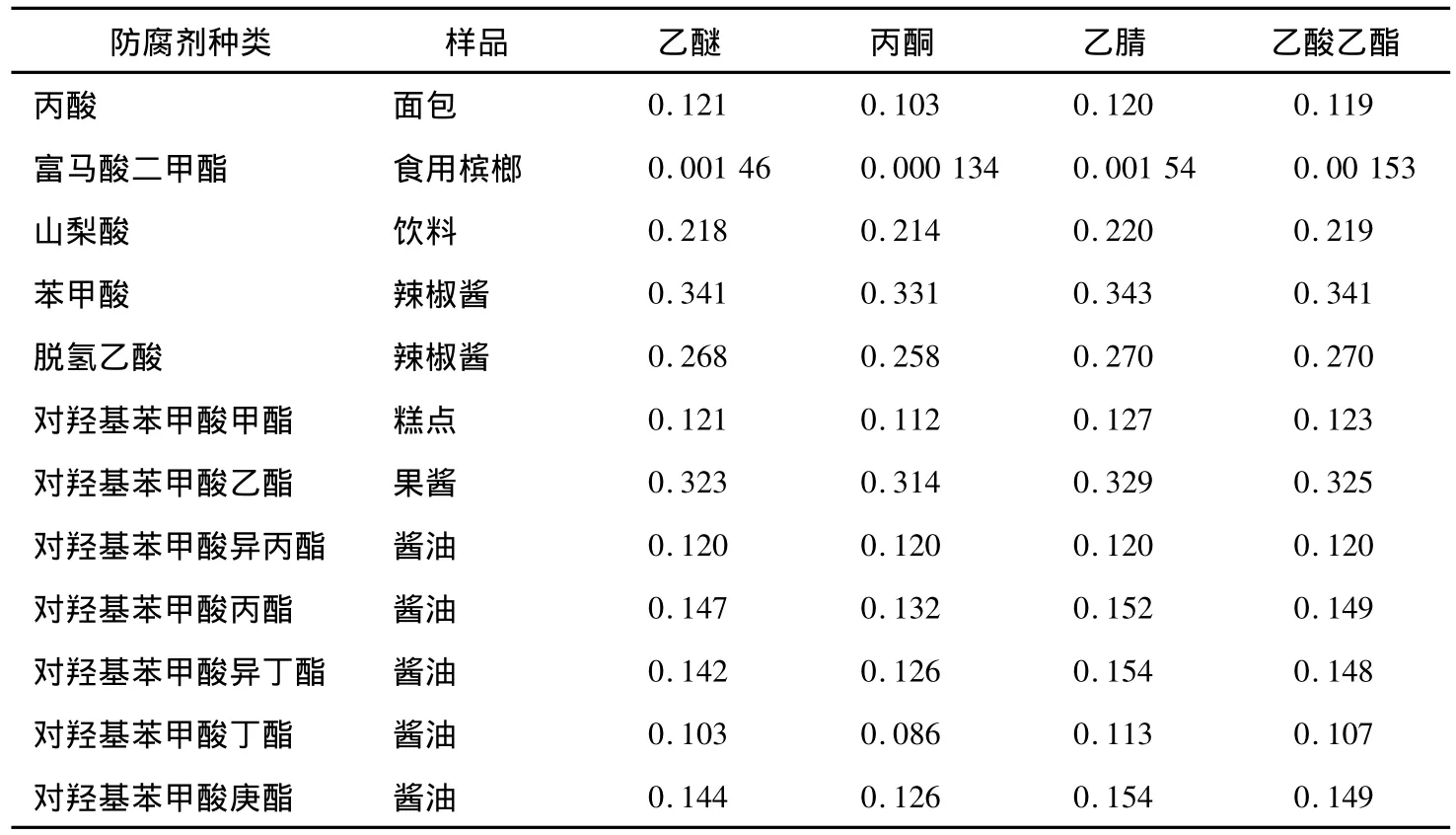
表1 不同溶剂提取的效果Table 1 Effect of different solvents extraction (g·kg-1)

表2 提取方式对酱油中防腐剂提取效果的影响Table 2 Effect of extraction way on the extraction efficiency of the preservatives in the soy sauce (g·kg-1)

表3 平行测定的实验室内变异系数Table 3 Parallel determination of the coefficient of variation in the laboratory
2.4.3 方法检出限 根据3倍信噪比,测得12种防腐剂的最低检出限(见表5),与国家标准、地方标准的相当。
2.4.4 方法的回收率 本试验选取面包、酱油、食用槟榔、饮料、辣椒酱、腐乳等食品样品进行了加标回收试验,测得12种防腐剂回收率在92.1% ~108.3%(见表6),符合《实验室质量控制规范 食品理化检测》(GB/T 27404—2008)附录F要求的被测组分含量为1~100 mg/kg样品的回收率范围为90% ~110%;被测组分含量为大于100 mg/kg样品的回收率范围为95%~105%的要求,说明本试验方法的测定结果准确可靠。
2.5 方法的验证
采用本法与《食品中丙酸钠、丙酸钙的测定》(GB/T 5009.120—2003)两种方法分别对不同样品如面包、蛋黄派、酱油、醋等样品中丙酸含量进行测定,比对结果见表7,相对偏差符合《实验室质量控制规范 食品理化检测》(GB/T 27404—2008)附录F要求的含量为10~1 000mg/kg样品的检测结果偏差范围为<15%的要求。
表4 各组分线性范围Table 4 The linear range of matter

表4 各组分线性范围Table 4 The linear range of matter
各组分线性范围均为1~1 000 μg/mL。
防腐剂种类 线性方程 相关系数丙酸 y=1 714.0x-7 009.6 0.999 9-2 429.4 0.999 9富马酸二甲酯 y=1 613.5x-1 305.9 0.999 9山梨酸 y=2 398.6x-8 365.1 0.999 9苯甲酸 y=2 383.1x-8 059.1 0.999 9脱氢乙酸 y=1 619.8x-5 384.8 0.999 9对羟基苯甲酸甲酯 y=2 517.2x-4 893.9 0.999 9对羟基苯甲酸乙酯 y=2 251.8x-5 286.0 0.999 9对羟基苯甲酸异丙酯 y=2 627.6x-6 359.8 0.999 9对羟基苯甲酸丙酯 y=2 677.4x-6 464.4 0.999 9对羟基苯甲酸异丁酯 y=2 814.1x-6 989.3 0.999 9对羟基苯甲酸丁酯 y=2 677.4x-6 822.8 0.999 9对羟基苯甲酸庚酯 y=2 490.1x

表5 方法的最低检出限Table 5 The minimum detection limit of the method (mg·kg-1)

表6 方法的回收率Table 6 Recoveries of the method

表7 食品中丙酸本法与国标方法测定的比对结果Table 7 Results compared of the method with national standard method of propionic acid in food
采用本法与《食品中富马酸二甲酯测定气相色谱法》(DB43/T 353—2007)两种方法分别对不同样品如食用槟榔、酱油、果汁、熟食等样品中富马酸二甲酯含量进行测定,比对结果见表8,相对偏差符合《实验室质量控制规范 食品理化检测》(GB/T 27404—2008)附录 F要求的含量为0.01~10.00 mg/kg样品的检测结果偏差范围为-20% ~+10%的要求。

表8 食品中富马酸二甲酯本法与地标方法测定的比对结果Table 8 Results compared of the method with local standard method of dimethyl fumarate in food
采用《食品中脱氢乙酸的测定》(GB/T 23377—2009)、《食品中苯甲酸、山梨酸和糖精钠的测定高效液相色谱法》(GB/T 23495—2009)相结合与本法分别对面包、辣椒酱、酱油、果汁中山梨酸、苯甲酸、脱氢乙酸含量进行测定,比对结果见表9。相对偏差符合《实验室质量控制规范食品理化检测》(GB/T27404—2008)附录F要求的含量为10~1 000 mg/kg样品的检测结果偏差范围为<15%的要求。

表9 食品中山梨酸、苯甲酸、脱氢乙酸本法与国家标准液相色谱法测定的比对结果Table 9 Results compared of the method with national standard method(HPLC)of sorbic acid,benzoic acid and dehydroacetic acid in food

表10 本法与国标法测定食品中对羟基苯甲酸酯类的比对结果Table 10 Results compared of the method with national standard method of p-hydroxy benzoic acid esters in food
采用《食品中对羟基苯甲酸酯类的测定》(GB/T 5009.31—2003)与本法分别对食用槟榔、酱油、果汁、果酱中对羟基苯甲酸酯的含量进行测定,比对结果见表10。相对偏差符合《实验室质量控制规范 食品理化检测》(GB/T 27404—2008)附录F的要求。
3 结论
本试验建立了采用气相色谱仪一次性同时检测12种食品中防腐剂的检验方法。该方法选择了毒性较低、稳定性较好,费用较低的乙酸乙酯作为溶剂。通过涡旋提取2 min、超声波提取20 min,待测组分提取完全,分离度好,灵敏度高、干扰少,具有操作简便、效率高、能耗低、时间短等优点,解决了多种防腐剂提取过程过于繁杂的问题,并采用毛细管柱和程序升温进行气相色谱分离测定。本方法的回收率为92.1% ~108.3%,平均回收率 98.5%,回收率标准偏差 3.0%,测定结果准确可靠。通过与标准方法规定的气相色谱方法、液相色谱方法进行比对,结果偏差符合方法学要求。
1 中华人民共和国卫生部.GB/T 5009.120—2003食品中丙酸钠、丙酸钙的测定[S].北京:中国标准出版社,2011.
2 中华人民共和国卫生部.GB/T 5009.29—2003食品中山梨酸、苯甲酸的测定[S].北京:中国标准出版社,2003.
3 中华人民共和国卫生部.GB/T 5009.121—2003食品中脱氢乙酸的测定[S].北京:中国标准出版社,2003.
4 中华人民共和国卫生部.GB/T 5009.31—2003食品中对羟基苯甲酸酯类的测定[S].北京:中国标准出版社,2003.
5 湖南省质量技术监督局.DB43/T 353—2007食品中富马酸二甲酯测定气相色谱法[S].长沙:湖南省质量技术监督局,2007.
6 高杨,郑玉山.气相色谱法及气相色谱—质谱法测定调味品中的对羟基苯甲酸酯[J].中国调味品,2014,39(8):106 ~108.
7 曹淑瑞,刘治勇,张雷,等.高效液相色谱法同时测定食品中6种对羟基苯甲酸酯[J].分析化学,2012,40(4):529 ~533.
8 王祖翔,周洪斌,蒋俊,等.气相色谱—串联质谱法测定复合调味料中的微量苯甲酸[J].食品与机械,2011,27(3):84 ~87.
9 陈利国,曹小彦,黄辉,等.毛细管气相色谱法直接测定食品中4种对羟基苯甲酸酯[J].食品与机械,2010,26(1):67 ~69.
10 青岛市质量技术监督局.GB/T 23377-2009食品中脱氢乙酸的测定 高效液相色谱法[S].北京:中国标准出版社,2009.
11 中国标准化研究院.GB/T 23495-2009食品中苯甲酸、山梨酸和糖精钠的测定[S].北京:中国标准出版社,2009.
