正交试验优化醇碱法脱除魔芋葡甘露聚糖乙酰基工艺
2015-12-29裴剑飞李文浩张国权
张 伟,裴剑飞,李文浩,熊 森,郑 旻,张国权*
(西北农林科技大学食品科学与工程学院,陕西 杨凌 712100)
正交试验优化醇碱法脱除魔芋葡甘露聚糖乙酰基工艺
张 伟,裴剑飞,李文浩,熊 森,郑 旻,张国权*
(西北农林科技大学食品科学与工程学院,陕西 杨凌 712100)
为提高魔芋葡甘露聚糖在面食中的添加量,通过脱乙酰降低其吸水倍率。以魔芋葡甘露聚糖为材料,对影响其乙酰基脱除效果的乙醇体积分数、NaOH溶液浓度、反应温度、处理时间等条件进行了优化,采用红外光谱法分析并测定吸水倍率对其验证,结果表明:乙酰基脱除的适宜工艺条件为乙醇体积分数40%、NaOH溶液浓度0.12 mol/L、反应温度60 ℃、处理时间12 min,在此条件下乙酰基完全脱除,且吸水倍率为原样品的9.3 2%。醇碱法可有效脱除魔芋葡甘露聚糖乙酰基,降低吸水倍率,增大其在面粉中的添加比例,改善 面粉粉质特性。
魔芋葡甘露聚糖;吸水倍率;乙酰基;粉质参数
魔芋(Amorphophallus konjac),又称蒟蒻、花莲杆、蛇六谷等,为天南星科魔芋属多年生草本植物,在我国主要分布于四川、湖北、云南、贵州、陕西等地区,具有产量高、质量优等特点[1-4]。魔芋含有丰富的魔芋葡甘露聚糖(konjac glucomannan polysaccharide,KGM)、蛋白质、以及镁、铁、钙、钾、钠、锰、铜等微量元素,其中KGM含量占50%以上[5-7]。KGM可降低血液中的中性脂质、胆固醇和血糖的浓度,能有效地控制体质量及预防结肠癌病[8]。KGM是由D-葡萄糖和D-甘露糖链通过β-1,4糖苷键聚合而成的天然高分子多糖,主链甘露糖C3位上存在β-1,3糖苷键支链,通常每32 个糖基有3 个支链,且每19 个糖基上有一个以酯键形式结合的乙酰基[9-13]。乙酰基的存在直接控制了KGM吸水性的大小[14],其吸水倍率与乙酰基含量呈正相关[15-16],吸水倍率可达自身质量的80~200 倍,极大地限制其在面制品等食品领域中的应用。
降低KGM吸水倍率的方法主要包括化学、物理及生物法[17]。化学法主要涉及乙酰化、脱乙酰等,效率较高;物理法包括超声波法、辐射法、超高压处理、超微粉碎、共混改性法等[18-19];生物法主要为酶法,其工艺复杂,处理量小。目前,国内外关于脱KGM乙酰基的研究主要为直接加碱法脱乙酰、机械力化学脱乙酰等[20]。本研究采用醇碱法脱除KGM乙酰基,对其乙酰基脱除的工艺条件进行优化,以吸水倍率和红外光谱分析验证脱除效果,以期降低KGM的吸水能力,扩大KGM在面制品加工中的添加比例,充分利用其功能。
1 材料与方法
1.1 材料与试剂
KGM(纯度≥95%) 陕西省安康市九龙贸易有限公司;面粉 陕西老牛面粉有限公司;NaOH、盐酸、硝酸银、无水乙醇、溴化钾等(均为分析纯) 四川西陇化工有限公司。
1.2 仪器与设备
KDC-40型离心机 科大创新股份有限公司中佳分公司;SHA-C型水浴恒温振荡器 常州国华电器有限公司;DK-S26型电热恒温水浴锅 上海森信实验仪器有限公司;SHB-Ⅲ型循环水式多用真空泵 郑州长城科工贸有限公司;HR-200型电子分子天平 东生兴业有限公司;101-1AB型电热鼓风干燥箱 天津市泰斯特仪器有限公司;PB-10型pH计 赛多利斯科学仪器有限公司;Vetex70傅里叶变换红外光谱仪 德国Bruker公司;粉质仪 德国Brabender公司。
1.3 方法
1.3.1 KGM脱乙酰基处理
参考刘锋[16]方法,并加以改进。将20 g KGM分散于120 mL乙醇溶液中,在室温(25 ℃)条件下搅拌溶胀30 min后,加入NaOH溶液,在合适温度条件下恒温反应一定时间后,加入6 mol/L盐酸溶液,调整pH 6.8,终止反应,再用30%乙醇溶液进行清洗数次,直至上清液用硝酸银检验不出含有氯离子为止,样品在60 ℃条件下烘干至质量恒定,即得到粉末状脱乙酰基KGM。
1.3.2 KGM脱乙酰基单因素试验
1.3.2.1 乙醇体积分数的确定
将KGM 20 g分别加入到乙醇体积分数为20%、30%、40%、50%、60%的溶液中,在NaOH溶液浓度0.09 mol/L、反应温度50 ℃、处理时间9 min条件下进行改性处理,测定产物的吸水倍率。
1.3.2.2 NaOH溶液浓度的确定
将KGM 20 g加入到40%乙醇溶液中,NaOH溶液浓度分别为0.03、0.06、0.09、0.12、0.15 mol/L,在反应温度50 ℃、处理时间9 min条件下进行改性处理,测定产物的吸水倍率。
1.3.2.3 反应温度的确定
将KGM 20 g加入到40%乙醇溶液中,NaOH溶液浓度0.09 mol/L,反应温度分别为30、40、50、60、70 ℃,处理时间9 min条件下进行改性处理,测定产物的吸水倍率。
1.3.2.4 处理时间的确定
将KGM 20 g加入到40%乙醇溶液中,NaOH溶液浓度0.09 mol/L、反应温度50 ℃,处理时间分别为3、6、9、12、15 min条件下进行改性处理,测定产物的吸水倍率。
1.3.3 KGM脱乙酰基条件的优化试验设计
选择乙醇体积分数、NaOH溶液浓度、反应温度、处理时间四因素进行L27(313)正交试验。
1.3.4 吸水倍率测定
参考Koroskenyi等[21]方法,并加以改进。精确称取0.100 0 g干样品,记为m0,放入50 mL的离心管中,总质量记为m1,准确加入30 mL蒸馏水,在25 ℃条件下水浴振荡1 h,静止1 h,3 000 r/min离心30 min,弃上清液,称质量记为m2。吸水倍率按如下公式计算:
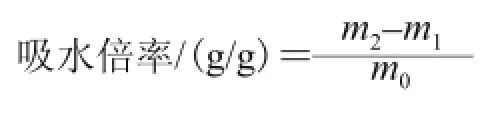
1.3.5 红外光谱扫描
将测试样品用纯KBr制成薄片,采用傅里叶红外吸收光谱仪在400~4 000 cm-1范围内进行扫描,分辨率为4 cm-1,扣除背景。
1.3.6 粉质参数测定
将普通面粉和添加1% KGM作为对照,测定添加5%脱乙酰基KGM的粉质参数,参照GB/T 14614—2006《小麦粉:面团的物理特性:吸水量和流变学特性的测定:粉质仪法》,采用德国布拉本德粉质仪测定。
1.4 数据分析处理
实验重复3 次,采用DPS 7.05、Microsoft Excel 2003及Origin 8.1进行数据处理。
2 结果与分析
2.1 单因素试验结果
2.1.1 乙醇体积分数对KGM脱乙酰基的影响
在过去,统治者的喜好往往会引领整个时代的审美。雍正帝对粉彩的偏好让粉彩花鸟瓷画焕发了前所未有的生机。这一时期的粉彩花鸟瓷画表现出浓烈的文人气息。从画面的整体布局来看,疏密有致,从格调来看,颜色清雅,让人过目难忘。这一时期更是成为粉彩花鸟瓷画的巅峰时期。
由图1a可知,乙醇体积分数在20%~40%的范围内,脱乙酰基KGM的吸水倍率随着乙醇体积分数的增加显著降低(P<0.05),当乙醇体积分数继续增加到50%~60%的范围内时,脱乙酰基KGM的吸水倍率随着乙醇体积分数的增加显著升高(P<0.05),乙醇体积分数在40%~50%的范围内,脱乙酰基KGM的吸水率无显著性差异。由图1b可知,位于1 732.02 cm-1的吸收峰代表—C=O的伸缩振动,表明KGM分子链中存在着乙酰基团。随着乙醇体积分数的增加,该峰位逐渐消失,当乙醇体积分数为40%~50%时,乙酰基几乎完全消失,乙醇体积分数为60%时,乙酰基重新出现。这是因为乙醇体积分数影响KGM的溶胀度,进而影响KGM的脱乙酰反应。当乙醇体积分数过低时,溶液的黏度较大,体系分散不均匀,影响了KGM与碱的反应,且KGM溶胶与碱易形成凝胶,不利于粉状改性产物的获得;乙醇体积分数高时,KGM的溶胀度低,碱液很难渗入KGM球体内部,脱乙酰基反应只能发生在KGM球体的表层,很难发生在KGM分子骨架上。此外,位于806.22 cm-1和873.73 cm-1的吸收峰是KGM 的特征峰,代表甘露聚糖中的基本单元[22],脱乙酰基KGM 主链结构并未发生本质的变化。乙醇体积分数以40%为佳。
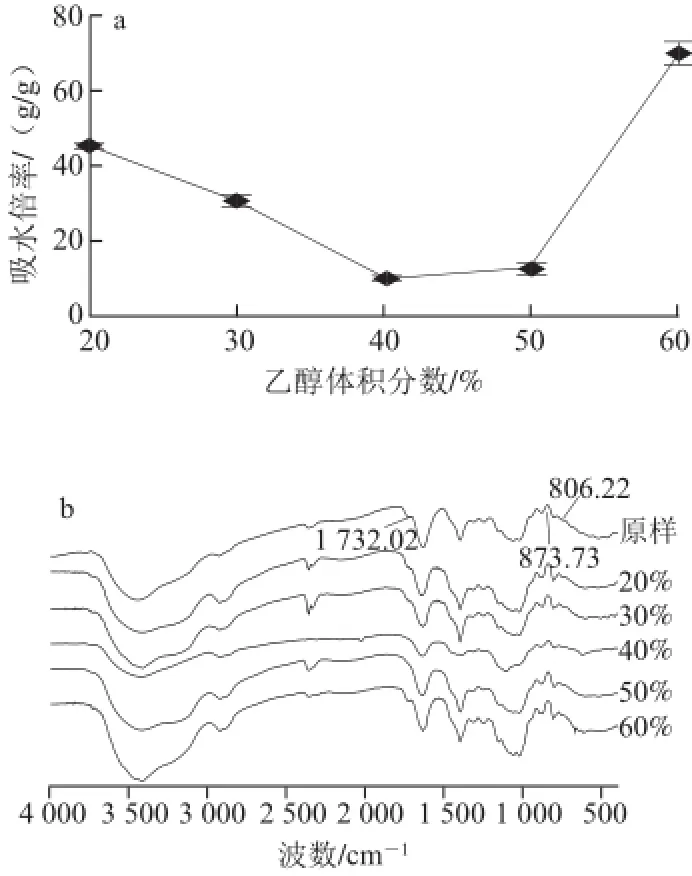
图 1 不同乙醇体积分数条件下脱乙酰基KGM的吸水倍率(a)和红外光谱图(bb)Fig.1 The water absorption rate (a) and FT-IR spectra (b) of KGM samples with various ethanol concentrations
2.1.2 NaOH溶液浓度对KGM脱乙酰基的影响
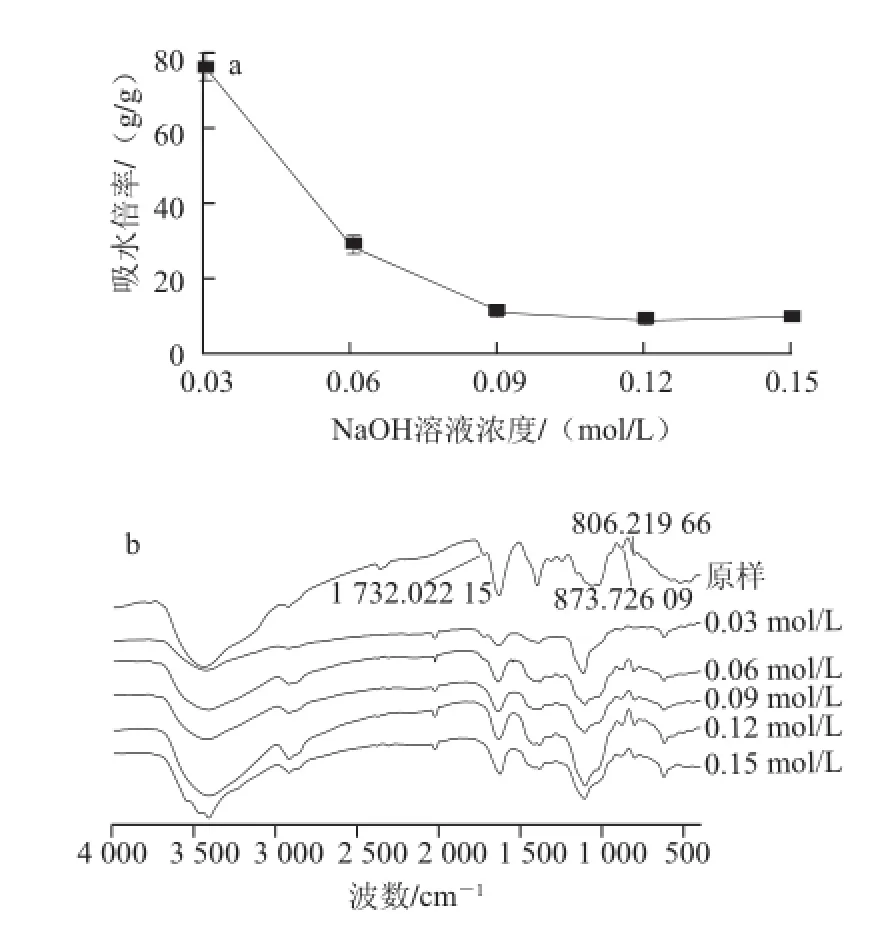
图 2 不同NaOH溶液浓度条件下脱乙酰基KGM的吸水倍率(a)和红外光谱图(bb)Fig.2 The water absorption rate (a) and FT-IR spectra (b) of KGM samples with various alkali concentrations
由图2a可知,NaOH溶液浓度在0.03~0.09 mol/L的范围内,脱乙酰基KGM的吸水倍率随着NaOH溶液浓度的增加显著降低(P<0.05),NaOH溶液浓度继续增加,其吸水倍率无显著性差异。图2b结果表明,随着NaOH溶液浓度的增加,乙酰基逐渐消失,当NaOH溶液浓度为0.09 mol/L时,乙酰基几乎完全消失,主链结构并未发生本质的变化。KGM脱乙酰基反应是酯的水解反应。在碱性条件下,酯键能完全水解,是一个不可逆过程。这是因为碱能中和水解生成的羧酸,使反应完全进行到底[14]。乙酰基的脱除影响KGM分子的水溶特性,从而使KGM吸水倍率发生巨大改变。适宜NaOH溶液浓度为0.09 mol/L。
2.1.3 反应温度对KGM脱乙酰基的影响
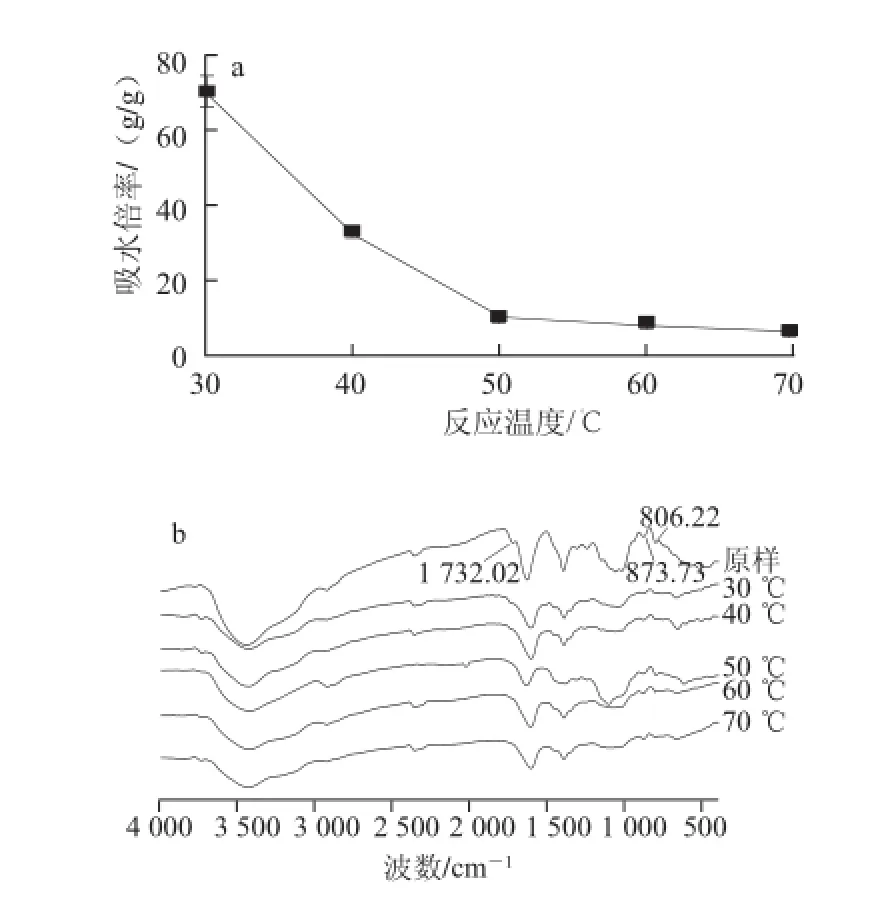
图 3 不同反应温度条件下脱乙酰基KGM的吸水倍率(a)和红外光谱图(bb)Fig.3 The water absorption rate (a) and FT-IR spectra (b) of KGM samples at different temperatures
由图3a可知,反应温度在30~50 ℃的范围内,脱乙酰基KGM的吸水倍率随着反应温度升高显著降低(P<0.05),反应温度继续升高,脱乙酰基KGM的吸水率无显著性差异。图3b结果表明,随着反应温度的升高,乙酰基逐渐消失,当温度为50 ℃时,乙酰基完全消失,主链结构未发生本质的变化。KGM脱乙酰基反应是一个吸热反应,升温有利于脱乙酰基反应的进行,当反应温度达到一定程度时,KGM脱乙酰基反应完成,吸水倍率不再随着反应温度的升高而发生显著变化,当反应温度过高时,乙醇挥发,易形成凝胶。反应温度为50~70 ℃的处理效果较好。
由图4a可知,处理时间在3~9 min的范围内,脱乙酰基KGM吸水倍率随着处理时间的延长显著降低(P<0.05)。图4b结果表明,随着处理时间的延长,乙酰基逐渐消失,当时间为9 min时,乙酰基几乎完全消失,主链结构未发生本质的变化。KGM中乙酰基的存在使之形成具有空隙的双螺旋结构,能保持大量水分,当乙酰基脱除后,螺旋结构被破坏,螺条相互交织成网状结构,并且脱乙酰后会产生明显的结晶区,导致其失去水溶性,吸水倍率下降[23]。处理时间继续延长,吸水倍率无显著性差异。这主要是因为当反应达到一定时间时,KGM脱乙酰基反应完全,吸水倍率不再随着反应时间的延长而发生显著变化。处理时间以9 min以上较为适宜。
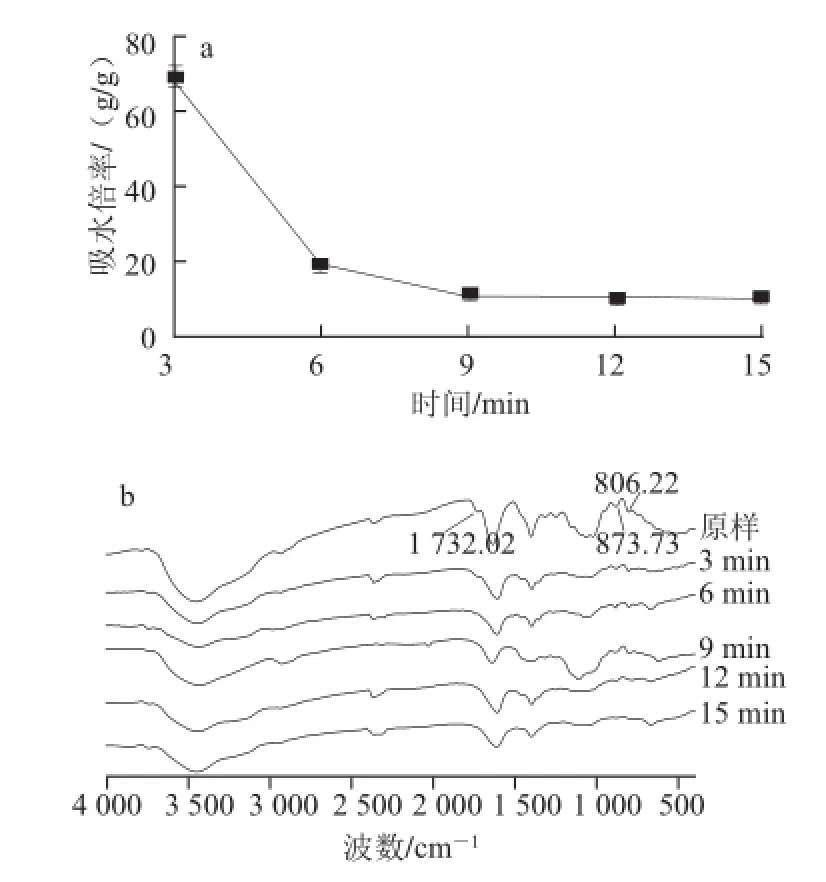
图 4 不同处理时间条件下KGM脱乙酰基产物的吸水倍率(a)和红外光谱图(bb)Fig.4 The water absorption rate (a) and FT-IR spectra (b) of KGM samples at different reaction times
2.2 KGM脱乙酰基的正交试验结果
极差分析表明(表1),乙醇体积分数、NaOH溶液浓度、反应温度、处理时间影响脱乙酰基KGM吸水倍率的主次顺序为B>C>D>A,即NaOH溶液浓度对KGM吸水倍率影响最大,反应温度、处理时间次之,乙醇体积分数影响最小。方差分析表明(表2),NaOH溶液浓度、反应温度、处理时间以及乙醇体积分数与处理时间、NaOH溶液浓度与处理时间的交互作用对KGM脱乙酰产物吸水倍率的影响达极显著水平(P<0.01),乙醇体积分数的影响不显著。优化组合为A2B3C3D3,即乙醇体积分数40%、NaOH溶液浓度0.12 mol/L、反应温度60 ℃、处理时间12 min,所得脱乙酰基KGM的吸水倍率为7.48 g/g,低于正交试验的任一组合。而原KGM的吸水倍率为80.24 g/g,脱乙酰基KGM的吸水倍率为原样品吸水倍率的9.32%。
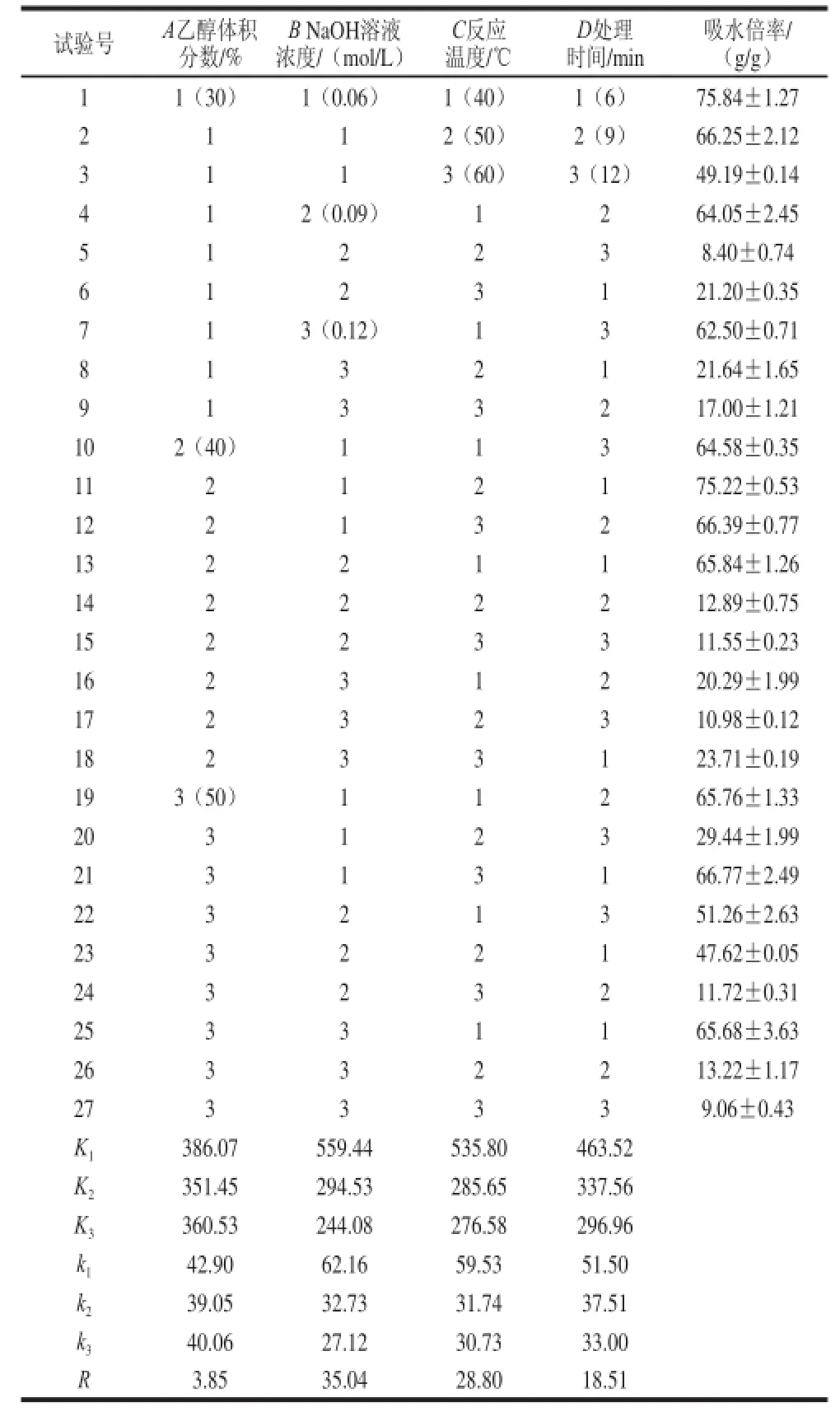
表 1 L27(313)正交试验方案及极差分析结果Table 1 L27(313) orthogonal experimental program and range analysis of the experimental results

表 2 试验结果方差分析表Table 2 Variance analysis of the experimental resultsTable 2 Variance analysis of the experimental results
2.3 影响脱乙酰基KGM吸水倍率的因素交互作用分析
从图5a可知,在较低乙醇体积分数条件下,吸水倍率随着处理时间的延长并无明显变化,当乙醇体积分数较高时,吸水倍率随着处理时间的延长明显下降;在较短时间内,吸水倍率随着乙醇体积分数的增加呈上升趋势,随着处理时间的延长,吸水倍率随着乙醇体积分数的增加而下降。从图5b可知,在低NaOH溶液浓度条件下,吸水倍率随着时间的延长呈现缓慢下降的趋势,高NaOH溶液浓度条件下,处理时间对吸水倍率影响不大;吸水倍率随着NaOH溶液浓度的增大显著下降,并且这种趋势随着反应时间的减少而趋于明显。
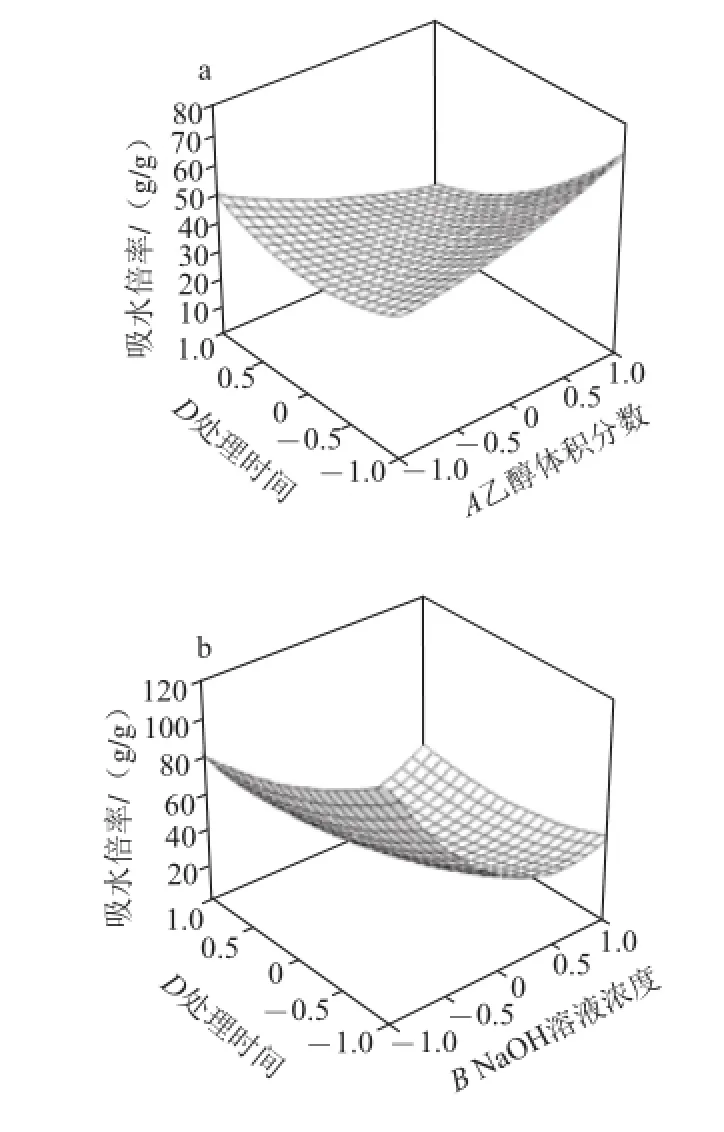
图 5 乙醇体积分数与处理时间(a)、NaOH溶液浓度与处理时间(b)交互作用对吸水倍率的影响Fig.5 Effects of interactions between ethanol concentration and reaction time (a), and between alkali concentration and reaction time (b) on water absorption rate
2.4 脱乙酰基KGM的红外光谱扫描分析
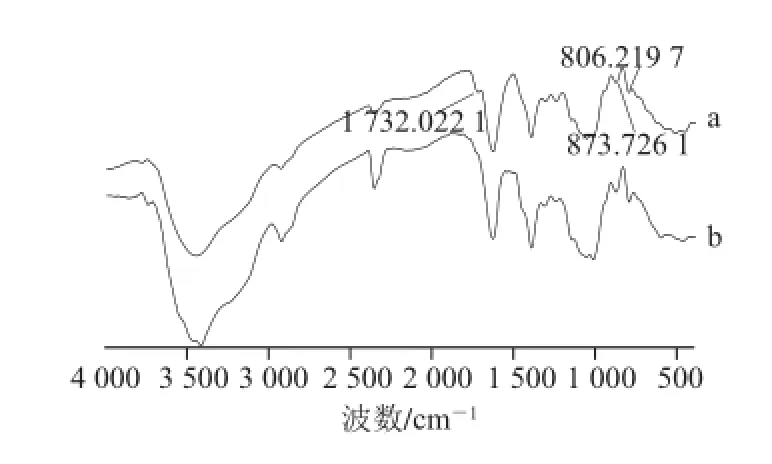
图 6 KGM(a)及最佳工艺条件下脱乙酰基KGM(b)的红外光谱图Fig.6 FT-IR spectra of KGM (a) and deacetylated KGM under optimum conditions (b)
图6 为原样及最佳工艺条件下KGM的红外光谱图,由图6可以看出,原样谱图中在1 732.02 cm-1处有吸收峰,此峰代表—C=O的伸缩振动,表明KGM分子链中存在着乙酰基团,位于806.22 cm-1和873.73 cm-1的吸收峰是KGM的特征峰,代表甘露聚糖中的基本单元,脱乙酰基KGM主链结构并未发生本质的变化。而采用醇碱法处理后,谱图在1 732.02 cm-1处没有吸收峰,表明可以有效地脱除KGM中的乙酰基,并且主链结构未发生本质变化。
2.5 脱乙酰基KGM对面粉粉质特性的影响

表 3 KGM及脱乙酰基KGM的粉质参数Table 3 Farinograph parameters of KGM and deacetyled KGM
表3为添加1%KGM及5%脱乙酰基KGM的面粉粉质参数,与原面粉相比,添加1%KGM及5%脱乙酰基KGM的面粉吸水率、形成时间、稳定时间、粉质质量指数显著增加,弱化度显著降低,粉质特性好;添加5%脱乙酰基KGM的面粉吸水率显著大于1%KGM,其他指标无显著性差异。结果表明,KGM经脱乙酰处理后,可显著增大其在面粉中的添加比例,改善面粉粉质特性,稳定时间在3.0 min以上,达到面条用小麦粉行业标准的要求(SB/T 10137—1993《面条用小麦粉》[24])。
3 结 论
采用醇碱法脱除KGM中乙酰基,影响改性产物吸水倍率的因素依次为NaOH溶液浓度、反应温度、处理时间、乙醇体积分数,适宜的工艺条件为乙醇体积分数40%、NaOH溶液浓度0.12 mol/L、反应温度60 ℃、处理时间12 min,所制备的脱乙酰基KGM的吸水倍率为7.48 g/g,为原样品吸水倍率的9.32%;红外光谱分析结果表明,醇碱法可以有效地脱除KGM中的乙酰基,且主链结构未发生本质变化;KGM经脱乙酰处理后,可显著增大其在面粉中的添加比例,改善面粉粉质特性。
[1] 牛义, 张盛林, 王志敏, 等. 中国魔芋资源的研究与利用[J]. 西南农业大学学报: 自然科学版, 2005, 27(5): 634-638.
[2] HERRANZ B, TOVAR C A, de ZALDÍVAR S, et al. Effect of alkalis on konjac glucomannan gels for use as potential gelling agents in restructured seafood products[J]. Food Hydrocolloids, 2012, 27: 145-153.
[3] 李娜. 改性魔芋葡甘聚糖成膜特性应用研究[D]. 重庆: 西南科技大学, 2006.
[4] 庞杰, 吴春华, 温成荣, 等. 魔芋葡甘聚糖凝胶研究进展及其问题[J].中国食品学报, 2011, 11(9): 181-186.
[5] 王成军, 郭剑伟, 鱼梅, 等. 魔芋的主要化学成分提取及应用研究概况[J]. 中国药物应用与监测, 2006(2): 32-34.
[6] 李娟. 魔芋化学成分的初步分析[D]. 成都: 中国科学院成都有机化学研究所, 2007.
[7] 黄麟杰. 魔芋化学成分分析及其提取分离的研究进展[J]. 国际中医中药杂志, 2013, 35(10): 941-943.
[8] OHYA Y, THARA K, MURATA J. Preparation and biological properties of dicarboxy-glucomannan: enzymatic degradation and stimulating activity against cultured marophages[J]. Carbohydrate Polymers, 1994, 25(2): 123-130.
[9] 李斌, 谢笔钧. 魔芋葡甘聚糖分子链形态的研究[J]. 中国农业科学, 2004, 37(2): 280-284.
[10] 许东颖, 盛家荣, 李光吉. 魔芋葡甘聚糖的改性及其在生物材料领域的应用概况[J]. 材料导报, 2008, 22(11): 47-50.
[11] KATSURAYA K, OKUYAMA K, HATANAKA K, et al. Constitution of konjac glucomannan chemical analysis and13C NMR spectroscopy[J]. Carbohydrate Polymers, 2003, 53: 183-189.
[12] 王永红, 张淑蓉, 卫飞. 改性处理对魔芋葡甘聚糖性质影响[J]. 粮食科技与经济, 2011, 36(2): 49-52.
[13] 林晓艳, 陈彦, 罗学刚. 魔芋葡甘露聚糖去乙酰基改性制膜特性研究[J]. 食品科学, 2002, 23(2): 21-24.
[14] MAEKAJI K. The mechanism of gelation of konjacmannan[J]. Agricultural and Biological Chemistry, 1974, 38: 315-321.
[15] DU Xuezhu, LI Jing, CHEN Jian, et al. Effect of degree of deacetylation on physicochemical and gelation properties of konjac glucomannan[J]. Food Research International, 2012, 46: 270-278.
[16] 刘锋. 魔芋葡甘聚糖疏水改性及吸附材料制备应用基础研究[D]. 重庆: 西南科技大学, 2010.
[17] 刘佩英. 魔芋学[M]. 北京: 中国农业出版社, 2003: 271-272.
[18] 丁金龙, 杨幼慧, 徐振林, 等. 超微粉碎对魔芋葡甘聚糖物性的影响[J].中国粮油学报, 2008, 23(1): 157-160.
[19] 潘廷跳, 陈丽萍, 王博华, 等. 魔芋葡甘聚糖的改性研究进展[J]. 中国粮油学报, 2012, 27(6): 124-128.
[20] 潘志东, 孟俊杰, 王燕民. 魔芋葡甘聚糖的机械力化学脱乙酰基和酯化改性[J]. 中国粉体技术, 2012, 18(1): 34-38.
[21] KOROSKENYI B, MCCARTHY S P. Synthesis of acetylated konjac glucomannan and effect of degree of acetylation on water absorbency[J]. Biomacromolecules, 2001, 2: 824-826.
[22] 孟俊杰, 潘志东, 王燕民. 采用氢氧化钾改性剂脱除魔芋中乙酰基团[J]. 农业工程学报, 2010, 26(2): 385-389.
[23] 李斌, 谢笔钧. 魔芋葡甘聚糖凝胶机理研究[J]. 中国农业科学, 2002, 35(11): 1411-1415.
[24] 商业部谷物油脂化学研究所. SB/T 10137—1993 面条用小麦粉[S].北京: 中国标准出版社, 1993.
Orthogonal Test Design for Optimization of Konjac Glucomannan Deacetylation by Ethanol-Alkali Method
ZHANG Wei, PEI Jianfei, LI Wenhao, XIONG Sen, ZHENG Min, ZHANG Guoquan*
(College of Food Science and Engineering, Northwest A&F University, Yangling 712100, China)
This study aimed to reduce the water absorption rate of konjac glucomannan by removing its acetyl group in order to promote its application in flour-based products. Factors influencing deacetylation efficiency, including ethanol concentration, NaOH concentration, temperature and time, were investigated in this study. Meanwhile, the removal efficiency of acetyl group was evaluated by Fourier transform infrared spectroscopy (FT-IR) analysis and water absorption rate. The optimum reaction parameters for deacetylation were determined as 40%, 0.12 mol/L, 60 ℃ and 12 min for ethanol concentration, NaOH concentration, reaction temperature and time, respectively. Under these conditions, the acetyl group in konjac glucomannan was completely removed and water absorption rate of deacetyled konjac glucomannan decreased to 9.32% of that of the original sample. In summary, the acetyl group in konjac glucomannan could be effectively removed by using ethanol-alkali method. Deacetylation could reduce the water absorption rate of konjac glucomannan and increase its proportion in flour, thus improving flour farinograph quality.
konjac glucomannan; water absorption rate; acetyl group; farinograms
S566.9
A
1002-6630(2015)08-0103-06
10.7506/spkx1002-6630-201508018
2014-09-13
张伟(1989—),女,硕士研究生,研究方向为农产品加工及贮藏工程。E-mail:zhangwei2012050601@163.com
*通信作者:张国权(1968—),男,教授,博士,研究方向为谷物品质评价及淀粉工程技术。E-mail:zhanggq98@126.com
