乙酸乙酯萃取-电感耦合等离子体原子发射光谱测定成品金锭中的痕量元素
2015-12-25吕红乌鲁木齐天山星贵金属冶炼有限公司乌鲁木齐830000
吕红(乌鲁木齐天山星贵金属冶炼有限公司 乌鲁木齐830000)
乙酸乙酯萃取-电感耦合等离子体原子发射光谱测定成品金锭中的痕量元素
吕红
(乌鲁木齐天山星贵金属冶炼有限公司乌鲁木齐830000)
摘要通过研究并建立了在同一体系中经溶剂萃取后用电感耦合等离子体原子发射光谱测定成品金锭中31种杂质元素的方法。仪器检测限为0.0005~0.0798 μg/mL,方法检测限为0.2~1.0 μg/mL。改进后分析结果更加精确,提高了实验室分析水平,缩短了工作时间、减小劳动强度、减少污染。
关键词电感耦合等离子体原子发射光谱成品金锭杂质元素乙酸乙酯萃取介质
0 引言
目前,在国内和国际尚无统一的成品金锭中化学分析方法,有关成品金锭中杂质元素分析的文献报道很少,为了满足上海交易所对我单位所生产的标准金锭的认证,以及样品仲裁检验金分析的需要,为我公司成品金锭分析提供技术保证。
通过多次反复的实验,最终使用乙酸乙酯萃取-电感耦合等离子体原子发射(ICP-7000DV)测定成品金锭的方法。该方法是在洁净的环境中,采用乙酸乙酯分离金基体,水相浓缩后定容到一定酸度的盐酸介质中,用ICP进行测定。该方法检测限低、精密度好,能够用于成品金锭中31中杂质元素的分析测定,因为上交所目前只要求6种(银、铜、铁、铅、锑、铋)杂质元素进行分析,本文只讨论这6种元素的结果。
1 实验部分
1.1仪器及工作参数
美国PE公司Optima 7000DV电感耦合等离子体原子发射光谱。
光谱仪工作参数:高频功率1150 W;雾化器实际压力283 kPa;棱镜温度27.39℃;检测器温度-8.43℃;光控制器板温度37.09℃。
1.2试剂及标准溶液
1.2.1盐酸:优级纯(ρ 1.19 g/mL)。
1.2.2硝酸:优级纯(ρ 1.42 g/mL)。
1.2.3硝酸:(1+1)优级纯。
1.2.4盐酸:(1+1)优级纯。
1.2.5盐酸:(1 mol/L)优级纯。
1.2.6盐酸:(1+9)优级纯。
1.2.7稀王水:硝酸(1.2.2)∶盐酸(1.2.1)∶水=1∶3∶3
1.2.8乙酸乙酯。
1.2.9高纯水:本实验室用的水都是高纯水。
1.2.10银标准贮存溶液:称取0.1000g银(质量分数≮99.95%)于100 mL烧杯中,加5 mL硝酸(1.2.3),加热溶解,移入100mL容量瓶中,加入60mL盐酸(1.2.1),以水稀释至刻度,混匀。此溶液1mL含1mg银。
1.2.11铜标准贮存溶液:称取1.0000 g金属铜(质量分数≮99.95%)于200 mL烧杯中,加10 mL硝酸(1.2.3),低温加热溶解,冷却至室温,移入500 mL容量瓶中,用水稀释至刻度,混匀。此溶液1 mL含2mg铜。
1.2.12铁标准贮存溶液:称取1.0000 g金属铁(质量分数≮99.95%)于200 mL烧杯中,先用水润湿,加20 mL盐酸(1.2.4),低温加热溶解,移入500 mL容量瓶中,用水稀释至刻度,混匀。此溶液1 mL含2 mg铁。
1.2.13铅标准贮存溶液:称取1.0000 g金属铅(质量分数≮99.95%)于200 mL烧杯中,加20 mL硝酸(1.2.3),低温加热溶解,移入500 mL容量瓶中,用水稀释至刻度,混匀。此溶液1 mL含2 mg铅。
1.2.14铋标准贮存溶液:称取1.0000 g金属铅(质量分数≮99.95%)于200 mL烧杯中,加20 mL硝酸(1.2.3),低温加热溶解,移入500 mL容量瓶中,用水稀释至刻度,混匀。此溶液1 mL含2 mg铋。
1.2.15锑标准贮存溶液:称取0.1000 g金属锑(质量分数≮99.95%)于100 mL烧杯中,加20 mL混合酸(1.2.7),低温加热溶解,冷却至室温,用盐酸(1.2.4)移入100 mL容量瓶中,并稀释至刻度,混匀。此溶液1 mL含1 mg锑。
1.2.16银标准溶液:准确移取银标准贮存溶液(1.2.10)10.00 mL于100 mL容量瓶中,用盐酸(1.2.4)稀释至刻度,混匀。此溶液1mL含100 μg银。
1.2.17铜、铁、铅、锑、铋混合标准溶液:分别移取铜、铁、铅、铋贮存溶液(1.2.11~1.2.14)5.00 mL,移取锑标准贮存溶液10.00 mL于100 mL容量瓶中,用盐酸(1.2.6)稀释至刻度,混匀。此溶液1mL含100 μg铜、铁、铅、锑、铋。
1.3分析步骤
⑴按表1称取试料置于100 mL烧杯中。
⑵按表1加入混合酸(1.2.7),盖上表面皿,低温加热使试料完全分解,低温蒸发至试液颜色呈棕褐色(冷却后不能析出单体金),打开表面皿挥发氮的氧化物,冷却至室温。
⑶用盐酸(1.2.5)洗涤表面皿并将试液移入125 mL分液漏斗中,并用盐酸(1.2.5)稀释体积至30 mL。
⑷加入20 mL乙酸乙酯,振荡60 s,静置分层,水相放入另一分液漏斗中,有机相加入2 mL盐酸(1.2.5),轻轻振荡20 s,静置分层,水相合并(保留有机相回收金)。
⑸合并后的水相按1.4.5重复操作一次,静置分层后的水相均放入原烧杯中制成试液。
⑹低温将试液蒸发至约3 mL,冷却至室温,用盐酸移入50 mL的容量瓶中并稀释至刻度,摇匀。
⑺在电感耦合等离子体原子发射光谱仪上,测量被测元素的谱线强度,扣除空白值,从工作曲线上确定被测元素的质量浓度。
1.4工作曲线的绘制
⑴标准使用溶液:准确移取0.00 mL、1 .00 mL、3.00 mL、5.00 mL、10.00 mL银(1.2.16.1)和铜、铁、铅、锑、铋混合标准溶液(1.2.16.2)于1组洗净的100 mL容量瓶中,用盐酸(1.2.6)稀释至刻度,摇匀。此溶液1 mL分别含0 μg/mL、1 μg/mL、5 μg/mL、10 μg/ mL、银、铜、铁、铅、铋、锑。
⑵在与试料测定相同条件下,测量标准溶液中各种元素的强度。以各被测元素的质量浓度为横坐标,谱线强度为纵坐标绘制工作曲线。
2 分析结果计算
按下式计算各元素的质量分数ω(X):
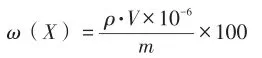
式中:X为被测元素;ρ为试液中杂质元素的质量浓度,μg/ mL;V为试液的总体积,mL;M为试料的质量,g。

表1
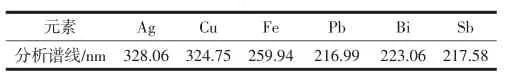
表2
3 萃取条件的选择
3.1萃取溶剂
纯金杂质元素分析中,金基体的分离采用液-液分配方式,溶剂为有机试剂,从萃取剂的成本、毒副作用以及选择性等多方面考虑,本实验室选择了乙酸乙酯作为萃取溶剂来分离金基体。实验证明,乙酸乙酯对金具有良好的选择性,而对于其它金属元素却基本不溶解,这正是我们所希望的结果。
3.2萃取酸度
萃取酸度是指萃取时水相的介质酸度。本实验中,萃取所用的酸为盐酸。对于部分杂质元素,当萃取酸度发生改变时,它们在两相中的分配比例将随之发生改变,只有在合适的酸度下,它们在有机相的溶解度才可以忽略不计。本实验考察了1 mol/L; 2 mol/和3 mol/L不同酸度下杂质元素在两相中的分配情况,结果以加入标准物质回收率为衡量指标。经实验发现,大部分杂质元素的加入标准
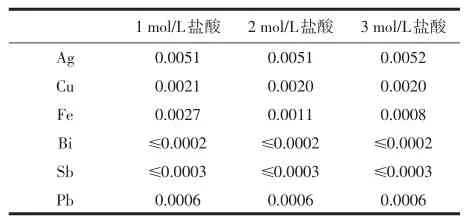
表3 不同盐酸浓度下的萃取结果
4 结论
在乙酸乙酯分离金基体后,利用ICP能够进行成品金锭中杂质含量的分析测试相比较原子吸收而言:结果更加精确,提高了实验室分析水平,缩短了工作时间、减小劳动强度、减少污染。
两种仪器的工作时间、最低检测值的比较见表4。
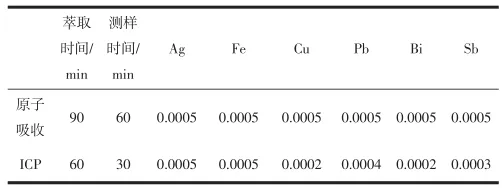
表4 两种仪器的工作时间、最低检测值的比较
参考文献
[1]陈永红,陈菲菲,黄蕊,等.乙酸乙酯萃取-ICP-AES测定高纯金中的痕量杂质[J].黄金,2009,30(7):54-57.
[2]国家质量监督检验检疫总局GB/T11066.7-2009金化学分析方法[S].北京:中国标准出版社,2009.
[3]长春国家金银质检中心GB/T11066.8-2009金化学分析方法.
[4]沈阳国家金银质检中心GB/T11066.8-2009金化学分析方法.
收稿:2015-01-26
DOI:10.16206/j.cnki.65-1136/tg.2015.02.027
