骨显像上颌骨额突浓聚灶随访及CT对照分析
2015-12-22SONGLe
宋 乐 SONG Le
袁慧书 YUAN Huishu
张卫方 ZHANG Weifang
张燕燕 ZHANG Yanyan
骨显像上颌骨额突浓聚灶随访及CT对照分析
宋 乐 SONG Le
袁慧书 YUAN Huishu
张卫方 ZHANG Weifang
张燕燕 ZHANG Yanyan
作者单位
北京大学第三医院核医学 北京 100191
目的 部分肿瘤患者骨显像发现上颌骨额突单发放射性浓聚灶,诊断困难,并且相关研究较少。本文旨在探讨骨显像上颌骨额突放射性浓聚灶的性质及原因,以提高对该病变的认识。资料与方法 选择上颌骨额突放射性浓聚但不伴其他骨转移瘤的21例患者,分析骨显像放射性浓聚灶的形态及分布,对比随访骨显像,观察病变有无变化,总结相应CT所见病变的部位、数目、大小、内部密度、边缘等形态学特点。结果 21例上颌骨额突浓聚灶累及单侧17例,双侧4例,1例伴其他颅骨病变。14例复查骨显像病变均未见变化,且未见新增病变。12例发现16个放射性浓聚灶,其中15个CT有异常表现,14个位于额突基底部鼻泪管周围。所有病变边界清楚,横截面最大径线平均7.1 mm。10个呈均匀磨玻璃密度,5个内部可见更低密度区。结论 骨显像上颌骨额突浓聚灶倾向良性病变,CT提示骨纤维异常增生症样病变为导致异常浓聚的原因之一。
上颌骨;体层摄影术,发射型计算机,单光子;体层摄影术,X线计算机;99m锝美罗酸盐;纤维发育不良,骨
在日常工作中,部分肿瘤患者骨显像发现上颌骨额突单发放射性浓聚灶,诊断较为困难。国内外仅见1篇关于上颌骨额突病变的CT研究报道[1],而骨显像的相关研究鲜有。本研究回顾性总结21例患者的骨显像资料,并与同期CT进行对照,分析上颌骨额突浓聚灶的原因及性质,以提高对该病变的认识。
1 资料与方法
1.1 研究对象 收集2010年5月—2013年11月北京大学第三医院骨显像发现上颌骨额突异常放射性浓聚且不伴有其他部位骨转移瘤的21例患者,其中男17例,女4例;年龄38~84岁,中位年龄65岁。恶性肿瘤20例,其中肺癌11例,前列腺癌4例,脊柱原发肿瘤2例,乳腺癌、膀胱癌、胸腺癌各1例;关节炎1例。14例患者于4~51个月(中位时间12个月)后复查全身骨显像。12例患者接受对照CT检查,其中颅脑CT 9例,鼻窦CT 2例,颈椎CT 1例。所有患者均无颌面部不适感,无颌面部肿瘤、外伤或手术史。
1.2 仪器与方法 患者静脉注射99Tcm-MDP(北京森科公司提供,放化纯度>95%)925 MBq,饮水500~1000 ml,4~6 h排尿后取仰卧位。采用Philips Skylight SPECT或GE millennium VG Hawkeye符合线路SPECT/CT,配备低能高分辨型准直器,能峰140 keV,窗宽20%,矩阵512×1024,步进式采集,每帧采集3 min,进行全身前、后位显像,总计数1000~2000 k。
1.3 图像分析 由2位核医学主治医师共同阅片,分析上颌骨额突放射性浓聚灶的形态、数目。对于骨显像随访患者,利用GE eNTEGRA后处理工作站调节对比度,使前后2次骨显像灰度及本底大致相同,对比上颌骨额突浓聚灶形态及放射性摄取程度有无变化,观察有无新增病变。在GE PACS系统中,采用CT骨窗观察上颌骨额突病变的部位、大小、数目、内部密度、边缘等形态学特点。
2 结果
2.1 骨显像表现 患者骨显像表现见表1。21例中,17例累及单侧上颌骨额突,其中12例累及右侧,5例累及左侧;4例累及双侧额突(图1~3)。1例合并其他颅骨放射性浓聚灶。所有病变均呈点状浓聚。14例骨显像随访,上颌骨额突浓聚灶形态及浓聚程度均无明显变化,全身骨未见新增病变。
2.2 CT表现 12例患者骨显像发现上颌骨额突放射性浓聚灶16个,其中15个对应CT有异常表现,见表1。病变均呈膨胀性改变,边界清楚。横断面病变呈类圆形11例,不规则形4例。10例呈均匀性磨玻璃密度(图1B、2B),5例密度不均匀,边缘为磨玻璃密度,内部伴更低密度区(图3B)。病变最大横截面径线约4.7~12.9 mm,平均(7.1±2.3)mm。14例病变位于上颌骨额突基底部鼻泪管周围,1例位于额突头端(图2)。4例患者分别于5、6、11、25个月后复查颅脑CT,所有病变均未见变化。1例患者2次骨显像均发现右侧上颌骨额突轻度放射性浓聚灶,而相应2次颅脑CT均未见明显异常(图3)。
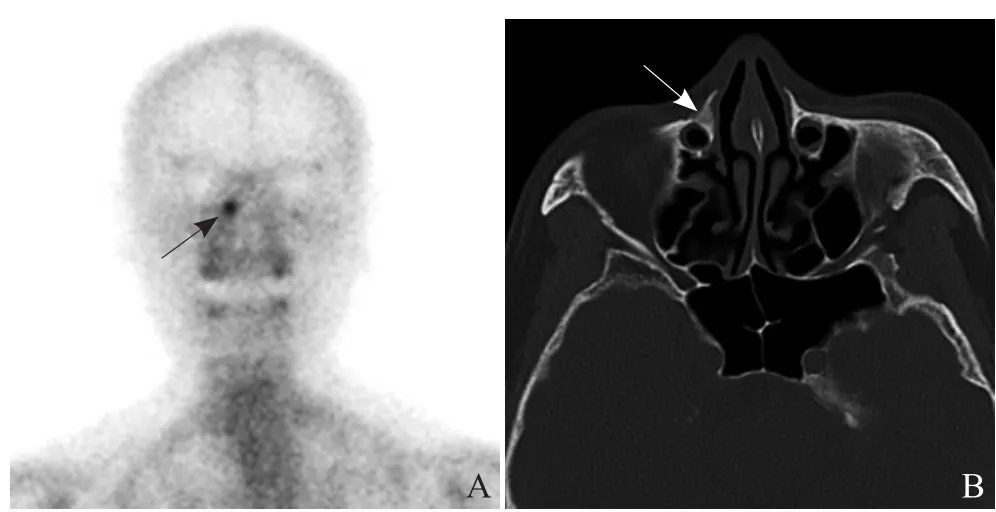
图1 男,80岁,前列腺癌。骨显像示右侧上颌骨额突放射性浓聚灶(箭,A);横断面CT图像示病变位于鼻泪管前方,呈均匀磨玻璃密度,边界清楚,轻度膨胀(箭,B)
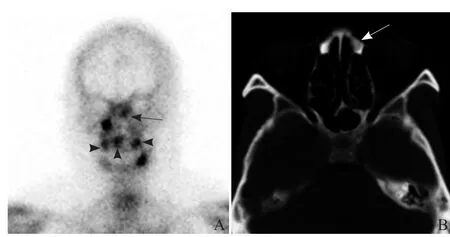
图2 男,76岁,肺癌。骨显像示双侧上颌骨额突放射性浓聚灶,左侧较小(箭),上颌骨牙槽突多发放射性浓聚灶为牙病所致(箭头,A);横断面CT图像示左侧病变位于额突头端,呈均匀磨玻璃密度(箭,B)
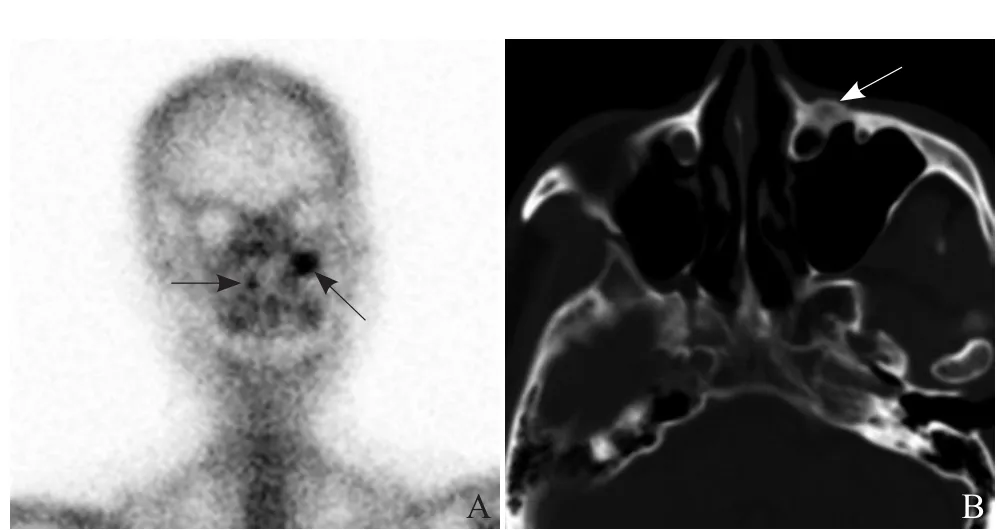
图3 男,59岁,肺癌。骨显像示双侧上颌骨额突放射性浓聚灶(箭,A);横断面CT图像示左侧病变位于鼻泪管前方,边缘呈磨玻璃密度,内部见低密度影(箭,B)
3 讨论
3.1 上颌骨额突解剖及骨显像表现 上颌骨额突形态不规则,连接额骨、筛骨、泪骨,是鼻泪管及泪囊的骨性构成部分。前位骨显像该结构位于鼻腔两侧,其外上为眼眶,外下为上颌窦,内上为筛窦,内下为鼻腔。骨显像上颌骨额突呈轻度均匀性放射性摄取,双侧对称,略高于周围眼眶、鼻窦及鼻腔内放射性。如果局部放射性摄取增高,则为异常,其机制尚不明确。本研究通过对照12例患者的骨显像及CT图像,发现15个上颌骨额突放射性浓聚灶CT呈典型的骨纤维异常增殖症样表现,该病变在日常工作中并不少见。Yang等[1]回顾性分析了1000例患者的鼻窦CT图像,发现上颌骨额突骨纤样病变发病率约为5.1%。

表1 21例患者上颌骨额突病变骨显像与CT表现
3.2 上颌骨额突骨纤维异常增殖症的CT征象及骨显像的应用价值 上颌骨额突骨纤维异常增殖症大部分累及基底部鼻泪管周围,少数位于头端。病变均呈膨胀性改变,大多累及单侧,呈类圆形。病变大多呈均匀磨玻璃密度,少数密度欠均匀,内部见溶骨性改变,周围包绕磨玻璃密度,类似“蛋壳样”表现。当病变以骨组织为主时,密度明显增高,呈畸形性骨炎型或硬化型改变[1],本组未见该型表现。上颌骨额突骨纤体积较小,本组最大平均径线约(7.1±2.3)mm,既往报道为9.8 mm[1]。本组患者中位年龄65岁,男性居多,而骨纤维异常增殖症好发于青少年,女性患者略多[2]。造成该差异的原因与本组大多为肿瘤患者、且均为骨显像偶然发现有关。这进一步说明骨显像能够早期发现较小的无症状性隐匿性病变[3-4],因而可以用于探测多骨病变。20%~30%的骨纤维异常增殖症患者累及多骨,而本组仅1例患者伴有额骨放射性浓聚灶。骨纤维异常增殖症摄取亲骨显像剂的机制尚不明晰,可能与病变内富含胶原成分以及不成熟编织骨组织表面积相对丰富有关[5-7]。由于纤维组织与编织骨构成比例不同,病变对骨显像剂摄取程度亦有所区别,因而骨显像能够反映病变的发展状态,从而用于病变随访[8]。本组14例患者平均12个月后复查骨显像,病变均未见明显变化,提示该病变处于良性稳定状态。在后续研究中,本课题组将对病变放射性计数进行前后对比,取得定量结果,以弥补本研究主观判断的不足。颌面部骨纤维异常增殖症若导致畸形或功能障碍,常常需要积极治疗。Makitie等[9]使用双磷酸盐治疗该病取得了满意的效果。骨显像不仅可以判断疗效,还能够早期发现双磷酸盐药物治疗的颌骨坏死等严重并发症[10-11]。
本组4例患者累及双侧上颌骨额突,而Yang等[1]报道的51例患者均为单发。此外,本组1例上颌骨浓聚灶CT未见明显异常,提示骨显像有助于发现更多较小、甚至CT呈等密度的病变,与Nakahara等[12]的研究报道一致。然而,部分骨纤维异常增殖症可无明显放射性浓聚,可能与病变逐渐骨化成熟导致骨代谢减低或出现骨梗死有关[13-14]。此外,该病偶尔可以发生出血或囊变,甚至合并动脉瘤样骨囊肿,导致骨显像呈放射性减低或缺损。通过对照分析CT征象或许有助于分析该病不摄取骨显像剂的原因,而本组未见CT异常、骨显像阴性病例。
总之,对于骨显像偶然发现的上颌骨额突放射性浓聚灶,首先应考虑良性,骨纤维异常增殖症可能是造成放射性摄取的原因之一。本文利用平面骨显像与异机CT图像对上颌骨额突病变进行主观识别及定位存在一定的困难,可能会有偏差。今后将利用SPECT/ CT同机断层融合显像,对病变精确定位[15-16],深入分析上颌骨额突病变放射性摄取与CT征象的关系。
[1] Yang BT, Wang YZ, Wang XY, et al. Fibrous dysplasialike appearance of the frontal process of the maxilla on CT: prevalence in North China. Am J Neuroradiol, 2011, 32(3): 471-473.
[2] Nguyen BD, Lugo-Olivieri CH, Mccarthy EF, et al. Fibrous dysplasia with secondary aneurysmal bone cyst. Skeletal Radiol, 1996, 25(1): 88-91.
[3] Suman Kc S, Sharma P, Singh H, et al. Fibrous dysplasia mimicking bone metastasis on both bone scintigraphy and (18) F-FDG PET-CT: diagnostic dilemma in a patient with breast cancer. Nucl Med Mol Imaging, 2012, 46(4): 318-319.
[4] Wang K, Allen L, Fung E, et al. Bone scintigraphy in common tumors with osteolytic components. Clin Nucl Med, 2005, 30(10): 655-671.
[5] Singnurkar A, Rush C. The "pirate sign" in fibrous dysplasia. Clin Nucl Med, 2006, 31(11): 727-728.
[6] Zhibin Y, Quanyong L, Libo C, et al. The role of radionuclidebone scintigraphy in fibrous dysplasia of bone. Clin Nucl Med, 2004, 29(3): 177-180.
[7] Kransdorf MJ, Moser RP Jr, Gilkey FW, et al. Fibrous dysplasia. Radiographics, 1990, 10(3): 519-537.
[8] Fujii M, Kosuda S, Jitsu M, et al. Long-term follow-up of a patient with McCune-Albright syndrome by whole-body bone scan and SPECT. Clin Nucl Med, 2004, 29(11): 712.
[9] Makitie AA, Törnwall J, Makitie O. Bisphosphonate treatment in craniofacial fibrous dysplasia-a case report and review of the literature. Clin Rheumatol, 2008, 27(6): 809-812.
[10] Hong CM, Ahn BC, Choi SY, et al. Implications of three-phase bone scintigraphy for the diagnosis of bisphosphonate-related osteonecrosis of the jaw. Nucl Med Mol Imaging, 2012, 46(3): 162-168.
[11] Joshi JK, Kushner GM, Bhatt G, et al. Role of nuclear medicine imaging in recognizing different causes of osteonecrosis of the jaw. Clin Nucl Med, 2013, 38(1): 40-43.
[12] Nakahara T, Fujii H, Hashimoto J, et al. Use of bone SPECT in the evaluation of fibrous dysplasia of the skull. Clin Nucl Med, 2004, 29(9): 554-559.
[13] Sood A, Raman R, Jhobta A, et al. Normal technetium-99m-MDP uptake in fibrous dysplasia of the hip. Hell J Nucl Med, 2009, 12(1): 72-73.
[14] Han J, Ryu JS, Shin MJ, et al. Fibrous dysplasia with barely increased uptake on bone scan: a case report. Clin Nucl Med, 2000, 25(10): 785-788.
[15] 赵峰, 王莹, 赵倩, 等. SPECT/CT断层融合显像对多发性骨髓瘤的诊断价值. 中国医学影像学杂志, 2012, 20(4): 303-305.
[16] 蔡自强, 闫培华, 郝培来, 等. MR全身扩散加权成像与SPECT骨显像对恶性肿瘤骨转移灶检出的对比研究. 中国医学影像学杂志, 2012, 20(12): 932-935.
(本文编辑冯婕)
Maxillary Frontal Process Radionuclide Uptake on Bone Scan: A Follow-up and Comparison with CT Findings
Purpose The increased radionuclide uptake of maxillary frontal process on bone scan is not uncommon but difficult to diagnose with relatively rare research. This study aims to explore this phenomenon through investigating its biological behavior and causes. Materials and Methods Twenty-one patients with increased uptake of maxillary frontal process but without typical feature of metastasis on bone scan were retrospectively enrolled in the study. The scintigraphic features were evaluated and compared with the bone scans in the follow up. The corresponding CT imaging features including the lesions'location, number, size, shape and attenuation were analyzed. Results Seventeen patients had unilateral involvement and 4 had bilateral ones. One patient was found accompanied with other cranial lesions. All the lesions remained stable and no new lesions were detected on the following bone scans in 14 patients. Sixteen lesions with increased radionuclide uptake in 12 patients were detected on bone scintigraphy, 15 of which were positive on CT and 14 of which were located around the nasolacrimal canal at the base of frontal process. All the lesions were well demarcated with mean axial maximum diameter of 7.1 mm. Ten had homogeneous ground-glass density and 5 showed heterogeneous with internal lower attenuation. Conclusion Lesions of maxillary frontal process with increased radionuclide uptake detected on bone scan are likely to be benign. Fibrous dysplasia-like lesions might help account for abnormal uptake indicated by CT.
Maxilla; Tomography, emission-computed, single-photon; Tomography, X-ray computed; Technetium Tc 99m medronate; Fibrous dysplasia of bone
10.3969/j.issn.1005-5185.2015.07.002
张卫方
Department of Nuclear Medicine, Peking
University Third Hospital, Beijing 100191, China
Address Correspondence to: ZHANG Weifang
E-mail: tsy1997@126.com
R445.3;R739.82
2015-01-10
2015-06-29
中国医学影像学杂志
2015年 第23卷 7期:486-488,493
Chinese Journal of Medical Imaging
2015 Volume 23(7): 486-488, 493
