荷叶黄酮的提取和纯化工艺研究
2015-12-18蔡敏李长春毕宏光唐正宇方翔
蔡敏 李长春 毕宏光 唐正宇 方翔

摘要:研究孝感本地生长的荷叶,通过超声波辅助乙醇提取法,获得荷叶黄酮的粗提物,再采用HPD-450、HPD-600、HPD-826 3种不同大孔吸附树脂进行分离纯化,通过静态吸附-解吸试验对3种树脂的纯化工艺进行选择。结果表明,在pH 6.5,温度30 ℃,转速180 r/min的恒温振荡器中,HPD-450的吸附量为95 mg/g、吸附率为39.38%、解吸率为50%,HPD-600的吸附量为98 mg/g、吸附率为40.66%、解吸率为70%,HPD-826的吸附量为112 mg/g、吸附率为46.89%、解吸率为56%。综合考虑HPD-826型大孔树脂对荷叶黄酮纯化效果最佳,适用于精制荷叶黄酮。
关键词:荷叶;黄酮;大孔树脂;纯化
中图分类号:S682.32;R284.2 文献标识码:A 文章编号:0439-8114(2015)22-5691-03
Abstract: The lotus leaf of Xiaogan local growth was studied. The total lotus leaf flavonoids were obtained by ethanol ultrasonic assisted extraction. Three different macro porous absorption resin of HPD-450, HPD-600 and HPD-826 were used to separate and purify the flavonoids. Three kinds of resin purification process were optimized by static adsorption-desorption experiment. The result showed that the adsorption quantity of three kinds of resin were 95 mg/g, 98 mg/g, 112 mg/g, the adsorption rate were 39.38%, 40.66%, 46.89% and the desorption rate were 50%, 70%, 56% for HPD-600, HPD-450 and HPD-826 respectively under the conditions of pH 6.5, temperature 30 ℃, thermostatic oscillator in the speed of 180 r/min. The effects of temperature and the pH on dynamic adsorption were discussed. Therefore, macroporous resin of HPD-826 was suitable to refine lotus leaf flavonoids.
Key words: lotus leaf; flavonoids; macroporous absorption resin; extraction and purification
荷叶为睡莲科(Nymphaeaceae)水生植物,资源丰富,主要分布在湖北、湖南、安徽、江西、福建、江苏、山东等省份。荷叶的化学成分十分复杂,至今已从荷叶中分离出生物碱、黄酮类化合物等多种主要化学成分[1,2]。研究表明,荷叶中含有以槲皮素为主要成分的黄酮类物质,且含量丰富[3]。张贇彬等[4]从荷叶中分离出山萘酚和槲皮素-3-丙酯。Elegami等[5]从荷叶中分离出了Myricetin-3-(6-p-coumaroyl)-glucoside,Nympholide A和Nympholide B等黄酮类物质。延玺等[6]通过研究发现黄酮类化合物具有多种生理功能和抵抗疾病的作用。
通过研究孝感本地生长的荷叶,在试验室条件下对荷叶黄酮类粗提物提取工艺研究的基础上,使用大孔吸附树脂HPD-450、HPD-600、HPD-826对荷叶黄酮类粗提物的分离纯化效果优化,采用静态吸附—解吸试验和动态吸附—解吸试验相结合的研究方法,获得静态吸附曲线、吸附率和解吸率,通过比较3种树脂的各种参数,选出适当的树脂对荷叶黄酮进行分离纯化[7,8]。并且在此基础上探讨了pH、乙醇体积分数、恒温振荡器的温度、转速对大孔吸附树脂吸附率和解吸率的影响[9,10]。
1 材料与方法
1.1 试验材料
新鲜荷叶分别于7月、8月和9月采集于孝感后湖公园中本土生长的荷叶品种。将采集的荷叶用电热鼓风干燥箱在70 ℃下烘8 h,中草药粉碎机粉碎,用60目筛子重复筛选3次得到荷叶粉末,装袋密封,放置冰箱内,备用[11]。
1.2 试剂与设备
试剂:芦丁标准品(贵州迪大科技有限公司);大孔吸附树脂(沧州宝恩吸附材料科技有限公司);无水乙醇、NaNO2、Al(NO3)3、NaOH 均为分析纯。
设备:中草药粉碎机(天津市泰斯特有限公司);电热鼓风干燥箱(上海福玛实验设备有限公司);电子天平(赛多利斯科学仪器有限公司);DL-480B型超声波清洗器(上海之信仪器有限公司);DT5-2型低速台式离心机(北京时代利离心机有限公司);SHZ-III型循环水真空泵(上海亚荣生化仪器厂);ZHWY-211B型恒温振荡器(上海智城分析仪器制造有限公司);UV-5200型紫外可见分光光度计(上海元析儀器有限公司);FE20型pH计(上海梅特勒-托利多仪器有限公司);TBD-2000型中压层析制备系统(SHANGHAI TAUTO BIOTECH CO.,LTD.);Φ5.0×40型层析柱(上海沪西分析仪器厂有限公司)。
1.3 试验方法
1.3.1 芦丁标准曲线的制定 称取10 mg芦丁标准品,用30%乙醇标定在50 mL容量瓶中,配成浓度为0.200 mg/mL的芦丁溶液,再分别取0、1、2、3、4、5 mL于25 mL的容量瓶中,在每个容量瓶中加入1 mL 5%的NaNO2振荡6 min后加入l mL 5% Al(NO3)3,振荡5 min,再加入10 mL 10%的NaOH,定容到刻度线,以空白试剂为参比液,于510 nm处测其吸光度,以吸光度A为纵坐标,浓度C为横坐标绘制标准曲线(图1)。
1.3.2 正交试验设计 以影响荷叶黄酮提取率的乙醇体积分数、料液比(g∶mL,下同)、提取时间和提取温度为4个影响因素,取各自的3个水平进行正交试验,试验的因素与水平见表1。
1.3.3 大孔吸附树脂静态吸附试验 主要采用HPD-450、HPD-600、HPD-826 3种树脂进行静态吸附和解吸试验,3种树脂均为白色不透明球状颗粒,它们的性能指标见表2。用电子天平准确称取已经预处理好的3种树脂各1 g,分别放入3个干净的150 mL的具塞锥形瓶,取荷叶黄酮提取液70 mL于烧杯,再准确量取60%乙醇140 mL加入烧杯,在每个150 mL的锥形瓶中加入稀释后的提取液40 mL(测得pH为6.5),在不改变提取液pH的条件下,放入恒温振荡器中(30 ℃,180 r/min)静态吸附,然后每间隔1 h测定锥形瓶上清液中黄酮的浓度。方法如下:分别用3个移液管,在每个移液管贴上标签,准确量取锥形瓶上清液1 mL于3个25 mL的小烧杯,测定方法同标准曲线。测定得到其吸光度,带入回归方程公式即可得到锥形瓶中上清液黄酮的浓度。
按照下列算式计算出各种树脂的静态吸附量(mg/g):
上式中,Q是静态吸附量(mg/g);C是初始浓度(mg/mL);Cv是剩余浓度(mg/mL);V是溶液体积(mL);W是树脂质量(g)。
假设吸附前与后提取液体积无变化,可按下列算式计算出树脂的静态吸附率:
1.3.4 大孔吸附树脂静态解吸试验 待静态吸附达到平衡状态后,取出上述吸附饱和的3种大孔树脂过滤,滤纸吸收树脂表面的残留溶液,然后放回锥形瓶,加入60%乙醇50 mL,置于恒温振荡器中(30 ℃,180 r/min)静态解吸,每隔1 h收集一次上清液测定黄酮的浓度。
2 结果与分析
2.1 荷叶黄酮提取工艺结果
正交试验优化荷叶黄酮试验结果见表3。由表3可知,荷叶中黄酮提取的最佳试验条件为B1A2C1D3,即料液比l∶20,60%乙醇,60 ℃,提取4 h。按照上述获得的荷叶黄酮提取条件,将7、8、9月采集于孝感后湖公园本土生长的荷叶样品分别进行浸提,通过紫外可见分光光度计检测,吸光度代入芦丁标准曲线线性回归方程可得,7、8、9月荷叶样品黄酮含量分别为7.84、7.92、7.87 mg/g,平均含量为7.88 mg/g,此时黄酮得率为0.788%。
2.2 大孔吸附树脂静态吸附结果
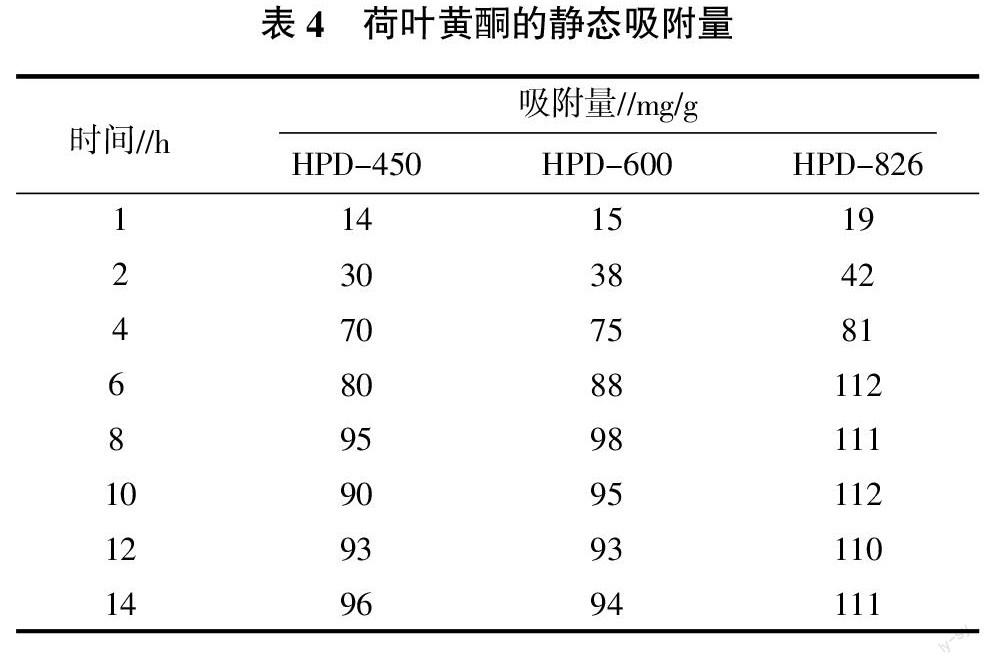
3种大孔树脂静态吸附在每个时间段的静态吸附量见表4。运用Excel软件绘制出3种树脂的静态吸附动力学曲线见图2。由表4和图2可知,HPD-826型大孔吸附树脂在6 h左右吸附量就可以达到最大值112 mg/g,而HPD-450和HPD-600需在8 h左右达到饱和吸附量,分别为95、98 mg/g。在相同分离纯化条件下HPD-826型大孔吸附树脂达到平衡的时间相对短,吸附量较大,吸附率较高。
2.3 大孔吸附树脂静态解吸结果
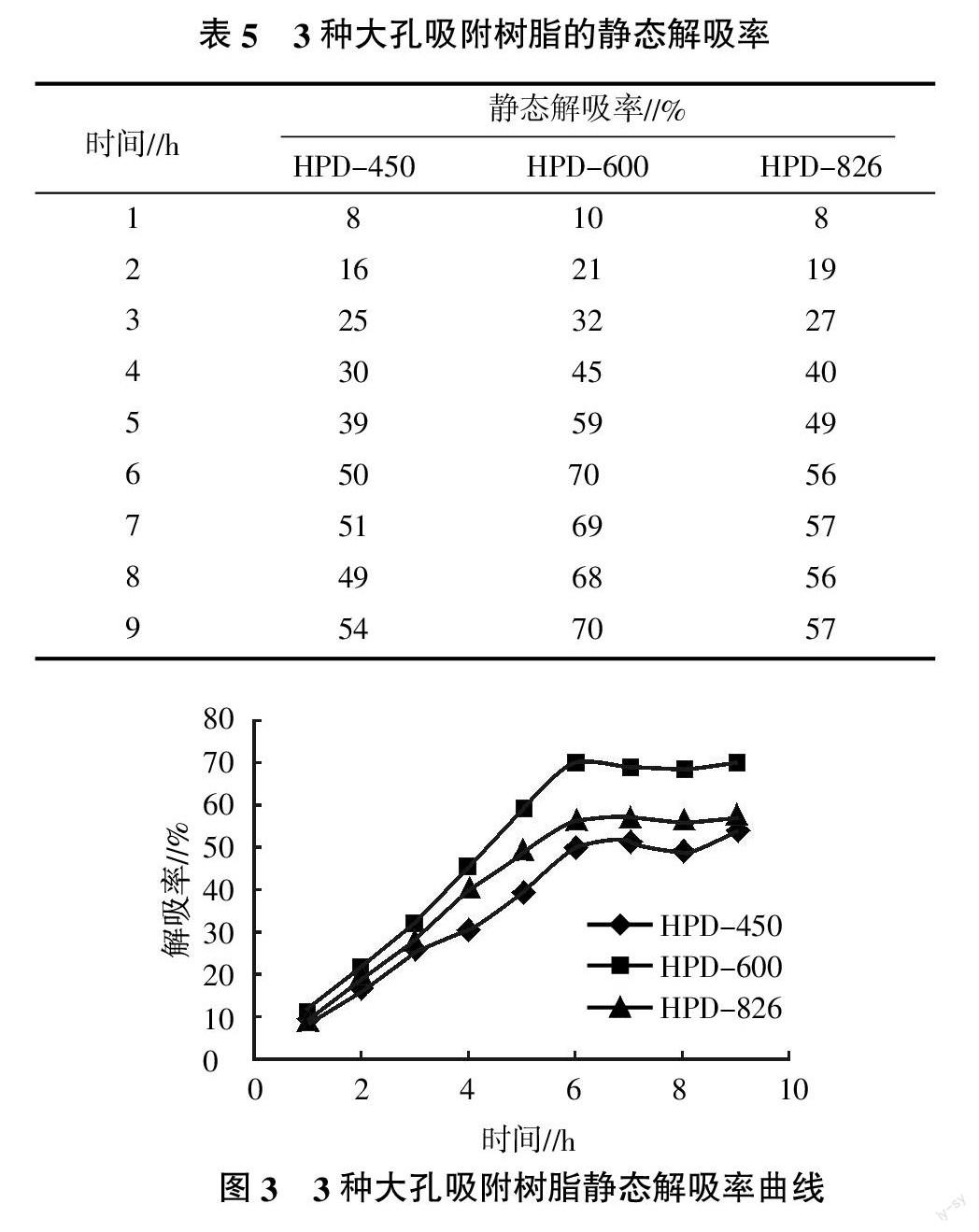
恒温振荡器中30 ℃,180 r/min静态解吸,每隔1 h收集一次上清液测定黄酮的浓度,3种大孔树脂在每个时间段的静态解吸率见表5。运用Excel软件绘出3种树脂的静态解吸率曲线见图3。由表5和图3可知,3种树脂的解吸平衡时间都在6 h左右,HPD-450、HPD-600和HPD-826型大孔吸附树脂的解吸率分别是50%、70%和56%。
3 小结与讨论
本研究首先通过正交优化试验,确定超声波辅助乙醇提取的最佳试验条件为料液比l∶20,60%乙醇,温度60 ℃,提取4 h。将处于生长期的荷叶样品分别进行浸提,通过紫外可见分光光度计检测,7、8、9月荷叶样品黄酮含量分别为7.84、7.92、7.87 mg/g,平均含量为7.88 mg/g,此时黄酮得率为0.788%。
采用HPD-450、HPD-600、HPD-826 3种大孔吸附树脂进行静态吸附-解吸试验,分析吸附量、吸附率和解吸率,结果表明,3种大孔吸附树脂的吸附量和吸附率HPD-826>HPD-600>HPD-450,解吸率HPD-600>HPD-826>HPD-450。综合3种大孔吸附树脂的性能指标,HPD-826的吸附量最高,吸附平衡时间最短,而且解吸率适中,因此选取HPD-826型大孔吸附树脂对荷叶黄酮纯化精制。
对HPD-826型大孔树脂动态吸附-解吸试验过程发现,上清液的pH和温度变化会影响荷叶黄酮与树脂之间的吸附和解吸能力,大孔树脂的吸附性随着pH的增加先变大后减小,随着温度的增加变大。
参考文献:
[1] 杨冀艳,胡 磊,许 杨.荷叶黄酮类化合物的研究进展[J].食品科学,2007,28(8):554-558.
[2] 许金蓉.荷叶黄酮提取工艺及抗氧性研究[J].轻工科技,2014, 31(10):15-18.
[3] 赵昕岚,邓放明.荷叶中总黄酮和荷叶碱含量变化规律[J].食品与机械,2013,29(2):37-40.
[4] 张贇彬,戴妙妙,李彩侠.荷叶中黄酮类化合物的化学结构鉴定[J].食品研究与开发,2006,27(6):45.
[5] ELEGAMI A A ,BATESC G,GRYAI H,et al. Two very unusual macrocylic flavonoids from water lilynymohaca lotus[J].Phytochemistry,2003,63(6):731.
[6] 延 玺,刘会青,邹永青,等. 黄酮类化合物生理活性及合成研究进展[J].有机化学,2008,28(9):1534-1544.
[7] 于智峰, 王 敏.大孔吸附树酯在黄酮类化合物分离中的应用[J].中药材,2006,29(12):1380-1382.
[8] 刘 云,刘良燚,朱欣婷.D140型大孔树脂纯化荷叶总黄酮的研究[J].安徽农业科学,2009,37(32):16163-16164.
[9] 黄阿根,董瑞建,韦 红,等.大孔树脂对荷叶黄酮的分离纯化[J].现代食品科技,2008,24(12):1202-1206.
[10] 张 蕾,李梅香,吴秀玲,等.AB-8樹脂分离纯化荷叶总黄酮的研究[J].食品研究与开发,2014,35(10):42-45.
[11] 高 丽,王燕龙,熊云景,等.HPD-100大孔树脂分离纯化荷叶黄酮的研究[J].中国酿造,2012,31(8):127-129.
(责任编辑 龙小玲)
