氨基化MCM-41介孔分子筛改性超滤膜去除水中Cr(VI)的研究
2015-12-14包一翔谢小妮周佳璐晏晓敏李来胜
包一翔,谢小妮,周佳璐,晏晓敏* ,李来胜
(1. 华南师范大学化学与环境学院,广州510006;2. 广州大学土木工程学院,广州510006)
去除污水中的重金属铬对保护环境和人类健康都具有重大意义[1].吸附是去除水中重金属行之有效且经济的方法.各种天然矿物[2-3],人工合成硅基分子筛[4-5]等均被成功应用于吸附水中的重金属甚至有机污染物.但是,吸附剂的回收是亟待解决的问题.负载型或固定型吸附材料可在一定程度上实现吸附剂的回收利用.
超滤膜技术具有很好的分离效果,但由于超滤膜孔径在2 ~50 nm,远大于一般重金属离子的大小,直接使用超滤膜去除重金属受到限制.膜吸附是将吸附与膜分离相结合,具有去除率高、处理能力强、吸附速度快、可重复使用的特点[6]. 将膜吸附和膜分离有机结合,可强化超滤过程对水质的净化效果.已有较多研究致力于吸附膜材料的制备及其应用. Salehid 等[7]通过氨基改性多壁碳纳米管/壳聚糖/聚乙烯醇杂化膜,处理水中的Cu(II)取得了良好的效果;利用水合锰氧化物制备PES/HMO 混合基超滤膜,提高超滤膜对Pb(II)的吸附能力,超滤出水Pb(II)的质量浓度低于15 μg/L[8].
氨基改性的MCM-41(NH2-MCM-41)作为吸附剂可有效去除水中Ni (II)、Cd (II)、Pb (II)和Cr(VI)等重金属[4-5]. 本研究制备了氨基化改性MCM-41,并通过界面聚合方法将其接枝于复合PVDF 超滤膜表面,旨在提升超滤膜抗污染能力和提高其对重金属Cr(VI)的去除能力.
1 材料与方法
1.1 实验材料
聚偏氟乙烯(PVDF)购于美国苏威;间苯二胺(MPD)、均苯三甲酰氯(TMC)、氨丙基三乙氧基硅烷(APTS,98%)购于阿拉丁;铬标准溶液(1 000 mg/L)购于国家有色金属及电子材料分析测试中心.其他试剂均为分析纯.
1.2 NH2-MCM-41 分子筛的制备
通过水热法合成MCM-41 介孔分子筛[9],将一定量的Na2SiO3·9H2O 溶于去离子水中,35 ℃搅拌10 min,用稀硫酸调节pH 至11 后搅拌30 min,加入溶解好的CTAB,搅拌30 min.将所得溶液在145 ℃晶化48 h,冷却后洗涤至中性,烘干,550 ℃下煅烧3 h 得到MCM-41 介孔分子筛. 将所得分子筛研磨后,与一定量APTS 在正己烷中回流6 h,洗涤,干燥得到NH2-MCM-41[10].
1.3 复合超滤膜的制备
将16 g PVDF 和2 g PVP(聚乙烯吡咯烷酮)加热搅拌溶解于100 mL DMAc(二甲基乙酰胺)中,得到透明的铸膜液,脱泡,用刮膜刀将铸膜液刮制于洁净玻璃板上,迅速放入去离子水的凝固浴中,使其固化成膜(PVDF),保存于去离子水中待用. 将所得滤膜依次浸泡于高锰酸钾(w 为4%)和亚硫酸氢钠(w为2%)各30 min,脱去滤膜表面部分F 原子,用去离子水冲洗干净.然后进行界面聚合改性,将PVDF滤膜浸泡于w(MPD)为2%水溶液中3 min,将其取出,再浸入w(TMC)为0.15% 的正己烷溶液中2 min,得到复合超滤膜(c-PVDF). 最后将其置入w(NH2-MCM-41)为0.3%的正己烷中接枝2 min,得到氨基化MCM-41 改性复合PVDF 超滤膜(g-PVDF),取出80 ℃烘干后备用.
1.4 复合超滤膜的表征
样品喷金处理,用场发射扫描电镜(SEM,ZEISS Ultra 55)对样品表面形貌进行观测. 用接触角仪(SL200B,Kino,USA)测定膜表面纯水的接触角,测量10 次后取平均值.用衰减全反射-傅里叶变换红外光谱仪(Nicolet 6700)表征材料表面官能团变化,扫描范围600 ~4 000 cm-1,分辨率为0.4 cm-1.
1.5 复合超滤膜抗污染性能测试
超滤实验装置如图1 所示,采用氮气提供推动力,电子天平实时记录单位时间内透过膜的水量,按照下式计算超滤膜的纯水通量(J):
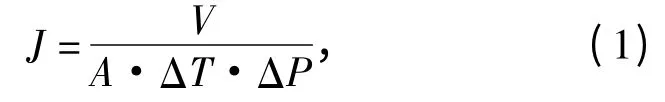
其中,V 为透水量的体积(L),A 为膜的有效面积(m2),ΔT 为取样时间(h),ΔP 为跨膜压力(bar),超滤杯(MSC 300,Mosu,Shanghai)的有效面积A 为50.24 cm2.
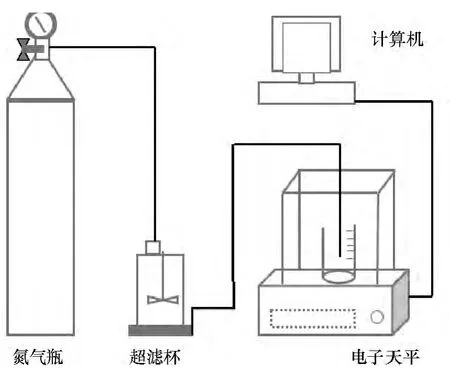
图1 实验装置示意图Figure 1 Schematic of ultrafiltration device
采用腐殖酸(humic acid,10 mg/L)模拟废水中的残余有机物.为了表征截留腐殖酸过程中超滤膜通量衰减情况,定义通量衰减率(η)为某时刻通量减小量(J0-Jt)与初始通量(J0)的比值,按照下式

计算得出.
1.6 复合超滤膜对去除铬的作用
用重铬酸钾配制成2 000 mg/L 的Cr(VI)储备液.溶液pH 用0.1 mol/L 的HCl 或NaOH 调节. 超滤膜对Cr 的吸附试验在25 ℃、转速130 r/min 的条件下进行.称取0.1 g 干燥后的超滤膜置于100 mL含一定铬质量浓度溶液中,按一定时间间隔取样,上清液铬离子质量浓度用岛津AA7000 原子吸收仪测定.膜材料对重金属吸附容量根据下式计算得出:其中c0、ce分别为溶液中铬离子的初始质量浓度和吸附平衡时的质量浓度.
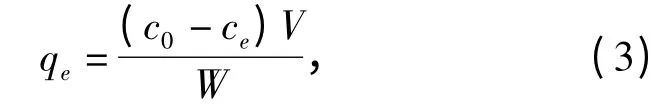
超滤去除铬在超滤杯中进行,将调节好pH 的含铬溶液装入超滤杯中,在0.5 bar 的压力下使进水通过膜,按一定时间间隔取样,测定滤液中铬离子质量浓度.
2 结果与讨论
2.1 膜材料的表征与分析
3 种膜均在1 100 cm-1和1 400 cm-1处有强烈吸收峰(图2),对应PVDF 材料的—CF2键;1 660 cm-1附近出现的新峰代表酰胺基团中的CO 键,1 547 cm-1附近的吸收峰来自N—H 键面内振动和C—N 振动吸收,1 610 cm-1处的吸收峰代表氨基的N—H 振动吸收.这些新的吸收峰都归于PVDF 膜表面聚酰胺超薄层[11-12].1 040 ~1 080 cm-1之间的宽吸收峰源于分子筛的Si—O—Si 和Si—OH 键(如图中虚线标注所示),属于NH2-MCM-41 分子筛的1 541.1 cm-1处的氨基吸收峰与酰胺键的1 547 cm-1处吸收峰重合[13].接枝于g-PVDF 上的分子筛对膜表面性质有显著的改变.
与PVDF 原膜(图3A)对比,界面聚合过程使c-PVDF 膜表面形成一层聚酰胺薄膜(图3B),NH2-MCM-41 成功接枝于g-PVDF 膜表面(图3C). 对比接触角照片,未改性的PVDF 膜具有较强的疏水性,其接触角达到了73°(图3D);表面具有聚酰胺薄层c-PVDF 膜,其接触角达到了80°(图3E),同样具有较强的疏水性;而表面具有NH2-MCM-41 分子筛的g-PVDF,其接触角下降到了13°(图3F).g-PVDF 膜亲水性显著提高的原因是分子筛上的NH2-和Si-OH基团和水分子之间具有较强的亲和性,同时膜表面的介孔分子筛薄层提高了膜表面的粗糙度,增大了膜与水的接触面积,有利于进一步降低亲水性表面接触角.
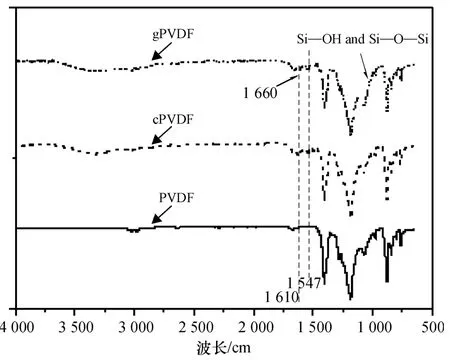
图2 PVDF、c-PVDF 和g-PVDF 膜的红外谱图Figure 2 ATR-FTIR spectra of PVDF,c-PVDF and g-PVDF

图3 PVDF、c-PVDF 和g-PVDF 膜的扫描电镜图(A、B 和C)及接触角(D、E 和F)Figure 3 SEM photographs (A,B and C)and contact angle (D,E and F)of PVDF,c-PVDF and g-PVDF membranes
2.2 膜的抗污染性能
超滤膜应用过程中,膜的抗污染性是重要性能之一,而水体有机质是影响膜污染物的重要因素.从对模拟有机物水样超滤过程中水通量衰减可以看出,超滤1 h 后,PVDF 膜通量衰减最为严重,衰减率达到了51.4%,c-PVDF 为31.5%,而g-PVDF 只有24.8%(图4). 这表明膜表面接枝层的NH2-MCM-41 可以有效阻止腐殖酸分子进入并吸附于膜孔道,从而有效减少腐殖酸导致的膜污染,进而降低通量衰减速率.更重要的是,由于g-PVDF 膜表面的NH2-具有很好的亲水性,如前所述,接触角大大降低,更有利于水透过膜材料,g-PVDF 膜的初始通量为58.4 L/(m2·h·bar),达到c-PVDF 膜初始通量(22.5 L/(m2·h·bar))的2.6 倍.因此,通过NH2-MCM-41 改性PVDF 膜,极大地提高了膜的过水通量和抗污染物性.
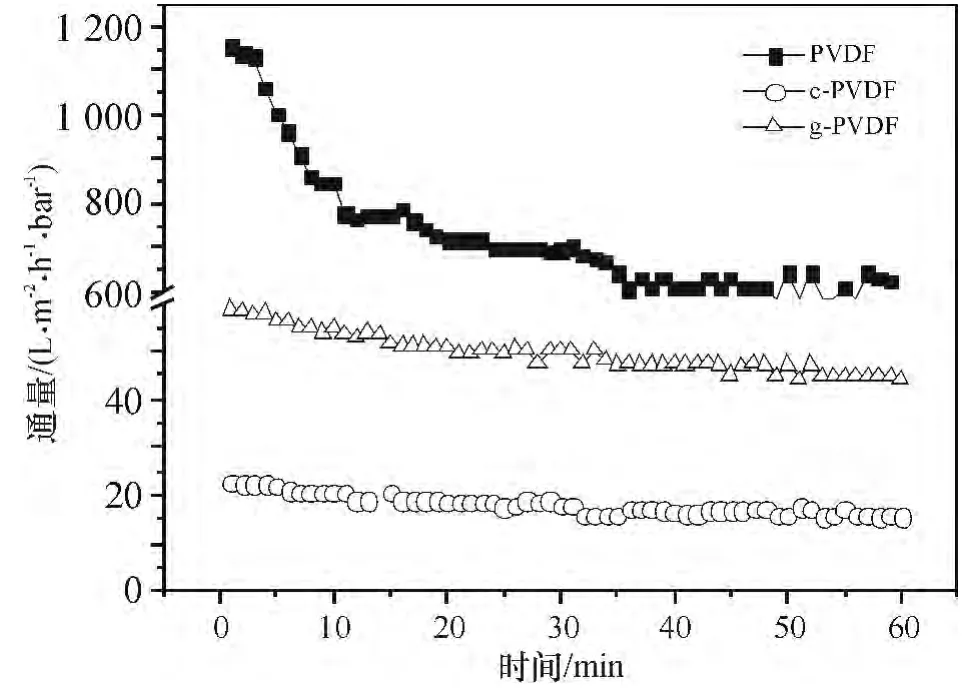
图4 PVDF、c-PVDF、g-PVDF 膜通量衰减曲线Figure 4 Flux decline as function of time during filtration of NOM model water of PVDF,c-PVDF and g-PVDF
2.3 重金属铬的超滤去除
六价铬在水中主要有H2CrO4、或几种形式,在pH 中性及弱酸性下,多以和为主[14]. 在预实验中,发现在pH 3 ~4 之间时,改性超滤膜对Cr 的吸附性能最好.酸性条件下,膜对Cr(VI)的吸附能力源于质子化的氨基基团(NH+3-)和水中以阴离子形式存在的Cr(VI)离子之间的作用力. 从吸附动力学上,g-PVDF 对Cr(VI)的吸附在5 min 就能达到平衡(图5),最大吸附容量达到2.8 mg/g,而c-PVDF 膜对Cr(VI)几乎没有吸附能力.与已报道的很多吸附膜材料相比,g-PVDF 膜具有明显的优势(表1).
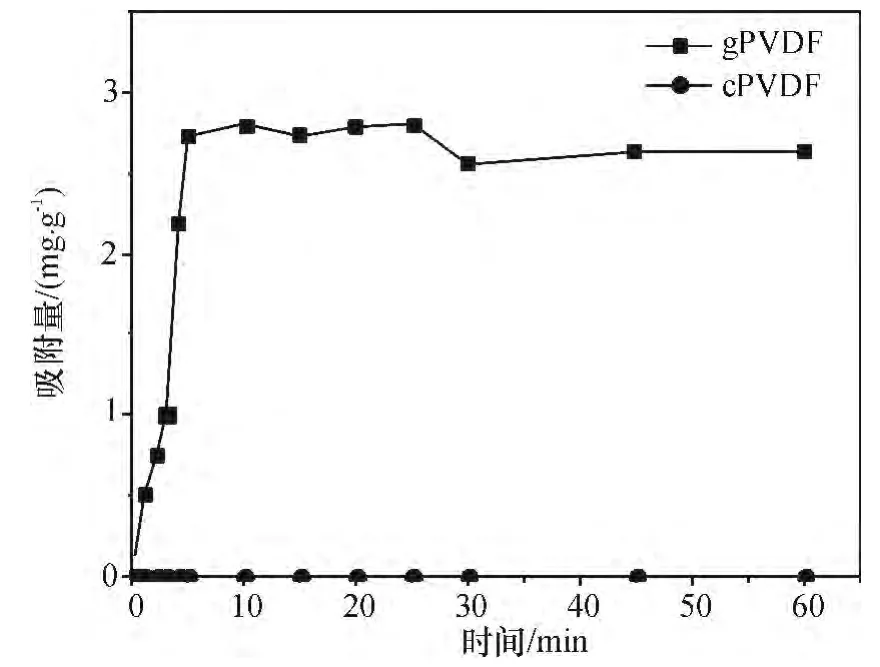
图5 Cr(VI)在c-PVDF 和g-PVDF 膜上的吸附动力学(pH 3.5,c0 =20 mg/L)Figure 5 Adsorption kinetics of Cr(VI)on c-PVDF and g-PVDF membranes
进水质量浓度0.62 mg/L 的Cr(VI)通过g-PVDF 后,出水Cr(VI)质量浓度一直维持低于0.5mg/L (图6). 由于g-PVDF 对Cr 的吸附在5 min 左右即达到平衡,在较高渗透速率的情况下,g-PVDF膜依然保持对重金属良好的去除效果.在连续11 h的过滤中,膜对Cr(VI)的去除率从60%降低到了40%,随后的2 h 中,去除率下降较为明显. 这是因为随着NH2-MCM-41 层吸附的Cr(VI)逐渐增多,导致纳米颗粒层上吸附位点减少.与新膜相比,重复使用的g-PVDF 膜对Cr(VI)的去除率变化曲线,其趋势几乎保持一致,但是整体去除率略下降.这由于部分NH2-MCM-41 纳米颗粒未与膜以化学键的形式结合,清洗过程中会有部分脱落,导致去除率整体有所降低. 而未接枝NH2-MCM-41 的c-PVDF 膜对Cr(VI)几乎没有去除能力. 这从另一方面说明g-PVDF 膜对Cr(VI)的去除能力主要是源于接枝的NH2-MCM-41 对Cr(VI)的吸附.
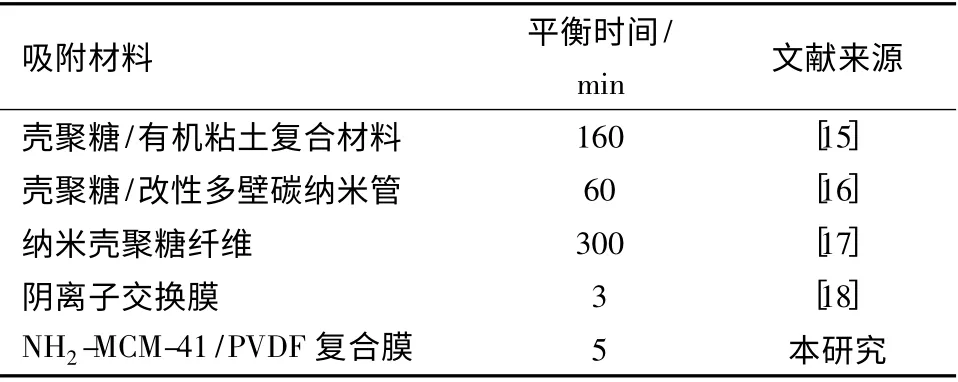
表1 不同材料吸附Cr(VI)平衡时间的对比Table 1 Comparison of adsorption equilibrium time of Cr(VI)
图6 表明,经酸洗恢复后的g-PVDF 膜在重复超滤使用过程中,效果依然稳定,出水铬质量浓度一直保持在0.5 mg/L 以下. 若以出水质量浓度高于0.4 mg/L 的时刻作为参考,酸洗后的膜吸附容量可以恢复到新膜的96.2%.R. Jamshidi Gohari 等[8]利用pH 2 的强酸溶液使PES/HMO 共混膜97.5%的吸附容量得以恢复. 良好的重复使用性能可以实现超滤膜的回用.
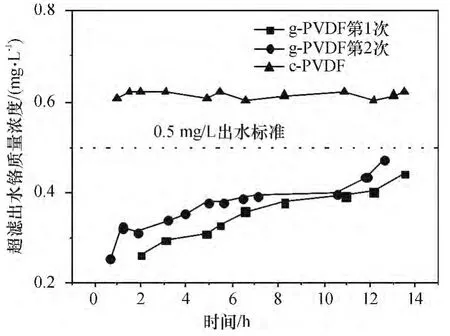
图6 g-PVDF 和c-PVDF 膜对Cr(VI)的去除效果(pH 3.5)Figure 6 Removal efficiency of Cr(VI)with the ultrafiltration time for g-PVDF and c-PVDF membranes (pH 3.5)
3 结论
采用NH2-MCM-41 介孔分子筛接枝改性制备了PVDF 复合超滤膜,考察了其对模拟有机物水样的抗污染能力以及去除水中重金属Cr(VI)的能力,结果表明:
(1)NH2-MCM-41 介孔分子筛成功接枝于超滤膜表面,并在超滤膜表面形成一层均匀的亲水纳米颗粒层. NH2-MCM-41 层使超滤膜抗污染性能得到显著提升,同时对重金属Cr(VI)具有较大的吸附能力.
(2)改性超滤膜对低质量浓度0.62 mg/L 的Cr(VI)水样可以实现进一步的净化,在持续超滤11 h 内,透过液中Cr(VI)的质量浓度维持在0.5 mg/L 以下. 膜的吸附性能可以通过浸泡在0.5 mol/L 的HNO3中得以恢复.
[1]Cai W Q,Tan L J,Yu J G,et al. Synthesis of aminofunctionalized mesoporous alumina with enhanced affinity towards Cr(VI)and CO2[J]. Chemical Engineering Journal,2014,239:207-215.
[2]Ayari F,Srasra E,Trabelsi-Ayadi M. Retention of lead from an aqueous solution by use of bentonite as adsorbent for reducing leaching from industrial effluents[J]. Desalination,2007,206:270-278.
[3]Abollino O,Giacomino A,Malandrino M,et al. Interaction of metal ions with montmorillonite and vermiculite[J]. Applied Clay Science,2008,38:227-236.
[4]Raji F,Pakizeh M. Kinetic and thermodynamic studies of Hg (II)adsorption onto MCM-41 modified by ZnCl2[J].Applied Surface Science,2014,30:568-575.
[5]马国正,刘聪,南俊民,等. Al-MCM-41 介孔分子筛对镉离子吸附性能的研究[J]. 华南师范大学学报:自然科学版,2008(3):76-81.Ma G Z,Liu C,Nan J M,et al. Study on adsorption of cadmium on mesoporous molecular sieves Al-MCM-41[J]. Journal of South China Normal University:Natural Science Edition,2008(3):76-81.
[6]Shariaty-Niassar M,Ghaee A,Barzin J,et al. Effects of chitosan membrane morphology on copper ion adsorption[J]. Chemical Engineering Journal,2010,165:46-55.
[7]Salehi E,Madaen S,Rajabi L,et al. Novel chitosan/poly (vinyl)alcohol thin adsorptive membranes modified with amino functionalized multi-walled carbon nanotubes for Cu (II)removal from water:Preparation,characterization,adsorption kinetics and thermodynamics[J].Separation and Purification Technology,2012,89:309-319.
[8]Gohari R J,Lau W J,Matsuura A T,et al. Adsorptive removal of Pb (II)from aqueous solution by novel PES/HMO ultrafiltration mixed matrix membrane[J]. Separation and Purification Technology,2013,120:59-68.
[9]Shao Y,Wang X,Kang Y,et al. Application of Mn/MCM-41 as an adsorbent to remove methyl blue from aqueous solution[J]. Journal of Colloid Interface Science,2014,429:25-33.
[10]Wu Y H,Jin Y P,Cao J L,et al. Optimizing adsorption of arsenic (III)by NH2-MCM-41 using response surface methodology[J]. Journal of Industrial and Engineering Chemistry,2014,20:1285-1292.
[11]Yin J,Kim E S,Yang J,et al. Fabrication of a novel thin-film nanocomposite (TFN)membrane containing MCM-41 silica nanoparticles (NPs)for water purification[J]. Journal of Membrane Science,2012,423/424:238-246.
[12]Rana D,Tarboush B J A,Matsuura T,et al. Preparation of thin-film-composite polyamide membranes for desalination using novel hydrophilic surface modifying macromolecules[J]. Journal of Membrane Science,2008,325:166-175.
[13]Cao J L,Wu Y H,Jin Y P,et al. Response surface methodology approach for optimization of the removal of chromium (VI)by NH2-MCM-41[J]. Journal of the Taiwan Institute of Chemical Engineers,2014,45:860-868.
[14]Parida K,Mishra K G,Dash S K. Adsorption of toxic metal ion Cr(VI)from aqueous state by TiO2-MCM-41:Equilibrium and kinetic studies[J]. Journal of Hazardous Materials,2012,241/242:395-403.
[15]Pandey S,Mishra S B. Organic-inorganic hybrid of chitosan/organoclay bionanocomposites for hexavalent chromium uptake[J]. Journal of Colloid and Interface Science,2011,361:509-520.
[16]Kim M K,Shanmuga K,Gopalan S,et al. A novel chitosan functional gel included with multiwall carbon nanotube and substituted polyaniline as adsorbent for efficient removal of chromium ion[J]. Chemical Engineering Journal,2015,267:51-64.
[17]Li L,Li Y X,Cao L X,et al. Enhanced chromium (VI)adsorption using nanosized chitosan fibers tailored by electrospinning[J]. Carbohydrate Polymers,2015,125:206-213.
[18]Vinodh R,Padmavathi R,Sangeetha D. Separation of heavy metals from water samples using anion exchange polymers by adsorption process[J]. Desalination,2011,267:267-276.
