丁二酮肟分离-EDTA络合返滴定法测定哈氏合金中的镍
2015-12-11许洁瑜麦丽碧陈晓东
许洁瑜,麦丽碧,陈晓东
广东省工业技术研究院(广州有色金属研究院分析测试中心),广东 广州 510650
哈氏合金是由Ni,Cr,Mo,Fe和Si等元素组成的,属于镍基合金中的 Ni-Mo系、Ni-Cr-Mo系及Ni-Si系耐蚀耐热合金.虽然哈氏合金的价格通常会让很多用户望而却步,但它具有其他材料所无法比拟的耐腐蚀性能,用其制造的设备在使用十年之后腐蚀不到1mm.因此,哈氏合金在工业中得到越来越广泛的应用[1].
常量镍的测定方法主要有丁二酮肟重量法[2-4]、EDTA 络合滴定法[5-7]和丁二酮肟分光光度法[8-9].由于哈氏合金中的镍含量较高,采用分光光度法测定误差较大,而丁二酮肟重量法检测流程繁杂冗长,无法满足快速分析的要求.参照这些方法的基本原理,本文采用丁二酮肟沉淀镍,使其与铬、铁、钨等干扰元素分离,沉淀溶于盐酸,加入过量的EDTA标准溶液,以二甲酚橙为指示剂,在pH值为5.5~6的HAC-NaAC缓冲介质中用标准锌盐溶液返滴定.该方法终点敏锐,选择性和准确度高.
1 实验部分
1.1 试剂制备
乙酸-乙酸钠缓冲溶液:称取200g结晶的乙酸钠,用水溶解后加10mL冰乙酸,用水定容至1L,溶液pH值为5.5~6.
丁二酮肟乙醇溶液:称取5g丁二酮肟,溶于500mL乙醇中,溶液浓度为10g/L.
二甲酚橙溶液:称取0.1g二甲酚橙溶解于100mL水中,溶液浓度为0.1%.
Ni标准溶液:称取1.0000g金属(w(Ni)≥99.95%),加入20mL的 HNO3(3+2),加热溶解完全后蒸至稠状,再加入10mL硫酸(1+1)并加热蒸发至冒SO3白烟,冷却,然后用水冲洗表面皿及杯壁,加热蒸发至冒SO3白烟后冷却,再加水约100mL,加热使盐类溶解,冷至室温后移入1L容量瓶中,用水定容,此溶液中Ni含量为1g/L.
EDTA标准溶液:称取16.38g乙二胺四乙酸二钠,加水溶解,移入1L容量瓶中,用水定容,c(EDTA)≈0.044mol/L.
Zn标准滴定溶液:称取13.09g的Zn(NO3)2·6H2O于250mL烧杯中,加水使其溶解,移入1L容量瓶中,用水定容,c(Zn2+)≈0.044mol/L.
硝酸、硫酸、氢氟酸、冰乙酸、无水乙醇、乙酸钠、乙二胺四乙酸二钠、丁二酮肟,所用试剂均为分析纯;所用水为二级水.
1.2 方 法
称取0.2g(精确至0.0001g)试样于聚四氟乙烯烧杯中,加入5mL氢氟酸及5mL硝酸,在电炉上加热溶解,反复补加氢氟酸和硝酸至试样完全溶解.溶解完全后将试液转入250mL玻璃烧杯中,加入4mL的硫酸(1+1),盖上表面皿,继续加热至冒SO3白烟,待2~3min后取下冷却,用水冲洗表面皿及杯壁,加入10mL水,加热使可溶性盐溶解,冷却后将溶液转入100mL容量瓶中,用水稀释至刻度,摇匀试液.
准确移取10mL试液于250mL烧杯中,加沸水至150mL左右,搅拌下加入10mL浓度为300g/L的柠檬酸铵溶液,再加入1~2g的氯化铵,用氨水调至溶液pH≈9,最后加入30mL浓度为10g/L的丁二酮肟乙醇溶液,保温30min后用定性滤纸过滤,用热水洗表面皿及杯壁2~3次,洗沉淀8~10次,然后将沉淀用热盐酸(1+1)溶于原烧杯中[10].用热水和盐酸(1+1)交替洗涤滤纸(溶液体积不超过150mL).用滴定管准确加入10~20mL的EDTA标准液(其用量为使Ni完全络合并过量5~10mL),搅匀,记下所加入的体积(V1).滴加2~3滴二甲酚橙指示剂,用氨水(1+1)调节至溶液出现紫红色,再用盐酸(1+1)调节溶液至黄色刚好出现,加入10mL浓度为200g/L的乙酸-乙酸钠缓冲溶液,用Zn(NO3)2滴定液滴定至溶液颜色由黄色刚好变为橙红色,记下所消耗的体积(V2).
1.3 计 算
按下式计算镍的质量分数w(Ni):

式(1)中:c为 EDTA 标准溶液的浓度,moL/L;V1为加入EDTA标准溶液的体积,mL;V2为滴定时所消耗的Zn(NO3)2标准滴定溶液的体积,mL;K 为Zn(NO3)2标准滴定溶液换算成EDTA标准溶液体积的系数;m为试料的质量,g;镍的摩尔质量为56.89g/moL,试液分取比例为10.
K值的确定:吸取20mL的EDTA标准溶液于250mL烧杯中,加入10mL浓度为200g/L的乙酸-乙酸钠缓冲溶液,加入20~30mL水,滴加2~3滴二甲酚橙,用Zn(NO3)2标准滴定液滴定至溶液颜色由黄色刚好变为橙红色,即为终点.

式(2)中:V3为吸取EDTA标准溶液的体积,mL;V4为滴定Zn(NO3)2标准液的体积,mL.
EDTA标准溶液的标定:准确吸取3份20mL的Ni标准溶液置于3个250mL烧杯中,用滴定管准确加入20mL的EDTA标准液,搅匀.滴加2~3滴二甲酚橙指示剂,用氨水(1+1)调节至溶液出现紫红色,再用盐酸(1+1)调节溶液至黄色刚好出现,加入10mL浓度为200g/L的乙酸-乙酸钠缓冲溶液,用Zn(NO3)2滴定液滴定至溶液颜色由黄色刚好变为橙红色,记下所消耗的体积V.
EDTA标准溶液的浓度按以下公式计算:
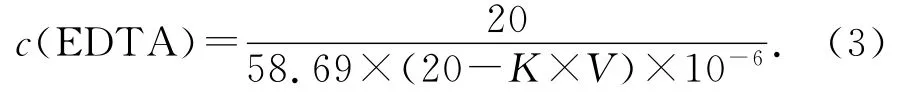
式(3)中V 为标定时所消耗Zn(NO3)2标准滴定溶液的体积,mL.
2 结果与讨论
考虑到哈氏合金的共存元素中较高含量且耐氯离子腐蚀的铬、钼元素,以及钨和硅等元素,经过反复试验,选择用氢氟酸+硝酸混合酸溶解样品.在加热条件下,先加5mL氢氟酸和5mL硝酸溶解样品,并在溶解过程中不断补加氢氟酸和硝酸,直至样品完全溶解.
2.1 酸度的影响
以二甲酚橙作指示剂的EDTA滴定法中,溶液的酸度值应控制在pH=5~6.酸度过高或过低会影响指示剂的显色[11].因此,选用乙酸-乙酸钠缓冲溶液,将pH值稳定在5.5~6之间.
2.2 共存离子的影响
试样用氢氟酸和硝酸溶解后,在氨性介质中,镍与丁二肟酮生成红色丁二酮肟镍的沉淀,可与其它铬、钼、铁、钨等干扰元素分离,因而共存离子均不影响结果的测定.
2.3 丁二酮肟加入量的影响
表1为丁二酮肟加入量对试验结果的影响.

表1 丁二酮肟加入量对结果的影响Table 1 Influence of the content of dimethylglyoxime
由表1可知:当丁二酮肟加入量小于20mL时,镍的测定结果与参考值相差较大,说明丁二酮肟加入量偏少,溶液中的镍未完全沉淀,使镍的测定值偏低;当丁二酮肟加入量大于20mL时,镍的测定结果与参考值接近,表明溶液中的镍已完全沉淀.因此,选择丁二酮肟的适宜加入量为30mL.
2.4 精密度试验
取5个不同的试样,按实验方法独立地进行7次测定,实验结果列于表2.由表2可知,本方法精密度高,重视性好,稳定性好.

表2 精密度试验Table 2 Precision test
2.5 回收试验
为了考察本法的准确度,在1号和2号试样中分别加入20mL和50mL浓度为1g/L的镍标准溶液,进行加标回收试验.测试过程与样品分析过程一致,结果列于表3.由表3可知,在拟定的试验条件下,镍回收率在98.15%~101.36%之间,符合常量分析要求.

表3 加标回收试验Table 3 Recovery test
3 结 论
采用丁二酮肟分离-EDTA络合返滴定法测定哈氏合金中的镍,实验结果表明,该方法精密度高、准确度高及稳定性好,能够满足哈氏合金中镍含量测定的要求.
[1]张汝松,李志国,刘昌峰.哈氏合金的选用[J].石油化工腐蚀与防护,2012,29(1):33-35.
[2]戴学谦,乌静,胡建春.GB/T 21933.1-2008镍铁镍含量的测定:丁二酮肟重量法[S].北京:中国标准出版社,2008.
[3]朱宝璋,吕毕生.GB/T 223.25-1994钢铁及合金化学分析方法:丁二酮肟重量法测定镍量[S].北京:中国标准出版社,1994.
[4]张发志,于乾勇,吕庆成,等.YS/T 707-2009羰基镍铁粉化学分析方法镍量的测定:丁二酮肟重量法[S].北京:中国标准出版社,2010.
[5]金娅秋,吴瑞林,安中庆,等.GB/T 15072.10-2008贵金属合金化学分析方法金合金中镍量的测定:EDTA络合返滴定法[S].北京:中国标准出版社,2008.
[6]戴凤英,张鸣,张永进,等.YS/T 325.1-2009镍铜合金化学分析方法镍量的测定:Na2EDTA滴定法[S].北京:中国标准出版社,2010.
[7]刘海东,喻生洁,林秀英,等.YS/T 341.1-2006镍精矿化学分析方法镍量的测定:丁二酮肟沉淀分析-EDTA滴定法[S].北京:中国标准出版社,2006.
[8]王玉娟,崔秋红,郭蕴珊.GB/T 223.23-2008钢铁及合金镍含量的测定:丁二酮肟分光光度法[S].北京:中国标准出版社,2008.
[9]佚名.YS/T 820.2-2012镍量的测定:丁二酮肟分光光度法[S].北京:中国标准出版社,2013.
[10]北京矿冶研究总院分析室.矿石及有色金属分析手册[M].北京:冶金工业出版社,1990.
[11]王瑞斌,张成孝.EDTA差减滴定法测定汞污染土壤中汞[J].冶金分析,2007,27(12):54-56.
