在铜镁合金表面制备MgO/Cu复合材料内氧化层的组织和性能
2015-12-09王庆福张彦敏国秀花宋克兴
王庆福,张彦敏,国秀花,2,宋克兴
(1.河南科技大学材料科学与工程学院,河南省有色金属材料科学与加工技术重点实验室,有色金属共性技术河南省协同创新中心,洛阳471023;2.西安理工大学材料科学与工程学院,西安710048)
0 引 言
颗粒弥散强化铜基复合材料广泛应用于电气工程开关触桥、连铸机结晶器、集成电路引线框架等,其制备方法是在铜基体中人为添加或通过一定工艺原位生成弥散分布的第二相粒子,从而使复合材料具备优良的强度以及高的导电性和导热性。按照引入增强相颗粒的途径,可以将颗粒增强铜基复合材料的制备方法分为外加颗粒法和原位合成法[1-4],内氧化法作为原位合成法的代表,在制备Al2O3增强铜基复合材料方面已具备比较成熟的工艺。常用的增强相颗粒主要为Al2O3、MgO和SiO2,它们的种类、粒径以及在复合材料中的形态和分布决定了颗粒增强铜基复合材料的综合性能[1-3]。目前关于内氧化原位合成颗粒增强铜基复合材料的研究主要集中在内氧化法制备Al2O3/Cu复合材料,而对于采用内氧化法制备MgO/Cu复合材料的研究却鲜有报道。MgO的密度为3.85g·cm-3,熔点为2 852℃,沸点为3 600℃,具有很高的强度、硬度、导电性、导热性、耐磨性和高温性能。因此,作者以MgO为增强相,采用内氧化法在铜镁合金表面制备了镁质量分数为1%的MgO/Cu复合材料内氧化层(简称内氧化层),研究了内氧化时间对内氧化层厚度、硬度和导电率的影响,并分析了铜镁合金的内氧化热力学。
1 试样制备与试验方法
1.1 试样制备
选用紫铜(纯度不小于99.95%)和Cu-20%Mg中间合金(质量分数)为原材料,采用真空熔炼法(熔炼温度为1 200℃、熔炼时间为30min)制备镁质量分数为1.0%的铜镁合金;去除两端缺陷和氧化皮后,热挤压成φ30mm的棒材,再切割成φ5mm×20mm的棒材,用金相砂纸对试样表面进行打磨以消除线切割的影响。
采用由30%Cu2O粉、20%铜粉和50%Al2O3粉(体积分数)组成的混合粉将铜镁合金试样包埋起来,再一起放入自制的铜管内,并用高温粘土和水玻璃密封;然后将铜管放入高温炉中加热,内氧化温度为1 173K,保温时间分别为5,10,15,20h。其中,混合粉中的Cu2O粉和铜粉是为了保证气氛中的氧分压而添加的,铜镁合金内氧化的最高氧分压即Cu2O的分解压;Al2O3粉则是为了防止铜粉与铜镁合金烧结而添加的。
1.2 试验方法
将内氧化后的试样打磨、抛光后制成金相试样,用OLYMPUS-PMG3型光学显微镜(OM)观察显微组织并测定内氧化层的厚度,厚度范围为试样表面到内氧化层与铜镁合金的界面处;用D60K型数字金属导电率测量仪测导电率;用MH-3型纤维硬度测量仪测硬度,加载载荷1.96N,保载时间10s;用EM2100(UHR)型超高分辨透射电镜(TEM)观察MgO颗粒的形态及分布情况。
2 试验结果与讨论
2.1 内氧化时间对内氧化层厚度的影响
内氧化不同时间后,铜镁合金表面均生成了MgO/Cu复合材料内氧化层(环形圈),如图1所示,MgO弥散强化相是由析出的镁与游离态氧[O]反应而形成的。
由图2可以看出,内氧化层厚度随着内氧化时间的延长而增加,内氧化时间为20h的内氧化层厚度最大,为1.032mm。内氧化主要有两个过程:其一,Cu2O分解产生的氧从外部扩散进入铜镁合金基体内部,这个过程遵循扩散定理;其二,扩散进入基体中的氧与镁发生反应生成MgO。在一定条件下,内氧化时间越长,Cu2O分解产生的氧越多,内氧化层越厚。另由图2还可以看出,随着内氧化时间的延长,内氧化速率逐渐减慢。这主要是因为[4-5],随着内氧化前沿面积的不断减少,氧的扩散通量增加,内氧化速率较高;MgO颗粒首先在晶界处形成,而晶内的镁原子在浓度梯度的驱动下向晶界处扩散,依附于已生成的 MgO晶体上氧化、形核、长大,越来越多的MgO颗粒阻碍了氧的扩散,降低了内氧化速率。这两方面的综合作用,使铜镁合金的内氧化曲线形似抛物线,符合Wagner抛物线理论。
2.2 内氧化时间对内氧化层硬度和导电率的影响
由图3可以看出,随着内氧化时间的延长,内氧化层的硬度先增加后降低,并在内氧化10h后达到最大值(123.3HV);内氧化层的导电率随着内氧化时间的延长而逐渐升高,并在保温时间为20h时达到最高,为88%IACS,导电率曲线具有抛物线特征。
相关研究表明[6-8],内氧化层硬度和导电率的变化是镁脱溶并与[O]形成 MgO粒子的结果,硬度、导电率随时间的变化趋势与生成MgO颗粒的多少有关。对于硬度而言,固溶在铜基体内部的镁在内氧化后以MgO形态析出,这些细小坚硬且化学稳定性和热稳定性极好的陶瓷颗粒作为位错源,阻碍了位错、晶界、亚晶界的运动,增加了位错密度,从而提高了内氧化层的硬度和强度;当内氧化时间超过10h后,硬度随着内氧化时间的延长逐渐下降,这可能与部分晶粒发生再结晶以及MgO粒子长大有关。

图1 在1 173K内氧化不同时间制备内氧化层的OM形貌Fig.1 OM morphology of internal oxidation layer prepared at 1 173Kfor different times

图2 内氧化层厚度与内氧化时间的关系曲线Fig.2 Curve of thickness versus internal oxidation time for internal oxidation layer
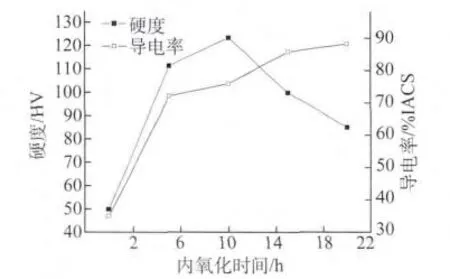
图3 内氧化层硬度和导电率随内氧化时间的变化曲线Fig.3 Curves of hardness and electric conductivity versus internal oxidation time for internal oxidation layer
另由图3可以看出,未内氧化的铜镁合金的导电率仅为35.1%IACS,而内氧化层的导电率最高可达88%IACS。这主要是因为内氧化前合金中的镁原子固溶于铜基体中,固溶原子的存在会使材料的晶格发生畸变,增加了导电过程中电子的散射作用,从而降低了材料的导电性。从导电角度来讲,固溶在铜基体中的镁原子和内氧化后生成的MgO粒子都为杂质,但前者引起的点阵畸变要比后者大得多。铜镁合金的内氧化处理对导电率具有双重作用:析出的MgO粒子使铜基体的导电率降低;MgO质点的析出消耗了铜镁合金中的镁,减少了晶格畸变程度,使导电率提高。但后者的作用显著大于前者的,因此内氧化层的导电率显著提高[9]。
2.3 内氧化层的显微组织
从图4(a)可以看出,内氧化层表层的晶粒比内部的更细小。这主要是因为在内氧化过程中,MgO颗粒主要经历形核、长大和粗化过程,在表层,由于氧的扩散距离较短,MgO颗粒较早地形核、析出、长大,钉扎了正在长大的晶粒边界,使晶粒得不到充分长大,而内部由于氧原子的扩散距离较长,MgO颗粒的形成较晚,晶粒充分长大。另外,由于表层中MgO颗粒的形成消耗了一部分氧,抑制了氧进一步向内部扩散,导致内部MgO颗粒的析出较少且较晚,阻碍晶粒长大以及使再结晶的影响逐渐减弱,晶粒逐渐长大[8,10-12]。
从图4(b)可知,从内氧化层的表层到心部,硬度逐渐降低;内氧化层的硬度较铜镁合金基体的有较大提高,最高可达123.3HV。这是因为内氧化形成的细小MgO颗粒弥散分布,阻碍了晶界、亚晶界和位错的移动,从而起到了良好的强化效果,使内氧化层具有较高的硬度[6,13-14]。表层先形成的MgO颗粒阻碍了晶粒长大,使表层的晶粒尺寸较小;在内氧化过程中,由于MgO颗粒基本上是原位析出,表层氧的扩散速度较快,使MgO颗粒来不及长大,从而导致MgO颗粒更加细小弥散地分布,进而使内氧化层表层的硬度更高,这与图4(a)的分析一致。

图4 在1 173K内氧化10h制备内氧化层的OM形貌及硬度分布Fig.4 OM morphology(a)and hardness distribution(b)of internal oxidation layer prepared at 1 173Kfor 10h

图5 在1 173K内氧化10h制备内氧化层的TEM形貌和电子衍射花样Fig.5 TEM morphology(a)and electron diffraction pattern(b)of internal oxidation layer prepared at 1 173Kfor 10h
从图5中可以看到,在1 173K内氧化10h制备内氧化层的基体上弥散分布着许多椭球形或球形的小颗粒,其大小为2~10nm,颗粒间距为10~60nm,经衍射花样标定为MgO。
2.4 内氧化热力学
从热力学角度讲,铜镁合金内氧化是镁的择优氧化。温度和氧分压pO2是控制氧化物分解与形成的关键,相关的氧化反应式如下[15]:
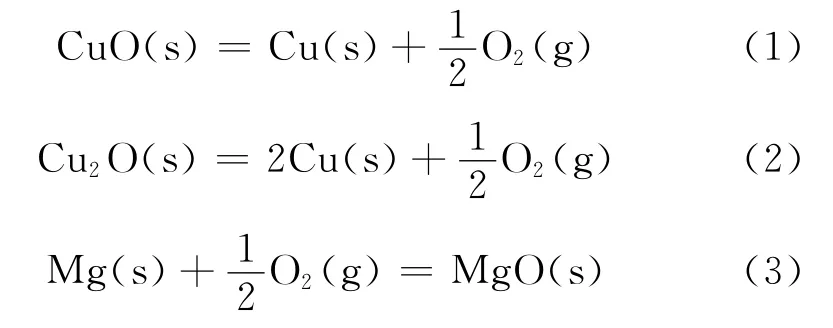
相应的吉布斯函数式为:
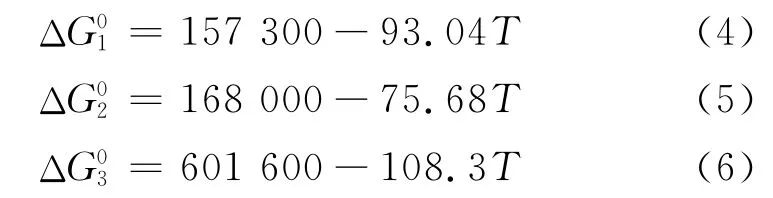
式中:ΔG为自由能;G0为标准吉布斯自由能;T为热力学温度。
ΔG=ΔG0+2.303RTlnQp(7)
根据吉布斯函数式(4),令ΔG=0,则

式中:Qp为分压商;p0=1 013 325Pa,为一个标准大气压;pO2为临界氧分压,Pa;R=8.314J·mol-1·K-1。
从而可得到温度T与Cu2O、CuO、MgO形成或分解的临界氧分压pO2间的函数关系分别如式(10~12)所示。
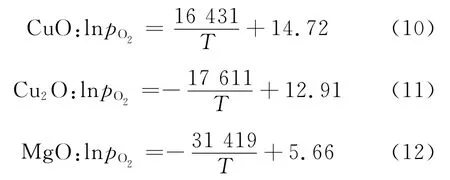
由式(10~12)可以计算出纯铜、纯镁氧化/无氧化时氧分压的门槛值,进而绘制出铜镁合金氧化、择优氧化、和无氧化的热力学条件区位图。
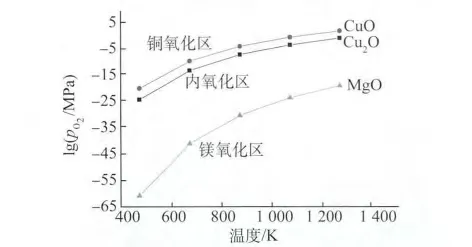
图6 铜镁合金内氧化、择优氧化和无氧化的热力学条件区位图Fig.6 Area chart of thermodynamic conditions of oxidation,preferential oxidation and free oxidation of Cu-Mg alloy
从图6中可以看出,择优氧化区中的温度和氧分压即为铜镁合金实现内氧化的热力学条件。内氧化的上限氧分压由式(11)确定,高于上限氧分压后铜将发生氧化,因此内氧化的氧分压应接近但不能超过上限氧分压。Cu2O粉分解供氧时,介质中的氧分压近似等于给定温度下的上限氧分压,由于上限氧分压随温度的升高而增大,为了加快铜镁合金的内氧化过程,应采用较高的内氧化温度。内氧化的下限氧分压由式(12)确定,总体上比较低,在具体的内氧化过程中,控制它的意义不大。因此,铜镁合金发生内氧化的临界氧分压为:
10-31419/T+5.66<pO2<10-17611/T+12.91(13)
3 结 论
(1)随着内氧化时间的延长,内氧化层的厚度和导电率均增加,且呈现出抛物线趋势,硬度先升高后降低;当内氧化时间为10h时,内氧化层的性能最佳,硬度为123.3HV,导电率为75.9%IACS。
(2)铜镁合金经内氧化后,固溶在铜基体中的镁以MgO的形式析出,形成内氧化层,内氧化层的晶粒比基体的细小;在内氧化层铜基体上弥散分布着粒径为2~10nm、间距为10~60nm的MgO颗粒是内氧化层综合性能得到大幅提高的根本原因。
(3)铜镁合金内氧化层形成的临界氧分压介于10-31 419/T+5.66和10-17 611/T+12.91之间。
[1]田宝红,宋克兴,刘平.高性能弥散强化铜基复合材料及其制备技术[M].北京:科学出版社,2011:22-27.
[2]林阳明.Cu-Al合金内氧化及内氧化法制备Al2O3/Cu复合材料新型工艺研究[D].洛阳:河南科技大学,2006:1-14.
[3]燕鹏,林晨光,崔舜,等.弥散强化铜合金的研究与应用现状[J].材料导报,2011,25(6):101-103.
[4]李红霞,田宝红,宋克兴,等.内氧化法制备表面弥散强化铜合金的组织和性能[J].兵器材料科学与工程,2005,28(2):44-47.
[5]刘勇,张金东,田宝红,等.Cu-0.8Cr-Ce合金薄板内氧化动力学研究[J].材料热处理技术,2010,39(22):23-26.
[6]程建奕,敖学文,余方新,等.Cu-Al合金内氧化工艺参数对性能影响的研究[J].材料工程,2010(7):29-33.
[7]NASER J,RIEHEMANN W,FERKEL H.Dispersion hardening of metals by nanoscaled ceramic powders[J].Materials Science and Engineering:A,1997,234/236:467-473.
[8]代永强,田宝红,陈卫,等.引线框架Cu-0.35Al-Ce合金薄板内氧化动力学研究[J].材料热处理技术,2009,38(6):9-12.
[9]申玉田,崔春翔,吴人洁,等.Cu-Al合金内氧化工艺及动力学的研究[J].稀有金属材料与工程,2001,30(1):44-49.
[10]王孝武,袁森,张卫华,等.影响内氧化生成Al2O3/Cu表面复合层厚度及组织的因素[J].复合材料学报,2001,18(3):56-59.
[11]SONG Ke-xing,XING Jian-dong.Internal oxidation of dilute Cu-Al alloy powders with oxidant of Cu2O[J].Materials Science and Engineering:A,2004,380:117-122.
[12]MOUSTSFA S F,ABDEL-HAMID Z,ABD-ELHAY A M.Copper matrix SiC and Al2O3particulate composites by powder metallurgy technique[J].Materials Letters,2002,53:244-249.
[13]SONG Ke-xing,XING Jian-dong,DONG Qi-ming,et al.Optimization of the processing parameters during internal oxidation of Cu-Al alloy powders using an artificial neural network[J].Materials and Design,2005,26:337-341.
[14]国秀花,宋克兴,郜建新,等.Cu-Al合金平板试样内氧化层的测定[J].兵器材料科学与工程,2007,30(1):21-23.
[15]申玉田,崔春翔,申玉发,等.Cu-Mg合金内氧化的热力学分析(热力学函数)[J].稀有金属材料与工程,2004,33(6):576-579.
