2,4-二硝基苯肼法对三种蔬菜维生素C含量的测定*
2015-12-09徐美玲
徐美玲
(菏泽学院化学化工系,山东菏泽274015)
引言
维生素C是一类人体不可缺少的微量低分子有机化合物,并广泛参与人体内一系列代谢反应[1],如:参与神经介质、激素的生物合成;能将胆固醇转化为胆汁酸,使高胆固醇血症患者的胆固醇下降;能将Fe3+还原为Fe2+,使其易于吸收,有利于血红蛋白的形成;还具有抗氧化、抗衰老、解毒和提高有机免疫力的作用.由于人体不能自身合成维生素C,因此必须依靠食物供给.食物中的维生素C被人体小肠上段吸收后,就分布到体内所有的水溶性结构中,正常情况下,维生素C绝大部分经人体代谢后随尿排出,少部分直接排出[2,3].如长期缺乏,将导致坏血病,以及心脏病,肝病等疾病.因此,食物的维生素C含量和食用对人体健康有重要意义.
目前维生素C含量的测定方法主要有碘量法,原子吸收光谱法,高效液相色谱法以及本实验所采用的2,4-二硝基苯肼法等[4].该方法是:还原型维生素C经活性炭催化氧化后,得到脱氢型维生素C,再经过水解与2,4-二硝基苯肼作用生成红色脎,再根据脎在硫酸溶液中的含量与维生素C的总含量成正比,进行比色定量测定[5].
1 实验仪器及试剂
722G型可见光分光光度计(上海精密科学仪器有限公司产品);超级数频恒温器(重庆四达实验仪器厂产品);ESJ180-4型电子天平(沈阳龙腾电子有限公司产品);九阳豆浆机;抽滤装置;BCD-218BP型海信冰箱;容量瓶(1000,500 mL各2个,棕色100 mL 10个);移液管(25,10 mL各1支);吸量管(1,5 mL各1支);玻璃烧杯(500,100 mL各2个);试管(16支);硫脲(A.R,天津市科密欧化学试剂有限公司产品);2,4-二硝基苯肼(A.R,天津市科密欧化学试剂有限公司产品);硫酸(质量分数98%,A.R,山东莱阳经济技术开发区精细化工厂产品);盐酸(质量分数36%~38%,G.R,山东莱阳经济技术开发区精细化工厂产品);草酸(A.R,济南化工厂产品);抗坏血酸(A.R,西陇化工股份有限公司产品).
2 实验部分
2.1 溶液的配制
2%(质量分数)的2,4-二硝基苯肼溶液:溶解2 g 2,4-二硝基苯肼于100 mL 4.5 mol/L硫酸内且过滤,不用时存于冰箱内且每次使用前需过滤.2%(质量分数)草酸:溶解20 g草酸于700 mL水中,用水稀释定容到1000 mL.1%(质量分数)草酸:取2%(质量分数)草酸溶液500 mL,用水稀释定容至1000 mL.2%(质量分数)硫脲:准确称取20 g硫脲,用1%(质量分数)草酸溶解,稀释定容至1000 mL.1%(质量分数)硫脲:取2%(质量分数)硫脲500 mL,用1%(质量分数)草酸稀释定容至1000 mL.活性炭:准确称取100 g活性炭粉,加入750 mL 1 mol/L盐酸中,在沸水浴中回流1~2 h,过滤,再用清水洗数次至滤液中无铁离子为止,然后置于110℃烘箱中烘干,备用.维生素C标准溶液:准确称取0.1000 g纯维生素C溶于1%(质量分数)草酸溶液中,用1%(质量分数)草酸溶液定容至100 mL容量瓶中,使其质量浓度为1 mg/mL.加入2 g活性炭粉于50 mL维生素C标准溶液中,振摇1 min后静置,过滤备用.取10 mL滤液加入5 g硫脲,放入500 mL容量瓶中,用1%(质量分数)草酸溶液稀释定容至刻度,使维生素C标准溶液质量浓度为20 μg/mL.从20μg/mL维生素C溶液中各取5,10,20,25,40,50,60 mL于7个100 mL容量瓶中,用1%(质量分数)硫脲溶液稀释定容,使标准溶液质量浓度分别为1,2,4,5,8,10,12μg/mL.分别取上述溶液4 mL置于2组试管中,1号为空白组,2号则分别继续加入1 mL 2%(质量分数)2,4-二硝基苯肼溶液混匀,然后将所有试管与待制备的样品溶液一同置于37℃恒温水浴箱中保温3 h.
2.2 样品的处理
取西红柿154.4 g置于1000 mL 2%(质量分数)草酸溶液中,混匀倒入豆浆机中打成匀浆.取匀浆10 mL用1%(质量分数)草酸溶液稀释定容至100 mL,静置15 min过滤,得到它的还原型维生素C提取液.
氧化处理:分别取上述提取液25 mL于烧杯中加入1 g活性炭振荡,混匀1 min后过滤,得到其氧化型维生素C提取液.取10 mL此氧化型提取液,加入10 mL 2%硫脲溶液混匀.
脎的形成:分别取4 mL上述溶液于2支试管中,1号为空白,2号则加入1 mL 2%(质量分数)2,4-二硝基苯肼溶液,与标准溶液一同置于37℃恒温水浴箱中保温3 h.
取甘蓝300g,青椒171g,处理方法与西红柿相同.
2.3 标准溶液与待测样品同步处理
脎的溶解:3 h后取出所有试管,置于冰水中.1 min后将空白组冷却至室温,加入1 mL 2%(质量分数)2,4-二硝基苯肼溶液,室温下静置10~15 min后,放入冰水中.然后向所有试管中逐滴加入5 mL 85%硫酸溶液,边加边振荡防止炭化,在室温下静置30~35 min.
比色:以空白液调零点,在500 nm波长处用1 cm比色皿测定其吸光度.
2.4 影响测定因素的确定
2.4.1 水浴时间影响
取溶液5份置于37℃下,活性炭加入量为1.0 g,水浴时间为1.0,2.0,3.0,3.5,4.0 h,用分光光度计在500 nm波长处测定其吸光度,选取最佳水浴时间.
2.4.2 活性炭用量影响
同样取溶液5份,置于37℃下水浴3 h,分别加入0.1,0.2,0.5,1.0,1.5 g活性炭,在500 nm波长处测定其吸光度,选择活性炭最佳加入量.
2.4.3 反应温度影响
同样取溶液5份,活性炭加入量为1.0 g,水浴时间3 h,分别置于29,34,37,39,42℃下,在500 nm波长处测定其吸光度,选择最佳反应温度.
3 结果与分析
3.1 测定条件的影响
3.1.1 水浴时间的影响
在一定的温度下,固定活性炭的用量,吸光度随水浴时间的变化如图1所示.

图1 水浴时间对吸光度的影响
由图1可知,水浴3 h前反应不完全,到3 h时吸光度达到最大值且随着时间的增加基本保持不变,故最佳水浴时间为3 h.
3.1.2 活性炭用量的影响
在一定的温度下,固定水浴时间,吸光度随活性炭加入质量的变化如图2所示.
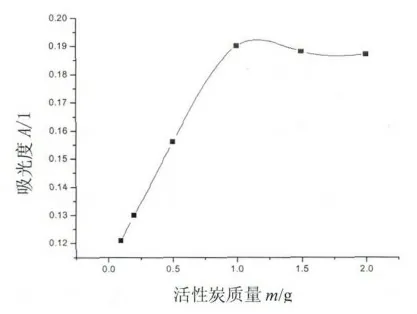
图2 活性炭的量对吸光度的影响
从图2可见,当活性炭加入量低于1.0 g时反应不完全,加入量达到1.0 g时反应完全,吸光度达到最大,且随着活性炭加入量的增加,吸光度基本保持不变,故选择活性炭加入量为1.0 g.
3.1.3 反应温度的影响
水浴时间一定的条件下,固定活性炭的用量,吸光度随反应温度的变化如图3所示.
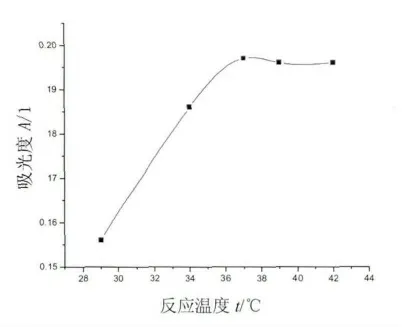
图3 温度对吸光度的影响
从图3可知,当温度低于30℃时反应不完全,温度上升至37℃以上水浴时间3 h后反应完全,吸光度达到最大,且随温度的增加基本保持不变,故最佳反应温度选择为37℃.
3.2 吸光度与标准溶液浓度关系曲线的绘制
3.2.1 实验数据
西红柿、甘蓝、青椒三种蔬菜提取液的标准溶液维生素C质量浓度及吸光度测定值,见表1.
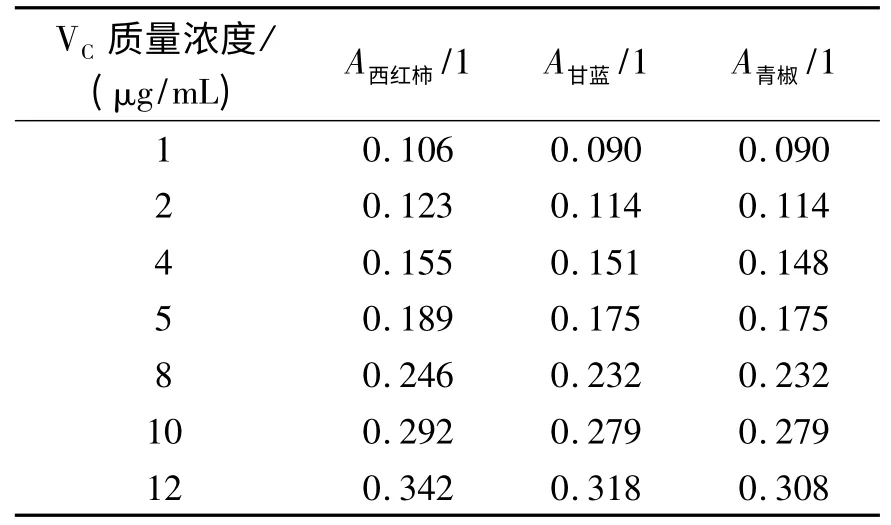
表1 标准溶液维生素C的质量浓度与吸光度的关系
3.2.2 标准曲线的绘制
根据表1实验数据绘制出维生素C溶液质量浓度与吸光度关系的标准曲线,如图4所示.从图4可知,质量浓度在1~12μg/mL间与吸光度A呈线性关系.

图4 维生素C溶液质量浓度与吸光度关系的标准曲线
3.3 维生素C含量的计算
对西红柿、甘蓝、青椒三种蔬菜的提取液吸光度进行平行测定,所用的线性回归方程分别为:y=0.0215 x+0.0785,y=0.0206x+0.0703,y=0.0201x+0.0716;相关系数分别为r2=0.9959,r2=0.9993,r2=0.9977.由回归方程计算得西红柿、甘蓝、青椒样品提取液VC质量浓度分别为:3.13μg/mL、5.91μg/mL、6.14μg/mL.根据下列公式计算得样品中维生素C的含量(g/kg)[6].
式中:ρ——由回归方程算得的样品提取液VC质量浓度(μg/mL);
V——样品提取液用2%(质量分数)草酸溶液定容的体积(mL);
f——样品提取液氧化过程中稀释倍数;
m——样品质量(g).
通过上式计算,西红柿中维生素C的含量为4.07 g/kg,甘蓝中维生素C的含量为3.94 g/kg,青椒中维生素C的含量为7.18 g/kg.
4 结论
由测定结果可知,青椒中维生素C含量相对较高,其次是西红柿,甘蓝含量最低,符合相关文献结果[7,8].该实验测定结果准确,操作简单,不需特殊仪器,精确度高,因此也进一步证实了该检测方法的可行性.由于维生素C为人体所必不可少,且广泛分布于植物组织和新鲜蔬菜和水果中,所以人们应注意摄食以补充维生素C[9~11].
[1]路纯明,赵二伟,李沛青.2,4-二硝基苯肼法测定白酒中甲醇的研究[J].郑州工程学院学报,2003,25(1):29-36.
[2]孟哲.分光光度法测定水果中维生素C含量的研究[J].邢台师范高专学报,2001,16(4):190-197.
[3]韩志萍.陕北不同地区红枣中VC含量的测定与比较[J].食品研究与开发,2006,27(11):90-93.
[4]薛刚,刘文红,黄海涛,等.2,4-二硝基苯肼比色法测定婴幼儿配方食品和乳粉及其制品中总抗坏血酸的含量[J].食品研究与开发,2000,21(3):48-49.
[5]杨艳.分光光度法测圆果化香树的抗坏血酸含量[J].安徽农业科学,2010,38(18):9523-9524,9526.
[6]潘乐,孙瑞敏.间接分光光度法测定药品中VC含量[J].黄山学院报,2011,13(3):47-49.
[7]魏培海,董信梅,陈小荣,等.分光光度法测定几种野菜中抗坏血酸的含量[J].山东教育学院报,2006(2):132-134.
[8]曾翔云.维生素C的生理功能与膳食保障[J].中国食物与营养,2005(4):52-54.
[9]孙艳丽.2,4-二硝基苯肼法测定两种饮料中VC的含量[J].饮料工业,2014,17(4):34-37.
[10]武文,詹秀环,宣亚文.碘量法测定蔬菜中维生素C的含量[J].安徽农业科学,2009,37(21):9845-9846.
[11]孙鹏,王宁,孙先锋.两种方法对苹果中维生素C含量测定的比较[J].湖北农业科学,2011,50(16):3386-3388.
