不同因素对多硫化钙处理地下水中Cr(ⅤⅠ)效果影响
2015-12-06胡月赵勇胜沈勇王冬梅刘娜
胡月,赵勇胜,沈勇,王冬梅,刘娜*
1. 吉林大学环境与资源学院,吉林 长春 130021;2. 长春水务集团,吉林 长春 130041
不同因素对多硫化钙处理地下水中Cr(ⅤⅠ)效果影响
胡月1,赵勇胜1,沈勇1,王冬梅2,刘娜1*
1. 吉林大学环境与资源学院,吉林 长春 130021;2. 长春水务集团,吉林 长春 130041
选用多硫化钙为还原剂,进行地下水中Cr(VI)去除效果的研究。主要考察了多硫化钙投加量、溶液pH、温度、Mn(II)、Fe(III)、腐殖酸(HA)存在条件下,对多硫化钙处理Cr(VI)效果的影响。结果表明:当多硫化钙与Cr(VI)的摩尔比由1∶1变到5∶1时,去除率从41.03%增加到100.00%;溶液pH值从6.0增上升到9.0时,去除率下降27.16%;水环境温度由(7±1)℃增加到(27±1)℃时,去除率达到100.00%所需反应时间,缩短了4~6倍;当地下水中含有Mn(II),随着Mn(II)质量浓度升高(0.00~10.00 mg·L-1),Cr(VI)浓度低于检测线所需要的时间缩短3倍;当地下水中含有Fe(III),Fe(III)质量浓度从0.00 mg·L-1增加到10.00 mg·L-1,去除率增加9.05%;当地下水中含有HA(0.00~15.00 mg·L-1),去除率由99.31%降低至90.28%。(7)多硫化钙与六价铬的反应产物的X射线衍射光谱图像中2θ值为18.2°、19.36°、26.67°与Cr(OH)3,2θ值为23.02°与单质S的标准卡片匹配度较高。另外,对含有11.36 mg·L-1Cr(VI)实际污染地下水的处理效果表明,Cr(VI)的去除率达到99.78%,残留浓度达到GB/T 1448—1993地下水质量标准III类标准,说明多硫化钙修复实际铬污染地下水具有良好的应用前景。
多硫化钙;Cr(VI);Mn(II);Fe(III);腐殖酸;XRD
近年来,频繁的人类活动使地表水、地下水和土壤污染日益严重。由于其稳定性和难降解性,重金属污染治理成为国内外研究的热点和重点。铬是最常见的重金属污染物之一,广泛应用于冶金、电镀、颜料生产等行业中,工业生产过程中含铬废水不合理排放以及矿山开采中铬矿渣的随意堆放,使地表环境受到污染,通过地下水的补径排从而污染地下水。严重危害到人类的生存和健康(Papp,2000)。环境中的铬主要以六价和三价两种形态存在。其中Cr(VI)剧毒且致癌,易迁移;Cr(III)无毒,在水环境中主要以Cr(OH)3沉淀形态存在,且少量的三价铬是人体必须的微量元素(Brookins,1988)。铬的存在形态决定了其毒性、可迁移性和处理方法,水中的铬污染修复通常应用化学还原剂将Cr(VI)还原成Cr(III)(Schwartz,1989)。
化学还原法治理铬污染的理论依据是向水体中加入化学还原剂,从而改变铬在水体中的存在形态,降低其在环境中的迁移能力和生物可利用性。目前,广泛应用于水污染治理的化学还原剂有还原性铁粉、二价硫化物、硫代硫酸盐、亚硫酸盐和多硫化钙等(Ponder,等,2000;Thornton和Amonette,1999;FRUCHTER等,2000;Jacobsa等,2001;Seaman等,1999;LV等,2011)。近年来,多硫化钙由于其具有操作简便、安全性好、成本低廉、去除效率高、不造成二次污染等优点日益受到人们的关注,其与铬反应方程式如下:
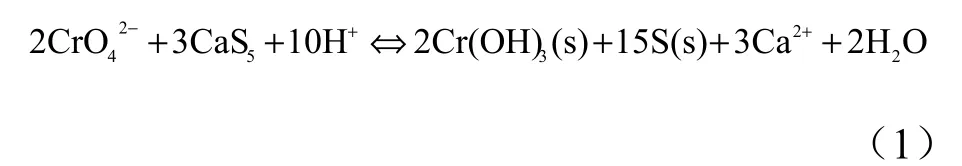
多硫化钙主要是将Cr(VI)还原成Cr(III)进而形成 Cr(OH)3沉淀去除,反应过程中产生的一部分Ca2+与水体中的SO42-结合生成CaSO4沉淀,缓解修复过程中对水体硬度的影响。目前,国外对多硫化钙的研究主要考察其对铬污染废水、地下水、铬渣及土壤污染的修复效果及降解动力学,鲜见环境中不同因素对其处理效果影响(MESSER等,2004;Charboneau等,2006;Storch等,2003;Jacobs,2001;Yahikozawa等,1978;Aratani等,1979)。在我国,未见应用多硫化钙修复铬污染地下水的报道。
本研究主要考察不同多硫化钙投加量、pH值、温度、铁锰阳离子、腐殖酸等因素对多硫化钙还原Cr(VI)的影响。同时对 Cr(VI)污染实际地下水样处理效果进行了探讨,处理前后硫及铬的形态进行了分析,该研究对Cr(VI)污染环境的修复具有一定的参考价值。
1 材料与方法
1.1 材料与仪器
1.1.1 实验材料
重铬酸钾,盐酸,活性炭,氢氧化钠,二苯基碳酰二肼,丙酮,HEPES,硫酸锰,三氯化铁,腐殖酸(北京化工厂)。以上除重铬酸钾为优级纯外,其余全是分析纯。实验所用多硫化钙来自上海某公司,体积分数为45%,每次实验开始时,取适量加水稀释到0.10 mg·L-1(0.58 mmol·L-1)。实验所用铬贮备液(100.00 mg·L-1),称取适量的重铬酸钾加水溶解。实验用水均为去离子水。
1.1.2 实验仪器
实验用到的实验仪器有PHS-3C型酸度计(杭州市东辰科技有限公司)、752型分光光度计(上海第三分析仪器厂)、SHIMADZU AUW220型分析天平(岛津国际贸易(上海)有限公司)、HJ-6型恒温磁力搅拌器(常州国华电器有限公司),881离子色谱仪(瑞士万通公司)。
1.2 实验方法
采用单一变量原则,研究多硫化钙投加量(CaS5与Cr(VI)摩尔比为1∶1、2∶1、3∶1、4∶1、5∶1)、pH(6.0、7.0、8.0、9.0)、温度((7±1)、(17±1)和(27±1) ℃)以及水中铁(0.00、1.70、5.00、10.00 mg·L-1)、锰(0.00、2.00、5.00、10.00 mg·L-1)、腐殖酸(0.00、5.00、10.00、15.00 mg·L-1)等存在时,模拟多硫化钙修复铬污染的影响,铬初始质量浓度为10.00 mg·L-1,pH实验的反应时间为24 min,其他模拟实验的反应时间为 2 h,磁力搅拌,每隔一定时间取样分析出水Cr(VI)浓度。另应用多硫化钙对沈阳某化工厂附近地下水样进行修复效果探究,水样中所含离子采用离子色谱法测定。
1.3 样品分析方法
1.3.1 Cr(ⅤⅠ)的测量方法
实验中所有样品中 Cr(VI)采用中国国家标准GB 7476—1987《二苯胺碳酰二肼分光光度法进行测定》(魏复盛,2002)。
1.3.2 X射线衍射
X射线衍射分析(XRD)通过D8 ADVANCE型X射线衍射仪(德国布鲁克公司)获得。其测试条件:Cuα靶,功率40 kV和80 mA,扫描速度为 0.1°/s,光源波长为 1.54 nm,角度范围为5°~60°。
2 结果与讨论
2.1 多硫化钙投加量对Cr(ⅤⅠ)去除效果的影响
设置CaS5与Cr(VI)摩尔比为1∶1、2∶1、3∶1、4∶1、5∶1,研究多硫化钙投加量对初始浓度为0.19 mmol·L-1(10.00 mg·L-1)的Cr(VI)的去除效果。结果(图1)表明,当CaS5与Cr(VI)摩尔比从1∶1变化到5∶1时,Cr(VI)的去除率从41.03%增加到接近100.00%。当CaS5与Cr(VI)摩尔比大于等于3时,反应24 min后,Cr(VI)的去除率无变化,出水 Cr(VI)质量浓度低于方法检测限(0.05 mg·L-1)。因此实验确定CaS5与Cr(VI)反应的最佳摩尔比为3∶1。
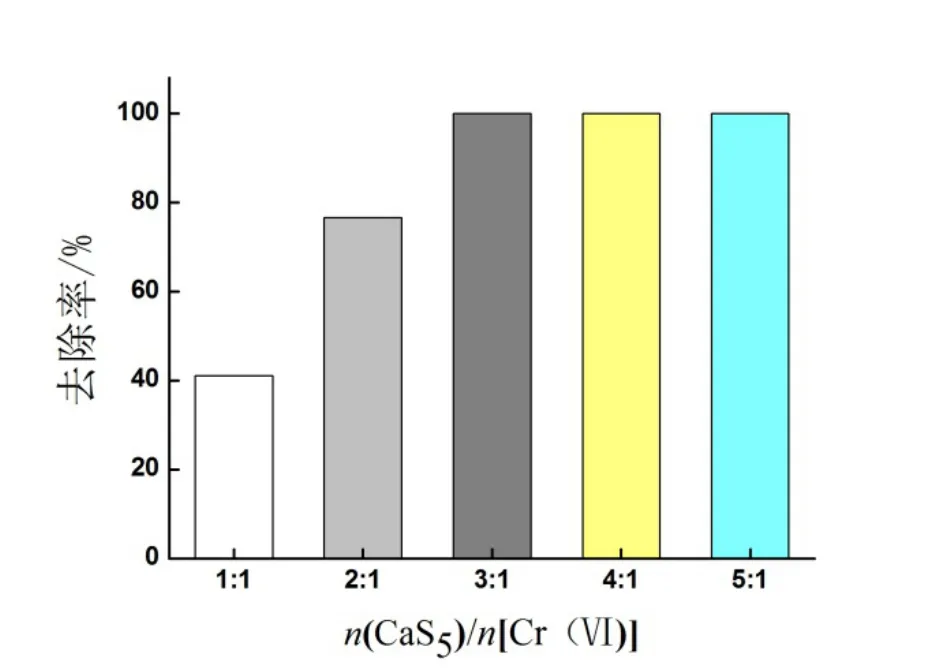
图1 CaS5与Cr(ⅤⅠ)的摩尔比对Cr(ⅤⅠ)去除率的影响Fig. 1 Effects on the removal rates by the different ratios of CaS5and Cr(VI)
2.2 初始pH与温度对Cr(ⅤⅠ)去除效果的影响
2.2.1 初始pH值对Cr(ⅤⅠ)去除效果的影响
调节溶液初始pH值为6.0、7.0、8.0、9.0时,考察多硫化钙对Cr(VI)的去除效果。由图2可知,当溶液初始pH值从9.0降低到6.0,Cr(VI)去除率增加;当初始pH为6.0反应初期Cr(VI)浓度迅速降低,时间为3 min时,去除率达100%。当初始pH为7.0时,反应24 min后,出水未检出Cr(VI)。而当初始pH为9.0时,反应3 min时,Cr(VI)质量浓度为5.91 mg·L-1,反应24 min后,Cr(VI)质量浓度为2.72 mg·L-1,去除率仅为72.8%,并没有被完全去除。以上研究结果表明,Cr(VI)污染地下水偏酸性时,有利于多硫化钙与Cr(VI)发生反应,根据方程式(1)可知,增加溶液中的H+浓度,有利于反应向生成物的方向进行。

图2 pH值变化对多硫化钙还原Cr(ⅤⅠ)效果的影响Fig. 2 Effects on the Cr(VI) reduction of Calcium polysulfide by the different pH values
2.2.2 温度对Cr(ⅤⅠ)去除效果的影响
模拟地下水环境温度,考察水环境温度发生变化时对Cr(VI)去除效果的影响,将反应体系温度设置为(7±1)、(17±1)和(27±1)℃。从图3可知,反应初期(3 min内)Cr(VI)的浓度迅速下降,在较高温度((27±1)℃)条件下,Cr(VI)的去除率达到100%,直到反应时间达到24 min,Cr(VI)一直没有被检出;在(7±1)和(17±1)℃条件下,反应12 min,Cr(VI)的去除率达到93.10%和97.51%,之后Cr(VI)的浓度缓慢降低,24 min时,去除率均接近100.00%。虽然较高温度有利于反应速度的加快,但反应时间达到24 min时,Cr(VI)的去除效果无明显差异。

图3 温度变化对多硫化钙还原Cr(ⅤⅠ)效果的影响Fig. 3 Effects on the Cr(VI) reduction of Calcium polysulfide by the different temperatures
2.3 Mn(Ⅰ)和Fe(ⅠⅠ)对Cr(ⅤⅠ)去除效果的影响
在天然水体中,尤其在东北三省地下水中普遍存在铁和锰含量超标的现象,而且,铁和锰均具有不同的氧化还原形态,因此有必要考察铁、锰浓度对多硫化钙还原Cr(VI)的影响。
2.3.1 Mn(ⅠⅠ)对Cr(ⅤⅠ)去除效果的影响
从图4可知,当Mn(II)的初始质量浓度为0.00、2.00、5.00、10.00 mg·L-1,当反应时间为15 min时,Cr(VI)去除率分别为 45.36%、64.78%、77.95%、91.53%;当反应时间60 min时,Cr(VI)去除率分别为83.06%、95.56%、99.72%、100.00%;当反应时间为2 h时,不添加Mn(II)的反应体系中Cr(VI)去除率为97.23%,其他添加不同浓度Mn(II)反应体系中,Cr(VI)的去除率均达到100%。由此可见,向反应体系中添加Mn(II),加快CaS5与Cr(VI)的反应速率,Mn(II)浓度越高,多硫化钙与 Cr(VI)反应速率越快。这主要是因为Mn(II)属于锰还原形态,可被Cr(VI)氧化形成MnO2,Cr(VI)被还原成Cr(III)。反应式为:


图4 Mn(Ⅰ)浓度变化对Cr(ⅤⅠ)浓度降低的影响Fig. 4 Effects on the Cr(VI) reduction of Calcium polysulfide by different Mn(II) concentrations
因此,随着 Mn(II)浓度的增加,Cr(VI)的去除率和去除速度增加。
2.3.2 Fe(ⅠⅠⅠ)对Cr(ⅤⅠ)去除效果的影响
选择Fe(III)质量浓度分别为0.00、1.70、5.00、10.00 mg·L-1,考察其对Cr(VI)去除效果的影响,结果如图 5所示。从整体处理效果而言,没有添加Fe(III)的反应体系处理效果优于添加 Fe(III)的反应体系,分析原因主要是因为Fe(III)可与多硫化钙发生氧化还原反应形成二价铁和硫,消耗部分多硫化钙,降低其对Cr(VI)的去除效果。然而在添加3种不同浓度Fe(III)的反应体系中,随着Fe(III)浓度的增加,Cr(VI)的去除率增加,主要是因为整个反应体系成碱性,Fe(OH)3的溶度积常数为 1.1×10-36,较低,当 Fe(III)浓度较高时,会形成大量的Fe(OH)3沉淀,Fe(OH)3具有较好的吸附性能,可与 Cr(VI)形成共沉淀,从而将其从溶液中去除。因此相比较而言较高的 Fe(III)浓度有利于其对Cr(VI)的去除。

图5 Fe(ⅠⅠ)浓度变化对Cr(ⅤⅠ)浓度降低的影响Fig. 5 Effects on the Cr(VI) reduction of Calcium polysulfide by the different Fe(III) concentrations
2.4 腐殖酸(HA)对Cr(ⅤⅠ)去除效果的影响
腐殖酸是地球生态环境中广泛存在的天然有机物,约占土壤有机物总量的 50%~80%。通过水循环,腐殖酸随水体流动从土壤、地表水体中淋滤渗漏到潜水含水层中。高腐殖酸地下水中铬污染修复问题少有报道。本节考察腐殖酸对多硫化钙还原Cr(VI)的影响。
腐殖酸对多硫化钙去除Cr(VI)的影响见图6。可以看出,HA的初始质量浓度分别为0.00、5.00、10.00和15.00 mg·L-1时,未添加HA的反应体系去除效果总体优于添加HA反应体系。可见 HA存在时,抑制多硫化钙与Cr(VI)的反应。而且HA的添加量越多对 Cr(VI)去除抑制作用越明显,主要原因可能为HA含有大量的羟基、羧基等基团与 Cr(VI)发生了螯合作用,降低其与多硫化钙的接触几率与反应效能。
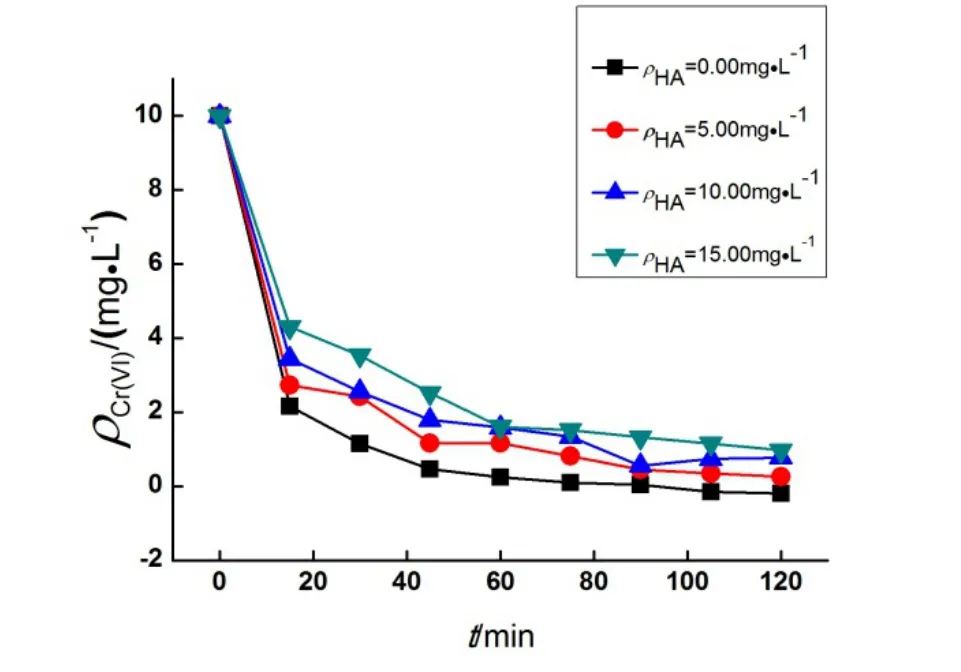
图6 HA浓度变化对Cr(ⅤⅠ)浓度降低的影响Fig. 6 Effects on the Cr(VI)reduction of Calcium polysulfide by the HA concentrations
2.5 XRD实验数据分析
2.5.1 多硫化钙性质简介
实验所用多硫化钙购买于上海某公司,该试剂是采用石灰与单质硫在特定条件下合成,其中多硫化钙的含量为 45%。试剂呈碱性,无毒,与氧气反应生成Ca2+、SO42-和S0,其XRD图谱如图 7所示。试剂中的主要成分为 CaS5,并含有CaSO4、CaO、S等杂质。XRD分析时,由于多硫化钙粉末暴露在空气中,与氧气反应,测定结果中含有硫酸钙。

图7 多硫化钙XRD图谱Fig. 7 XRD pattern for Calcium polysulfide

图8 XRD衍射图谱图像Fig. 8 XRD pattern for the precipitations
2.5.2 多硫化钙与Cr(ⅤⅠ)反应产物XRD分析
为研究Cr(VI)与多硫化钙的反应机制,收集反应生成的沉淀、风干、表征。X射线衍射图像(图8)表明多硫化钙与Cr(VI)反应后生成Cr(OH)3和单质S。其中2θ值为18.2°、19.36°、26.67°分别对应(001)、(100)、(101)晶型衍射峰(JCPDS No. 16-0817),证明Cr(VI)被还原成Cr(III)时,生成的Cr(OH)3沉淀结晶行较好。2θ值为23.08°与S标准卡片(S形态222晶型,JCPDS card No. 08-0247)匹配度较高,证明多硫离子发生氧化反应,产物为单质S。
2.6 多硫化钙修复铬污染地下水
实验所用铬污染水体来自沈阳某化工厂附近的地下含水层,水中含有铬11.36 mg·L-1,其pH值为6.67,含有Na+(199.40 mg·L-1)、K+(2.52 mg·L-1)、Ca2+(22.81 mg·L-1)、Mg2+(2.14 mg·L-1)、Cl-(4.30 mg·L-1)、SO42-(8.64 mg·L-1)、F-(0.138 mg·L-1)等常见离子。向水中加入0.10 mg·L-1的多硫化钙溶液,处理效果如图9所示。反应2 h,水中Cr(VI)的去除率达到99.78%,出水Cr(VI)浓度达到GB/T 1448—1993地下水质量标准III类标准。

图9 多硫化钙修复铬污染地下水Fig. 9 The reduction of chromiun by Calcium polysulfide
3 结论
多硫化钙去除地下水中 Cr(VI)具有较好的效果,对实际地下水Cr(VI)污染修复具有一定的指导作用。研究表明,10.00 mg·L-1Cr(VI)污染地下水投加0.10 mg·L-1CaS5,反应过程中,Cr(VI)彻底转化为Cr(OH)3沉淀,多硫离子被氧化成单质S,出水中Cr(VI)达到GB/T 1448—1993地下水质量标准III类标准,可用于工业、农业用水。水环境呈中性、弱酸性或温度较高时,有利于Cr(VI)从地下水中去除,可缩短Cr(VI)修复所需时间。当地下水中含有Mn(II)、Fe(III)、腐殖酸(HA)等物质时,Mn(II)与Cr(VI)反应和多硫化钙与 Cr(VI)反应相互促进;低浓度Fe(III)的存在可抑制CaS5与Cr(VI)反应,高浓度的Fe(III)可共沉淀去除Cr(VI)。地下水中的腐殖酸(HA)与低浓度的Cr(VI)形成螯合物,抑制多硫化钙与Cr(VI)反应。向含11.36 mg·L-1的铬污染地下水中投入0.10 mg·L-1的多硫化钙溶液,Cr(VI)的出水浓度达到GB/T 1448—1993地下水质量标准III类标准,证明多硫化钙修复地下水铬污染可行。
ARATANI T, YAGSUHARA S, MATOBA H, et al. 1979. Continuous removal of heavy metals by the lime sulfurated solution (calcium polysulfide) process[J]. Bulletin of the Chemical Society of Japan, 52(1): 218-222.
BROOKINS D G. 1988. Eh-pH diagrams for geochemistry[M]. Springer-Verlag, Berlin.
CHARBONEAU B, THOMSON K M, WILDE R, et al. 2006. Hanford groundwater remediation[J]. Proceedi-ngsof the WM'06 conference. Tuscon, AZ.
FRUCHTER J S, COLE C R, WILLIAMS M D, et al. 2000. Creation of a subsurface permeable treatment zone for aqueous chromate contamination using in situ redox manipulation[J]. Groundwater Monitoring & Remediation, 20(2): 66-77.
JACOBS J. 2001. In situ delivery methods for remediation of hexavalent chromium in soil and groundwater[J]. In National Meeting of the National Association of Engineering Geologists and American Institute of Professional Geologists, St. Louis, Mo.
JACOBSA J, HARDISION R L, ROSE J. 2001. In-situ remediation of heavy metals using sulfur-based treatment technologies[J]. Hydrovisions, 10(2): 1-4.
LV X, XU J, JIANG G, et al. 2011. Removal of chromium (VI) from wastewater by nanoscale zero-valent iron particles supported on multiwalled carbon nanotubes[J]. Chemosphere, 85(7): 1204-1209.
MESSER A, STORCH P, PALMER D. 2004. In-site remediation of chromium-contaminated site using calium polysulide[M]. Internal report URS Corporation.
PAPP J F. 2000. Chromium[EB], http://www.chromium-asoc.com/thcrfl. htm,6p.
PONDER S M, DARAB J G, MALLOUK T E. 2000. Remediation of Cr (VI) and Pb (II) aqueous solutions using supported, nanoscale zero-valent iron[J]. Environmental Science & Technology, 34(12): 2564-2569.
SCHWARTZ L M. 1989. More on autocatalytic reaction data analysis[J]. Journal of Chemical Education, 66(8): 677.
SEAMAN J C, BERTSCH P M, SCHWALLIE L. 1999. In situ Cr (VI) reduction within coarse-textured, oxide-coated soil and aquifer systems using Fe (II) solutions[J]. Environmental Science & Technology, 33(6): 938-944.
STORCH P, MESSER A, PALMER D, et al. 2003. Pilot test for in situ geochemical fixation of chromium(VI) using calcium polysulfide[J]. Proceedings of Third International Conference on Remediation of Chlorinated and Recalcitrant Compounds. Battelle Press, Monterey, California.
THORNTON E C, AMONETTE J E. 1999. Hydrogen sulfide gas treatment of Cr (VI)-contaminated sediment samples from a plating-waste disposal site implications for in-situ remediation[J]. Environmental Science & Technology, 33(22): 4096-4101.
YAHIKOZAWA K, ARATANI T, ITO R, et al. 1978. Kinetic studies on the lime sulfurated solution (calcium polysulfide) process for removal of heavy metals from wastewater[J]. Bulletin of the Chemical Society of Japan, 51(2): 613-617.
魏复盛. 2002. 国家环境保护总局和水和废水监测分析方法编委会. 水和废水监测分析方法[M]. 3版. 北京: 中国环境科学出版社: 346-349.
Effects of Different Factors on the Cr(VI)-contaminated Ground Water Treatment by Calcium Polysulfide
HU Yue1, ZHAO Yongsheng1, SHEN Yong1, WANG Dongmei2, LIU Na1*
1. College of Environment and Resource, Jilin University, Changchun 130021, China; 2. Changchun Water Group, Changchun 130041, China
Effectiveness of chromium reduction by calcium polysulfide was the obiective of this paper. Factrors were investigated such as pH, CaS5concentrations, temperature and Mn(II), Fe(III), HA-contained water. When the rato of CaS5and Cr(VI) ranged from 1∶1 to 5∶1, the Cr(VI) reduction rate inceased from 41.03% to 100.00%; The pH value of the water environmemt differed from 6.0 to 9.0, the reduction rate of Cr(VI) was 27.16%; The balance time was shorten 4~6 times when temperature of the water environmemt rised from (7±1) ℃ to (27±1) ℃; As Mn(II) was the principal component of Cr(VI)-contained water, the higher Mn(II) concentration(0.00~10.00 mg·L-1), the faster reaction velocity between CaS5and Cr(VI); The concentration of Fe(III) consisting in groundwater transfered from 0.00 mg·L-1to 10.00 mg·L-1, the removal rate increased by 9.05%; When HA existed in the ground water(0.00~15.00 mg·L-1), the Cr(VI) reduction rate varied from 99.31% to 90.28%; The XRD showed the products of the reaction between calcium polysulfide and hexalvant chromium were Cr(OH)3and S, whose 2θ degree corresponded to 18.2°, 19.36°, 26.67° and 23.02°. When calcium polysulfide treated 11.38 mg·L-1Cr(VI)-contami-nated ground water ,removal rate of Cr(VI) can reach 90.28%. Output concentration of Cr(VI) can reach to III class of Quality standard for groundwater GB/T 1448-93. Calcium polysulfide has been found a promising reductant in the treatment of Cr(VI)-contained groundwater.
calcium polysulfide; chromium; Mn(II); Fe(III); HA; XRD
10.16258/j.cnki.1674-5906.2015.02.017
X131.2
A
1674-5906(2015)02-0294-06
胡月,赵勇胜,沈勇,王冬梅,刘娜. 不同因素对多硫化钙处理地下水中Cr(VI)效果影响[J]. 生态环境学报, 2015, 24(2): 294-299.
HU Yue, ZHAO Yongsheng, SHEN Yong, WANG Dongmei, LIU Na. Effects of Different Factors on the Cr(VI)-contaminated Ground Water Treatment by Calcium Polysulfide [J]. Ecology and Environmental Sciences, 2015, 24(2): 294-299.
国家自然科学基金项目(41372236)
胡月(1989年生),女,硕士,主要从事地下水重金属污染修复。E-mail:huyuejj@126.com *通讯作者:刘娜,女,教授,博士生导师,主要从事污染水土生物修复研究。E-mail:liuna@jlu.edu.cn
2015-02-04
