吡咯烷酮-2类衍生物的合成及其抑菌活性
2015-12-02李齐激杨小生
李 伟,李齐激,杨小生,*
(1.贵州大学药学院,贵州 贵阳 550025;2.贵州省中国科学院天然产物化学重点实验室,贵州 贵阳 550002)
吡咯烷酮类化合物是自然界存在的一类生物碱,在合成药物中也有着广泛的应用。吡咯烷酮类作为经典的生物碱骨架表现出了各种显著的生理活性,很多吡咯烷酮类化合物及其衍生物被证实具有良好的抗菌活性[1-4],因此对此类活性化合物的研究开发一直是国内外热点。
郝小江等学者参考活性显著的吡咯烷酮结构[5-6]设计、合成了系列吡咯烷酮 -2类化合物,并发现抗老年痴呆候选药物—芬克罗酮,现已经通过II期临床试验[7]。我们在开展吡咯烷酮-2类化合物研究时发现某些化合物表现出一定的抑菌活性。鉴于此,我们参考相关文献资料[8-11],以芬克罗酮为起始原料,对其1位酰胺氮进行结构衍生,寻找具有较好抗菌活性的先导物。
1 材料与方法
1.1 材料
所用化学试剂乙酸乙酯、石油醚、二甲基甲酰胺、乙醇、二氧六环 (天津科密欧化学试剂有限公司)等均为分析纯;必要时经过干燥处理;柱层析硅胶为青岛海洋化工厂产品。
1.2 菌种
金黄色葡萄球菌、大肠杆菌、酵母菌均由贵州省、中国科学院天然产物化学重点实验室分离纯化。
1.3 仪器
油浴反应器(上海耀特仪器厂),真空干燥机(天津泰斯特仪器有限公司),INOVA 400M核磁共振波普仪(TMS内标)(美国瓦里安公司),HP-5973型质谱仪测定分子量,旋转蒸发仪,磁力搅拌器(上海司乐仪器有限公司),DHZ-C恒温培养箱(江苏太仓市实验设备厂),80-2电动离心机(金坛市晶玻实验仪器厂),LDZX-50KBS立式压力蒸汽灭菌器(上海中安医疗器械厂)。
1.4 实验方法
1.4.1 目标产物设计合成 以吡咯环的N位活性位点为切入点,参考[8-11]等文献资料,进行化学修饰。产物合成图示及方法见图1。

图1 目标产物合成Fig.1 synthesis of target compounds
1.4.1.1 化合物2的合成:取0.1 mol化合物1于反应瓶中,以20ml二甲基甲酰胺溶解,后加入0.1 mol溴代乙酸乙酯,磁力搅拌下加入约0.2 mol的碳酸钾,室温下氮气保护反应,TLC检测反应进度。4 h后反应完毕,反应液以乙酸乙酯和水萃取,有机相回收,产物粗品经硅胶减压柱分离(石油醚∶乙酸乙酯=1∶1)得到产物2,白色固体,收率84%。
1.4.1.2 化合物3的合成:取0.05 mol化合物2于反应瓶中,加15 ml无水乙醇溶解,以滴管加入0.1 mol的乙胺和0.1 mol的碳酸钾,室温搅拌10 min后置于回流装置,80℃下回流反应。7 h后反应完毕,反应液以乙酸乙酯和水萃取,有机相回收,产物粗品经硅胶减压柱分离(石油醚∶乙酸乙酯=1∶2)得到产物3,淡黄色固体,收率75%。
1.4.1.3 化合物4的合成:取0.1 mol的化合物1于反应瓶中,取20ml二甲基甲酰胺将其溶解,后加入0.12 mol的碘甲烷,磁力搅拌下加入0.2 mol的氢化钠,氮气保护下室温条件反应,TLC检测反应进度。4 h后反应完毕,反应液以0.2 mol/L氯化铵溶液淬灭,乙酸乙酯和水萃取,有机相回收,产物粗品经硅胶减压柱分离(石油醚∶乙酸乙酯=1∶1)得到产物4,白色固体,收率96%。
1.4.1.4 化合物5的合成:取0.1 mol的化合物1溶解于25 ml干燥的二氧六环中,加入0.15 mol的丙烯酰胺,磁力搅拌下溶解。后加入0.2 mol的氢化钠,室温下氮气保护反应,TLC检测反应进度。5 h后反应完毕,反应液以0.2 mol/L氯化铵溶液淬灭,乙酸乙酯和水萃取,有机相回收,产物粗品经硅胶减压柱分离(石油醚∶乙酸乙酯=1∶2)得到产物5,黄色固体,收率81%。
1.4.1.5 化合物6的合成:取0.1 mol的化合物1于反应瓶中,取20 ml二甲基甲酰胺将其溶解后,加入0.12 mol的溴代戊烷,磁力搅拌下加入0.2 mol的氢化钠,氮气保护室温条件下反应,TLC检测反应进度。4 h后反应完毕,反应液以0.2 mol/L氯化铵溶液淬灭,乙酸乙酯和水萃取,有机相回收,产物粗品经硅胶减压柱分离(石油醚∶乙酸乙酯=1∶1)得到产物6,白色固体,收率95%。
1.4.2 抑菌试验 采用滤纸片法[12-13],对目标产物进行活性测试。选择了G+菌(金葡菌)、G—(大肠杆菌)和真菌(酵母菌)三个菌种,以四环素和纳他霉素作阳性对照药,设置药物浓度为1.0 mmol/L,每个药物设置三个平行试验取平均值。圆形滤纸片直径5 mm,置于配制好浓度的药液中浸泡5 min以上,备用;将活化的菌种于液体培养基中培养24 h,以移液枪取30 uL均匀涂于平板培养基表面,于平板背面取均匀取六个点,并用记号笔打点、标记,作为滤纸片放置点。然后取在一定浓度药液中浸泡的滤纸片轻放于对应的标记点上,密封,所有操作均应在无菌环境中进行。将密封好的培养基分类,细菌组培养基放置在35℃恒温箱中,真菌组置于28℃恒温箱,24 h后取出观察是否有抑菌圈,并以电子卡尺测量抑菌圈直径。
2 结果与分析
2.1 目标产物的合成
合成了5个化合物,其中产物2和3分别为N-H的酯取代和酰胺取代产物,产物4和6为N-H直链脂肪烃取代衍生物,产物5是经迈克尔加成得到的β-酰胺衍生物,且末端胺为裸露伯胺。各产物经MS、1H NMR、13C NMR进行结构鉴定(见表1)。

表1 目标产物波谱数据Tab.1 Chemical Properties of Target Compounds
2.2 目标产物的抗菌结果
对五个产物以及阳性对照药进行抑菌试验,电子卡尺精密测量抑菌圈直径,取三组平行试验的平均值,结果见表2。化合物4和6抑菌圈大小接近于阳性对照药,对金葡菌有较好的抑菌效果,同时对酵母菌也有明显的抑制作用。化合物3显示有一定的酵母菌抑制效果,而5则表现出较强的酵母菌抑制效果。
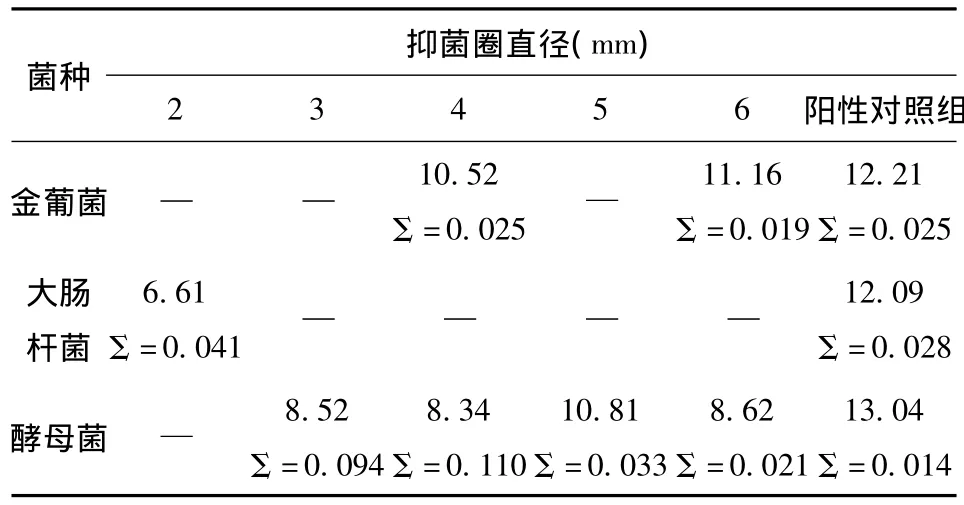
表2 各化合物抑菌效果Tab.2 Antibacterial effect of compounds
3 结论与讨论
实验结果表明,对芬克罗酮的1-NH进行化学修饰后显现出较为明显的抗菌活性。被脂肪烃取代的化合物4和6对金葡菌抑制效果明显,虽不及阳性对照四环素,但在结构上可能具有独特的优势,且这两个化合物对酵母菌也有明显的抑制作用,显示其抑菌谱较广;化合物3和5的1-NH被酰胺取代,对酵母菌表现出抑菌效果,其中5的末端酰胺为伯胺,抑菌活性强于末端酰胺为仲胺的化合物3;而1-NH被酯取代时,没有表现出抑菌活性。本实验基于对若干衍生物活性的初步考察,考察菌种比较局限,因此对其他菌种如铜绿假单胞、白色念珠菌以及其他霉菌、孢菌的抑菌能力尚不明确,我们将在后续研究中进行考察,同时与文献报道的 cynthichlorine[3]和 N-hydroxyaristolam[4]等抑菌活性良好的吡咯烷酮类化合物进行比较。研究结果表明此类衍生结构有一定应用价值,同时也显示出其它类似物值得进行更广泛的研究。
[1]李园园,卢 鑫,朱显峰,等.微米级花状结构铜/聚乙烯吡咯烷酮的制备及其抗菌性能[J].化学研究,2012,23(4):65-69.
[2]Abourriche A,Abboud Y,M aoufoud S,et al.Cynthichlorine:a bioactive alkaloid from the tunicate Cynthia savignyir[J].IlFarmaco,2003,58:1 351-1 354.
[3]Qureshi A,Colin P L,Faulkner D J.Microsclerodermins F-I,antitum or and antifungal cyclic peptides from the Lithistid-Sponge Micruscleroderma sp.[J].Tetrahedron,2000,56:3 679-3 685.
[4]Tabopda T K,Ngoupayo J,Iiu J,et al.Bioaetive aristolaetams from Piper umbellatum[J].Phytochemistry,2008,69:1 726-1 731.
[5]Hou RL,Bi LY,Wang F,et al.Clausenamide improves COX-2 expression in diabetic rats[J].Afr.J.Pharm.Pharmacol.,2012,6:1 520-1 525.
[6]Alex HG,Alexander S.Piracetam and other structurally related nootropics[J].Brain Res Rev,1994,19:180-222.
[7]张雯雯,钱 洁.抗老年痴呆新药开发完成Ⅰ期临床[J].中国科学基金,2008,5:316.
[8]郭 瑞,赵艳艳,韦 鹏,等.4-(1-甲基胍基)丁酸的合成、表征和抑菌活性[J].食品工业科技,2011,32(9):87-89.
[9]燕乐乐,刘幸平,程康华,等.三唑类化合物的合成及抑菌活性[J].南京林业大学学报,2014,38(2):161-164.
[10]王 丽,何深远,程康华,等.粉唑醇的化学改性及其衍生物的抑菌活性[J].东北林业大学学报,2014,42(8):153-155.
[11]宁国慧,赵温涛,唐向阳.3-(2,6二氯苯基)-5-(1-吡咯烷酮基)-2,3-异噁唑啉的合成及抑菌活性研究[J].化学与生物工程,2014,31(9):36-38.
[12]王 英,尹显慧,王 梅,等.几种杀菌剂对番茄青枯病菌的抑菌活性[J].山地农业生物学报,2014,33(3):8-12.
[13]易 萌,王艳明,董德成,等.淫羊藿内生真菌的分离及抑菌活性研究[J].江苏农业科学,2014,42(3):327-329.
