先天性肾性尿崩症伴低促性腺激素性性腺功能减退症1例并文献复习
2015-12-02刘静王永华陈志红李堂
刘静,王永华,陈志红,李堂
(青岛大学附属医院,山东青岛266003)
肾性尿崩症是由于精氨酸加压素(AVP)不能与肾脏AVP受体有效作用,以致肾小管不能浓缩尿液,从而持续排出大量低渗尿的一组临床综合征。肾性尿崩症包括先天性和获得性两大类,先天性肾性尿崩症(CNDI)是由于编码AVP受体的相关基因突变,导致AVP受体合成或功能发生障碍,其中约90%为定位于染色体Xq28的编码AVP受体2(AVPR2)基因突变所致,不足10%为定位于常染色体12q13上的编码水孔蛋白2(AQP2)基因突变引起[1,2]。CNDI临床较少见,目前国内尚缺乏相关流行病学调查资料。本研究回顾性分析2014年2月我院收治的1例AVPR2基因突变所致CNDI同时伴低促性腺激素性性腺功能减退症(HH)患者的临床资料,并复习相关文献。
1 病例资料
患儿男,10岁,因“多饮、多尿10年,体质量快速增加4年”收入青岛大学附属医院内分泌儿科。患儿为第一胎第一产,足月剖宫产,出生体质量3 500 g。自幼多饮、多尿,1岁时于外院就诊,考虑为精神性烦渴,建议适当限水,未给予特殊治疗。近4年来体质量增加快速并伴有轻度学习障碍。父母非近亲结婚,否认家族中有类似疾病史。体格检查:身高 144 cm,体质量61 kg,BMI 29.41,HR 98 次/min,呼吸18次/min,血压120/80 mmHg。全身皮肤未见紫纹、痤疮,无颈蹼,颈部皮肤可见黑棘皮样改变;水牛背;嗅觉正常;心、肺、腹查体无异常;外生殖器检查阴茎长4 cm,双侧睾丸体积均1.5 mL。临床检查:①针对多饮、多尿行禁水试验、泌尿系统超声及颅脑磁共振检查。禁水试验:试验前体质量61 kg、血压120/80 mmHg、血钠 142.9 mmol/L、血渗透压302.56 mOsm/L、尿渗透压 80 mOsm/L、尿比重1.002,禁水 6 h 体质量 59.5 kg、血压 115/70 mm/Hg、血钠 147 mmol/L、血渗透压 311.4 mOsm/L、尿渗透压200 mOsm/L。给予试验性醋酸去氨加压素治疗3天,患儿多饮、多尿症状无改善。泌尿系统超声及颅脑磁共振检查均无明显异常。②针对体型肥胖行血皮质醇、促肾上腺皮质激素、胰岛素检测,生化全套及腹部超声检查。血皮质醇8:00 228.66 nmol/L、16:00 213.52 nmol/L,促肾上腺皮质激素8:00 11.6 pg/mL,胰岛素 116.82 pmol/L,ALT 68 U/L,AST 43.9 U/L,TG 2.69 mmol/L,TC 5.49 mmol/L,HDL-C 1.11 mmol/L,LDL-C 3.8 mmol/L,空腹血糖4.74 mmol/L;腹部超声示中度脂肪肝。③性激素检查示卵泡刺激素<0.05 IU/L,黄体生成素 0.02 IU/L,睾酮 0.52 ng/mL,雌二醇 < 10 pg/mL;促性腺激素释放激素激发试验示卵泡刺激素2.99 IU/L,黄体生成素 0.76 IU/L;三日绒毛膜促性腺激素激发试验示睾酮1.017 ng/mL。④采用目标区域捕获测序技术检测OMIM数据库中与遗传病相关的全部基因。取患儿血液样本,DNA提取试剂盒提取基因组DNA;利用Bioruptor全自动超声破碎仪将DNA片段化,使用DNA文库构建试剂盒构建文库;目标区域捕获富集,序列捕获采用定制的罗氏Nimblegen特异性芯片进行,捕获后对目标区域进行PCR扩增;使用Hiseq 2500高通量模式对上述产物进行测序;通过数据过滤去掉低质量的测序序列,与参考基因组系列比对,对点突变、插入缺失突变等进行统计和分析;对阳性结果采用聚合酶链反应结合Sanger测序进行验证。基因检测发现该患儿存在AVPR2基因的一个点突变:C.875T>C,即AVPR2基因第875位点的碱基T被C替换,致使受体蛋白第292位的亮氨酸被脯氨酸所替代(图1)。
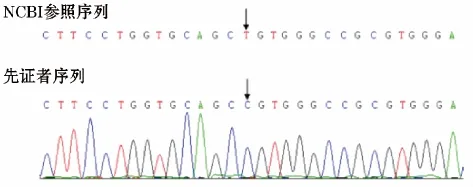
图1 基因检测结果
根据上述检查结果结合临床症状、体征,AVPR2基因突变所致CNDI诊断明确,同时考虑伴有HH。给予调整饮食结构,低钠饮食;口服氢氯噻嗪50 mg/次、2次/天,肌肉注射绒毛膜促性腺激素2 000 IU/次、2次/周,治疗1个月;1个月后复诊,患儿多饮、多尿症状明显改善,继续用上述药物治疗;3个月后复诊,睾丸体积无明显改善,睾酮0.38 ng/mL,考虑临床效果欠佳,遂给予人绒毛膜促性腺激素(2 000 IU/次、2次/周)联合人绝经期促性腺激素(75 IU/次、2次/周)治疗;6个月后复查睾丸体积增大(2 mL),睾酮0.6 ng/mL,效果较好。后因个人原因自行停用促性腺激素类药物,目前患儿睾丸体积增长不满意,睾酮水平未再检测。
2 讨论
CNDI是一组较为少见的遗传异质性疾病,仅占所有尿崩症患者的10%。目前研究认为,该病的发生机制主要是AVPR2基因或AQP2基因突变导致AVP受体合成或功能发生障碍,其中由AVPR2基因突变引起的 X-连锁 CNDI是其主要类型。自1992年van den Ouweland等首次报道人AVPR2基因突变致X-连锁CNDI以来,到目前为止,全世界已报道约221种AVPR2致病基因突变和21种未致病基因突变[3,4]。
AVPR2基因突变类型上最常见的为错义突变(约占48%),其次为无义突变、缺失突变、插入突变、剪接位点突变等[5,6]。目前研究认为,AVPR2 基因突变导致受体缺陷主要分为四型[4,7]:Ⅰ型:突变基因干扰 mRNA正常转录和翻译,如 W71X、458delG等。Ⅱ型:突变受体滞留在内质网,该型突变基因尽管能被正常转录和翻译,但是编码的受体因错误折叠而滞留在内质网中,同时被蛋白酶体降解,造成受体后信号转导途径中断,如S167T等,此型突变最为常见(约占50%)。Ⅲa型:突变受体与G蛋白耦联障碍。突变受体蛋白虽错误折叠却未被滞留在内质网中,仍能表达于细胞膜表面,但是干扰了信号转导途径中与G蛋白的结合,进而减少细胞内cAMP活性及下游信号分子的产生,如D85N、P322S等。Ⅲb型:突变受体与AVP结合异常。突变受体虽然能在细胞膜表面正常表达,但是与AVP结合能力减弱或丧失,如delR202。Ⅳ型:突变受体异常定位于胞质内囊泡结构中。突变基因能编码合成正常受体蛋白,但在细胞内错误定位,不能正常表达于细胞膜表面,如R137H。
本例通过基因检测发现其AVPR2基因第875位点存在1个错义突变,即C.875T>C,致使受体蛋白第292位的亮氨酸被脯氨酸所替代。该突变又称为L292P突变,曾于1994年由Wenkert等[8]报道并作了详细的功能性研究。研究发现,L292P突变属于Ⅱ型AVPR2基因突变,即L292P突变受体可能因错误折叠而滞留在细胞内,因不能组装到细胞膜上以致无法与AVP结合,从而出现CNDI的相关临床症状[9]。
CNDI的所有临床表现几乎都是由于多尿而引起的。成人患者常表现为多尿、多饮、低渗尿液;新生儿易出现反复易激惹、呕吐、喂养困难、体质量增长缓慢、发热、便秘及脱水等,长期反复脱水与高钠血症可导致生长发育迟缓、智力低下以及泌尿系统相关并发症,如双侧输尿管轻度扩张至严重肾积水及肾功能受损等[10,11]。值得注意的是,国内一项较大样本CNDI临床研究发现,国内患者就诊时间及确诊时间(平均8岁)均明显晚于国外报道(平均9个月),误诊率亦较高[12]。本例患儿亦符合这一研究结果。其原因可能与国内患儿临床表现不明显、家长忽视以及临床工作者对该病诊断意识相对缺乏有关。提高对CNDI的认识,早期诊断CNDI,避免出现相应并发症和生活质量下降是CNDI临床诊疗的关键。
目前,CNDI的治疗方法主要是针对尿液浓缩功能障碍的对症治疗,常规采用低钠饮食,补充足量水分防止脱水的发生,治疗药物包括氢氯噻嗪、阿米洛利和吲哚美辛等[13]。本例采用氢氯噻嗪单药治疗,多饮、多尿症状明显改善。但是传统治疗方法仅在一定程度上缓解多尿、多饮的临床症状,并非是对因治疗。近年来药物伴侣如AVPR2拮抗剂与AVPR2激动剂等在恢复突变受体功能活性方面取得较大进展,为CNDI的治疗开辟了新的途径[14]。但由于其药效受多种因素影响以及安全性等问题,目前尚未应用于临床,仍需更多的研究来进一步评价。
HH是由于下丘脑和(或)垂体异常,导致促性腺激素和性激素分泌减少,进而引起性腺功能减退的一组异质性疾病。HH可分为先天性和获得性两大类,联合采用促性腺激素释放激素激发试验和三日绒毛膜促性腺激素激发试验诊断先天性HH的特异性可达100%,敏感性可达90%[15]。本例合并HH,无嗅觉减退或缺失,无其他垂体分泌激素异常,排除下丘脑-垂体-性腺轴的占位性、浸润性等病理改变,考虑为先天性HH。在治疗上,首先给予人绒毛膜促性腺激素治疗,3个月后随访临床效果欠佳,遂改用人绒毛膜促性腺激素+人绝经期促性腺激素治疗,6个月后随访临床效果满意。
既往国内赵丹青等[16]曾报道1例CNDI合并生长激素缺乏症的病例。CNDI合并HH在国内外尚属首次报道,CNDI是否可以合并出现生长激素、性激素分泌障碍等多种内分泌紊乱,其在发病机制上两者是否存在相关性,尚有待于进一步研究。
[1]Moeller HB,Rittig S,Fenton RA.Nephrogenic diabetes insipidus:essential insights into the molecular background and potential therapies for treatment[J].Endocr Rev,2013,34(2):278-301.
[2]Hong CR,Kang HG,Choi HJ,et al.X-linked recessive nephrogenic diabetes insipidus:a clinico-genetic study[J].J Pediatr Endocrinol Metab,2014,27(1-2):93-99.
[3]Spanakis E,Milord E,Gragnoli C.AVPR2 variants and mutations in nephrogenic diabetes insipidus:review and missense mutation significance[J].J Cell Physiol,2008,217(3):605-617.
[4]Wesche D,Deen PM,Knoers NV.Congenital nephrogenic diabetes insipidus:the current state of affairs[J].Pediatr Nephrol,2012,27(12):2183-2204.
[5]Sasaki S,Chiga M,Kikuchi E,et al.Hereditary nephrogenic diabetes insipidus in Japanese patients:analysis of 78 families and report of 22 new mutations in AVPR2 and AQP2[J].Clin Exp Nephrol,2013,17(3):338-344.
[6]Anesi L,de Gemmis P,Galla D,et al.Two new large deletions of the AVPR2 gene causing nephrogenic diabetes insipidus and a review of previously published deletions[J].Nephrol Dial Transplant,2012,27(10):3705-3712.
[7]Duzenli D,Saglar E,Deniz F,et al.Mutations in the AVPR2,AVP-NP11,and AQP2 genes in Turkish patients with diabetes insipidus[J].Endocrine,2012,42(3):664-669.
[8]Wenkert D,Merendino JJ Jr,Shenker A,et al.Novel mutations in the V2 vasopressin receptor gene of patients with X-linked nephrogenic diabetes insipidus[J].Hum Mol Genet,1994,3(8):1429-1430.
[9] Wenkert D,Schoneberg T,Merendino JJ Jr,et al.Functional characterization of five V2 vasopressin receptor gene mutations[J].Mol Cell Endocrinol,1996,124(1-2):43-50.
[10]Ryu HH,Chung JH,Shin BC,et al.Congenital nephrogenic diabetes insipidus with end-stage renal disease[J].Korean J Intern Med,2015,30(2):259-261.
[11]Janchevska A,Tasic V,Gucev Z,et al.X-linked recessive form of nephrogenic diabetes insipidus in a 7-year-old boy[J].Balkan J Med Genet,2015,17(2):81-85.
[12]顾锋,金自孟,史轶蘩,等.先天性肾性尿崩症的病因及临床特点[J].中华医学杂志,2004,84(17):1448-1449.
[13]Fujimoto M,Okada S,Kawashima Y,et al.Clinical overview of nephrogenic diabetes insipidus based on a nationwide survey in Japan[J].Yonago Acta Med,2014,57(2):85-91.
[14]Jean-Alphonse F,Perkovska S,Frantz,MC,et al.Biased agonist pharmacochaperones of AVP V2 receptor may treat congenital nephrogenic diabetes insipidus[J].J Am Soc Nephrol,2009,20(10):2190-2203.
[15]Segal TY,Mehta A,Anazodo A,et al.Role of gonadotropin-releasing hormone and human chorionic gonadotropin stimulation tests in differentiating patients with hypogon adotropic hypogonadism from those with constitutional delay of growth and puberty[J].J Clin Endocrinol Metab,2009,94(3):780-785.
[16]赵丹青,平凡,朱慧娟.AVPR2基因突变所致先天性肾型尿崩伴生长激素缺乏症的临床特征[J].中华临床医师杂志,2013,7(23):10559-10562.
