氢在FLiNaK(LiF-NaF-KF)熔盐中的渗透行为
2015-12-01曾友石吴胜伟渊王广华朱海云
曾友石 杜 林 皮 力 吴胜伟 钱 渊王广华 黄 豫 朱海云 刘 卫
1(中国科学院上海应用物理研究所 嘉定园区 上海 201800)
2(中国科学院核辐射与核能技术重点实验室 上海 201800)
3(中国科学院大学 北京 100049)
氢在FLiNaK(LiF-NaF-KF)熔盐中的渗透行为
曾友石1,2,3杜 林1,2,3皮 力1,2,3吴胜伟1,2钱 渊1,2王广华1,2黄 豫1,2朱海云1,2刘 卫1,2
1(中国科学院上海应用物理研究所 嘉定园区 上海 201800)
2(中国科学院核辐射与核能技术重点实验室 上海 201800)
3(中国科学院大学 北京 100049)
FLiNaK(LiF-NaF-KF)熔盐在高温熔盐堆或聚变堆的应用中面临着氚扩散渗透的问题。研究H2在FLiNaK熔盐中的渗透行为,能够为FLiNaK熔盐中氚的控制提供依据。氢同位素在熔盐中的扩散渗透特性测试系统主要用于测定熔盐中氢同位素的渗透行为,以获得氢同位素在熔盐中的扩散系数和溶解度常数等相关参数。通过该系统,本文对FLiNaK熔盐中H2的渗透、扩散和溶解等行为进行了研究。结果表明,受实验装置和实验方法的限制,H2在FLiNaK熔盐中的渗透主要以氢原子(或离子)的方式进行。在500−700 °C时,FLiNaK熔盐中H2的扩散系数与温度的关系满足:DFLiNaK-H=1.12×10−4exp(−66.40×103/RgT) (m2·s−1),其扩散活化能为66.40kJ·mol−1。而对于FLiNaK熔盐中H2的溶解常数,其与温度的关系可表述为:KFLiNaK-H=2.1×10−5exp(−0.94×103/RgT) (mol·m−3·Pa−1/2)。
FLiNaK熔盐,氢,渗透,扩散,溶解
FLiNaK(LiF-NaF-KF)熔盐在高温时,化学性质稳定,同时具有较好的传热性能,被认为是一种很有应用潜力的传热介质,可作为高温熔盐堆的传热流体[1−2]。其中,LiF、NaF和KF的摩尔比分别为46.5%、11.5%和42%的熔盐是研究较多的一种FLiNaK熔盐,其熔点为454 °C[3]。第IV代先进高温堆的设计中,将FLiNaK熔盐作为二回路传热流体的备选[4]。此外,在聚变堆研究中,提出了以FLiNaK熔盐作为氚增殖包层的可能[5]。然而,无论是作为熔盐堆的传热盐还是聚变堆的氚增殖包层,在使用时均面临着高温时氚(T)的扩散渗透问题[6]。熔盐中的锂(Li)受中子辐照后会产生氚,氚在高温下极易透过热交换器及回路管道进入环境中,产生对人体危害极大的氚化水(HTO)。因此,研究熔盐中氚的扩散渗透行为,对于熔盐中氚的控制和回收有着非常重要的意义。
目前,对FLiNaK熔盐中氚行为性质的研究,国内外相关报道很少。另外,在这些研究中,由于实验条件和实验方法之间的差异,造成彼此间数据差异较大。本文通过自建的氢同位素在熔盐中的扩散渗透特性测试系统,对FLiNaK熔盐中H2的渗透、扩散和溶解行为进行研究,获得FLiNaK熔盐中H2的扩散和溶解行为的参数。通过与相关文献的实验方法和实验结果的比较,探讨实验方法对实验结果的影响,以期获得较为准确的FLiNaK熔盐中H2的扩散和溶解参数,从而为FLiNaK熔盐中氚的行为性质研究提供参考依据。
1 实验方法
本实验在氢同位素扩散渗透特性测试系统中进行(图1)。该测试系统分为:供气系统、渗透罐与加热系统、检测系统和辅助部件。其中,供气系统可为实验提供Ar、H2、D2以及Ar和H2(或D2)的混合气。渗透罐分为内外两个腔体,均由316L不锈钢焊接而成。内腔通过焊接镍板分割成上下两个腔室。实验时,上腔填入熔盐,并通过加热系统使熔盐达到实验指定温度。下腔充入H2(或D2)气,高温时H2(或D2)通过镍板进入熔盐。熔盐中的H2(或D2)通过渗透,最终在熔盐表面释放。释放出来的H2(或D2)被上腔吹扫气体(Ar)载入检测系统,检测系统可检测载气中H2(或D2)的浓度。通过载气中H2(或D2)的渗透通量与时间的拟合关系,可计算出熔盐中H2(或D2)的扩散系数与溶解度。详细的实验装置与实验方法的介绍参见文献[7]。
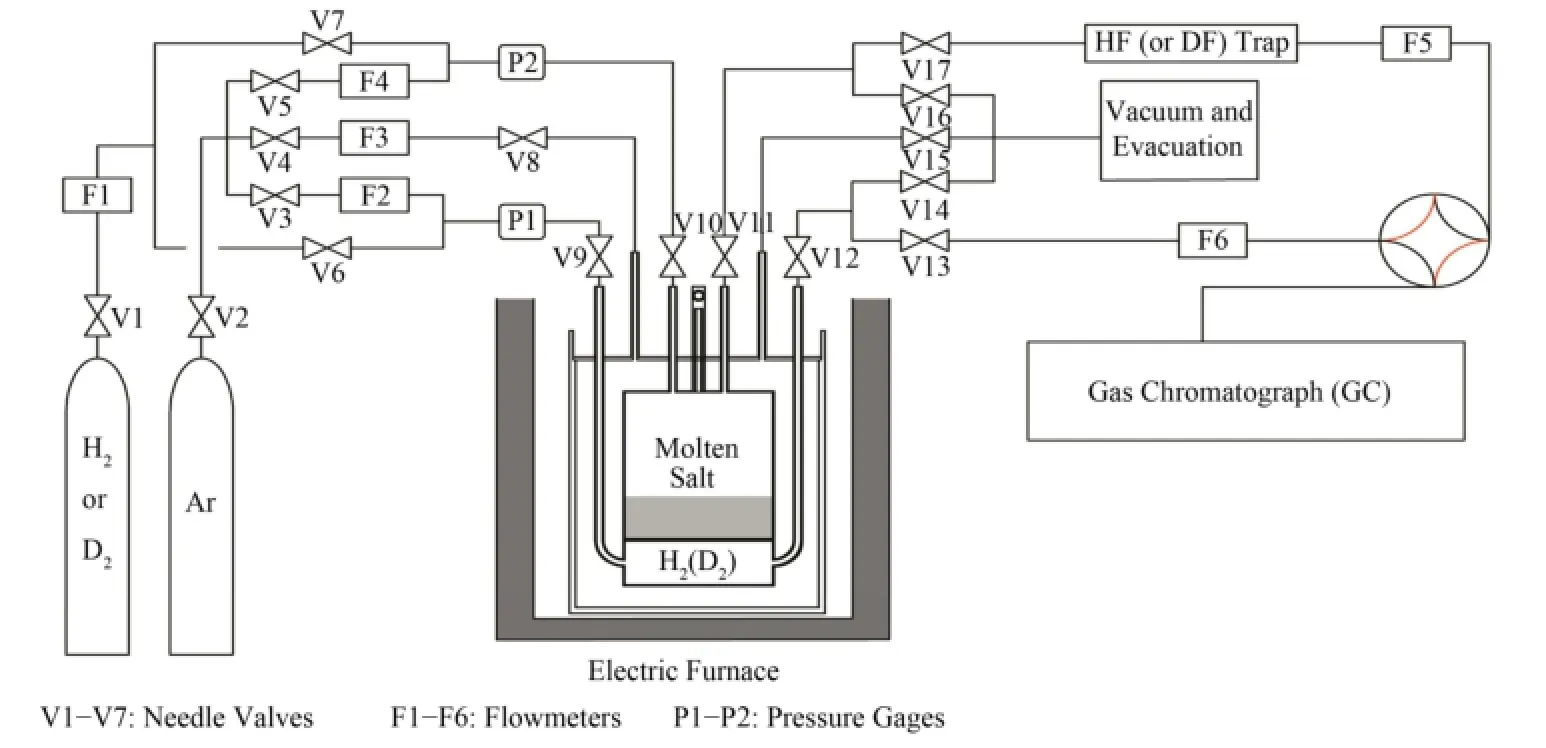
图1 氢同位素在熔盐中的扩散渗透特性测试系统简图Fig.1 A schematic diagram of the testing system for permeation and diffusion characteristics of hydrogen isotope in molten salt.
实验用熔盐为摩尔比分别为46.5% LiF、11.5% NaF和42% KF的混合盐,装填厚度为30 mm。熔盐在装填前经过净化处理,为保证熔盐的纯度,实验操作均在Ar气氛围中进行。实验开始前,使用Ar气吹扫熔盐,直至无法检测到吹扫气中H2(或D2)。实验时,对渗透罐的外腔抽真空,以消除从渗透罐内腔壁渗透的H2产生的影响。实验过程分为:(1) 温度为500 °C、550 °C、600 °C、650 °C和700 °C时,FLiNaK熔盐中H2的渗透行为研究,用以测定FLiNaK熔盐中H2的扩散和溶解系数与温度的依赖关系;(2) 不同H2分压(10 kPa、100 kPa和500 kPa)时,FLiNaK熔盐中H2的渗透行为研究,以检测FLiNaK熔盐中H2的渗透方式。
2 结果与讨论
图2是500−700 °C时FLiNaK熔盐中H2渗透通量与时间的关系以及相应的拟合结果。
拟合方程为[7]:
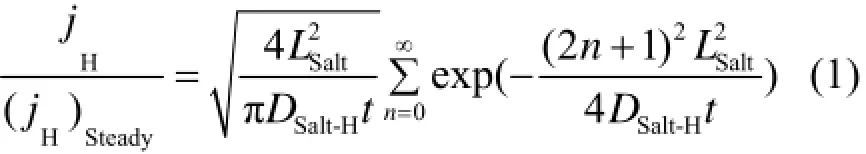
式中,jH为瞬态时,氢在熔盐中的渗透通量,mol-H2·m−2·s−1;(jH)Steady为稳态时,氢在熔盐中的渗透通量,mol-H2·m−2·s−1;LSalt为熔盐厚度,m;DSalt-H为熔盐中氢的扩散系数,m2·s−1;t为渗透时间,s。
通过调节DSalt-H,使实验结果与拟合值吻合,此时得到的扩散系数即为熔盐中氢的扩散系数。
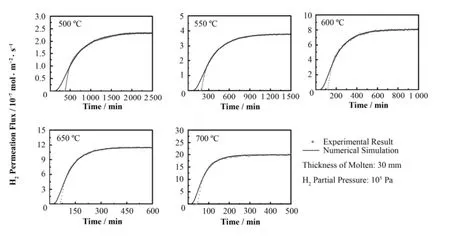
图2 500−700 °C时FLiNaK熔盐中H2渗透通量与时间关系的实验和拟合结果Fig.2 H2 permeation flux with time and the numerical calculations in molten FLiNaK at 500−700 °C.
由图2,除渗透初始时间外,500−700 °C时FLiNaK熔盐中H2渗透的实验结果与拟合结果是非常吻合的。而在渗透初始时测量结果与拟合结果的偏差,其原因可归结为:(1) H2从供气系统经过管路到达渗透罐时需要一定的时间(死时间),造成H2渗透时,初始渗透的时间与测量的时间出现偏差;(2) 实验开始时,将下腔的Ar换成H2后,H2会与管道和腔内残留的Ar混合,最终影响初始渗透时上游端H2的分压值。另外,由于H2在FLiNaK熔盐中的扩散过程随温度升高而加快,因此随实验温度的升高,测量结果与拟合结果出现差异的时间范围也逐渐减小。
图3是不同H2分压以及不同温度下,FLiNaK熔盐中H2的稳态渗透通量。H2在熔盐中的渗透有两种方式:(1) 以氢分子方式渗透;(2) 以氢原子(或离子)方式渗透。不同的渗透方式,将导致H2的稳态渗透通量与渗透上游H2分压的关系存在以下两种可能:
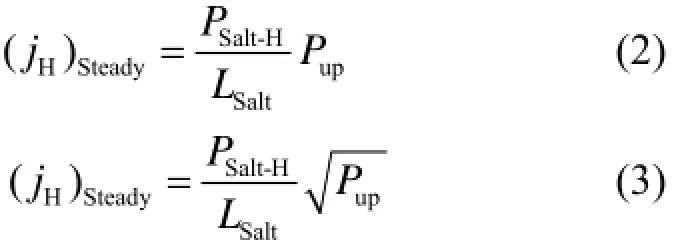
式中,PSalt-H为熔盐中H2的渗透率,mol·m−1·s−1·Pa−1或mol·m−1·s−1·Pa−1/2;Pup为渗透上游H2分压,Pa。
由图3,在对数坐标图中,同一温度下,FLiNaK熔盐中H2的稳态渗透通量与渗透上游H2分压成正比。其中,在500 °C、650 °C和700 °C时,两者的斜率分别为0.64、0.67和0.57。这一斜率关系更接近于式(3)中H2的稳态渗透通量与渗透上游H2分压的关系,说明在本实验中,H2在FLiNaK熔盐中主要以氢原子(或离子)的方式进行渗透。而在类似的实验中,Fukada等[8]同样得到了FLiNaK熔盐中H2的稳态渗透通量与渗透上游H2分压成正比的关系,但两者的斜率却更接近于1.0,即满足式(2)。同时,也说明了在Fukada的实验中,氢在FLiNaK熔盐中主要以氢分子的方式进行渗透。实验中出现两种氢渗透方式,其原因可能是充氢方式不同。在本实验中,采用的是下腔充氢的方式,而在Fukada等[8]的实验中,采用的是上腔充氢的方式。下腔充氢时,H2先通过镍板再进入熔盐中。此时,H2在镍板中先离解成氢原子,氢原子再透过镍板进入熔盐中,因此熔盐中的氢可能会以氢原子(或转变为氢离子)的方式存在。而上腔充氢时,H2先通过熔盐再进入镍板,因此熔盐中的氢可能会以氢分子的方式存在。由此可见,充氢方式的不同,可能造成熔盐中H2的渗透方式的差异。另一方面,FLiNaK熔盐中H2的稳态渗透通量与渗透上游H2分压的斜率比0.5稍大,说明在本实验中,FLiNaK熔盐中同时存在氢分子的渗透。其来源可能是氢原子透过镍板后复合成氢分子,而氢分子再进入熔盐中进行渗透。
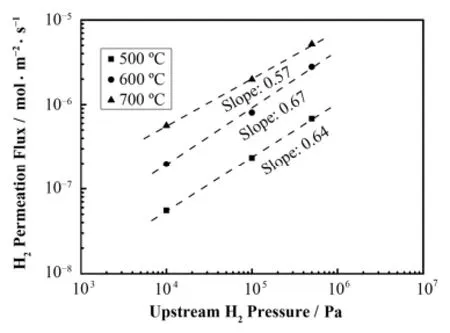
图3 500 °C、600 °C和700 °C时,FLiNaK熔盐中H2的稳态渗透通量与渗透端上游H2分压关系Fig.3 Steady-state H2 permeation flux in molten FLiNaK with upstream H2 partial pressure at 500 °C, 600 °C and 700 °C.
在实验中,由于充氢方式的差异,可能造成熔盐中不同的氢渗透方式,从而导致氢扩散机理发生变化。另外,在不同的熔盐中,氢的扩散机理也存在差异。表1是FLiNaK熔盐与其它熔盐中氢的扩散方式。

表1 不同熔盐中氢的扩散方式Table 1 Diffusion form of hydrogen in different molten salts.
在液态锂铅合金(Li17Pb83)中,氢的扩散行为主要通过Li-H(H−)的形成以及溶解的H原子(H0)来完成[9]。在液体锂(Li)中,氢的扩散行为则主要通过Li-H(H−)中H原子的迁移来完成[10]。在熔盐Li2BeF4中,以HF形式结合的H原子及其迁移是H2扩散的主要方式[11]。对于FLiNaK熔盐,Fukada等[8]的实验表明,H2在FLiNaK熔盐的扩散是以H2分子形式为主的,而低温时才受熔盐中H+影响;在本研究中,FLiNaK熔盐中H2的扩散则表现出以H原子(H0)或H离子(H+或H−)的形式为主,同时还存在少量的H2。在这一方式下,H2的扩散可能与熔盐Li2BeF4中H2的扩散类似,即通过以HF的结合来完成氢的迁移。
图4是H2在FLiNaK熔盐中扩散系数的拟合结果,同时图4中也给出了其他相关的文献数据。通过实验,FLiNaK熔盐中H2的扩散系数可拟合为以下Arrhenius方程:
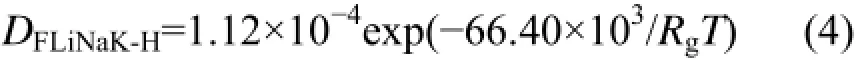
式中,DFLiNaK-H为FLiNaK熔盐中氢的扩散系数,m2·s−1;Rg为理想气体常数,J·mol−1·K−1;T为温度,K。
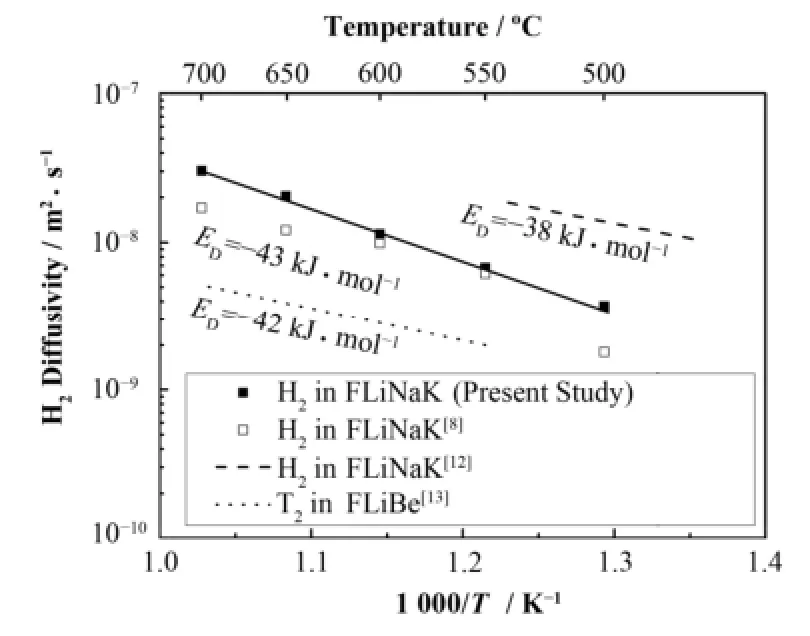
图4 熔盐FLiNaK中H2的扩散系数与温度关系Fig.4 Diffusivity of H2 through FLiNaK as a function of the reciprocal of temperature.
从图4中可看出,相较于Fukada[8]的实验结果,本研究的扩散系数在500−700 °C时具有更好的拟合结果(R2=0.998)。同时,在500 °C、650 °C和700 °C时,其扩散系数比Fukada得到的扩散系数偏大,特别是在500 °C时。另外,在Fukada的实验结果中,舍弃500 °C时偏离的扩散系数后,得到的FLiNaK熔盐中H2的扩散活化能为43 kJ·mol−1(550−700 °C)。而在本研究中,FLiNaK熔盐中H2的扩散活化能为(66.40±1.57) kJ·mol−1(500−700 °C)。研究得到的扩散系数和扩散活化能与文献[8]中的差异原因可能是FLiNaK熔盐中H2的扩散机理不同。一方面,Fukada的实验中,在550 °C和600 °C时,FLiNaK熔盐中H2的扩散受熔盐中H+的影响。而本研究中H2在FLiNaK熔盐中主要以氢原子(或离子)的方式进行扩散。因此在550 °C和600 °C时,两者中FLiNaK熔盐中H2的扩散可能都以H+为主,从而导致两者在550 °C和600 °C时得到的扩散系数比较接近。
另一方面,与FLiBe熔盐中T2的扩散活化能(42kJ·mol−1)[13]相比,本研究得到FLiNaK熔盐中H2的扩散活化能明显偏大(忽略H2和T2的同位素效应)。尽管FLiBe熔盐和FLiNaK熔盐中H2的扩散均可能以H+(HF)为主,但文献[14]表明,FLiBe熔盐中存在正四面体结构的BeF2−4离子,而BeF2−4离子将对H+(HF)的迁移产生影响。例如,相比于自由F−与H+形成的HF,由BeF2−4离子中的F−与H+形成的HF更不稳定,从而导致了FLiBe熔盐中更低的H2扩散活化能。
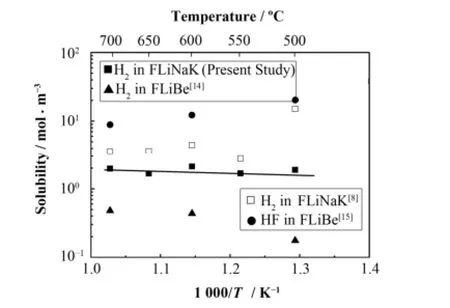
图5 熔盐FLiNaK中H2的溶解度与温度关系Fig.5 Solubility of H2 in FLiNaK as a function of the reciprocal of temperature.
通过扩散系数与稳态渗透通量的关系,可推导出FLiNaK熔盐中H2的溶解度常数[7]。在本研究中,由于H2的扩散是通过H+的形式进行,因此其溶解度可通过Sieverts定律来拟合。图5是1 atm-H2在FLiNaK熔盐中的溶解度以及熔盐和气体的相关文献值。而在本研究中,H2在FLiNaK熔盐中的溶解度常数可表述为以下Arrhenius方程:
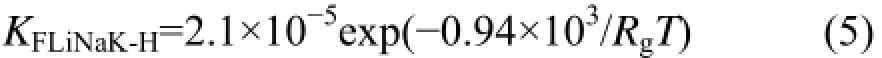
式中,KFLiNaK-H为FLiNaK熔盐中氢的溶解度常数,mol·m−3·Pa−1/2。
由图5,相较于FLiBe熔盐,在500−700 °C时,FLiNaK熔盐中H2的溶解度要大于FLiBe熔盐中H2的溶解度[13],但小于FLiBe熔盐中HF的溶解度[15]。另外,本文得到的H2溶解度均比Fukada[8]得到的溶解度偏小。在本研究中,H2先透过镍板后才能进入熔盐,这无疑会降低H2在FLiNaK熔盐中溶解量;而在Fukada的实验中,H2直接与熔盐接触,因此其溶解度会相对增大。事实上,本研究得到的FLiNaK熔盐中H2的溶解度在550−700 °C时与Fukada得到的结果相差并不明显,只有500 °C时才具有明显的差异。这充分说明了镍板对H2渗透的阻力相对于熔盐对H2渗透的阻力要小很多。而对于500 °C的差异,从上文FLiNaK熔盐中H2的扩散系数可看出,在Fukada的实验中,500 °C时FLiNaK熔盐中H2扩散系数相对较小,在通过渗透率进行溶解常数的计算时,将导致H2的计算溶解度常数偏大。
对于FLiNaK熔盐中H2的熔解热,其值为(−0.94±4.70) kJ·mol−1,负的熔解热表明FLiNaK熔盐中H2的溶解过程可能为吸热的过程。这与FLiBe熔盐中H2的溶解过程相同,但不同于FLiBe熔盐中HF的溶解过程。另外,相对较小的熔解热,表明FLiNaK熔盐中H2的溶解度与温度的依赖关系相对较小,与550−700 °C时Fukada得到的结果相似。
3 结语
使用氢同位素在熔盐中的扩散渗透特性测试系统,对FLiNaK熔盐中H2的渗透与扩散行为进行了研究。结果表明,在该实验装置中,H2在FLiNaK熔盐中的渗透方式与实验过程有关。采用下腔充氢的方式,H2在FLiNaK熔盐中的渗透将主要以氢原子(或离子)的方式进行。在这一条件下,500−700 °C时H2的扩散系数可拟合为:DFLiNaK-H=1.12×10−4exp(−66.40×103/RgT)。而溶解度常数则可表述为:KFLiNaK-H=2.1×10−5exp(−0.94×103/RgT)。与文献[8]值相比,相关参数的差异主要在于实验方法(充氢方式)上的差别。
1 Ambrosek J, Anderson M, Sridharan K, et al. Current status of knowledge of fluoride salt (FLiNaK) heat transfer[J]. Nuclear Technology, 2009, 165: 166−173
2 Khokhlov V, Ignatiev V, Afonichkin V. Evaluating physical properties of molten salt reactor fluoride mixture[J]. Journal of Fluorine Chemistry, 2009, 130: 30−37
3 Holcomb D E, Cetiner S M. An overview of liquid-fluoride-salt heat transport systems[R]. Oak Ridge National Laboratory, ORNL/TM-2010/156, 2010
4 Sherman S R. 2005 DOE hydrogen program: NHI system interface and support system[R]. 2005 DOE H2Annual Review, Project ID #PD31, 2005
5 Yamanishi H, Sagara A. Annual report of National Institute for fusion science[R]. Japan, April 1999-March 2000
6 黄豫, 刘卫, 肖德涛, 等. 熔盐堆中氚的控制和检测[J].核技术, 2011, 34(8): 632−666
HUANG Yu, LIU Wei, XIAO Detao, et al. Control and monitoring of tritium in molten salt reactor[J]. Nuclear Techniques, 2011, 34(8): 632−636
7 Zeng Y S, Wu S W, Qian Y, et al. Apparatus for determining permeability of hydrogen isotope in molten salt[J]. Nuclear Science and Techniques, 2014, 25(4): 040602
8 Fukada S, Morisaki A. Hydrogen permeabiligy through a mixed molten salt of LiF, NaF and KF (FLiNaK) as a heat-transfer fluid[J]. Journal of Nuclear Materials, 2006, 358: 235−242
9 Masuyama D, Oda T, Fukada S, et al. Chemical state and diffusion behavior of hydrogen isotopes in liquid lithium-lead[J]. Chemical Physics Letters, 2009, 483: 214−218
10 Fukada S, Kinoshita M, Kuroki K, et al. Hydrogen diffusion in liquid lithium from 500 °C to 650 °C[J]. Journal of Nuclear Materials, 2005, 346: 293−297
11 Klix A, Suzuki A, Terai T. Study of tritium migration in liquid Li2BeF4with ab initio molecular dynamics[J]. Fusion Engineering and Design, 2006, 81: 713−717
12 Katsuta H, Furukawa K. Diffusivity and solubility of hydrogen in molten fluoride mixture (LiF-NaF-KF)[J]. Journal of Nuclear Materials, 1978, 71: 375−376
13 Calderoni P, Sharpe P, Hara M, et al. Measurement of tritium permeation in FLiBe(2LiF-BeF2)[J]. Fusion Engineering and Design, 2008, 83: 1331−1334
14 Malinauskas A P, Richardson D M. The solubilities of hydrogen, deuterium, and helium in molten Li2BeF4[J]. Industrial and Engineering Chemistry Research Fundamentals, 1974, 13: 242−245
15 Field P E, Shaffer J H. The solubilities of hydrogen fluoride and deuterium fluoride in molten fluorides[J]. The Journal of Physical Chemistry, 1967, 71: 3218−3222
CLC TL281
Permeability of hydrogen in molten salt FLiNaK(LiF-NaF-KF)
ZENG Youshi1,2,3DU Lin1,2,3PI Li1,2,3WU Shengwei1,2QIAN Yuan1,2WANG Guanghua1,2HUANG Yu1,2ZHU Haiyun1,2LIU Wei1,2
1(Shanghai Institute of Applied Physics, Chinese Academy of Sciences, Jiading Campus, Shanghai 201800, China)
2(Key Laboratory of Nuclear Radiation and Nuclear Energy Technology, Chinese Academy of Sciences, Shanghai 201800, China)
3(University of Chinese Academy of Sciences, Beijing 100049, China)
Background: Molten salt FLiNaK(LiF-NaF-KF) has potential to be used as heat-transfer fluid of molten salt nuclear reactor, because of its high chemical stability, moderate specific heat and sufficient thermal conductivity. One adverse characteristic was that tritium was produced at relatively high rates in such reactors, which could diffuse through metals at high temperature and thus required to evaluate the behavior of tritium in FLiNaK. Purpose: This study aims to the permeation behavior of hydrogen in molten salt FLiNaK, providing the basis for tritium permeation behavior in molten salt. Methods: Plentiful experiments were conducted in a testing system for permeation and diffusion characteristics of hydrogen isotope in molten salt. Numerical fitting method of experimental results was performed to obtain the hydrogen permeation characteristics in molten salt FLiNaK. Results: The results showed that hydrogen was diffusing as H+species in molten salt FLiNaK. The diffusion coefficients and solubility constants of hydrogen in molten salt FLiNaK can be correlated to DFLiNaK-H=1.12×10−4exp(−66.40×103/RgT) (m2·s−1) and KFLiNaK-H=2.1×10−5exp(−0.94×103/RgT) (mol·m−3·Pa−1/2). Conclusion: The diffusion coefficients and solubility constants of hydrogen in molten salt FLiNaK were derived from the experimental results.
Molten salt FLiNaK, Hydrogen, Permeability, Diffusion, Solubility
TL281
10.11889/j.0253-3219.2015.hjs.38.020603
中国科学院先导专项(No.XDA020200)资助
曾友石,男,1987年出生,2014年于中国科学院上海应用物理研究所获博士学位,研究领域为熔盐堆中氚的控制
刘卫,E-mail: liuwei@sinap.ac.cn
2014-09-22,
2014-10-21
