二元配合物中电镀锌镍合金的结构与抗腐蚀性
2015-11-30龙晋明裴和中由劲博
张 秀,龙晋明,裴和中,由劲博,黄 攀
(昆明理工大学材料科学与工程学院,昆明 650093)
锌镍合金镀层一般指含镍质量分数20%以下的合金镀层.含镍质量分数在10%~15%的锌镍合金镀层的耐蚀性和耐磨性是纯锌镀层的3~6倍,钝化后的合金镀层的耐蚀性是锌镀层钝化后的3~5倍,和镉镀层的性能相近,甚至更好[1-3].碱性电镀锌镍合金的氢脆小,在宽的电流密度下含镍量均匀,镀液对设备的腐蚀小,镀液成本低且废液易处理,而且镀层的机械性能和加工性能(上漆性,焊接性能等)优良[4-5].
电镀锌镍合金工艺由 Schoch和Cocks在20世纪初提出,经过数十年的发展,已经发展出酸性、碱性多种电镀体系,镀层的性能也有了很大的提高[6-8].此技术近年来已开始应用于汽车、航空、电子等工业中,用来提高产品的抗腐蚀能力[9].作为一种较新的钢铁和镁合金等材料的表面防护性镀层,锌镍合金镀层受到国内外研究者的关注.虽然在酸性和弱酸性镀液体系中所得锌镍合金镀层的组成结构及性能已有较多研究报道[2,10-12],但对于碱性锌酸盐体系中电镀锌镍合金的研究还不够充分,尤其是该体系中络合剂或配位剂的选择及其影响的研究较少.已有的研究表明,碱性镀液中只有在合适的锌镍比范围内才能得到γ单相锌镍合金.杨房祖等[13]在不同锌镍比的锌酸盐镀液中,以三乙醇胺为络合剂电沉积得到不同结构的锌镍合金;Mülle等[14]选择三乙烯四胺、四乙烯五胺、二乙基三胺等物质作为配位剂,对锌酸盐体系电镀锌镍合金作了初步研究.
本文针对碱性锌酸盐镀液体系,采用四乙烯五胺和三乙醇胺(TEA)两种物质组成不同的二元配合物,研究不同电镀条件参数对镀层的组成结构和抗腐蚀性能的影响,以期为工艺优化及应用提供参考.
1 实验
1.1 电镀工艺
实验室用1 cm×1 cm×1 mm的低碳钢片作基体材料,电镀使用高纯镍板作阳极材料,使用试剂均为分析纯试剂,试验用水为去离子水,在室温下电镀.电镀液的主要成分如下:NaOH,质量浓度120 g/L;ZnO,质量浓度 12 g/L;NiSO4·7H2O,质量浓度4.61~17.77 g/L(Ni2+/Ni2++Zn2+原子数分数x=10%~30%);镀锌光亮剂(FK-303,福州八达表面工程技术研究所),体积分数3.2 mL/L;糖精钠,质量浓度0.6 g/L;1,4-丁炔二醇,质量浓度0.4 g/L;十二烷基苯磺酸钠,质量浓度0.1 g/L;四乙烯五胺,质量浓度15.45 g/L;三乙醇胺,质量浓度4~20 g/L(TEA/Ni2+原子个数比=2).电镀阴阳极的面积比为1∶2,电流密度为1~5 A/dm2,电镀时间40 min.电镀完毕后用水清洗试样并烘干.
1.2 腐蚀电化学测试
用质量分数3.5%的NaCl水溶液作为腐蚀介质(模拟海水条件),通过测试镀层的极化曲线和交流阻抗谱来考察其耐腐蚀特性.使用CS350型电化学工作站(武汉科思特仪器有限公司)和标准三电极体系进行电化学测试,温度为室温(20±5)℃.以铂电极为辅助电极,饱和甘汞电极(SCE)为参比电极,镀层试片为工作电极.极化曲线测试的电位范围为稳态下开路电位±300 mV,扫描速度0.5 mV/s;交流阻抗测试时,工作电极的电位设定于开路电位,交流信号频率100 000~0.01 Hz,振幅±10 mV.本文所提到的电位均相对于SCE.
1.3 镀层分析
采用能谱仪(PHOENIX型,美国 EDAX公司)对镀层进行表面成分分析.使用多晶转靶X-射线衍射仪(Model D/max-2200,日本Rigaku公司)测定镀层的相组成和织构,实验条件:Cu靶0.154 2 nm,30 mA,36 kV,扫描速率 10(°)/min.
镀层的择优取向用(hkl)晶面择优取向密度Jhkl(也称为织构系数)表征,根据 Harris法[15]可由式(1)计算Jhkl:

式中:Ihkl为实测镀层(hkl)晶面的衍射线相对强度;I0
hkl为标准图谱中(hkl)的衍射线相对强度;n为计算时所取图谱中的衍射线条数目.若各晶面的择优取向度Jhkl均为1,则表示镀层中的晶粒呈现无序取向;若各晶面的Jhkl不等于1,说明镀层晶粒存在择优取向或织构.当干涉面的Jhkl大于1,表明大多数晶粒的(hkl)晶面与镀面平行,此时该晶面称为择优取向面;若某干涉面的Jhkl等于n时(其余晶面的Jhkl等于0),则表示其为唯一的择优取向面[16].
2 结果与讨论
2.1 镀液中镍离子含量对镀层的影响
2.1.1 耐腐蚀性
许多文献指出,改变镀液中金属主盐含量会使镀层的结构组成以及电化学性能发生变化[2,11-13].图1为电沉积电流密度 2 A/dm2、镀液的TEA/Ni2+原子个数比保持为2的条件下,不同镍原子数分数x(Ni2+/Ni2++Zn2+)=10%~30%的镀液中所制备的锌镍合金镀层的极化曲线.由图1可以看到:当镀液中镍离子含量较低(原子数分数x=10%)时,镀层在质量分数3.5%的NaCl水溶液中的腐蚀电位很低,为-1.020 3 V,而腐蚀电流密度较高,阳极活性溶解的电位范围较宽;随着镍离子含量的提高,镀层的腐蚀电位正移,腐蚀电流密度减小,阳极活性溶解的电位范围变窄;当镍离子原子数分数增加到25%时,镀层的腐蚀电位达到最高,腐蚀电流密度最小,阳极活性溶解的电位范围最窄,表明此时镀层的耐蚀性最好.

图1 不同镍离子原子数分数镀液制备的锌镍合金镀层在3.5%NaCl溶液中的极化曲线
图2为镀层在质量分数3.5%的NaCl溶液中的交流阻抗谱图.采用Zsimpwin阻抗分析软件对阻抗谱进行拟合,得到对应的等效电路见图3,其中Rs为溶液电阻,常相位元件CEPdl为双电层电容,Rt为电荷传递电阻.

图2 不同镍离子原子数分数镀液制备的锌镍合金镀层在质量分数3.5%NaCl溶液中的交流阻抗谱

图3 锌镍合金镀层在质量分数3.5%NaCl溶液中的交流阻抗谱的等效电路
由图2可以看到,随着镀液中镍含量的增加,镀层在腐蚀介质中的容抗弧的直径增加,电荷传递电阻变大.根据镀层在质量分数3.5%NaCl溶液中的极化曲线和交流阻抗谱,得到腐蚀电化学参数,列于表1中.由表1数据可见:当镍离子原子数分数为25%时,镀层在质量分数3.5%NaCl溶液中腐蚀反应的电荷传递电阻最大,为1 683 Ω·cm2,相应的腐蚀电流密度最小,为2.6 μA/cm2;而镍离子原子数分数低于或高于25%时,得到的镀层耐蚀性要稍低一些,但差别并不十分明显,表明对于本实验的锌镍合金镀液体系,其允许的镍离子原子数分数范围较宽,x(Ni2+/Ni2++Zn2+)=15%~30%.在实际电镀生产中,当镀液在较宽的镍离子浓度范围内变化时,对于得到抗腐蚀性能较好的锌镍合金镀层是有利的.
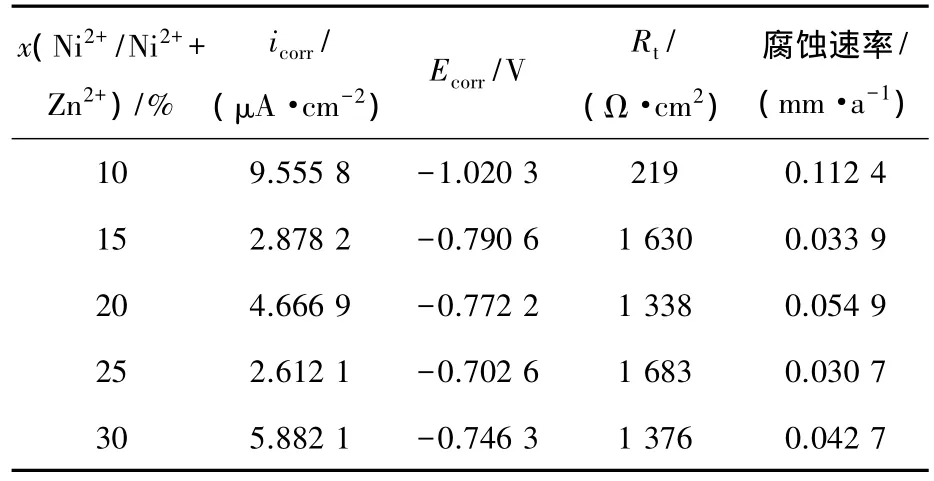
表1 不同镍离子原子数分数镀液制备的锌镍合金镀层在3.5%NaCl溶液中的腐蚀电化学参数
2.1.2 镀层镍含量、相结构与择优取向
EDS和XRD分析发现,镀液中镍离子的相对含量对镀层的镍的原子数分数、相结构与择优取向有显著影响.图4为锌镍合金镀层中的镍原子数分数与镀液中的镍离子原子数分数间的关系曲线,其中CRL线表示镀液对应的镍含量.

图4 电流密度2 A/dm2时锌镍合金镀层中含镍量与镀液中的镍离子含量间的关系曲线
由图4可看出,在x(Ni2+/Ni2++Zn2+)=10%~30%内,随着镀液中镍离子浓度的提高,镀层的含镍量也相应增加;当镍离子原子数分数超过20%后,镀层的镍含量开始显著低于镀液中的镍含量,并且两者的差值随溶液中镍离子浓度的提高而进一步增大,即表明此时锌镍合金异常共沉积的倾向加剧.
图5为锌镍合金镀层的XRD谱图,由式(1)计算出的镀层择优取向度列于表2中.对于在x(Ni2+/Ni2++Zn2+)=10%的镀液中得到的镀层,镍原子数分数为11.5%(图4).根据XRD物相分析可知,其由γ-Ni2Zn11和纯Zn两相组成,镀层的择优取向性不明显.

图5 在不同镍离子原子数分数镀液中电沉积(ic=2 A/dm2)制备的锌镍合金镀层的X射线衍射谱图
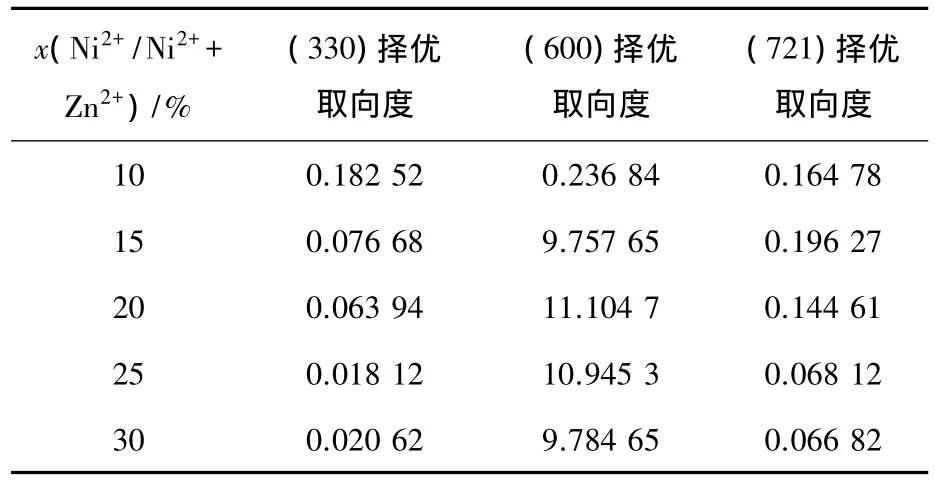
表2 在不同镍离子含量镀液中电沉积(ic=2 A/dm2)制备的锌镍合金镀层的择优取向度
当镀液中镍原子数分数超过15%后,镀层中的纯Zn相已经不存在,成为单相(γ-Ni2Zn11)结构,这种γ相结构的镀层表现出明显的(600)晶面择优取向性(见表2).结合图5和表2可以看出,随着锌镍合金镀层含镍量的变化,镀层的相结构也有所变化.在x(Ni2+/Ni2++Zn2+)=10%的镀液中得到的镀层含有纯锌相,所以镀层的腐蚀电位接近锌在质量分数3.5%的NaCl溶液中的腐蚀电位(约为-1 100 mV),而且γ相在(600)方向上的生长受到强烈地抑制;随着镀层中镍含量的增加,γ相的生长方式也发生了变化:(222)方向上基本上没有生长,(330)和(721)方向的生长受到进一步抑制,衍射峰的强度减弱.尤其是当镍原子数分数达到20%后,γ相沿(721)方向的生长变得非常弱,导致该衍射峰消失.在x(Ni2+/Ni2++Zn2+)=15%~30%的镀液中得到的镀层均具有γ单相(γ-Ni2Zn11)结构,且其结晶晶粒均呈现(600)面择优生长.
金属电沉积一般需要经过基体外延生长、无序取向、择优取向3个状态[16].由于镀液中金属离子的浓度、络合物的稳定性以及电沉积电流密度等工艺条件的影响,不同晶面的生长速度不同,使电结晶形成的多晶体镀层出现择优取向.通过对照锌镍二元合金相图[17]可知,在镍原子数分数为16.81%~19.40%时,锌镍合金的平衡相组成应为单一的γ相(镍含量可在一定范围内变化),而此处(镀液x(Ni2+/Ni2++Zn2+)=15%~30%)所得的同样含镍量范围的锌镍合金镀层,也具有γ单相结构,因此可认为本实验条件下得到的锌镍合金镀层的相组成,与相图反映的热力学相平衡状态基本上是接近的.
通过上述分析可知,镀液中镍含量的变化将引起镀层中镍含量、相组成结构和结晶生长方式发生变化,从而导致合金镀层在腐蚀介质中的抗腐蚀性能发生变化.
2.2 电沉积电流密度对镀层的影响
2.2.1 耐腐蚀性
图6和图7分别为镍原子数分数x(Ni2+/Ni2++Zn2+)=15%的镀液中,以不同电沉积电流密度制备的锌镍合金镀层的极化曲线和电化学阻抗谱,主要的腐蚀电化学参数列于表3中.
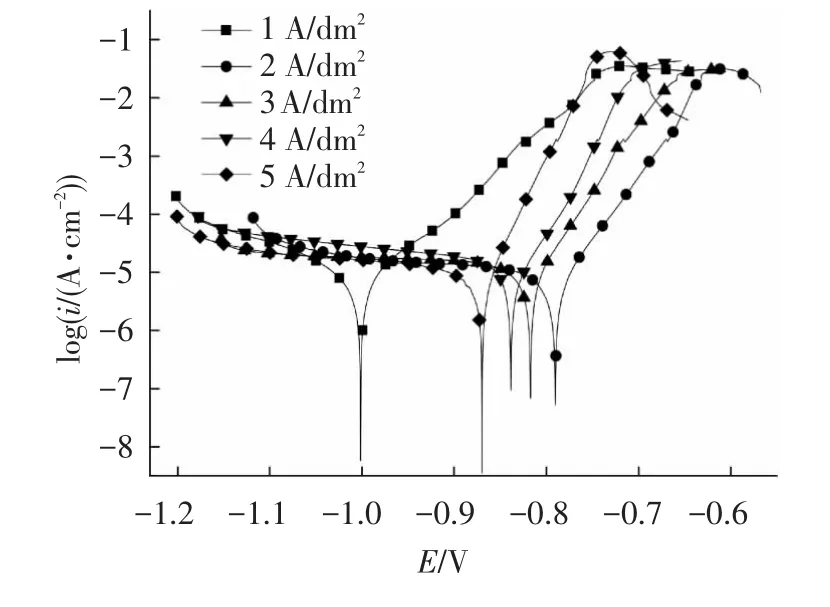
图6 以不同电沉积电流密度制备的锌镍合金镀层在3.5%NaCl溶液中的极化曲线

图7 以不同电沉积电流密度制备的锌镍合金镀层在3.5%NaCl溶液中的交流阻抗谱
由图6可以看到:除电流密度为1 A/dm2外,其他试样的极化曲线在阴极极化区都出现电流平台,表明反应过程受到扩散控制[18];在阳极极化区的末端出现钝化现象,且随着电流增大钝化区的维钝电流增加.
由图7可以看到,电流密度为1 A/dm2时得到镀层的阻抗最小(496 Ω·cm2),而当电流密度提高到2 A/dm2时镀层的阻抗最大(1 630 Ω·cm2).值得注意的是,当进一步增大电流密度时,镀层的阻抗反而减小.观察发现,在电镀过程中提高电流密度会加剧氢气的析出,同时使镀层镍含量增加[19],结晶择优取向改变.显然,镀层耐腐蚀性的变化与此有密切联系.在电流密度为2 A/dm2时,得到的镀层相对其他电流密度下得到的镀层具有更强的抗腐蚀性能,这与其具有最大的(600)择优取向度有关(见2.2.2节讨论).

表3 以不同电沉积电流密度(ic)制备的锌镍合金镀层的腐蚀电化学参数
2.2.2 镀层镍含量、相结构与择优取向
在合金电镀中,电沉积电流密度对合金成分的影响非常明显,电流密度提高使得阴极极化过电位增大,这有利于合金中电位较负金属的含量增加[20].图8为镀液中 x(Ni2+/Ni2++Zn2+)=15%时锌镍合金镀层中的镍原子数分数与电沉积电流密度间的关系曲线,其中CRL线表示镀液对应的镍原子数分数.由图8可以看到,随着电流密度的增加,镀层中镍的原子数分数由15.23%增加到16.93%,超过镀液中x(Ni2+/Ni2++Zn2+),这说明增加电沉积电流密度可以促进被络合剂(TEPA、TEA)络合、电位变负的镍离子的沉积,抑制锌镍金属离子异常共沉积.
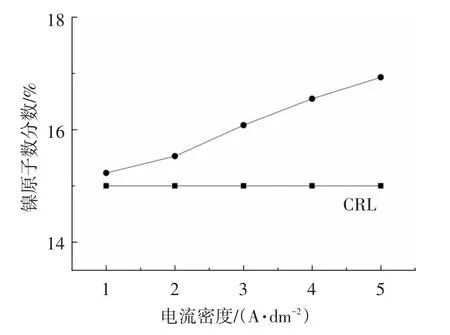
图8 镀液中x(Ni2+/Ni2++Zn2+)=15%时锌镍合金镀层中的镍含量与电沉积电流密度间的关系曲线
在图9和表4中可以看到:增加电沉积电流密度会使组成镀层相的生长方式发生改变,出现不同的择优取向;当电流密度由1 A/dm2增大到2 A/dm2时,(600)衍射峰强度变得最大,即具有最显著的(600)择优取向;当电流密度大于2 A/dm2后,镀层的(600)峰强度开始急剧下降,(600)择优取向度变小,说明当电流密度超过一定值(2 A/dm2)时,晶粒在(600)方向上的生长开始受到强烈地抑制;同样,增加电流密度使合金γ相在(721)方向上生长有一定择优取向,择优取向度随电流密度的增加而变大,衍射峰的强度有一定的增强.

图9 镀液中x(Ni2+/Ni2++Zn2+)=15%时不同电沉积电流密度下制备的锌镍合金镀层的X射线衍射谱图

表4 镀液中x(Ni2+/Ni2++Zn2+)=15%时不同电沉积电流密度下制备的锌镍合金镀层的择优取向度
比较表3和表4中数据可发现:(600)晶面的择优取向对镀层的抗腐蚀性能有很大的影响;在2 A/dm2时(600)晶面择优取向度最大(9.611 33),镀层的抗腐蚀性能相应也最强;随着电流密度的增加,镀层(600)晶面的择优取向度减小,镀层的抗腐蚀性能也相应降低.
3 结论
1)在以四乙烯五胺(TEPA)和三乙醇胺(TEA)为络合剂的碱性镀液中,镍离子的相对浓度和电沉积电流密度对锌镍合金镀层的成分、相结构、结晶取向和耐腐蚀性具有显著影响.
2)在电流密度为2 A/dm2时,随着镀液中镍离子含量的增加,镀层中镍含量相应增加.当镍离子原子数分数超过10%后,镀层的相组成由γ+Zn两相变为γ单相.γ相晶粒在(330)、(721)方向上的生长受到抑制,在(600)方向的生长得到促进,使得其在氯化钠溶液中的抗腐蚀能力增强.
3)镀液中镍原子数分数为15%时,随着电沉积电流密度的增加,镀层中镍含量增加,镀层在(330)、(721)方向的择优取向度增加.电流密度由1 A/dm2提高到2 A/dm2时,镀层γ相具有最大的(600)择优取向度,同时显示出最优的耐腐蚀性能.
4)锌镍合金镀层的耐腐蚀性除了与镍含量有关外,在很大程度上还与镀层γ相晶粒的择优取向度有关.
[1] HAMMAMI O,DHOUIBI L,TRIKI E.Influence of Zn-Ni alloy electrodeposition techniques on the coating corrosion behaviour in chloride solution[J].Surface and Coatings Technology,2009,203(19):2863-2870.
[2] BYK T V,GAEVSKAYA T V,TSYBULSKAYA L S.Effect of electrodeposition conditions on the composition,microstructure,and corrosion resistance of Zn-Ni alloy coatings[J].Surface and Coatings Technology,2008,202(24):5817-5823.
[3] WYKPIS K,POPCZYK M,BUDNIOK A.Electrolytic deposition and corrosion resistance of Zn-Ni coatings obtained from sulphate-chloride bath[J].Bulletin of Materials Science,2011,34(4):997-1001.
[4] 曹浪,左正忠,田志斌,等.电镀锌镍合金的研究现状与展望 [J].材料保护,2010,43(4):33-37.CAO Lang,ZUO Zhengzhong,TIAN Zhibin,et al.Research status and prospect of Zn-Ni alloy electroplating[J].Materials Protection,2010,43(4):33-37.
[5] 黄攀,裴和中,张国亮,等.碱性锌镍合金电镀的研究现状及展望[J].热加工工艺,2012,41(2):161-164.HUANG Pan,PEI Hezhong,ZHANG Guoliang,et al.Study on reality and prospect of alkaline zinc nickel alloy electroplating [J].Hot Working Technology,2012,41(2):161-164.
[6] MOSAVAT S H,SHARIAT M H,BAHROLOLOOM M E.Study of corrosion performance of electrodeposited nanocrystalline Zn-Ni alloy coatings[J].Corrosion Science,2012,59:81-87.
[7] WYKPIS K,POPCZYK M,NIEDBAŁA J,et al.Influence ofthermaltreatmenton the corrosion resistance of electrolytic Zn-Ni coatings[J].Materials Science-Poland,2011,29(3):177-183.
[8] YOGESHA S,HEGDE A C.Optimization of bright zinc-nickel alloy bath for better corrosion resistance[J].Transactions of the Indian Institute of Metals,2010,63(6):841-846.
[9] 田伟,吴向清,谢发勤.Zn-Ni合金电镀的研究进展[J].材料保护,2004,37(4):26-29.TIAN Wei,WU Xiangqing,XIE Faqin.Research and development of zinc-nickel alloy electroplating [J].Materials Protection,2004,37(4):26-29.
[10] QIAO Xiaoping,LI Helin,ZHAO Wenzhen,et al.Effects of deposition temperature on electrodeposition of zinc-nickel alloy coatings[J].Electrochimica Acta,2013,89:771-777.
[11] RAVINDRAN V,MURALIDHARAN V S.Characterization of zinc-nickel alloy electrodeposits obtained from sulphamate bath containing substituted aldehydes[J].Bulletin of Materials Science,2006,29(3):293-301.
[12] De OLIVEIRA E M,CARLOS I A.Study of the effect of mannitol on ZnNi alloy electrodeposition from acid baths and on the morphology,composition,and structure of the deposit[J].Journal of Applied Electrochemistry,2009,39(10):1849-1856.
[13] 杨房祖,许书楷,周绍民.锌镍合金镀层的组成与相结构的关系[J].厦门大学学报:自然科学版,1994,33(1):63-67.YANG Fangzu,XU Shukai,ZHOU Shaomin.Relationship between the composition and phase structure of the Zn-Ni alloy deposits[J].Journal of Xiamen University(Natural Science),1994,33(1):63-67.
[14] MÜLLE C,SARRET M.Complexing agents for a Zn-Ni alkaline bath [J].Journal of Electroanalytical Chemistry,2002,519(1/2):85-92.
[15] 王英华.X光衍射技术基础[M].北京:原子能出版社,1993:230-262.
[16] 周绍民.金属电沉积——原理与研究方法[M].上海:上海科学技术出版社,1987,437.
[17] 长崎诚三,平林真,刘安生.二元合金状态图集[M].北京:冶金工业出版社,2004:240.
[18] DESLOUIS C,TRIBOLLER B,MENGOLI G.Electrochemical behavior of copper in mentral aerated chloride solutionⅠ:steady-state investigation[J].Journal of Applied Electrochemistry,1988,18(3):374-383.
[19] 鹿文珊,徐天凤,陈宇,等.碱性电镀锌镍合金的研究[J].中国腐蚀与防护学报,2012,32(6):443-448.LU Wenshan,XU Tianfeng,CHEN Yu,et al.Zincnickel alloy electroplating in an alkaline bath [J].Journal of Chinese Society for Corrosion and Protection,2012,32(6):443-448.
[20] 屠振密.电镀合金原理与工艺[M].北京:国防工业出版社,1993:207-213.
